Madopar® 62,5 mg
Hartkapseln
Levodopa 50 mg
Benserazid 12,5 mg (als Benserazidhydrochlorid)
Madopar® 125 mg
Hartkapseln
Levodopa 100 mg
Benserazid 25 mg (als Benserazidhydrochlorid)
Madopar® 125 mg T
Tabletten
Levodopa 100 mg
Benserazid 25 mg (als Benserazidhydrochlorid)
Madopar® 250 mg
Tabletten
Levodopa 200 mg
Benserazid 50 mg (als Benserazidhydrochlorid)
Madopar® LT
Tabletten zur Herstellung einer Suspension zum Einnehmen
Levodopa 100 mg
Benserazid 25 mg (als Benserazidhydrochlorid)
Madopar 62,5 mg
Jede Hartkapsel enthält 50 mg Levodopa und 14,25 mg Benserazidhydrochlorid, entsprechend 12,5 mg Benserazid.
Madopar 125 mg
Jede Hartkapsel enthält 100 mg Levodopa und 28,5 mg Benserazidhydrochlorid, entsprechend 25 mg Benserazid.
Madopar 125 mg T
Jede Tablette enthält 100 mg Levodopa und 28,5 mg Benserazidhydrochlorid, entsprechend 25 mg Benserazid.
Madopar 250 mg
Jede Tablette enthält 200 mg Levodopa und 57 mg Benserazidhydrochlorid, entsprechend 50 mg Benserazid.
Madopar LT
Jede Tablette enthält 100 mg Levodopa und 28,5 mg Benserazidhydrochlorid, entsprechend 25 mg Benserazid.
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
Madopar 62,5 mg
Hartkapsel.
Madopar 62,5 mg sind blau-graue Hartkapseln. Sie tragen auf einer Seite die Aufschrift „ROCHE“.
Madopar 125 mg
Hartkapsel.
Madopar 125 mg sind blau-rosa Hartkapseln. Sie tragen auf einer Seite die Aufschrift „ROCHE“.
Madopar 125 mg T
Tablette.
Madopar 125 mg T sind hell-rote, leicht gesprenkelte Tabletten mit Kreuzbruchrille.
Die Tablette kann in 2 oder 4 gleiche Dosen geteilt werden.
Madopar 250 mg
Tablette.
Madopar 250 mg sind hell-rote, leicht gesprenkelte Tabletten mit Kreuzbruchrille.
Die Tablette kann in 2 oder 4 gleiche Dosen geteilt werden.
Madopar LT
Tablette zur Herstellung einer Suspension zum Einnehmen.
Madopar LT sind weiße Tabletten mit Bruchrille.
Die Tablette kann in gleiche Dosen geteilt werden.
Parkinson-Krankheit (Schüttellähmung, eine Erkrankung mit grobschlägigem Zittern, Bewegungsverlangsamung und Starre der Muskeln).
Symptomatische Parkinson-Syndrome (Krankheitserscheinungen, die der Parkinson´schen Krankheit entsprechen, aber infolge von Vergiftungen, Hirnentzündungen und arteriosklerotischen Hirnveränderungen auftreten). Ausgenommen hiervon ist das medikamentös induzierte Parkinson-Syndrom (Parkinson-ähnliche Krankheitserscheinungen, die durch bestimmte Arzneimittel ausgelöst werden).
Die Dosierung richtet sich nach der Schwere der extrapyramidalen Symptomatik und der Verträglichkeit im Einzelfall. Hohe Einzeldosen sollten vermieden werden. Die Behandlung wird mit langsam ansteigender Dosierung durchgeführt.
Die Behandlung muss langsam einschleichend erfolgen, um das Ausmaß der Nebenwirkungen gering zu halten und einen möglichen Behandlungserfolg nicht zu gefährden.
Dosierung
Madopar 62,5 mg
Bei bisher unbehandelten Kranken wird mit einer Tagesdosis von 2 bis 4 Hartkapseln Madopar 62,5 mg (100 mg bis 200 mg Levodopa in Kombination mit 28,5 mg bis 57 mg Benserazidhydrochlorid) begonnen.
Eine Dosissteigerung kann um 1 bis 2 Hartkapseln Madopar 62,5 mg (50 mg bis 100 mg Levodopa und 14,25 mg bis 28,5 mg Benserazidhydrochlorid) jeden 3. bis 7. Tag vorgenommen werden. Es empfiehlt sich, in diesen Fällen höher dosierte Formen von Madopar einzusetzen.
Tagesdosen von 16 Hartkapseln Madopar 62,5 mg (800 mg Levodopa und 228 mg Benserazidhydrochlorid) sollen in der Regel nicht überschritten werden.
Madopar 125 mg, Madopar 125 mg T und Madopar LT
Bei bisher unbehandelten Kranken wird mit einer Tagesdosis von 1 bis 2 Hartkapseln Madopar 125 mg oder mit 1 bis 2 Tabletten Madopar 125 mg T bzw. Madopar LT (100 mg bis 200 mg Levodopa in Kombination mit 28,5 mg bis 57 mg Benserazidhydrochlorid) begonnen.
Eine Dosissteigerung kann um ½ Tablette Madopar 125 mg T bzw. Madopar LT (50 mg Levodopa und 14,25 mg Benserazidhydrochlorid) oder um 1 Hartkapsel Madopar 125 mg bzw. 1 Tablette Madopar 125 mg T bzw. Madopar LT (100 mg Levodopa und 28,5 mg Benserazidhydrochlorid) jeden 3. bis 7. Tag vorgenommen werden.
Tagesdosen von 8 Hartkapseln Madopar 125 mg oder 8 Tabletten Madopar 125 mg T bzw. Madopar LT (800 mg Levodopa und 228 mg Benserazidhydrochlorid) sollen in der Regel nicht überschritten werden.
Die Standardform von Madopar kann durch Madopar LT ersetzt werden, wenn ein schnellerer Wirkungseintritt erwünscht ist.
Madopar 250 mg
Bei bisher unbehandelten Kranken wird mit einer Tagesdosis von ½ bis 1 Tablette Madopar 250 mg (100 mg bis 200 mg Levodopa in Kombination mit 28,5 mg bis 57 mg Benserazidhydrochlorid) begonnen.
Eine Dosissteigerung kann um ¼ bis ½ Tablette Madopar 250 mg (50 mg bis 100 mg Levodopa und 14,25 mg bis 28,5 mg Benserazidhydrochlorid) jeden 3. bis 7. Tag vorgenommen werden.
Tagesdosen von 4 Tabletten Madopar 250 mg (800 mg Levodopa und 228 mg Benserazidhydrochlorid) sollen in der Regel nicht überschritten werden.
Anfangs wird die Tagesdosis auf 1 bis 4 Einzelgaben verteilt. Später soll die Tagesdosis in wenigstens 4 Einzeldosen genommen werden.
Bei Auftreten von Nebenwirkungen (siehe Abschnitt 4.8) wird die Dosissteigerung zunächst unterbrochen oder die Dosis vorübergehend gesenkt und die weitere Erhöhung langsamer vorgenommen. Bei gastrointestinalen Beschwerden können Antiemetika, wie z. B. Domperidon, verabreicht werden.
Bei der Umstellung von einem reinen Levodopa-Präparat ist zu berücksichtigen, dass zur Erreichung vergleichbarer klinischer Effekte mit der Kombination Levodopa und Benserazid nur etwa 20 % der bisherigen Levodopa-Dosis benötigt werden. Ein medikationsfreies Intervall von 12 Stunden ist einzuhalten.
Spezielle Dosierungsanweisungen
Nierenfunktionsstörung
Bei Patienten mit leichten bis mäßigen Nierenfunktionsstörungen (Creatinin-Clearance ≥ 30 ml/min) ist keine Dosisanpassung erforderlich (siehe Abschnitt 4.3).
Bei älteren Patienten muss die Behandlung langsam und einschleichend erfolgen.
Parkinson-Patienten, die bereits mit einem anderen Antiparkinson-Präparat behandelt werden, können zusätzlich Madopar einnehmen. Sobald jedoch der Wirkungseintritt von Madopar ersichtlich ist, sollte die Dosierung der anderen Medikamente überprüft und gegebenenfalls langsam reduziert und dann abgesetzt werden.
Madopar LT, Tabletten zur Herstellung einer Suspension zum Einnehmen, ist eine spezielle Darreichungsform für Patienten, bei denen ein schnellerer Wirkungseintritt gewünscht wird oder für Patienten mit einer Akinesie, die frühmorgens oder nachmittags auftritt, für Patienten mit einem verzögerten „ON”‑ oder „Wearing OFF”‑Phänomen oder für Patienten mit Schluckbeschwerden.
Patienten, die unter schweren Fluktuationsschwankungen während des Tages leiden („ON‑OFF”-Phänomene), sollten öfters geringere Einzelgaben erhalten oder auf Madopar® Depot umgestellt werden.
Art der Anwendung
Wenn möglich, sollte Madopar mindestens 30 Minuten vor oder 1 Stunde nach einer Mahlzeit eingenommen werden, sodass der kompetitive Effekt von Proteinen aus der Nahrung auf die Aufnahme von Levodopa vermieden und ein schnellerer Wirkungseintritt ermöglicht wird (siehe Abschnitt 4.5). Unerwünschte gastrointestinale Wirkungen, die hauptsächlich in einem frühen Stadium der Behandlung auftreten, können durch Einnahme von Madopar mit etwas proteinarmer Nahrung (z. B. Gebäck, Zwieback oder Ähnliches), Flüssigkeit oder durch langsame Dosissteigerung weitgehend beherrscht werden.
Madopar Hartkapseln sollen nur als Ganzes geschluckt werden und dürfen nicht gekaut werden.
Madopar Tabletten dürfen geteilt werden, um den Patienten das Schlucken oder die Feindosierung zu erleichtern.
Madopar LT kann auch nach Suspendierung in Wasser eingenommen werden. Dazu lässt man die Tabletten in einem Glas Wasser zerfallen. Es bildet sich eine trinkbare Suspension, die sofort eingenommen werden soll.
Madopar wird in der Regel über einen längeren Zeitraum eingenommen (Substitutionstherapie). Die Anwendung ist bei guter Verträglichkeit nicht begrenzt.
Überempfindlichkeit gegen die Wirkstoffe oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile,
Patienten unter 25 Jahren (die skelettale Entwicklung muss abgeschlossen sein),
schwere endokrine Funktionsstörungen, wie z. B. Schilddrüsenüberfunktion, Cushing-Syndrom und Phäochromozytom,
schwere Stoffwechsel‑, Leber‑, Nieren‑ und Knochenmarkserkrankungen,
schwere Herzerkrankungen, wie z. B. schwere Tachykardien, schwere Herzrhythmusstörungen und Herzversagen,
endogene und exogene Psychosen,
Behandlung mit Reserpin,
Behandlung mit nicht selektiven MAO-Hemmern oder einer Kombination von MAO-A- und MAO-B-Hemmern wegen des Risikos des Auftretens von hypertensiven Krisen (siehe Abschnitt 4.5),
Engwinkelglaukom.
Madopar darf von Schwangeren oder Frauen im gebärfähigen Alter ohne gesicherten Empfängnisschutz nicht eingenommen werden (siehe Abschnitt 4.6). Wenn es bei einer Frau, die mit Madopar behandelt wird, zu einer Schwangerschaft kommt, muss das Arzneimittel nach Anweisung des verschreibenden Arztes abgesetzt werden.
Überempfindlichkeitsreaktionen können bei hierfür empfindlichen Individuen auftreten.
Veränderungen des Blutbildes (hämolytische Anämie, Leukopenie und Thrombozytopenie) wurden berichtet (siehe Abschnitt 4.8). Einzelfälle von Agranulozytose und Panzytopenie wurden von Patienten mit Levodopa/Benserazid-Behandlung berichtet; ein Zusammenhang mit der Madopar Behandlung konnte weder belegt noch vollständig ausgeschlossen werden. Deshalb sollte das Blutbild der Patienten in der Einstellungsphase häufig und während der Dauer der Behandlung regelmäßig kontrolliert werden.
Bei Patienten mit Herzinfarktanamnese, bestehenden Herzrhythmusstörungen, koronaren Durchblutungsstörungen oder Herzversagen ist Vorsicht geboten. Kreislauf- und EKG-Kontrollen sollen deshalb in der Einstellungsphase häufig und während der Dauer der Behandlung regelmäßig vorgenommen werden.
Patienten mit Magen-Darm-Ulcera in der Vorgeschichte sowie Osteomalazie sollten ärztlich besonders beobachtet werden.
Bei Patienten mit Weitwinkelglaukom sind regelmäßige Kontrollen des intraokulären Druckes angezeigt, da Levodopa theoretisch das Potenzial besitzt, den Augeninnendruck zu erhöhen.
Bei Patienten mit Risikofaktoren (z. B. ältere Patienten, gleichzeitige Einnahme von Blutdrucksenkern oder anderen Medikamenten mit orthostatischem Potenzial) können gelegentlich hypotone orthostatische Kreislaufregulationsstörungen auftreten (siehe Abschnitt 4.8). Diese Patienten sollten, ebenso wie Patienten mit hypotonen orthostatischen Kreislaufregulationsstörungen, besonders zu Beginn der Behandlung oder bei Dosissteigerungen sorgfältig überwacht werden. Hypothone Kreislaufstörungen können aber in der Regel durch Dosisreduktion von Madopar beherrscht werden.
Gastrointestinale Nebenwirkungen wie Übelkeit, Erbrechen und Diarrhö (siehe Abschnitt 4.8), die vor allem bei Behandlungsbeginn auftreten, können weitgehend durch Einnahme von Madopar mit etwas proteinarmer Nahrung (z. B. Gebäck, Zwieback oder Ähnliches), Flüssigkeit oder durch langsamere Dosissteigerung beherrscht werden.
Unter der Behandlung mit Madopar können Depressionen auftreten (siehe Abschnitt 4.8). Diese können jedoch bei Patienten mit Parkinson-Krankheit auch Teil des klinischen Krankheitsbildes sein. Alle Patienten sollten deshalb sorgfältig auf psychische Veränderungen und Depressionen mit und ohne Suizidgedanken überwacht werden.
Dopaminerges Dysregulations-Syndrom (DDS): Eine kleine Gruppe von Patienten leidet unter kognitiven und Verhaltensstörungen, die direkt der Einnahme zunehmend hoher Dosen des Arzneimittels, entgegen dem medizinischen Rat, zugeordnet werden können.
Eine Behandlung mit Madopar darf nicht plötzlich beendet werden. Nach langjähriger Behandlung mit Präparaten, die Levodopa enthalten, kann ein plötzliches Absetzen zu einem malignen Levodopa-Entzugssyndrom mit Hyperpyrexie, Muskelrigidität, gegebenenfalls psychischen Auffälligkeiten und einem Anstieg der Serumkreatin-Phosphokinase führen. In schweren Fällen kann es auch zu Myoglobinurie, Rhabdomyolyse und akutem Nierenversagen oder einer akinetischen Krise kommen. Diese Zustände sind lebensbedrohlich. Falls diese Symptome auftreten, muss der Patient überwacht und erforderlichenfalls stationär aufgenommen werden. Es muss umgehend eine geeignete symptomatische Behandlung eingeleitet werden, einschließlich einer möglichen Wiederaufnahme der Therapie mit Madopar nach angemessener Prüfung. Aus therapeutischen Gründen indizierte Levodopa-Pausen dürfen daher nur in der Klinik durchgeführt werden.
Dyskinesien (z. B. choreiform oder athetotisch; siehe Abschnitt 4.8) im fortgeschrittenen Stadium der Behandlung können in der Regel durch Dosisreduktion beherrscht werden.
Fluktuationen im therapeutischen Ansprechen („Freezing”-, „End‑of‑Dose”- und „ON‑OFF”-Phänomene; siehe Abschnitt 4.8) können nach Langzeitbehandlung auftreten und werden gewöhnlich durch Dosisanpassung und durch häufigere Gabe kleiner Dosen vermindert oder tolerabel. Ein Versuch, die Dosis von Levodopa zur Verbesserung der therapeutischen Wirkung wieder anzuheben, kann dann stufenweise unternommen werden (siehe Abschnitt 4.2).
Im Falle einer Allgemeinanästhesie soll die Behandlung mit Madopar so weit wie möglich bis zum Zeitpunkt der Operation fortgesetzt werden, außer wenn Halothan gegeben wird. Falls eine Allgemeinanästhesie mit Halothan benötigt wird, muss Madopar 12 bis 48 Stunden vor der Operation abgesetzt werden, da es bei der gleichzeitigen Verabreichung von Madopar und Halothan zu Blutdruckschwankungen und/oder zu Arrhythmien kommen kann. Nach der Operation kann die Therapie mit Madopar wieder, mit langsam ansteigender Dosierung bis auf die Ausgangswerte vor der Operation, aufgenommen werden.
Levodopa wurde mit Somnolenz und plötzlich auftretenden Schlafattacken in Verbindung gebracht. In sehr seltenen Fällen wurde über plötzlich auftretende Schlafattacken während der Aktivitäten des täglichen Lebens berichtet, welche in manchen Fällen unbewusst oder völlig unerwartet auftraten. Patienten müssen darüber informiert und darauf hingewiesen werden, während einer Behandlung mit Levodopa im Straßenverkehr oder beim Bedienen von Maschinen vorsichtig zu sein. Patienten, bei denen Somnolenz und/oder plötzlich auftretende Schlafattacken aufgetreten sind, dürfen kein Fahrzeug führen und keine Maschinen bedienen. Darüber hinaus sollte eine Dosisreduktion oder eine Beendigung der Therapie erwogen werden (siehe Abschnitt 4.7).
Impulskontrollstörungen
Die Patienten sollten regelmäßig hinsichtlich der Entwicklung von Impulskontrollstörungen überwacht werden. Patienten und Betreuer sollten darauf aufmerksam gemacht werden, dass bei Patienten, die mit Dopaminagonisten und/oder anderen dopaminergen, Levodopa-haltigen Arzneimitteln, einschließlich Madopar, behandelt werden, Verhaltensauffälligkeiten im Sinne von Impulskontrollstörungen auftreten können. Hierunter fallen pathologische Spielsucht, Libidosteigerung, Hypersexualität, zwanghaftes Geldausgeben oder Einkaufen, Essattacken und Esszwang. Die Überprüfung der Behandlung wird empfohlen, wenn solche Symptome auftreten.
Laboruntersuchungen
Während der Behandlung mit Madopar sollten regelmäßige Kontrollen des Blutbildes sowie der Leber-, Nieren- und Herzfunktion durchgeführt werden. Bei Diabetikern sollen die Blutzuckerwerte öfter überprüft und die Dosierung der antidiabetischen Therapie an die Blutzuckerwerte angepasst werden.
Malignes Melanom
Epidemiologische Untersuchungen haben gezeigt, dass Parkinson-Patienten im Vergleich zur Allgemeinbevölkerung ein ca. 2- bis 6‑fach erhöhtes Risiko haben, Melanome zu entwickeln. Es ist nicht bekannt, ob das erhöhte Risiko der Krankheit selbst oder anderen Faktoren, wie z. B. der Behandlung mit Levodopa, zuzuschreiben ist. Deshalb sollten Patienten und medizinisches Fachpersonal bei einer Madopar Behandlung die Haut regelmäßig auf verdächtige Veränderungen hin untersuchen, die auf ein Melanom hinweisen können. Die regelmäßigen Hautuntersuchungen sollten durch geeignete Fachkräfte (z. B. Dermatologen) erfolgen.
Natrium (Madopar 125mg T und Madopar 250 mg Tabletten)
Diese Arzneimittel enthält weniger als 1 mmol (23 mg) Natrium pro Tablette, d. h. es ist nahezu „natriumfrei“.
Pharmakokinetische Wechselwirkungen
Die gleichzeitige Anwendung des anticholinergen Arzneimittels Trihexyphenidyl mit einer Standard-Levodopa-Benserazid-Darreichungsform reduziert die Geschwindigkeit, nicht aber den Umfang der Levodopa-Resorption. Die gleichzeitige Anwendung von Trihexyphenidyl und der retardierten Levodopa-Benserazid-Darreichungsformen beeinflusst die Pharmakokinetik von Levodopa nicht.
Eisensulfat erniedrigt die maximale Plasmakonzentration und die AUC von Levodopa um 30 % ‑ 50 %. Die pharmakokinetischen Veränderungen, die während einer gleichzeitigen Behandlung mit Eisensulfat beobachtet wurden, scheinen bei einigen, aber nicht bei allen Patienten, klinisch signifikant zu sein.
Metoclopramid erhöht die Geschwindigkeit der Levodopa-Resorption.
Domperidon kann als Ergebnis einer erhöhten Resorption von Levodopa im Darm die Bioverfügbarkeit von Levodopa erhöhen. Möglicherweise besteht durch gleichzeitige Einnahme von Levodopa und Domperidon ein erhöhtes Risiko kardialer Arrhythmien.
Pharmakodynamische Wechselwirkungen
Arzneimittel mit Wirkung auf das extrapyramidalmotorische System:
Die Wirkung von Madopar wird eingeschränkt durch Opioide, reserpinhaltige Antihypertensiva und Neuroleptika.
Antipsychotika
Die gleichzeitige Anwendung von Antipsychotika mit dopaminrezeptorblockierenden Eigenschaften, insbesondere D2-Rezeptorantagonisten, kann die Wirkung von Madopar hemmen und sollte deshalb mit Vorsicht erfolgen. Die Patienten sollten hinsichtlich eines möglichen Verlustes der Wirkung und einer Verschlechterung der Parkinson-Symptomatik sorgfältig überwacht werden.
MAO-Hemmstoffe
Madopar darf nicht gleichzeitig mit einem irreversiblen, nicht selektiven Monoaminoxidase(MAO)-Hemmer verabreicht werden. Die Gabe eines reinen MAO‑B-Hemmers (z. B. Selegilin, bis zu 10 mg täglich, oder Rasagilin) oder eines selektiven MAO‑A-Hemmers (z. B. Moclobemid) ist nicht kontraindiziert. Selegilin kann unter Umständen die Antiparkinson-Wirkung von Levodopa verstärken, ohne gefährliche Interaktionen auszulösen.
Die gleichzeitige Gabe von MAO‑A- und MAO‑B-Hemmern entspricht in der Wirkung einer nicht selektiven MAO-Hemmung. Aus diesem Grund darf diese Kombination nicht gleichzeitig mit Madopar verabreicht werden (siehe Abschnitt 4.3).
Bei gleichzeitiger Gabe eines nicht selektiven, irreversiblen MAO-Hemmers (z. B. Tranylcypromin) kann es – unter Umständen bis zu 2 Wochen nach Absetzen des MAO-Hemmstoffes – zu hypertensiven Krisen kommen. Zwischen dem Absetzen einer Therapie mit einem nicht selektiven MAO-Hemmer und dem Beginn einer Behandlung mit Madopar muss deshalb ein behandlungsfreies Intervall von mindestens 2 Wochen liegen.
Sympathomimetika
Die gleichzeitige Einnahme von Madopar und Sympathomimetika, wie Epinephrin, Norepinephrin, Isoproterenol oder Amphetamin, kann deren Wirkung verstärken und wird deshalb nicht empfohlen. Sollte eine gleichzeitige Anwendung notwendig sein, ist eine engmaschige Überwachung des kardiovaskulären Systems unverzichtbar und die Dosierung des Sympathomimetikums muss gegebenenfalls reduziert werden.
Andere Antiparkinsonmittel
Es ist möglich, Madopar mit anderen Antiparkinsonmitteln (z. B. Dopaminagonisten, Amantadin, Anticholinergika, Selegilin, Bromocriptin) zu kombinieren. Dabei können jedoch sowohl die erwünschten als auch die unerwünschten Wirkungen der Behandlung verstärkt und eine Dosisverminderung von Madopar oder der anderen Substanzen kann notwendig werden. Wenn eine adjuvante Therapie mit einem COMT-Hemmer begonnen wird, kann eine Reduzierung der Dosis von Madopar notwendig werden. Bei Ergänzung einer Therapie um den Bestandteil Madopar sollte die vorbestehende Behandlung mit Anticholinergika nicht abrupt beendet werden, da die Levodopa-Wirkung nicht sofort einsetzt.
Antihypertensiva
Symptomatische orthostatische Blutdruckabfälle wurden beobachtet, wenn Levodopa in Kombination mit einem Decarboxylasehemmer bei Patienten angewendet wurde, die bereits Antihypertensiva erhielten. Da es zu einer verstärkten Wirkung von Antihypertensiva kommen kann, muss der Blutdruck regelmäßig kontrolliert werden und es müssen, soweit erforderlich, Dosisanpassungen vorgenommen werden.
Proteinreiche Mahlzeiten
Die gleichzeitige Einnahme einer proteinreichen Mahlzeit kann zu einer Wirkungsverminderung von Madopar führen, da Levodopa eine große neutrale Aminosäure (large neutral amino acid, LNAA) ist und mit großen neutralen Aminosäuren (LNAAs) aus Nahrungsproteinen um den Transport über die Magenschleimhaut und die Blut-Hirn-Schranke konkurriert.
Veränderungen von labordiagnostischen Messungen:
Es können verschiedene labordiagnostische Messungen gestört sein:
Levodopa kann die labordiagnostischen Messergebnisse von Katecholaminen, Creatinin, Harnsäure und Glucose (bei Glucosurie) beeinflussen;
falsch‑positiver Ketonnachweis bei Verwendung von Teststreifen (durch Kochen der Urinprobe wird diese Reaktion nicht verändert);
falsch‑negativer Harnzuckernachweis bei Verwendung der Glucose‑Oxidase‑Methode;
falsch‑positiver Coombs‑Test.
Hinweis
Allgemeinanästhesie mit Halothan
Falls eine Allgemeinanästhesie mit Halothan benötigt wird, muss Madopar 12 bis 48 Stunden vor der Operation abgesetzt werden, da es zu Blutdruckschwankungen und/oder zu Arrhythmien kommen kann.
Zur Allgemeinanästhesie mit anderen Narkotika siehe Abschnitt 4.4.
Fertilität
Es wurden keine Fertilitätsstudien durchgeführt.
Schwangerschaft
Vor Beginn der Behandlung wird ein Schwangerschaftstest empfohlen, um eine Schwangerschaft auszuschließen. Madopar darf in der Schwangerschaft nicht angewendet werden (siehe Abschnitt 4.3), da keine Erfahrungen beim Menschen vorliegen und in Tierversuchen für beide Wirkstoffe Reproduktionstoxizität beschrieben wurde (siehe Abschnitt 5.3). Frauen im gebärfähigen Alter müssen während der Behandlung mit Madopar geeignete Maßnahmen zur Empfängnisverhütung ergreifen. Bei Eintreten einer Schwangerschaft muss Madopar unter schrittweiser Dosisreduktion abgesetzt werden.
Stillzeit
Levodopa hemmt die Prolaktinausschüttung und somit die Laktation. Da nicht bekannt ist, ob Benserazid in die Muttermilch übergeht, und da bei heranwachsenden Tieren nach Gabe von Benserazid degenerative Skelettveränderungen beobachtet wurden, dürfen Frauen während der Behandlung mit Madopar nicht stillen. Ist eine Behandlung mit Madopar während der Stillzeit erforderlich, muss abgestillt werden.
Madopar kann einen großen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen haben.
Wenn es bei Patienten unter der Einnahme von Madopar zu Somnolenz und/oder plötzlich auftretenden Schlafattacken kommt, müssen sie darüber informiert werden, dass sie kein Fahrzeug führen oder Tätigkeiten ausüben dürfen, bei denen eine Beeinträchtigung der Aufmerksamkeit das Risiko schwerwiegender Verletzungen oder des Todes für sich selbst oder andere nach sich ziehen kann, bis Somnolenz und Schlafattacken nicht mehr auftreten (siehe Abschnitt 4.4).
Bei der Einnahme von Madopar kann es zu den nachstehenden Nebenwirkungen kommen, deren Häufigkeit nicht bekannt ist, d. h. auf Grundlage der verfügbaren Daten nicht abgeschätzt werden kann.
Der Bewertung von Nebenwirkungen werden folgende Häufigkeiten zugrunde gelegt:
Sehr häufig (≥ 1/10)
Häufig (≥ 1/100, < 1/10)
Gelegentlich (≥ 1/1 000, < 1/100)
Selten (≥ 1/10 000, < 1/1 000)
Sehr selten (< 1/10 000)
Nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar).
Infektionen und parasitäre Erkrankungen: | |
Nicht bekannt |
Fieberhafte Infektionen, Bronchitis, Schnupfen |
Erkrankungen des Blutes und des Lymphsystems: | |
Nicht bekannt |
Hämolytische Anämie, Thrombozytopenie, Leukopenie |
Stoffwechsel- und Ernährungsstörungen: | |
Nicht bekannt |
Anorexie |
Psychiatrische Erkrankungen: | |
Nicht bekannt |
Dopaminerges Dysregulations-Syndrom (DDS), Verwirrtheit, Depressionen, innere Unruhe*, Ängstlichkeit*, Schlafstörungen*, Halluzinationen*, Wahnvorstellungen*, zeitliche Desorientierung*, pathologische Spielsucht, Libidosteigerung, Hypersexualität, zwanghaftes Geldausgeben oder Einkaufen, Essattacken, Esszwang |
Erkrankungen des Nervensystems: | |
Nicht bekannt |
Geschmacksverlust, Änderungen des Geschmacksempfindens, Dyskinesie (choreiform und athetotisch), Fluktuationen im therapeutischen Ansprechen („Freezing”-, „End-of-Dose”- und „ON-OFF”-Phänomene), Müdigkeit, übermäßige Tagesmüdigkeit, plötzlich auftretende Schlafattacken, Schwindel, Kopfschmerzen, Mundtrockenheit |
Herzerkrankungen: | |
Nicht bekannt |
Arrhythmie |
Gefäßerkrankungen: | |
Nicht bekannt |
Orthostatische Hypotonie |
Erkrankungen des Gastrointestinaltrakts: | |
Nicht bekannt |
Übelkeit, Erbrechen, Diarrhö, Verfärbungen von Speichel, Zunge, Zähnen und Mundschleimhaut |
Leber- und Gallenerkrankungen: | |
Nicht bekannt |
Erhöhte Lebertransaminasen, alkalische Phosphatase und γ-Glutamyltransferase |
Erkrankungen der Haut und des Unterhautgewebes: | |
Nicht bekannt |
Allergische Hautreaktionen (z. B. Pruritus, Rash) |
Erkrankungen der Nieren und Harnwege: | |
Nicht bekannt |
Erhöhte Harnstoff-Stickstoff-Werte (BUN), Chromaturie |
* Diese Nebenwirkungen können insbesondere bei älteren Patienten oder bei Patienten mit entsprechender Anamnese auftreten.
Impulskontrollstörungen
Pathologische Spielsucht, Libidosteigerung, Hypersexualität, zwanghaftes Geldausgeben oder Einkaufen, Essattacken und Esszwang können bei Patienten auftreten, die mit Dopaminagonisten oder anderen dopaminergen, Levodopa-haltigen Arzneimitteln, einschließlich Madopar, behandelt werden (siehe Abschnitt 4.4).
Erkrankungen des Nervensystems
Im fortgeschrittenen Stadium der Behandlung mit Madopar können Dyskinesien auftreten (z. B. choreiform oder athetotisch) (siehe Abschnitt 4.4). Diese können normalerweise durch Dosisreduktion verhindert oder erträglich gemacht werden.
Nach Langzeitbehandlung können auch Fluktuationen im therapeutischen Ansprechen auftreten („Freezing”-, „End‑of‑Dose”- und „ON‑OFF”-Phänomene) (siehe Abschnitt 4.4). Auch diese Ereignisse können normalerweise durch Dosisanpassung oder häufigere Gabe kleinerer Dosen verhindert oder erträglich gemacht werden. Ein Versuch, die Dosis von Levodopa zur Verbesserung der therapeutischen Wirkung wieder anzuheben, kann dann stufenweise unternommen werden.
Madopar wurde mit Müdigkeit, sehr selten mit übermäßiger Tagesmüdigkeit und plötzlich auftretenden Schlafattacken in Verbindung gebracht (siehe Abschnitt 4.4).
Gefäßerkrankungen
Orthostatische Ereignisse verbessern sich üblicherweise nach Dosisreduktion.
Erkrankungen des Gastrointestinaltrakts
Unerwünschte gastrointestinale Wirkungen, die meist zu Behandlungsbeginn auftreten, können in der Regel durch die Einnahme von Madopar zusammen mit etwas proteinarmer Nahrung (z. B. Gebäck, Zwieback oder Ähnliches), Flüssigkeit oder durch langsame Dosissteigerung kontrolliert werden.
Untersuchungen
Harnverfärbungen (meist eine leichte Rotfärbung, die sich bei längerem Stehenlassen dunkel färbt). Andere Körperflüssigkeiten und Gewebe, einschließlich Speichel, Zunge, Zähne oder Mundschleimhaut können auch von einer Farbänderung betroffen oder gefärbt sein.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem
Bundesinstitut für Arzneimittel und Medizinprodukte
Abt. Pharmakovigilanz
Kurt-Georg-Kiesinger-Allee 3
53175 Bonn
Website: www.bfarm.de
anzuzeigen.
Symptome einer Überdosierung
Die Symptome und Anzeichen einer Überdosierung entsprechen qualitativ den Nebenwirkungen von Madopar in therapeutischer Dosierung, sie können jedoch stärker ausgeprägt sein. Eine Überdosierung kann somit zu kardiovaskulären Nebenwirkungen (z. B. kardialen Arrhythmien), psychiatrischen Störungen (z. B. Verwirrtheit und Schlaflosigkeit), gastrointestinalen Nebenwirkungen (z. B. Übelkeit und Erbrechen) und unwillkürlichen Bewegungen führen (siehe Abschnitt 4.8).
Wenn ein Patient eine Überdosierung einer retardierten Levodopa-Benserazid‑Darreichungsform genommen hat, können das Einsetzen der Symptome und die Anzeichen einer Überdosierung aufgrund der verzögerten Resorption des Wirkstoffs im Magen verspätet auftreten.
Behandlung einer Überdosierung
Die Vitalparameter des Patienten sind zu beobachten und unterstützende Maßnahmen entsprechend dem klinischen Bild des Patienten sind zu ergreifen. Insbesondere können kardiovaskuläre Nebenwirkungen die Anwendung von Antiarrhythmika und zentralnervöse Nebenwirkungen die Gabe von Atemstimulanzien oder Neuroleptika erforderlich machen.
Zusätzlich sollte bei der Anwendung retardierter Darreichungsformen die weitere Resorption des Wirkstoffs durch geeignete Maßnahmen verhindert werden.
Pharmakotherapeutische Gruppe: Levodopa und Decarboxylaseinhibitor, ATC‑Code: N04BA02.
Wirkmechanismus
Levodopa ist eine Aminosäure, die in Kombination mit dem peripheren Decarboxylasehemmer Benserazid der Substitution eines zentralnervösen Dopaminmangels dient.
Klinische Wirksamkeit und Sicherheit
Da wenigstens 95 % des oral verabreichten Levodopa bereits in extrazerebralen Organen (Darm, Leber, Niere, Herz, Magen) decarboxyliert werden, gelangen bei einer Levodopa‑Monotherapie nur geringe Mengen in das Zentralnervensystem. Aufgrund des extrazerebral gebildeten Dopamins und der aus ihm entstehenden adrenergen Substanzen wurden zahlreiche gastrointestinale und kardiovaskuläre Nebenwirkungen der Monotherapie mit Levodopa berichtet.
Der Decarboxylasehemmer Benserazid tritt in der vorliegenden Dosierung nicht in nennenswertem Umfang in das Gehirn über (weniger als 6 % der Plasmakonzentration). Durch die gleichzeitige Gabe von Benserazid wird die Decarboxylierung von Levodopa in der Peripherie, vor allem in der Darmschleimhaut, nahezu vollständig verhindert. Dadurch kann die Dosis Levodopa, die zur Erreichung vergleichbarer klinischer Effekte notwendig ist, auf ca. 20 % der bei der Monotherapie notwendigen Dosis gesenkt werden. Die gastrointestinalen und kardiovaskulären Nebenwirkungen von peripher gebildetem Dopamin werden dadurch weitgehend vermieden.
Der Benserazid‑Anteil in der Kombination führt infolge der Decarboxylasehemmung zu einer Erhöhung der Prolaktinkonzentration.
Resorption
Levodopa wird hauptsächlich im oberen Abschnitt des Dünndarmes resorbiert, unabhängig von der Region. Die maximale Plasmakonzentration (tmax) von Levodopa wird etwa eine Stunde nach der Einnahme einer Standardform von Madopar (Madopar 62,5 mg oder Madopar 125 mg Hartkapseln, oder Madopar 125 mg T oder Madopar 250 mg, Tabletten) erreicht. Die maximale Plasmakonzentration von Levodopa und das Ausmaß der Resorption von Levodopa (AUC) steigt dosisproportional im Bereich von 50 mg ‑ 200 mg Levodopa.
Nahrungsaufnahme reduziert die Geschwindigkeit und das Ausmaß der Resorption von Levodopa. Die maximale Plasmakonzentration von Levodopa ist um 30 % niedriger und wird erst nach der doppelten oder dreifachen Zeit erreicht, wenn Madopar zusammen mit einer Standardmahlzeit eingenommen wird. Das Ausmaß der Resorption des Wirkstoffs wird bei gleichzeitiger Nahrungsaufnahme um 15 % reduziert. Ferner beeinflussen Änderungen in der Entleerungszeit des Magens die Resorption von Levodopa.
Verteilung
Levodopa überwindet die Magenschleimhaut und die Blut-Hirn-Schranke durch einen sättigbaren Transportmechanismus. Es wird nicht an Plasmaproteine gebunden. Sein Verteilungsvolumen beträgt 57 Liter. Die AUC von Levodopa in der Zerebrospinalflüssigkeit beträgt 12 % von derjenigen im Plasma.
Im Gegensatz zu Levodopa überwindet Benserazid in therapeutischen Dosen nicht die Blut-Hirn-Schranke. Die Benserazid- Konzentrationen sind in den Nieren, in der Lunge, im Dünndarm und in der Leber am höchsten. Benserazid passiert die Plazenta.
Biotransformation
Levodopa wird hauptsächlich durch Decarboxylierung, O‑Methylierung, Transaminierung und Oxidation metabolisiert. Die Decarboxylierung von Levodopa zu Dopamin erfolgt durch die aromatische Aminosäure-Decarboxylase, die zusätzlich zur Leber im Verdauungstrakt, den Nieren und dem Herzen reichlich vorhanden ist.
Die Hauptmetaboliten sind Homovanillinsäure und Dihydroxyphenylessigsäure. Die Methoxylierung von Levodopa zu 3‑O‑Methyldopa durch die Catechol‑O‑Methyltransferase (COMT) stellt einen zweiten Metabolisierungsweg dar. Die Eliminationshalbwertszeit von 3‑O‑Methyldopa beträgt 15 Stunden. Daher akkumuliert dieser Metabolit bei Patienten, die therapeutische Dosen von Madopar erhalten.
Gleichzeitige Verabreichung von Levodopa und Benserazid verringert die periphere Decarboxylierung. Dies zeigt sich in erhöhten Plasmaspiegeln von Aminosäuren (Levodopa, 3‑O‑Methyldopa) und niedrigeren Plasmaspiegeln von Katecholaminen (Dopamin, Noradrenalin) und Phenylcarbonsäuren (Homovanillinsäure, Dihydroxyphenylessigsäure).
Benserazid wird in der Darmwand und in der Leber zu Trihydroxybenzylhydrazin hydroxyliert. Dieser Metabolit ist ein wirkungsvoller Inhibitor der aromatischen Aminosäure-Decarboxylase.
Elimination
Bei peripherer Hemmung der Levodopa-Decarboxylase beträgt die Eliminationshalbwertszeit von Levodopa etwa 1,5 Stunden. Bei älteren Parkinson‑Patienten (Alter 65 ‑ 78 Jahre) ist die Eliminationshalbwertszeit um ca. 25 % verlängert. Die Clearance von Levodopa beträgt 430 ml/min.
Benserazid wird fast vollständig in Form von Metaboliten eliminiert. Die Metaboliten werden hauptsächlich über die Niere (64 %) und zu einem geringeren Anteil über die Fäzes (24 %) ausgeschieden.
Pharmakokinetische Zusammenhänge
Die absolute Bioverfügbarkeit von Levodopa bei gleichzeitiger Gabe von Benserazid zur Hemmung der peripheren Decarboxylase beträgt im Mittel 98 % (Bereich: 74 % ‑ 112 %).
Eine im Jahr 1986 durchgeführte Bioverfügbarkeitsuntersuchung (offen, cross‑over) an 23 gesunden männlichen Probanden (18 bis 34 Jahre), bei der nach Einmalgabe von 2 Tabletten Madopar 125 mg T bzw. 2 Hartkapseln Madopar 125 mg als Referenzpräparat (entsprechend jeweils 200 mg Levodopa plus 50 mg Benserazid) die Levodopa-Konzentrationen im Plasma gemessen wurden, führte zu folgenden Ergebnissen:
Tabelle 1:
Testpräparat |
Referenzpräparat |
|
Cmax (μg/ml) |
3,23 ± 1,31 |
3,24 ± 1,12 |
tmax (h) |
0,75 ± 0,35 |
0,82 ± 0,28 |
AUC0-12 (h μg/ml) |
6,05 ± 1,16 |
5,82 ± 1,09 |
Cmax - Maximale Plasmakonzentration
tmax - Zeitpunkt der maximalen Plasmakonzentration
AUC - Fläche unter der Konzentrations-Zeit-Kurve
Angegeben sind jeweils der Mittelwert und die Standardabweichung.
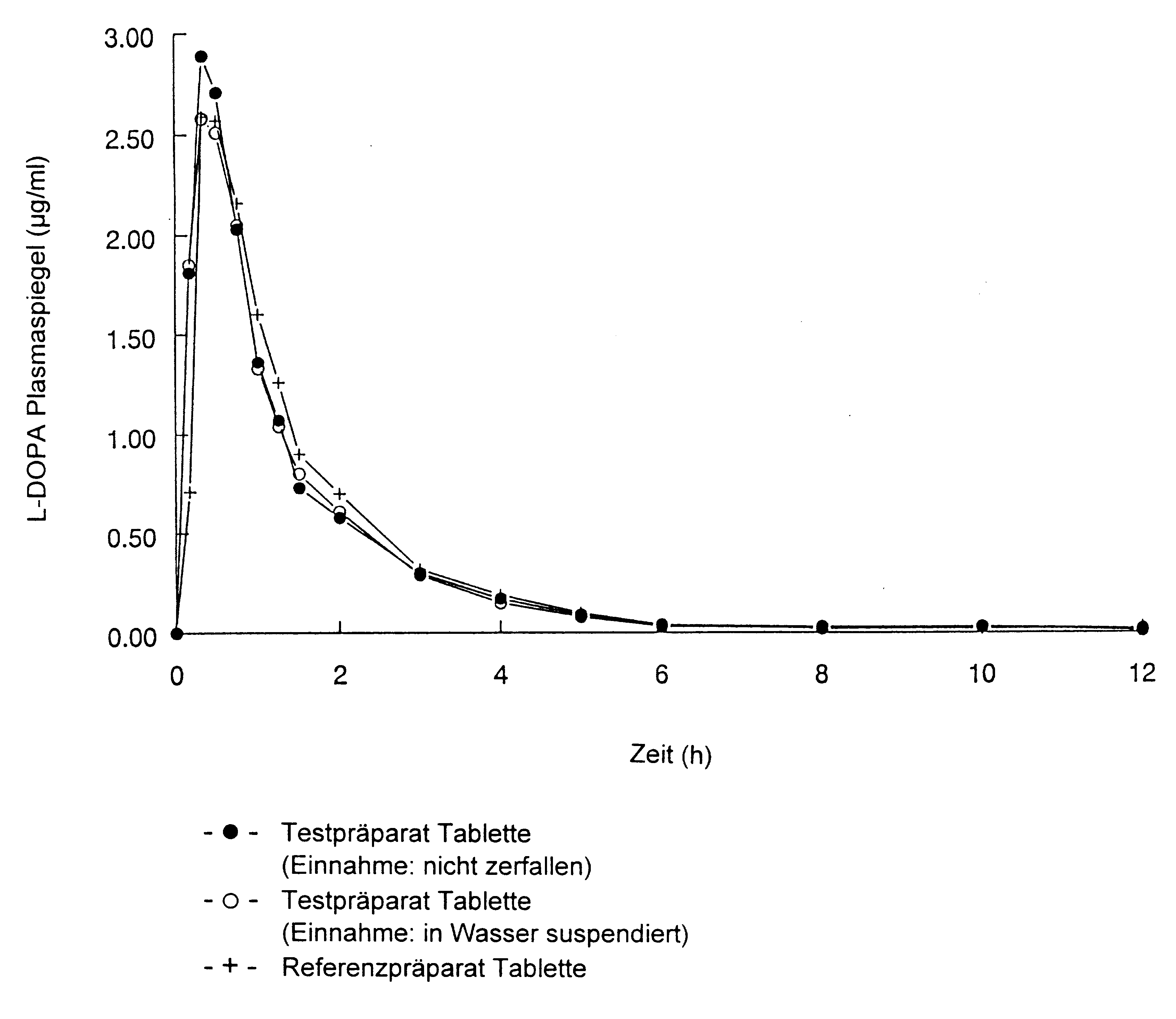
Das pharmakokinetische Profil von Madopar LT, als wässrige Suspension oder feste Tablette eingenommen, ist dem Profil einer vergleichbaren Standardform von Madopar sehr ähnlich, mit Ausnahme einer klinisch erwünschten, kürzeren Zeitdauer bis zum Erreichen maximaler Plasmaspiegel.
Eine im Jahr 1994 durchgeführte vergleichende Bioverfügbarkeitsuntersuchung (offen, cross-over) an 18 männlichen und weiblichen gesunden Probanden (18 bis 30 Jahre) ergab nach einmaliger Gabe von einer in Wasser gelösten Tablette im Vergleich zu einer nicht aufgelösten Tablette und zu einer Standardtablette als Referenzpräparat (entsprechend jeweils 100 mg Levodopa plus 25 mg Benserazid) folgende Werte:
Tabelle 2:
Testpräparat |
Testpräparat |
Referenz |
|
Cmax (µg/ml) |
3,11 ± 1,02 |
3,36 ± 1,14 |
3,50 ± 1,39 |
tmax (h) |
0,43 ± 0,18 |
0,42 ± 0,22 |
0,66 ± 0,43 |
AUC0‑12 (h µg/ml) |
3,76 ± 0,96 |
3,87 ± 1,06 |
3,92 ± 1,09 |
Angabe der Werte als Mittelwerte und Streubreite (Standardabweichung).
Siehe Abbildung
Abb. 1: Mittlere Plasmaspiegelverläufe im Vergleich zu einem Referenzpräparat in einem Konzentrations-Zeit-Diagramm.
Chronische Toxizität
In Studien zur chronischen Toxizität an Ratten verursachte die orale Gabe von Levodopa plus Benserazid dosisabhängig ausgeprägte Skelettveränderungen, die ihren Ausgangspunkt von den noch nicht geschlossenen Epiphysenfugen nahmen. Knochenveränderungen traten nur im wachsenden Organismus auf und wurden durch Benserazid verursacht. Bei Hunden wurden dosisabhängig ein Anstieg der Leberenzyme sowie eine Leberverfettung, eine Verlängerung der Thromboplastinzeit sowie eine Verminderung des blutbildenden Gewebes im Knochenmark nach hohen Dosen beobachtet.
Genotoxizität
Im Ames-Test konnte für Madopar bzw. seine wirksamen Bestandteile Levodopa und Benserazid keine mutagene Wirkung beobachtet werden. Weitere Befunde liegen nicht vor.
Karzinogenes Potenzial
Studien zur Karzinogenität liegen nicht vor.
Reproduktionstoxizität
Mit Levodopa/Benserazid wurden keine Fertilitätsstudien durchgeführt.
Studien zur Reproduktionstoxizität von Levodopa/Benserazid zeigten bei Mäusen (400 mg/kg), Ratten (600 mg/kg; 250 mg/kg) und Kaninchen (120 mg/kg; 150 mg/kg) keine teratogene Wirkung oder Beeinflussung der Skelettentwicklung.
Dosierungen im maternaltoxischen Bereich verursachten bei Kaninchen eine Erhöhung der Embryoletalität und bei Ratten eine Gewichtsabnahme beim Fötus.
Madopar 62,5 mg, Hartkapseln
Mikrokristalline Cellulose
Mannitol (Ph.Eur.)
Talkum
Povidon K 90
Magnesiumstearat (Ph.Eur.)
Kapselhülle
Gelatine
Titandioxid (E171)
Eisen(II,III)-oxid (E172)
Indigocarmin (E132)
Drucktinte
Eisen(II,III)-oxid (E172)
Schellack
Propylenglycol
Kaliumhydroxid
Madopar 125 mg, Hartkapseln
Mikrokristalline Cellulose
Talkum
Povidon K 90
Magnesiumstearat (Ph.Eur.)
Kapselhülle
Gelatine
Titandioxid (E171)
Eisen(III)-oxid (E172)
Indigocarmin (E132)
Drucktinte
Eisen(II,III)-oxid (E172)
Schellack
Propylenglycol
Kaliumhydroxid
Madopar 125 mg T, Tabletten
Mikrokristalline Cellulose
Mannitol (Ph.Eur.)
Calciumhydrogenphosphat
Vorverkleisterte Stärke (Mais)
Crospovidon
Ethylcellulose
Hochdisperses Siliciumdioxid
Docusat‑Natrium
Magnesiumstearat (Ph.Eur.)
Eisen(III)-oxid (E172)
Madopar 250 mg, Tabletten
Mikrokristalline Cellulose
Mannitol (Ph.Eur.)
Calciumhydrogenphosphat
Vorverkleisterte Stärke (Mais)
Crospovidon
Ethylcellulose
Hochdisperses Siliciumdioxid
Docusat‑Natrium
Magnesiumstearat (Ph.Eur.)
Eisen(III)-oxid (E172)
Madopar LT, Tabletten zur Herstellung einer Suspension zum Einnehmen
Mikrokristalline Cellulose
Vorverkleisterte Stärke (Mais)
Magnesiumstearat (Ph.Eur.)
Wasserfreie Citronensäure (Ph.Eur.)
Nicht zutreffend.
Madopar 62,5 mg, Hartkapseln: 3 Jahre
Madopar 125 mg, Hartkapseln: 3 Jahre
Madopar 125 mg T, Tabletten: 4 Jahre
Madopar 250 mg, Tabletten: 3 Jahre
Madopar LT, Tabletten zur Herstellung
einer Suspension zum Einnehmen: 3 Jahre
Die trinkfertige Suspension von Madopar LT sollte innerhalb einer halben Stunde nach Auflösen der Tablette eingenommen werden.
Madopar 62,5 mg und Madopar 125 mg, Hartkapseln
Nicht über 30 °C lagern.
Die Flaschen fest verschlossen halten, um den Inhalt vor Feuchtigkeit zu schützen.
Madopar 125 mg T und Madopar 250 mg, Tabletten, sowie Madopar LT, Tabletten zur Herstellung einer Suspension zum Einnehmen
Nicht über 25 °C lagern.
Die Flaschen fest verschlossen halten, um den Inhalt vor Feuchtigkeit zu schützen.
Behältnis
Flaschen aus braunem Glas, Glasart III (Ph.Eur.).
Verschluss
Stopfen aus Polyethylen mit Kammer für Trocknungsmittel (Silicagel).
Packungsgrößen:
Madopar 62,5 mg, Hartkapseln
50 Hartkapseln
100 Hartkapseln
Madopar 125 mg, Hartkapseln
50 Hartkapseln
100 Hartkapseln
Madopar 125 mg T, Tabletten
20 Tabletten
50 Tabletten
100 Tabletten
Klinikpackung zu 100 Tabletten (Bündelpackung zu 5 x 20 Tabletten)
Madopar 250 mg, Tabletten
50 Tabletten
100 Tabletten
Klinikpackung zu 250 Tabletten (Bündelpackung zu 5 x 50 Tabletten) und 1 000 Tabletten (Bündelpackung zu 20 x 50 Tabletten)
Madopar LT, Tabletten zur Herstellung einer Suspension zum Einnehmen
20 Tabletten
50 Tabletten
100 Tabletten
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
Keine besonderen Anforderungen.
Roche Pharma AG
Emil‑Barell‑Straße 1
79639 Grenzach‑Wyhlen
Telefon (07624) 14‑0
Telefax (07624) 10 19
Madopar 62,5 mg: 861.00.00
Madopar 125 mg: 6036937.00.00
Madopar 125 mg T: 6036937.00.01
Madopar 250 mg: 861.00.01
Madopar LT: 32582.01.00
Madopar 62,5 mg:
Datum der Erteilung der Zulassung: 20. Dezember 1979
Datum der letzten Verlängerung der Zulassung: 19. Dezember 2003
Madopar 125 mg und Madopar 125 mg T:
Datum der Erteilung der Zulassung: 30. Januar 2003
Datum der letzten Verlängerung der Zulassung: 19. Dezember 2003
Madopar 250 mg:
Datum der Erteilung der Zulassung: 19. Dezember 1988
Datum der letzten Verlängerung der Zulassung: 19. Dezember 2003
Madopar LT:
Datum der Erteilung der Zulassung: 03. April 1996
Datum der letzten Verlängerung der Zulassung: 19. Dezember 2003
September 2024
Verschreibungspflichtig