CellCept® 1 g/5 ml Pulver zur Herstellung einer Suspension zum Einnehmen
Jede Flasche enthält 35 g Mycophenolatmofetil in 110 g Pulver zur Herstellung einer Suspension zum Einnehmen. 5 ml der Suspension enthalten nach Zubereitung 1 g Mycophenolatmofetil.
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
Pulver zur Herstellung einer Suspension zum Einnehmen
CellCept 1 g/5 ml Pulver zur Herstellung einer Suspension zum Einnehmen ist in Kombination mit Ciclosporin und Corticosteroiden zur Prophylaxe von akuten Transplantatabstoßungsreaktionen bei Erwachsenen sowie Kindern und Jugendlichen (im Alter von 1 bis 18 Jahren) mit allogener Nieren-, Herz- oder Lebertransplantation angezeigt.
Die Behandlung soll von entsprechend qualifizierten Transplantationsspezialisten eingeleitet und fortgeführt werden.
Dosierung
Erwachsene
Nierentransplantation
Eine Behandlung mit 1 g/5 ml Pulver zur Herstellung einer Suspension zum Einnehmen sollte innerhalb von 72 Stunden nach der Transplantation eingeleitet werden. Die empfohlene Dosis für Nierentransplantationspatienten beträgt zweimal täglich 1 g (Tagesdosis: 2 g), d. h. zweimal täglich 5 ml der oralen Suspension.
Herztransplantation
Eine Behandlung sollte innerhalb von 5 Tagen nach der Transplantation eingeleitet werden. Die empfohlene Dosis für Herztransplantationspatienten beträgt zweimal täglich 1,5 g (Tagesdosis: 3 g).
Lebertransplantation
In den ersten 4 Tagen nach einer Lebertransplantation sollte Mycophenolatmofetil intravenös verabreicht werden, wobei mit der oralen Gabe von Mycophenolatmofetil so schnell wie möglich begonnen werden sollte, wenn sie vertragen wird. Bei Lebertransplantationspatienten beträgt die empfohlene orale Dosis zweimal täglich 1,5 g (Tagesdosis: 3 g).
Kinder und Jugendliche (1 bis 18 Jahre)
Die Dosierungsangaben für Kinder und Jugendliche in diesem Abschnitt gelten für alle oralen Formulierungen innerhalb der Mycophenolatmofetil-Produktpalette, soweit zutreffend. Verschiedene orale Formulierungen sollten nicht ohne klinische Überwachung ausgetauscht werden.
Die empfohlene Anfangsdosis Mycophenolatmofetil für Kinder und Jugendliche mit Nieren-, Herz- oder Lebertransplantation beträgt 600 mg/m2 [Körperoberfläche (KOF)] zweimal täglich oral angewendet (anfängliche Tagesgesamtdosis darf 2 g bzw. 10 ml der Suspension zum Einnehmen nicht überschreiten).
Dosis und Darreichungsform sollten auf Basis der klinischen Beurteilung individuell angepasst werden. Wenn die empfohlene Anfangsdosis gut vertragen wird, aber bei pädiatrischen Herz- und Lebertransplantationspatienten keine klinisch angemessenen Immunsuppression erreicht wird, kann die Dosis auf 900 mg/m2 KOF zweimal täglich erhöht werden (maximale tägliche Tagesgesamtdosis: 3 g oder 15 ml der Suspension zum Einnehmen). Die empfohlene Erhaltungsdosis für pädiatrische Nierentransplantationspatienten beträgt weiterhin 600 mg/m2 zweimal täglich (maximale tägliche Gesamtdosis von 2 g oder 10 ml der Suspension zum Einnehmen).
Das Mycophenolatmofetil-Pulver zur Herstellung einer Suspension zum Einnehmen sollte von Patienten angewendet werden, die keine Kapseln und Tabletten schlucken können und/oder eine KOF von weniger als 1,25 m2 haben, da hier eine erhöhte Erstickungsgefahr besteht. Patienten mit einer KOF von 1,25 bis 1,5 m2 können Mycophenolatmofetil-Kapseln in einer Dosis von zweimal täglich 750 mg (Tagesdosis: 1,5 g) verordnet werden. Patienten mit einer KOF von mehr als 1,5 m2 können Mycophenolatmofetil in Form von Kapseln oder Tabletten in einer Dosis von zweimal täglich 1 g verordnet werden (Tagesdosis: 2 g). Da in dieser Altersgruppe im Vergleich zu Erwachsenen einige Nebenwirkungen häufiger auftreten (siehe Abschnitt 4.8), kann eine vorübergehende Herabsetzung der Dosis oder ein Abbruch der Behandlung notwendig sein; hierbei müssen relevante klinische Faktoren wie die Stärke der Reaktion berücksichtigt werden.
In der untenstehenden Tabelle wird für Bereiche der Körperoberfläche die Dosis (mg) in Volumen (ml) umgerechnet, die mit dem oralen Dispenser bestimmt wird.
Tabelle 1: Umrechnung Dosis (mg) in Volumen (ml) der Suspension (1 g/ 5 ml), mit dem oralen Dispenser
600 mg/m2 Dosisspiegel |
900 mg/m2 Dosisspiegel |
||||
Körperober-fläche (m2) des KindesA |
Zu verabreichende Gesamtdosis zweimal täglich |
Körperober-fläche (m2) des KindesA |
Zu verabreichende Gesamtdosis zweimal täglich |
||
mg |
ml |
mg |
ml |
||
0,5 |
300 |
1,5 |
0,5 |
450 |
2,25 |
0,58 |
350 |
1,75 |
0,56 |
500 |
2,5 |
0,67 |
400 |
2,0 |
0,61 |
550 |
2,75 |
0,75 |
450 |
2,25 |
0,67 |
600 |
3,0 |
0,83 |
500 |
2,5 |
0,72 |
650 |
3,25 |
0,92 |
550 |
2,75 |
0,78 |
700 |
3,5 |
1,0 |
600 |
3,0 |
0,89 |
800 |
4,0 |
1,08 |
650 |
3,25 |
1,0 |
900 |
4,5 |
1,17 |
700 |
3,5 |
1,11 |
1000 |
5,0 B |
1,25 |
750 |
3,75 |
1,22 |
1100 |
5,5 B |
1,33 |
800 |
4,0 |
1,33 |
1200 |
6,0 B |
In der Tabelle sind die Dosierungen und Volumina aufgeführt, die theoretisch für die beiden Dosierungsschemata berechnet wurden. Da der orale Dispenser nur Markierungen von 0,25 ml aufweist (was einer Dosiserhöhung um 50 mg entspricht), wurde das Volumen in ml auf die nächstgelegene Markierung aufgerundet.
Abasierend auf der Mosteller-Formel für die Berechnung der Körperoberfläche (KOF):
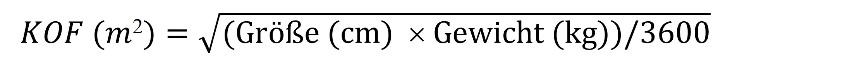
B Für Dosen von mehr als 5 ml sind zwei Entnahmen von jeweils mindestens 1 ml notwendig. Wenn möglich, wechseln Sie bei den Patienten, die schlucken können, zur festen Darreichungsform zum Einnehmen.
Anwendung bei besonderen Patientengruppen
Ältere Menschen
Bei älteren Menschen erweist sich die empfohlene Dosis von zweimal täglich 1 g für nierentransplantierte Patienten und von zweimal täglich 1,5 g für Herz- oder Lebertransplantierte als geeignet.
Niereninsuffizienz
Bei Nierentransplantationspatienten mit schwerer chronischer Niereninsuffizienz (glomeruläre Filtrationsrate < 25 ml/min/1,73 m²) sind außerhalb der unmittelbaren postoperativen Periode Dosen von mehr als 1 g zweimal täglich zu vermeiden. Diese Patienten sollen zudem sorgfältig überwacht werden. Bei Patienten mit verzögertem Funktionseintritt des Nierentransplantats nach der Operation ist keine Anpassung der Dosis erforderlich (siehe Abschnitt 5.2). Zu Herz- oder Lebertransplantationspatienten mit schwerer chronischer Niereninsuffizienz liegen keine Daten vor.
Schwere Leberinsuffizienz
Bei nierentransplantierten Patienten mit schweren Leberparenchymschäden sind Dosisanpassungen nicht erforderlich. Zu herztransplantierten Patienten mit schweren Leberparenchymschäden liegen keine Daten vor.
Behandlung während einer Abstoßungsreaktion
Erwachsene
Mycophenolsäure (MPA) ist der aktive Metabolit von Mycophenolatmofetil. Eine renale Transplantatabstoßung führt nicht zu einer Änderung der Pharmakokinetik von MPA; eine Dosisreduktion oder Unterbrechung der Behandlung ist nicht erforderlich. Es liegt kein Grund für eine Dosisanpassung nach einer Herztransplantatabstoßung vor. Pharmakokinetische Daten bei Lebertransplantatabstoßung liegen nicht vor.
Kinder und Jugendliche
Es liegen keine Daten zur Behandlung einer ersten oder refraktären Abstoßungsreaktion bei pädiatrischen Transplantationspatienten vor.
Art der Anwendung
Zum Einnehmen
Hinweis: Falls erforderlich, kann CellCept 1 g/5 ml Pulver zur Herstellung einer Suspension zum Einnehmen über eine Nasen-Magen-Sonde mit einem Durchmesser von mindestens 8 French (Mindestmaß des inneren Durchmessers 1,7 mm) verabreicht werden.
Vorsichtsmaßnahmen vor/bei der Handhabung bzw. vor/während der Anwendung des Arzneimittels
Da Mycophenolatmofetil bei Ratten und Kaninchen eine teratogene Wirkung gezeigt hat, sollte die Inhalation des trockenen Pulvers oder ein direkter Kontakt mit Haut oder Schleimhäuten vermieden werden, genauso wie direkter Hautkontakt mit der rekonstituierten Suspension. Falls es zu einem solchen Kontakt kommt, gründlich mit Seife und Wasser waschen; Augen mit klarem Wasser spülen.
Hinweise zur Rekonstitution und Verdünnung des Arzneimittels vor der Anwendung, siehe Abschnitt 6.6.
CellCept darf bei Patienten, die überempfindlich gegen Mycophenolatmofetil, Mycophenolsäure oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile sind, nicht angewendet werden. Überempfindlichkeitsreaktionen gegen das Arzneimittel wurden beobachtet (siehe Abschnitt 4.8).
Frauen im gebärfähigen Alter, die keine hochwirksame Verhütungsmethode verwenden, dürfen die Behandlung nicht erhalten (siehe Abschnitt 4.6).
Die Behandlung darf bei Frauen im gebärfähigen Alter ohne Vorlage eines negativen Schwangerschaftstestergebnisses nicht begonnen werden, um eine unbeabsichtigte Anwendung während der Schwangerschaft auszuschließen (siehe Abschnitt 4.6).
Die Behandlung darf in der Schwangerschaft nicht angewendet werden, außer wenn keine geeignete alternative Behandlung zur Verhinderung einer Transplantatabstoßung zur Verfügung steht (siehe Abschnitt 4.6).
Stillende Frauen dürfen die Behandlung nicht erhalten (siehe Abschnitt 4.6).
Neoplasien
Patienten, die unter einer Behandlung mit Immunsuppressiva stehen und hierzu eine Kombination von Arzneimitteln, einschließlich CellCept, erhalten, sind einem erhöhten Risiko von Lymphomen und anderen Malignomen, insbesondere der Haut, ausgesetzt (siehe Abschnitt 4.8). Das Risiko scheint hierbei eher von der Intensität und der Dauer der Immunsuppression als von der Verwendung eines bestimmten Mittels abzuhängen.
Um das Hautkrebsrisiko auf ein Minimum zu reduzieren, wird grundsätzlich geraten, sich nur begrenzt und mit schützender Kleidung dem Sonnen- und UV-Licht auszusetzen und ein Sonnenschutzmittel mit hohem Lichtschutzfaktor zu benutzen.
Infektionen
Patienten, die mit Immunsuppressiva, einschließlich Mycophenolatmofetil, behandelt werden, haben ein erhöhtes Risiko für opportunistische (durch Bakterien, Pilze, Viren und Protozoen verursachte) Infektionen, tödliche Infektionen und Sepsis (siehe Abschnitt 4.8). Derartige Infektionen schließen latente virale Reaktivierung, wie z. B. Hepatitis-B- oder Hepatitis-C-Reaktivierung und durch Polyomaviren hervorgerufene Infektionen (BK-Virus-Nephropathie, JC-Virus verbundene progressive multifokale Leukoenzephalopathie [PML]) ein. Fälle von Hepatitis durch Hepatitis-B- oder Hepatitis-C-Reaktivierung sind bei Virusträgern unter Anwendung von Immunsuppressiva berichtet worden. Diese Infektionen sind häufig mit einer hohen immunsuppressiven Gesamtbelastung verbunden und können zu einer schwerwiegenden oder tödlichen Erkrankung führen, die Ärzte bei immunsupprimierten Patienten mit sich verschlechternder Nierenfunktion oder neurologischen Symptomen differentialdiagnostisch in Betracht ziehen müssen. Mycophenolsäure hat eine zytostatische Wirkung auf B- und T-Lymphozyten, daher kann COVID-19 mit höheren Schweregraden auftreten, und geeignete klinische Maßnahmen sind in Betracht zu ziehen.
Bei Patienten, die Mycophenolatmofetil in Kombination mit anderen Immunsuppressiva erhielten, ist über Hypogammaglobulinämie in Verbindung mit wiederkehrenden Infektionen berichtet worden. In einigen dieser Fälle führte die Umstellung von Mycophenolatmofetil auf ein alternatives Immunsuppressivum zu einer Normalisierung der Serum-IgG-Werte. Bei Patienten mit wiederkehrenden Infektionen, die mit Mycophenolatmofetil behandelt werden, sollten die Serum-Immunglobuline gemessen werden. In Fällen von anhaltender, klinisch relevanter Hypogammaglobulinämie sollten geeignete klinische Maßnahmen, unter Beachtung der starken zytostatischen Wirkung, die Mycophenolsäure auf T- und B-Lymphozyten hat, in Betracht gezogen werden.
Bei Erwachsenen und Kindern, die Mycophenolatmofetil in Kombination mit anderen Immunsuppressiva erhielten, sind Fälle von Bronchiektasie berichtet worden. In einigen dieser Fälle führte die Umstellung von Mycophenolatmofetil auf ein anderes Immunsuppressivum zu einer Verbesserung der Atemwegsbeschwerden. Das Risiko einer Bronchiektasie kann mit einer Hypogammaglobulinämie assoziiert oder eine direkte Auswirkung auf die Lunge sein. In Einzelfällen wurden auch interstitielle Lungenerkrankung und Lungenfibrose berichtet, von denen einige einen tödlichen Ausgang hatten (siehe Abschnitt 4.8). Es wird empfohlen, Patienten, die anhaltende pulmonale Symptome, wie Husten oder Dyspnoe entwickeln, umgehend ärztlich zu untersuchen.
Blut und Immunsystem
Patienten, die mit Mycophenolatmofetil behandelt werden, sind bezüglich des Auftretens einer Neutropenie zu überwachen, die auf die Behandlung selbst, auf die Begleitmedikation, virale Infektionen oder eine Kombination dieser Ursachen zurückzuführen sein kann. Bei Patienten, die mit Mycophenolatmofetil behandelt werden, soll ein komplettes Blutbild während des ersten Monats der Behandlung wöchentlich, während des zweiten und dritten Monats der Behandlung zweimal pro Monat und dann monatlich für die restlichen 9 Monate des ersten Behandlungsjahres erhoben werden. Wenn sich eine Neutropenie entwickelt (absolute Neutrophilen-Zahl < 1,3 • 103/μl), könnte es angebracht sein, die Behandlung mit Mycophenolatmofetil abzubrechen oder zu unterbrechen.
Fälle von Erythroblastopenien (pure red cell aplasia [PRCA]) wurden bei Patienten, die mit Mycophenolatmofetil in Kombination mit anderen Immunsuppressiva behandelt wurden, berichtet. Der Mechanismus einer durch Mycophenolatmofetil induzierten PRCA ist unbekannt. Eine PRCA kann nach einer Dosisreduktion oder einem Abbruch der Therapie mit Mycophenolatmofetil reversibel sein. Bei Transplantationspatienten sollte eine Änderung der Behandlung mit Mycophenolatmofetil nur unter geeigneter Kontrolle vorgenommen werden, um das Risiko einer Abstoßungsreaktion so gering wie möglich zu halten (siehe Abschnitt 4.8).
Patienten, die mit Mycophenolatmofetil behandelt werden, sollen angewiesen werden, sofort über jedes Anzeichen einer Infektion, unerwartete Blutergüsse, Blutungen oder andere Manifestationen einer Knochenmarkinsuffizienz zu berichten.
Die Patienten sollen informiert werden, dass Impfungen während der Behandlung mit Mycophenolatmofetil weniger wirksam sein können und dass die Anwendung von attenuierten Lebendimpfstoffen vermieden werden soll (siehe Abschnitt 4.5). Eine Grippeimpfung könnte vorteilhaft sein. Der verschreibende Arzt soll sich an die nationalen Richtlinien zur Grippeimpfung halten.
Verdauungstrakt
Mycophenolatmofetil ist mit einer erhöhten Inzidenz von Nebenwirkungen im Verdauungstrakt - einschließlich seltener Fälle von gastrointestinalen Ulcera, Blutungen und Perforationen - in Zusammenhang gebracht worden. Die Behandlung sollte bei Patienten mit aktiven, schwerwiegenden Erkrankungen des Verdauungstraktes nur mit Vorsicht erfolgen.
Mycophenolat ist ein Inhibitor der IMPDH (Inosinmonophosphatdehydrogenase). Aus diesem Grund soll das Präparat bei Patienten mit seltener erblicher Defizienz der Hypoxanthin‑Guanin-Phosphoribosyltransferase (HGPRT) wie dem Lesch-Nyhan- und dem Kelley‑Seegmiller-Syndrom nicht angewandt werden.
Wechselwirkungen
Vorsicht ist geboten bei der Umstellung von Kombinationstherapien, die Immunsuppressiva enthalten, die den enterohepatischen Kreislauf von MPA beeinflussen, z. B. Ciclosporin, auf andere Kombinationstherapien, die keine solchen Auswirkungen haben, z. B. Tacrolimus, Sirolimus, Belatacept, oder umgekehrt, da dies zu Veränderungen der MPA-Exposition führen kann. Arzneimittel, die den enterohepatischen Kreislauf von MPA beeinflussen (z. B. Colestyramin, Antibiotika), sollten mit Vorsicht angewendet werden, da sie die Plasmaspiegel von Mycophenolat und dessen Wirksamkeit verringern können (siehe auch Abschnitt 4.5).
Es wird empfohlen, Mycophenolatmofetil nicht zusammen mit Azathioprin zu geben, da die gleichzeitige Anwendung nicht untersucht worden ist.
CellCept 1 g/5 ml Pulver zur Herstellung einer Suspension zum Einnehmen enthält Aspartam. Daher sollte CellCept 1 g/5 ml Pulver zur Herstellung einer Suspension zum Einnehmen nur unter Vorsicht an Patienten mit Phenylketonurie verabreicht werden (siehe Abschnitt 6.1).
Das Nutzen-Risiko-Verhältnis von Mycophenolatmofetil in Kombination mit Sirolimus wurde noch nicht untersucht (siehe auch Abschnitt 4.5).
Dieses Arzneimittel enthält Sorbitol. Patienten mit der seltenen hereditären Fructose-Intoleranz sollten dieses Arzneimittel nicht anwenden.
Therapeutisches Arzneimittelmonitoring
Ein therapeutisches Arzneimittelmonitoring von MPA kann bei einer Umstellung von Kombinationstherapien angebracht sein (z. B. Umstellung von Ciclosporin auf Tacrolimus oder umgekehrt) oder zur Sicherstellung einer adäquaten Immunsuppression bei Patienten mit hohem immunologischem Risiko (z. B. Abstoßungsrisiko, Behandlung mit Antibiotika, zusätzliche Gabe oder Absetzen eines wechselwirkenden Arzneimittels).
Besondere Patientengruppen
Kinder und Jugendliche
Sehr begrenzte Informationen nach der Markteinführung deuten auf eine höhere Häufigkeit der folgenden Nebenwirkungen bei Patienten unter 6 Jahren im Vergleich zu älteren Patienten hin:
Lymphome und andere bösartige Erkrankungen, insbesondere lymphoproliferative Erkrankungen bei Herztransplantationspatienten nach der Transplantation.
Erkrankungen des Blutes und des Lymphsystems, einschließlich Anämie und Neutropenie bei Herztransplantationspatienten. Dies gilt für Kinder unter 6 Jahren im Vergleich zu älteren Patienten und im Vergleich zu pädiatrischen Leber-/Nierentransplantatempfängern.
Bei Patienten, die Mycophenolatmofetil einnehmen, ist im ersten Monat wöchentlich ein vollständiges Blutbild zu erstellen, im zweiten und dritten Monat der Behandlung zweimal monatlich und dann während des ersten Jahres monatlich. Wenn sich eine Neutropenie entwickelt, kann es angemessen sein, die Behandlung mit Mycophenolatmofetil zu unterbrechen oder abzusetzen.
Gastrointestinale Störungen, einschließlich Diarrhö und Erbrechen.
Die Behandlung ist bei Patienten mit aktiven schweren Erkrankungen des Verdauungssystems mit Vorsicht durchzuführen.
Ältere Patienten
Bei älteren Patienten kann das Risiko für Nebenwirkungen im Vergleich zu jüngeren erhöht sein; dazu zählen bestimmte Infektionen (einschließlich invasiver Gewebebefall durch das Zytomegalie-Virus) und möglicherweise gastrointestinale Blutungen und Lungenödem (siehe Abschnitt 4.8).
Teratogene Wirkungen
Mycophenolat wirkt beim Menschen stark teratogen. Fehlgeburten (Rate 45 % bis 49 %) und kongenitale Missbildungen (geschätzte Rate 23 % bis 27 %) sind nach Mycophenolatmofetil-Exposition in der Schwangerschaft berichtet worden. Daher ist eine Behandlung in der Schwangerschaft kontraindiziert, außer wenn keine geeignete alternative Behandlung zur Verfügung steht, um eine Transplantatabstoßung zu verhindern. Patientinnen im gebärfähigen Alter müssen über die Risiken aufgeklärt werden und vor, während und nach Behandlung mit Mycophenolatmofetil die Empfehlungen in Abschnitt 4.6 befolgen (z. B. Verhütungsmethoden, Schwangerschaftstests). Ärzte sollen sicherstellen, dass Frauen, die Mycophenolatmofetil anwenden, die Risiken einer Schädigung des Babys, die Notwendigkeit einer wirksamen Verhütung und die Notwendigkeit im Fall einer möglichen Schwangerschaft ihren Arzt sofort zu benachrichtigen, verstehen.
Verhütung (siehe Abschnitt 4.6)
Belastbare klinische Daten zeigen ein hohes Risiko für Fehlgeburten und kongenitale Missbildungen bei Anwendung von Mycophenolatmofetil während der Schwangerschaft, sodass eine Schwangerschaft während der Behandlung unbedingt zu vermeiden ist. Daher müssen Frauen im gebärfähigen Alter vor Beginn der Behandlung, während der Behandlung sowie noch für 6 Wochen nach Beendigung der Behandlung mit Mycophenolatmofetil mindestens eine zuverlässige Form der Kontrazeption (siehe Abschnitt 4.3) anwenden, es sei denn, Abstinenz wird als Verhütungsmethode gewählt. Vorzugsweise sind zwei ergänzende Formen der Kontrazeption gleichzeitig anzuwenden, um das Risiko für ein Versagen der Verhütung und eine ungewollte Schwangerschaft zu minimieren.
Empfehlungen zur Verhütung für Männer, siehe Abschnitt 4.6.
Schulungsmaterialien
Der Inhaber der Genehmigung für das Inverkehrbringen stellt Angehörigen der Gesundheitsberufe Schulungsmaterialien zur Verfügung, um Patienten zu unterstützen, eine Exposition des Fetus gegenüber Mycophenolat zu vermeiden, und um weitere wichtige Sicherheitsinformationen bereitzustellen. Die Schulungsmaterialien werden die Warnhinweise zur Teratogenität von Mycophenolat stützen, Ratschläge zur Verhütung vor Beginn der Therapie und Anweisungen über die Notwendigkeit von Schwangerschaftstests geben. Der Arzt soll Frauen im gebärfähigen Alter und, soweit erforderlich, den männlichen Patienten vollumfängliche Patienteninformationen über das teratogene Risiko und die Schwangerschaftsverhütungsmaßnahmen geben.
Zusätzliche Vorsichtsmaßnahmen
Patienten dürfen während und für mindestens 6 Wochen nach Abbruch einer Behandlung mit Mycophenolatmofetil kein Blut spenden. Männer dürfen während und für 90 Tage nach Abbruch einer Behandlung mit Mycophenolatmofetil keinen Samen spenden.
Methyl-4-hydroxybenzoatgehalt
Dieses Arzneimittel enthält Methyl-4-hydroxybenzoat (E218) und kann allergische Reaktionen, auch Spätreaktionen, hervorrufen.
Natriumgehalt
Dieses Arzneimittel enthält weniger als 1 mmol (23 mg) Natrium pro Dosis, d. h. es ist nahezu „natriumfrei“.
Aciclovir
Im Vergleich zur alleinigen Gabe von Aciclovir wurden höhere Plasmakonzentrationen von Aciclovir beobachtet, wenn Mycophenolatmofetil und Aciclovir zusammen verabreicht wurden. Die Veränderungen der Pharmakokinetik von MPAG (dem phenolischen Glucuronid von MPA) waren minimal (MPAG-Anstieg um 8 %) und werden als klinisch nicht signifikant betrachtet. Da die Plasmakonzentrationen von MPAG und von Aciclovir bei Niereninsuffizienz erhöht sind, besteht die Möglichkeit, dass Mycophenolatmofetil und Aciclovir oder dessen Prodrugs, z. B. Valaciclovir, um die tubuläre Sekretion konkurrieren und es zu einem weiteren Konzentrationsanstieg der beiden Substanzen kommen kann.
Antazida und Protonenpumpeninhibitoren (PPIs)
Bei gleichzeitiger Verabreichung von Mycophenolatmofetil mit Antazida, wie z. B. Magnesium- und Aluminiumhydroxid und Protonenpumpeninhibitoren, einschließlich Lansoprazol und Pantoprazol, wurde eine verringerte MPA-Exposition beobachtet. Ein Vergleich der Häufigkeit des Auftretens von Transplantatabstoßungen oder Transplantatverlusten zwischen Patienten, die mit Mycophenolatmofetil und Protonenpumpeninhibitoren und Patienten, die mit Mycophenolatmofetil ohne Protonenpumpeninhibitoren behandelt wurden, ergab keine signifikanten Unterschiede. Diese Daten stützen die Extrapolation dieses Ergebnisses auf alle Antazida, da die Verringerung der Exposition bei gleichzeitiger Anwendung von Mycophenolatmofetil mit Magnesium- und Aluminiumhydroxid weitaus geringer war als bei gleichzeitiger Anwendung von Mycophenolatmofetil mit Protonenpumpeninhibitoren.
Arzneimittel, die den enterohepatischen Kreislauf beeinflussen (z. B. Colestyramin, Ciclosporin A, Antibiotika)
Vorsicht ist aufgrund ihres Potenzials, die Wirksamkeit von Mycophenolatmofetil zu reduzieren, bei Arzneimitteln geboten, die den enterohepatischen Kreislauf beeinflussen.
Colestyramin
Nach Gabe einer Einzeldosis von 1,5 g Mycophenolatmofetil an gesunde Probanden, die vier Tage lang mit dreimal täglich 4 g Colestyramin vorbehandelt worden waren, ging die AUC von MPA um 40 % zurück (siehe Abschnitt 4.4 und Abschnitt 5.2). Aufgrund des Potenzials, die Wirksamkeit von Mycophenolatmofetil zu reduzieren, ist bei gleichzeitiger Anwendung Vorsicht geboten.
Ciclosporin A
Die Pharmakokinetik von Ciclosporin A (CsA) wird durch Mycophenolatmofetil nicht beeinflusst.
Im Gegensatz dazu ist ein Anstieg der AUC von MPA um ca. 30 % zu erwarten, wenn die Begleitbehandlung mit CsA abgebrochen wird. CsA beeinflusst den enterohepatischen Kreislauf von MPA, was bei Nierentransplantationspatienten, die mit Mycophenolatmofetil und CsA behandelt werden, im Vergleich zu Patienten, die Sirolimus oder Belatacept und vergleichbare Dosen von Mycophenolatmofetil erhielten, zu einem Abfall der MPA-Exposition um 30 % - 50 % führte (siehe auch Abschnitt 4.4). Umgekehrt sind Veränderungen in der MPA-Exposition zu erwarten, wenn Patienten von CsA auf ein Immunsuppressivum umgestellt werden, das den enterohepatischen Kreislauf von MPA nicht beeinflusst.
Antibiotika, die β-Glucuronidase-bildende Bakterien im Darm eliminieren (z. B. Antibiotika aus den Klassen der Aminoglykoside, Cephalosporine, Fluorchinolone und Penicilline), können den enterohepatischen Kreislauf von MPAG/MPA beeinflussen und dadurch die systemische MPA-Exposition verringern. Zu folgenden Antibiotika liegen Informationen vor:
Ciprofloxacin oder Amoxicillin plus Clavulansäure
In den ersten Tagen nach Beginn einer oralen Therapie mit Ciprofloxacin oder Amoxicillin plus Clavulansäure wurde bei Nierentransplantationspatienten eine Reduktion der MPA-Talspiegel um ca. 50 % berichtet. Dieser Effekt tendierte während einer andauernden Antibiotikagabe dazu, sich abzuschwächen und innerhalb weniger Tage nach dem antibiotischen Absetzen wegzufallen. Die Veränderung der Talspiegel könnte möglicherweise die Veränderungen der Gesamt-MPA-Exposition nicht korrekt widerspiegeln. Daher sollte normalerweise und solange keine klinische Evidenz einer Dysfunktion des transplantierten Organs vorliegt, eine Änderung der Dosis von Mycophenolatmofetil nicht notwendig sein. Während der Kombinationstherapie und für kurze Zeit nach der Antibiotikabehandlung sollte jedoch eine intensive klinische Kontrolle erfolgen.
Norfloxacin und Metronidazol
Bei gesunden Freiwilligen wurde keine signifikante Interaktion beobachtet, wenn Mycophenolatmofetil zusammen mit Norfloxacin oder Metronidazol zeitlich getrennt verabreicht wurde. Die kombinierte Gabe von Norfloxacin und Metronidazol reduzierte jedoch die MPA-Exposition nach einer Einzeldosis von Mycophenolatmofetil um ca. 30 %.
Trimethoprim/Sulfamethoxazol
Es wurde keine Auswirkung auf die Bioverfügbarkeit von MPA beobachtet.
Arzneimittel mit Einfluss auf die Glucuronidierung (z. B. Isavuconazol, Telmisartan)
Die gleichzeitige Anwendung von Arzneimitteln, die die Glucuronidierung von MPA beeinflussen, kann zu einer Veränderung der MPA-Exposition führen. Daher sollte die Anwendung solcher Arzneimittel zusammen mit Mycophenolatmofetil mit Vorsicht erfolgen.
Isavuconazol
Bei gleichzeitiger Gabe von Isavuconazol wurde ein Anstieg der MPA-Exposition (AUC0-∞) um 35 % beobachtet.
Telmisartan
Die gleichzeitige Anwendung von Telmisartan und Mycophenolatmofetil führte zu einer Verringerung der MPA-Konzentrationen von ungefähr 30 %. Telmisartan beeinflusst die Ausscheidung von MPA durch eine Verstärkung der PPAR-Gamma-Expression (Peroxisom-Proliferator-aktivierte Rezeptoren Gamma), was wiederum zu einer verstärkten Uridindiphosphat-Glucuronyltransferase Isoform 1A9(UGT1A9)-Expression und -Aktivität führt. Bei einem Vergleich der Transplantatabstoßungsraten, Transplantatverlustraten oder Nebenwirkungsprofilen zwischen Mycophenolatmofetil-Patienten mit und ohne gleichzeitiger Anwendung von Telmisartan wurden keine klinischen Konsequenzen der pharmakokinetischen Wechselwirkungen zwischen Arzneimitteln beobachtet.
Ganciclovir
Basierend auf den Resultaten einer Einzeldosisstudie mit der empfohlenen Dosis von oral verabreichtem Mycophenolatmofetil und intravenös verabreichtem Ganciclovir sowie den bekannten Effekten einer Niereninsuffizienz auf die Pharmakokinetik von Mycophenolatmofetil (siehe Abschnitt 4.2) und Ganciclovir wird erwartet, dass die gleichzeitige Verabreichung dieser Wirkstoffe (die um die renale tubuläre Sekretion konkurrieren) in erhöhten Konzentrationen von MPAG und Ganciclovir resultieren wird. Es wird keine wesentliche Veränderung der MPA‑Pharmakokinetik erwartet, demzufolge ist eine Dosisanpassung von Mycophenolatmofetil nicht erforderlich. Bei Patienten mit Niereninsuffizienz, denen Mycophenolatmofetil und Ganciclovir oder dessen Prodrugs, z. B. Valganciclovir, gleichzeitig verabreicht werden, sind die Dosierungsempfehlungen für Ganciclovir zu beachten und die Patienten müssen sorgfältig überwacht werden.
Orale Kontrazeptiva
Die Pharmakodynamik und Pharmakokinetik oraler Kontrazeptiva wurden durch gleichzeitige Verabreichung von Mycophenolatmofetil nicht in einem klinisch relevanten Ausmaß beeinflusst (siehe auch Abschnitt 5.2).
Rifampicin
Bei Patienten, die kein Ciclosporin einnehmen, führte die gleichzeitige Anwendung von Mycophenolatmofetil und Rifampicin zu einem Abfall der MPA-Exposition (AUC0-12h) um 18 % bis 70 %. Es wird empfohlen, die MPA-Exposition zu überwachen und die Dosis von Mycophenolatmofetil entsprechend anzupassen, um die klinische Wirksamkeit aufrechtzuerhalten, wenn gleichzeitig Rifampicin verabreicht wird.
Sevelamer
Ein Abfall der Cmax und der AUC0-12h von MPA um 30 % bzw. 25 % wurde beobachtet, wenn Mycophenolatmofetil zusammen mit Sevelamer verabreicht wurde, dies hatte jedoch keine klinischen Konsequenzen (d. h. Transplantatabstoßungsreaktion). Es ist dennoch empfehlenswert, Mycophenolatmofetil mindestens eine Stunde vor oder drei Stunden nach der Einnahme von Sevelamer zu verabreichen, um die Auswirkungen auf die Resorption von MPA so gering wie möglich zu halten. Zur Kombination von Mycophenolatmofetil mit anderen Phosphatbindern als Sevelamer liegen keine Daten vor.
Tacrolimus
Bei Lebertransplantationspatienten, die von Anfang an Mycophenolatmofetil und Tacrolimus erhielten, wurden die AUC und die Cmax von MPA, dem aktiven Metaboliten von Mycophenolatmofetil, durch gleichzeitige Verabreichung von Tacrolimus nicht signifikant beeinflusst. Im Gegensatz dazu kam es bei wiederholter Gabe von Mycophenolatmofetil (1,5 g zweimal täglich) an Lebertransplantationspatienten, die gleichzeitig mit Tacrolimus behandelt wurden, zu einer Erhöhung der Tacrolimus-AUC um ca. 20 %. Bei Nierentransplantationspatienten scheint Mycophenolatmofetil die Konzentration von Tacrolimus jedoch nicht zu verändern (siehe auch Abschnitt 4.4).
Lebendimpfstoffe
Patienten mit einer geschwächten Immunantwort sollen nicht mit Lebendimpfstoffen immunisiert werden. Die Bildung von Antikörpern auf andere Impfstoffe könnte abgeschwächt sein (siehe auch Abschnitt 4.4).
Kinder und Jugendliche
Studien zur Erfassung von Wechselwirkungen wurden nur bei Erwachsenen durchgeführt.
Potenzielle Interaktionen
Die gleichzeitige Verabreichung von Probenecid und Mycophenolatmofetil an Affen bewirkt einen dreifachen Anstieg der AUC von MPAG. Daher können andere Substanzen, die bekanntermaßen in den Nierentubuli sezerniert werden, mit MPAG in Konkurrenz treten, wodurch es zu einer Erhöhung der Plasmakonzentration von MPAG oder der anderen Substanz, die der tubulären Sekretion unterworfen ist, kommen kann.
Frauen im gebärfähigen Alter
Eine Schwangerschaft während der Anwendung von Mycophenolatmofetil ist unbedingt zu vermeiden. Daher müssen Frauen im gebärfähigen Alter vor Beginn der Behandlung, während der Behandlung sowie noch für 6 Wochen nach Beendigung der Behandlung mindestens eine zuverlässige Form der Kontrazeption (siehe Abschnitt 4.3) anwenden, es sei denn, Abstinenz wird als Verhütungsmethode gewählt. Vorzugsweise sind zwei ergänzende Formen der Kontrazeption gleichzeitig anzuwenden.
Schwangerschaft
Mycophenolatmofetil ist in der Schwangerschaft kontraindiziert, außer wenn es keine geeignete alternative Behandlung zur Verhinderung einer Transplantatabstoßung gibt. Eine Behandlung darf ohne Vorlage eines negativen Schwangerschaftstestergebnisses nicht begonnen werden, um eine unbeabsichtigte Anwendung während der Schwangerschaft auszuschließen (siehe Abschnitt 4.3).
Patientinnen im gebärfähigen Alter müssen zu Beginn der Behandlung über das erhöhte Risiko für Fehlgeburten und kongenitale Missbildungen informiert werden und zu Schwangerschaftsverhütung und –planung beraten werden.
Vor Beginn einer Behandlung müssen Frauen im gebärfähigen Alter zwei negative Serum- oder Urin-Schwangerschaftstests mit einer Sensitivität von mindestens 25 mIE/ml vorweisen, um eine unbeabsichtigte Exposition eines Embryos gegenüber Mycophenolat auszuschließen. Es wird empfohlen, 8 – 10 Tage nach dem ersten Test den zweiten Test durchzuführen. Wenn es bei Transplantaten verstorbener Spender nicht möglich ist, zwei Tests im Abstand von 8 – 10 Tagen vor Behandlungsbeginn durchzuführen (aufgrund der zeitlich nicht planbaren Verfügbarkeit eines Transplantats), muss ein Schwangerschaftstest unmittelbar vor Behandlungsbeginn und ein weiterer Test 8 – 10 Tage danach durchgeführt werden. Schwangerschaftstests sollen wiederholt werden, falls klinisch indiziert (z. B. nachdem eine Verhütungslücke berichtet wurde). Die Ergebnisse aller Schwangerschaftstests sollen mit den Patientinnen besprochen werden. Die Patientinnen sind darauf hinzuweisen, dass sie ihren Arzt sofort benachrichtigen müssen, falls sie schwanger geworden sind.
Mycophenolat ist ein beim Menschen stark wirksames Teratogen, bei dem bei Exposition in der Schwangerschaft ein erhöhtes Risiko für Fehlgeburten und kongenitale Missbildungen besteht.
Fehlgeburten wurden bei 45 % bis 49 % der schwangeren Frauen berichtet, die Mycophenolatmofetil angewendet haben, verglichen mit einer berichteten Rate von 12 % bis 33 % bei Patienten mit solider Organtransplantation, die mit anderen Immunsuppressiva als Mycophenolatmofetil behandelt wurden.
Nach Berichten in der Literatur traten Missbildungen bei 23 % bis 27 % der Lebendgeburten bei Frauen auf, die Mycophenolatmofetil während der Schwangerschaft angewendet hatten (verglichen mit 2 % bis 3 % bei Lebendgeburten in der Allgemeinpopulation und ungefähr 4 % bis 5 % bei Lebendgeburten bei soliden Organtransplantationsempfängern, die mit anderen Immunsuppressiva als Mycophenolatmofetil behandelt wurden).
Nach der Markteinführung wurde bei Kindern von mit Mycophenolat in Kombination mit anderen Immunsuppressiva während der Schwangerschaft behandelten Patienten, über angeborene Missbildungen, einschließlich multipler Missbildungen, berichtet. Die folgenden Missbildungen wurden am häufigsten berichtet:
Missbildungen der Ohren (z. B. anormal geformtes oder fehlendes Außenohr), Atresie des äußeren Gehörgangs (Mittelohr);
Missbildungen im Gesicht, wie z. B. Lippenspalte, Gaumenspalte, Mikrognathie und Hypertelorismus der Augenhöhlen;
Anomalien der Augen (z. B. Kolobom);
Kongenitale Herzerkrankungen, wie z. B. atriale und ventrikuläre Septumdefekte;
Missbildungen der Finger (z. B. Polydaktylie, Syndaktylie);
Tracheoösophageale Missbildungen (z. B. ösophageale Atresie);
Missbildungen des Nervensystems, wie z. B. Spina bifida;
Anomalien der Niere.
Zusätzlich gab es einzelne Berichte über folgende Missbildungen:
Mikrophthalmie;
Kongenitale Plexus choroideus–Zysten;
Agenesie des Septum pellucidum;
Agenesie des olfaktorischen Nervs.
Tierexperimentelle Studien haben eine Reproduktionstoxizität gezeigt (siehe Abschnitt 5.3).
Stillzeit
Begrenzte Daten zeigen, dass Mycophenolsäure in die menschliche Muttermilch übergeht. Aufgrund des Risikos schwerwiegender Nebenwirkungen von Mycophenolsäure beim gestillten Kind, ist eine Behandlung bei stillenden Müttern kontraindiziert (siehe Abschnitt 4.3).
Männer
Die begrenzten verfügbaren klinischen Daten deuten nicht darauf hin, dass ein erhöhtes Risiko für Missbildungen oder Fehlgeburten infolge einer Mycophenolatmofetil-Exposition des Vaters besteht.
MPA ist ein stark wirksames Teratogen. Es ist nicht bekannt, ob MPA in den Samen gelangt. Berechnungen anhand von tierexperimentellen Daten zeigen, dass die Höchstmenge MPA, die möglicherweise auf Frauen übertragen werden könnte, so gering ist, dass sie wahrscheinlich keine Auswirkung haben würde. In Tierversuchen war Mycophenolat in Konzentrationen genotoxisch, die nur geringfügig über der therapeutischen Exposition beim Menschen liegen, sodass das Risiko genotoxischer Effekte auf Spermazellen nicht völlig ausgeschlossen werden kann.
Deswegen werden folgende Vorsichtsmaßnahmen empfohlen: Sexuell aktive männliche Patienten oder ihre Partnerinnen sollen während der Behandlung des Patienten und für mindestens 90 Tage nach Beendigung der Behandlung mit Mycophenolatmofetil eine hochwirksame Verhütungsmethode anwenden. Fortpflanzungsfähige männliche Patienten sollen von qualifiziertem medizinischem Fachpersonal über die möglichen Risiken ein Kind zu zeugen informiert und entsprechend beraten werden.
Fertilität
Mycophenolatmofetil beeinflusste in oralen Dosen von bis zu 20 mg/kg/Tag die Fertilität männlicher Ratten nicht. Die systemische Verfügbarkeit dieser Dosis entspricht dem 2‑ bis 3-Fachen der empfohlenen klinischen Dosis von 2 g/Tag für Nierentransplantationspatienten und der 1,3- bis 2‑fachen empfohlenen klinischen Dosis von 3 g/Tag für Herztransplantationspatienten. In einer Studie über die weibliche Fertilität und Fortpflanzung bei Ratten traten nach Verabreichung oraler Dosen von 4,5 mg/kg/Tag in der ersten Generation Missbildungen (einschließlich Anophthalmie, Agnathie und Hydrocephalus) auf, ohne dass beim Muttertier toxische Symptome beobachtet wurden. Die systemische Verfügbarkeit dieser Dosis entsprach ungefähr dem 0,5-Fachen der empfohlenen klinischen Dosis von 2 g/Tag für Nierentransplantationspatienten und ungefähr dem 0,3-Fachen der empfohlenen klinischen Dosis von 3 g/Tag für Herztransplantationspatienten. Bei den behandelten Weibchen sowie bei den Nachkommen wurden keine Auswirkungen auf die Fertilität und die Fortpflanzungsparameter festgestellt.
Mycophenolatmofetil hat mäßigen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Die Behandlung kann Somnolenz, Verwirrung, Benommenheit, Tremor oder Hypotonie verursachen. Deswegen werden Patienten darauf hingewiesen, vorsichtig zu sein, wenn sie ein Fahrzeug führen oder Maschinen bedienen.
Zusammenfassung des Sicherheitsprofils
Diarrhö (bis zu 52,6 %), Leukopenie (bis zu 45,8 %), bakterielle Infektionen (bis zu 39,9 %) und Erbrechen (bis zu 39,1 %) zählten zu den häufigsten und/oder schwerwiegendsten Nebenwirkungen, die mit der Anwendung von Mycophenolatmofetil in Kombination mit Ciclosporin und Corticosteroiden in Zusammenhang standen. Zudem ist erwiesen, dass bestimmte Infektionsarten häufiger auftreten (siehe Abschnitt 4.4).
Tabelle der Nebenwirkungen
Die Nebenwirkungen aus klinischen Studien und Erfahrung nach Markteinführung sind in Tabelle 2 nach MedDRA Systemorganklasse und dazugehörigen Häufigkeitskategorien aufgelistet. Bei den Häufigkeitsangaben zu Nebenwirkungen werden folgende Kategorien zugrundegelegt: sehr häufig (≥ 1/10), häufig (≥ 1/100, < 1/10), gelegentlich (≥ 1/1 000, < 1/100), selten (≥ 1/10 000, < 1/1 000), sehr selten (< 1/10 000) und nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar). Aufgrund der beobachteten großen Unterschiede in der Häufigkeit bestimmter Nebenwirkungen in den unterschiedlichen Transplantationsindikationen ist die Häufigkeit für Patienten mit Nieren-, Leber- und Herztransplantation separat aufgeführt.
Tabelle 2: Nebenwirkungen in Studien zur Untersuchung der Behandlung mit Mycophenolatmofetil bei Erwachsenen und Jugendlichen oder im Rahmen der Überwachung nach der Markteinführung
|
Nebenwirkung (MedDRA) Systemorganklasse |
Nierentransplantation |
Lebertransplantation |
Herztransplantation |
Häufigkeit |
Häufigkeit |
Häufigkeit |
|
Infektionen und parasitäre Erkrankungen | |||
Bakterielle Infektionen |
Sehr häufig |
Sehr häufig |
Sehr häufig |
Pilzinfektionen |
Häufig |
Sehr häufig |
Sehr häufig |
Durch Protozoen verursachte Infektionen |
Gelegentlich |
Gelegentlich |
Gelegentlich |
Virale Infektionen |
Sehr häufig |
Sehr häufig |
Sehr häufig |
Gutartige, bösartige und nicht spezifizierte Neubildungen (einschl. Zysten und Polypen) | |||
Benigne Neoplasie der Haut |
Häufig |
Häufig |
Häufig |
Lymphom |
Gelegentlich |
Gelegentlich |
Gelegentlich |
Lymphoproliferative Erkrankung |
Gelegentlich |
Gelegentlich |
Gelegentlich |
Neoplasie |
Häufig |
Häufig |
Häufig |
Hautkrebs |
Häufig |
Gelegentlich |
Häufig |
Erkrankungen des Blutes und des Lymphsystems | |||
Anämie |
Sehr häufig |
Sehr häufig |
Sehr häufig |
Erythroblastopenie |
Gelegentlich |
Gelegentlich |
Gelegentlich |
Knochenmarkinsuffi-zienz |
Gelegentlich |
Gelegentlich |
Gelegentlich |
Ekchymose |
Häufig |
Häufig |
Sehr häufig |
Leukozytose |
Häufig |
Sehr häufig |
Sehr häufig |
Leukopenie |
Sehr häufig |
Sehr häufig |
Sehr häufig |
Panzytopenie |
Häufig |
Häufig |
Gelegentlich |
Pseudolymphom |
Gelegentlich |
Gelegentlich |
Häufig |
Thrombozytopenie |
Häufig |
Sehr häufig |
Sehr häufig |
Stoffwechsel- und Ernährungsstörungen | |||
Azidose |
Häufig |
Häufig |
Sehr häufig |
Hypercholesterinämie |
Sehr häufig |
Häufig |
Sehr häufig |
Hyperglykämie |
Häufig |
Sehr häufig |
Sehr häufig |
Hyperkaliämie |
Häufig |
Sehr häufig |
Sehr häufig |
Hyperlipidämie |
Häufig |
Häufig |
Sehr häufig |
Hypokalziämie |
Häufig |
Sehr häufig |
Häufig |
Hypokaliämie |
Häufig |
Sehr häufig |
Sehr häufig |
Hypomagnesiämie |
Häufig |
Sehr häufig |
Sehr häufig |
Hypophosphatämie |
Sehr häufig |
Sehr häufig |
Häufig |
Hyperurikämie |
Häufig |
Häufig |
Sehr häufig |
Gicht |
Häufig |
Häufig |
Sehr häufig |
Gewichtsverlust |
Häufig |
Häufig |
Häufig |
Psychiatrische Erkrankungen | |||
Verwirrung |
Häufig |
Sehr häufig |
Sehr häufig |
Depression |
Häufig |
Sehr häufig |
Sehr häufig |
Schlaflosigkeit |
Häufig |
Sehr häufig |
Sehr häufig |
Erregung |
Gelegentlich |
Häufig |
Sehr häufig |
Angst |
Häufig |
Sehr häufig |
Sehr häufig |
Abnormes Denken |
Gelegentlich |
Häufig |
Häufig |
Erkrankungen des Nervensystems | |||
Benommenheit |
Häufig |
Sehr häufig |
Sehr häufig |
Kopfschmerzen |
Sehr häufig |
Sehr häufig |
Sehr häufig |
Erhöhter Muskeltonus |
Häufig |
Häufig |
Sehr häufig |
Parästhesie |
Häufig |
Sehr häufig |
Sehr häufig |
Somnolenz |
Häufig |
Häufig |
Sehr häufig |
Tremor |
Häufig |
Sehr häufig |
Sehr häufig |
Konvulsion |
Häufig |
Häufig |
Häufig |
Dysgeusie |
Gelegentlich |
Gelegentlich |
Häufig |
Herzerkrankungen | |||
Tachykardie |
Häufig |
Sehr häufig |
Sehr häufig |
Gefäßerkrankungen | |||
Hypertonie |
Sehr häufig |
Sehr häufig |
Sehr häufig |
Hypotonie |
Häufig |
Sehr häufig |
Sehr häufig |
Lymphozele |
Gelegentlich |
Gelegentlich |
Gelegentlich |
Venenthrombose |
Häufig |
Häufig |
Häufig |
Vasodilatation |
Häufig |
Häufig |
Sehr häufig |
Erkrankungen der Atemwege, des Brustraums und Mediastinums | |||
Bronchiektase |
Gelegentlich |
Gelegentlich |
Gelegentlich |
Husten |
Sehr häufig |
Sehr häufig |
Sehr häufig |
Dyspnoe |
Sehr häufig |
Sehr häufig |
Sehr häufig |
Interstitielle Lungenerkrankung |
Gelegentlich |
Sehr selten |
Sehr selten |
Pleuraerguss |
Häufig |
Sehr häufig |
Sehr häufig |
Lungenfibrose |
Sehr selten |
Gelegentlich |
Gelegentlich |
Erkrankungen des Gastrointestinaltrakts | |||
Aufgeblähter Bauch |
Häufig |
Sehr häufig |
Häufig |
Bauchschmerzen |
Sehr häufig |
Sehr häufig |
Sehr häufig |
Kolitis |
Häufig |
Häufig |
Häufig |
Verstopfung |
Sehr häufig |
Sehr häufig |
Sehr häufig |
Verminderter Appetit |
Häufig |
Sehr häufig |
Sehr häufig |
Diarrhö |
Sehr häufig |
Sehr häufig |
Sehr häufig |
Dyspepsie |
Sehr häufig |
Sehr häufig |
Sehr häufig |
Ösophagitis |
Häufig |
Häufig |
Häufig |
Aufstoßen |
Gelegentlich |
Gelegentlich |
Häufig |
Flatulenz |
Häufig |
Sehr häufig |
Sehr häufig |
Gastritis |
Häufig |
Häufig |
Häufig |
Gastrointestinale Blutung |
Häufig |
Häufig |
Häufig |
Gastrointestinales Geschwür |
Häufig |
Häufig |
Häufig |
Zahnfleischhyper-plasie |
Häufig |
Häufig |
Häufig |
Ileus |
Häufig |
Häufig |
Häufig |
Geschwürbildung im Mund |
Häufig |
Häufig |
Häufig |
Übelkeit |
Sehr häufig |
Sehr häufig |
Sehr häufig |
Pankreatitis |
Gelegentlich |
Häufig |
Gelegentlich |
Stomatitis |
Häufig |
Häufig |
Häufig |
Erbrechen |
Sehr häufig |
Sehr häufig |
Sehr häufig |
Erkrankungen des Immunsystems | |||
Überempfindlichkeit |
Gelegentlich |
Häufig |
Häufig |
Anaphylaktische Reaktionen |
Nicht bekannt |
Nicht bekannt |
Nicht bekannt |
Hypogammaglobulin-ämie |
Gelegentlich |
Sehr selten |
Sehr selten |
Leber- und Gallenerkrankungen | |||
Erhöhte alkalische Phosphatase im Blut |
Häufig |
Häufig |
Häufig |
Erhöhter Laktat-Dehydrogenase-Wert im Blut |
Häufig |
Gelegentlich |
Sehr häufig |
Erhöhter Leberenzymwert |
Häufig |
Sehr häufig |
Sehr häufig |
Hepatitis |
Häufig |
Sehr häufig |
Gelegentlich |
Hyperbilirubinämie |
Häufig |
Sehr häufig |
Sehr häufig |
Ikterus |
Gelegentlich |
Häufig |
Häufig |
Erkrankungen der Haut und des Unterhautgewebes | |||
Akne |
Häufig |
Häufig |
Sehr häufig |
Alopezie |
Häufig |
Häufig |
Häufig |
Exanthem |
Häufig |
Sehr häufig |
Sehr häufig |
Hypertrophie der Haut |
Häufig |
Häufig |
Sehr häufig |
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen | |||
Arthralgie |
Häufig |
Häufig |
Sehr häufig |
Muskelschwäche |
Häufig |
Häufig |
Sehr häufig |
Erkrankungen der Nieren und Harnwege | |||
Erhöhter Kreatininwert im Blut |
Häufig |
Sehr häufig |
Sehr häufig |
Erhöhter Blut-Harnstoff-Wert |
Gelegentlich |
Sehr häufig |
Sehr häufig |
Hämaturie |
Sehr häufig |
Häufig |
Häufig |
Niereninsuffizienz |
Häufig |
Sehr häufig |
Sehr häufig |
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort | |||
Asthenie |
Sehr häufig |
Sehr häufig |
Sehr häufig |
Schüttelfrost |
Häufig |
Sehr häufig |
Sehr häufig |
Ödem |
Sehr häufig |
Sehr häufig |
Sehr häufig |
Hernie |
Häufig |
Sehr häufig |
Sehr häufig |
Unwohlsein |
Häufig |
Häufig |
Häufig |
Schmerzen |
Häufig |
Sehr häufig |
Sehr häufig |
Fieber |
Sehr häufig |
Sehr häufig |
Sehr häufig |
De-novo-Purinsynthesehemmer assoziiertes akutes inflammatorisches Syndrom (de novo purine synthesis inhibitors associated acute inflammatory syndrome) |
Gelegentlich |
Gelegentlich |
Gelegentlich |
Beschreibung ausgewählter Nebenwirkungen
Malignome
Patienten, die unter Behandlung mit Immunsuppressiva stehen und hierzu eine Kombination von Arzneimitteln, einschließlich Mycophenolatmofetil, erhalten, sind einem erhöhten Risiko von Lymphomen und anderen Malignomen, insbesondere der Haut, ausgesetzt (siehe Abschnitt 4.4).
Sicherheitsdaten über 3 Jahre ergaben bei Nieren- und Herztransplantationspatienten im Vergleich zu den 1-Jahresdaten keine unerwarteten Veränderungen bei der Malignominzidenz. Lebertransplantationspatienten wurden mindestens 1 Jahr, aber weniger als 3 Jahre nachbeobachtet.
Infektionen
Alle mit Immunsuppressiva behandelten Patienten sind einem erhöhten Risiko für bakterielle, virale und Pilz-Infektionen ausgesetzt (davon können einige einen tödlichen Ausgang haben), einschließlich Infektionen, die durch opportunistische Erreger und latente virale Reaktivierung verursacht werden. Das Risiko steigt mit der Gesamtbelastung durch immunsuppressive Medikationen (siehe Abschnitt 4.4). Die schwerwiegendsten Infektionen waren Sepsis, Peritonitis, Meningitis, Endokarditis, Tuberkulose und atypische mykobakterielle Infektion. Die häufigsten opportunistischen Infektionen bei Patienten, die Mycophenolatmofetil (2 g oder 3 g täglich) zusammen mit anderen immunsuppressiven Substanzen in kontrollierten klinischen Studien mit Nieren-, Herz- und Lebertransplantationspatienten, die mindestens 1 Jahr nachbeobachtet wurden, erhielten, waren mukokutane Candidose, CMV-Virämie/Syndrom und Herpes simplex. Der Anteil der Patienten mit CMV-Virämie/Syndrom betrug 13,5 %. Fälle von BK-Virus-Nephropathie sowie mit dem JC-Virus verbundener progressiver multifokaler Leukoenzephalopathie (PML) wurden bei Patienten berichtet, die mit Immunsuppressiva einschließlich Mycophenolatmofetil behandelt wurden.
Erkrankungen des Blutes und des Lymphsystems
Zytopenien, einschließlich Leukopenie, Anämie, Thrombozytopenie und Panzytopenie sind bekannte Risiken, die mit Mycophenolatmofetil in Verbindung stehen und zum Auftreten von Infektionen und Blutungen führen oder dazu beitragen können (siehe Abschnitt 4.4). Agranulozytose und Neutropenie wurden berichtet. Deswegen wird eine regelmäßige Überwachung der mit Mycophenolatmofetil behandelten Patienten empfohlen (siehe Abschnitt 4.4).
Bei mit Mycophenolatmofetil behandelten Patienten gab es Berichte von aplastischer Anämie und Knochenmarkinsuffizienz, davon einige mit tödlichem Ausgang.
Fälle von Erythroblastopenien (pure red cell aplasia [PRCA]) wurden bei Patienten, die mit Mycophenolatmofetil behandelt wurden, berichtet (siehe Abschnitt 4.4).
Einzelfälle abnormaler Morphologie neutrophiler Granulozyten, wie die erworbene Pelger-Huët-Anomalie, wurden bei Patienten, die mit Mycophenolatmofetil behandelt wurden, beobachtet. Diese Veränderungen sind nicht mit einer Funktionseinschränkung der neutrophilen Granulozyten verbunden. Diese Veränderungen können bei Blutuntersuchungen eine „Linksverschiebung“ bei der Reifung der neutrophilen Granulozyten vermuten lassen, die bei immunsupprimierten Patienten, wie Patienten, die Mycophenolatmofetil erhalten, versehentlich als Infektion interpretiert werden kann.
Erkrankungen des Gastrointestinaltrakts
Die schwerwiegendsten gastrointestinalen Erkrankungen waren Geschwüre und Blutungen. Hierbei handelt es sich um bekannte mit Mycophenolatmofetil in Verbindung stehende Risiken. Geschwüre an Mund, Ösophagus, Duodenum und Darm, die oft mit Blutungen als Komplikation verbunden sind, genauso wie Hämatemese, Melaena und hämorrhagische Formen von Gastritis und Kolitis wurden während der klinischen Zulassungsstudien häufig berichtet. Die häufigsten gastrointestinalen Beschwerden waren jedoch Diarrhö, Übelkeit und Erbrechen. Endoskopische Untersuchungen von Patienten mit Diarrhö, die mit der Anwendung von Mycophenolatmofetil in Zusammenhang steht, haben einzelne Fälle von intestinaler villöser Atrophie gezeigt (siehe Abschnitt 4.4).
Überempfindlichkeit
Es wurden Überempfindlichkeitsreaktionen, einschließlich angioneurotischem Ödem und anaphylaktischer Reaktion, gemeldet.
Schwangerschaft, Wochenbett und perinatale Erkrankungen
Bei Patienten, die Mycophenolatmofetil angewendet haben, wurden Fälle von Fehlgeburten berichtet, die hauptsächlich im ersten Trimenon auftraten, siehe Abschnitt 4.6.
Kongenitale Erkrankungen
Nach der Markteinführung wurden bei Kindern von mit Mycophenolat in Kombination mit anderen Immunsuppressiva behandelten Patienten kongenitale Missbildungen beobachtet, siehe Abschnitt 4.6.
Erkrankungen der Atemwege, des Brustraums und Mediastinums
Bei Patienten, die eine Kombinationsbehandlung von Mycophenolatmofetil mit anderen Immunsuppressiva erhielten, gab es Einzelfallberichte über interstitielle Lungenerkrankungen und Lungenfibrosen, von denen einige einen tödlichen Ausgang hatten. Bei Kindern und Erwachsenen ist auch Bronchiektasie berichtet worden.
Erkrankungen des Immunsystems
Bei Patienten, die Mycophenolatmofetil in Kombination mit anderen Immunsuppressiva erhielten, ist Hypogammaglobulinämie berichtet worden.
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort
Ödeme, einschließlich periphere, Gesichts- und Scrotalödeme wurden während der Zulassungsstudien sehr häufig berichtet. Schmerzen der Skelettmuskulatur, darunter Myalgie und Nacken- und Rückenschmerzen, wurden ebenfalls sehr häufig berichtet.
Ein De-novo-Purinsynthesehemmer assoziiertes akutes inflammatorisches Syndrom wurde aus Erfahrungen nach der Markteinführung als paradoxe proinflammatorische Reaktion beschrieben, die mit Mycophenolatmofetil und Mycophenolsäure assoziiert und durch Fieber, Arthralgie, Arthritis, Muskelschmerzen und erhöhte Entzündungsmarker charakterisiert ist. Fallberichte aus der Literatur zeigten eine rasche Verbesserung nach Absetzen des Arzneimittels.
Besondere Patientengruppen
Kinder und Jugendliche
Art und Häufigkeit der Nebenwirkungen wurden in einer klinischen Langzeitstudie beurteilt, in die 33 pädiatrische Nierentransplantationspatienten im Alter von 3 bis 18 Jahren aufgenommen wurden, die zweimal täglich 23 mg/kg orales Mycophenolatmofetil erhielten. Insgesamt war das Sicherheitsprofil bei diesen 33 Kindern und Jugendlichen ähnlich wie bei erwachsenen Transplantatempfängern von soliden Organen.
Ähnliche Beobachtungen wurden in einer anderen klinischen Studie gemacht, in die 100 pädiatrische Nierentransplantationspatienten im Alter von 1 bis 18 Jahren aufgenommen wurden. Art und Häufigkeit der Nebenwirkungen bei Patienten, die zweimal täglich 600 mg/m2 bis 1 g/m2 Mycophenolatmofetil oral erhielten, waren mit denen vergleichbar, die bei erwachsenen Patienten beobachtet wurden, die zweimal täglich 1 g Mycophenolatmofetil erhielten. Eine Zusammenfassung der am häufigsten auftretenden Nebenwirkungen ist in der nachfolgenden Tabelle 3 aufgelistet:
Tabelle 3: Zusammenfassung der Nebenwirkungen, die in einer Studie zur Untersuchung von Mycophenolatmofetil bei 100 pädiatrischen Nierentransplantationspatienten häufger beobachtet wurden (alters- und flächenbezogene Dosierung [600 mg/m2, bis zu 1 g/m2 zweimal täglich.])
|
Nebenwirkung (MedDRA) Systemorganklasse |
< 6 Jahre (n = 33) |
6 - 11 Jahre (n = 34) |
12 - 18 Jahre (n = 33) |
Infektionen und parasitäre Erkrankungen |
Sehr häufig (48,5 %) |
Sehr häufig (44,1 %) |
Sehr häufig (51,5 %) |
Erkrankungen des Blutes und des Lymphsystems |
|||
Leukopenie |
Sehr häufig (30,3 %) |
Sehr häufig (29,4 %) |
Sehr häufig (12,1 %) |
Anämie |
Sehr häufig (51,5 %) |
Sehr häufig (32,4 %) |
Sehr häufig (27,3 %) |
Erkrankungen des Gastrointestinaltrakts |
|||
Diarrhö |
Sehr häufig (87,9 %) |
Sehr häufig (67,6 %) |
Sehr häufig (30,3 %) |
Erbrechen |
Sehr häufig (69,7 %) |
Sehr häufig (44,1 %) |
Sehr häufig (36,4 %) |
Basierend auf begrenzten Untergruppe-Daten (d. h. 33 von 100 Patienten) wurde eine höhere Inzidenz von schwerer Diarrhö (häufig, 9,1 %) und Candida mucocutane (sehr häufig, 21,2 %) bei Kindern unter 6 Jahren festgestellt, verglichen mit der älteren pädiatrischen Kohorte, in der keine Fälle von schwerer Diarrhö (0,0 %) und Candida mucocutane (häufig, 7,5 %) gemeldet wurden.
Die Überprüfung der verfügbaren medizinischen Literatur über pädiatrische Leber- und Herztransplantationspatienten zeigt, dass Art und Häufigkeit der gemeldeten Nebenwirkungen mit denen übereinstimmen, die bei pädiatrischen und erwachsenen Patienten nach einer Nierentransplantation beobachtet wurden.
Sehr begrenzte Daten nach der Markteinführung deuten auf eine höhere Häufigkeit der folgenden Nebenwirkungen bei Patienten unter 6 Jahren im Vergleich zu älteren Patienten hin (siehe Abschnitt 4.4):
Lymphome und andere bösartige Erkrankungen, insbesondere lymphoproliferative Posttransplantationsstörungen bei Herztransplantationspatienten
Erkrankungen des Blutes und des Lymphhsystems, einschließlich Anämie und Neutropenie, bei Herztransplantationspatienten unter 6 Jahren im Vergleich zu älteren Patienten und im Vergleich zu pädiatrischen Leber-/Nierentransplantatempfängern
gastrointestinale Störungen, einschließlich Diarrhö und Erbrechen.
Nierentransplantationspatienten unter 2 Jahren können im Vergleich zu älteren Patienten ein höheres Risiko für Infektionen und Atemwegserkrankungen aufweisen. Diese Daten sind jedoch mit Vorsicht zu interpretieren, da es nur eine sehr begrenzte Anzahl von Berichten nach der Markteinführung über dieselben Patienten gibt, die an mehreren Infektionen leiden.
Im Falle von Nebenwirkungen kann eine vorübergehende Dosisreduktion oder -unterbrechung in Betracht gezogen werden, wenn dies als klinisch notwendig erachtet wird.
Ältere Menschen
Ältere Patienten (≥ 65 Jahre) können grundsätzlich einem höheren Risiko für Nebenwirkungen aufgrund von Immunsuppression unterliegen. Für ältere Patienten, die Mycophenolatmofetil als Teil einer immunsuppressiven Kombinationstherapie erhalten, kann im Vergleich zu jüngeren Patienten ein erhöhtes Risiko für bestimmte Infektionen (einschließlich eines invasiven Gewebebefalls durch das Zytomegalie-Virus) und möglicherweise für gastrointestinale Blutungen und Lungenödeme bestehen.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem
Bundesinstitut für Arzneimittel und Medizinprodukte
Abt. Pharmakovigilanz
Kurt-Georg-Kiesinger-Allee 3
53175 Bonn
Website: http://www.bfarm.de
anzuzeigen.
Berichte zu Überdosierungen von Mycophenolatmofetil gingen während klinischer Prüfungen und nach der Markteinführung ein. Bei der überwiegenden Mehrheit dieser Fälle wurden entweder keine Nebenwirkungen gemeldet oder sie entsprachen dem bekannen Sicherheitsprofil des Arzneimittels und hatten einen günstigen Ausgang. Allerdings wurden in der Zeit nach der Markteinführung vereinzelte schwerwiegende Nebenwirkungen, darunter ein Todesfall, beobachtet.
Es ist zu erwarten, dass eine Überdosis Mycophenolatmofetil möglicherweise zu einer übermäßigen Unterdrückung des Immunsystems führt und die Infektionsanfälligkeit und die Suppression des Knochenmarks erhöht (siehe Abschnitt 4.4). Wenn sich eine Neutropenie entwickelt, muss die Verabreichung von Mycophenolatmofetil unterbrochen oder die Dosis reduziert werden (siehe Abschnitt 4.4).
Es ist nicht zu erwarten, dass durch Hämodialyse klinisch signifikante Mengen MPA oder MPAG eliminiert werden können. Gallensäurebindende Substanzen wie Colestyramin können MPA durch eine Verminderung der Wiederaufnahme des Arzneimittels in den enterohepatischen Kreislauf eliminieren (siehe Abschnitt 5.2).
Pharmakotherapeutische Gruppe: Immunsuppressiva, ATC-Code: L04AA06
Wirkmechanismus
Mycophenolatmofetil ist der 2‑Morpholinoethylester von MPA. MPA ist ein selektiver, nicht kompetitiver und reversibler IMPDH-Hemmer und hemmt daher den De-novo‑Weg der Guanosin-Nucleotidsynthese, ohne in die DNA eingebaut zu werden. Da für die Proliferation von T‑ und B‑Lymphozyten die De-novo-Synthese von Purinen unerlässlich ist, während andere Zellarten den Wiederverwertungsstoffwechsel benutzen können, wirkt MPA stärker zytostatisch auf Lymphozyten als auf andere Zellen.
Neben der Hemmung von IMPDH und dem daraus resultierenden Mangel an Lymphozyten beeinflusst MPA auch entscheidende zelluläre Kontrollpunkte (Checkpoints), die für die metabolische Programmierung der Lymphozyten verantwortlich sind. Anhand von humanen CD4+ T-Zellen wurde gezeigt, dass MPA die Transkriptionsaktivitäten in Lymphozyten von einem proliferativen Zustand auf katabole Prozesse verschiebt, die für den Stoffwechsel und das Überleben relevant sind, was zu einem anergischen Zustand der T-Zellen führt. Dabei reagieren die Zellen nicht mehr auf ihr spezifisches Antigen.
Resorption
Nach oraler Verabreichung wird Mycophenolatmofetil schnell und zu einem großen Teil resorbiert und in einer vollständigen präsystemischen Metabolisierung in MPA, den aktiven Metaboliten, umgewandelt. Wie durch die Suppression der akuten Abstoßungsreaktion nach Nierentransplantation gezeigt werden konnte, korreliert die immunsuppressive Wirkung von Mycophenolatmofetil mit der MPA‑Konzentration. Die mittlere Bioverfügbarkeit von oral verabreichtem Mycophenolatmofetil, basierend auf der AUC von MPA, beträgt 94 % im Vergleich zu intravenös verabreichtem Mycophenolatmofetil. Der Resorptionsgrad (MPA-AUC) von Mycophenolatmofetil wurde durch Nahrung nicht beeinflusst, wenn das Präparat in Dosen von zweimal täglich 1,5 g an Nierentransplantationspatienten verabreicht wurde. Hingegen nahm die Cmax von MPA in Gegenwart von Nahrung um 40 % ab. Mycophenolatmofetil ist nach oraler Verabreichung im Plasma nicht messbar.
Verteilung
Aufgrund des enterohepatischen Kreislaufs beobachtet man im Allgemeinen 6 ‑ 12 Stunden nach der Verabreichung einen sekundären Anstieg der Plasmakonzentration von MPA. Die AUC von MPA geht um ca. 40 % zurück, wenn Mycophenolatmofetil gleichzeitig mit Colestyramin (4 g dreimal täglich) verabreicht wird, was auf einen ausgeprägten enterohepatischen Kreislauf hinweist.
In klinisch relevanten Konzentrationen ist Mycophenolsäure zu 97 % an Plasmaalbumin gebunden.
In der frühen Posttransplantationsphase (< 40 Tage nach Transplantation) lag die mittlere MPA-AUC der Nieren-, Herz- und Lebertransplantationspatienten um ca. 30 % und die Cmax um ca. 40 % unter den entsprechenden Werten der späten Posttransplantationsphase (3 - 6 Monate nach Transplantation).
Biotransformation
MPA wird hauptsächlich durch Glucuronyltransferase (Isoform UGT1A9) in inaktives phenolisches MPA-Glucuronid (MPAG) umgewandelt. In vivo wird MPAG über den enterohepatischen Kreislauf wieder in freies MPA umgewandelt. Acylglucuronid (AcMPAG) wird ebenfalls geringfügig gebildet. AcMPAG ist pharmakologisch wirksam und steht im Verdacht, für einige der Nebenwirkungen von Mycophenolatmofetil verantwortlich zu sein (Diarrhö, Leukopenie).
Elimination
Vernachlässigbare Mengen der Substanz werden als MPA (< 1 % der Dosis) mit dem Urin ausgeschieden. Nach oraler Verabreichung von radioaktiv markiertem Mycophenolatmofetil wurde die verabreichte Dosis vollständig ausgeschieden, wobei 93 % der verabreichten Dosis mit dem Urin und 6 % mit den Fäzes eliminiert wurden. Der größte Teil (ca. 87 %) der verabreichten Dosis wird als MPAG mit dem Urin ausgeschieden.
Bei den üblichen klinischen Konzentrationen werden MPA und MPAG nicht durch Dialyse entfernt. Bei hohen MPAG-Plasmakonzentrationen (> 100 μg/ml) werden jedoch geringe Mengen MPAG entfernt. Durch die Beeinflussung des enterohepatischen Kreislaufs des Wirkstoffes verringern gallensäurebindende Substanzen wie Colestyramin die MPA-AUC (siehe Abschnitt 4.9).
Die Verteilung von MPA ist von verschiedenen Transportern abhängig. Organo-Anion-Transporter-Polypeptide (OATPs) und das multidrug resistance associated protein 2 (MRP2) sind an der MPA-Verteilung beteiligt; OATP-Isoformen, MRP2 und breast cancer resistance protein (BCRP) sind Transporter, die mit der Gallenausscheidung der Glucuronide in Verbindung gebracht werden. Das multidrug resistance protein 1 (MDR1) kann auch MPA transportieren, aber dessen Einfluss scheint auf den Resorptionsprozess beschränkt zu sein. In der Niere interagieren MPA und deren Metabolite wirksam mit den Organo-Anion-Transportern der Niere.
Der enterohepatische Kreislauf stört die genaue Bestimmung der Dispositionsparameter von MPA; es können nur scheinbare Werte angegeben werden. Bei gesunden Probanden und Patienten mit Autoimmunerkrankungen wurden ungefähre Clearance-Werte von 10,6 l/h bzw. 8,27 l/h und Halbwertszeiten von 17 h beobachtet. Bei Transplantationspatienten waren die mittleren Clearance-Werte höher (Bereich 11,9 - 34,9 l/h) und die mittleren Halbwertszeiten kürzer (5 – 11 h), wobei es kaum Unterschiede zwischen Nieren-, Leber- oder Herztransplantationspatienten gab. Bei den einzelnen Patienten variieren diese Eliminationsparameter abhängig von der Art der gleichzeitigen Behandlung mit anderen Immunsuppressiva, Zeit nach der Transplantation, Plasmaalbumin-Konzentration und Nierenfunktion. Diese Faktoren erklären, warum bei gleichzeitiger Verabreichung von Mycophenolatmofetil mit Ciclosporin eine reduzierte Exposition gegenüber Mycophenolat beobachtet wird (siehe Abschnitt 4.5) und warum die Plasmakonzentrationen im Laufe der Zeit tendenziell ansteigen, verglichen mit den Konzentrationen, die unmittelbar nach der Transplantation beobachtet werden.
Besondere Patientengruppen
Niereninsuffizienz
In einer Einzeldosisstudie (6 Probanden/Gruppe) waren die mittleren AUC von MPA im Plasma bei Patienten mit schwerer chronischer Niereninsuffizienz (glomeruläre Filtrationsrate < 25 ml/min/1,73 m2) um 28 % ‑ 75 % höher als die mittleren AUC gesunder Personen oder von Patienten mit Niereninsuffizienz geringeren Schweregrades. Die mittlere MPAG-AUC nach Einzeldosen war bei Patienten mit schwerer Niereninsuffizienz 3- bis 6-mal größer als bei solchen mit leichter Nierenfunktionsstörung oder gesunden Probanden, was mit der bekannten renalen Elimination von MPAG in Einklang steht. Die Verabreichung von Mycophenolatmofetil in Mehrfachdosen an Patienten mit schweren chronischen Nierenfunktionsstörungen ist nicht untersucht worden. Für herz- oder lebertransplantierte Patienten mit schwerer chronischer Niereninsuffizienz liegen keine Daten vor.
Verzögerte renale Transplantatfunktion
Bei Patienten mit verzögerter renaler Transplantatfunktion nach der Verpflanzung war die mittlere MPA-AUC0‑12h vergleichbar mit derjenigen von Patienten nach der Transplantation, bei denen die Organfunktion nicht verzögert einsetzte. Die durchschnittliche Plasma-MPAG-AUC0‑12h war 2- bis 3-mal größer als bei Patienten nach der Transplantation, bei denen die Organfunktion nicht verzögert war. Bei Patienten mit verzögerter renaler Transplantatfunktion kann ein vorübergehender Anstieg des freien MPA und der MPA‑Plasmakonzentration auftreten. Eine Dosisanpassung von Mycophenolatmofetil scheint nicht erforderlich zu sein.
Leberinsuffizienz
Bei Probanden mit Alkoholzirrhose waren die Glucuronidierungsprozesse von MPA in der Leber durch die Erkrankung des Leberparenchyms relativ wenig beeinträchtigt. Der Einfluss der Lebererkrankung auf diese Prozesse hängt wahrscheinlich von der jeweiligen Krankheit ab. Lebererkrankungen mit vorwiegender Schädigung der Galle, wie zum Beispiel die primäre biliäre Zirrhose, können sich anders auswirken.
Kinder und Jugendliche
Bei 33 pädiatrischen Nierentransplantatempfängern wurde festgestellt, dass die Dosis, die voraussichtlich zu einer MPA-AUC0-12h führt, die der Zielexposition von 27,2 h μg/ml am nächsten kommt, 600 mg/m2 betrug und, dass die auf Basis der geschätzten KOF berechneten Dosen die interindividuelle Variabilität (Variationskoeffizient [VK]) um etwa 10 % reduzierten. Daher ist eine auf der KOF-basierte Dosierung einer Körpergewicht-basierten Dosierung vorzuziehen.
Bei bis zu 55 pädiatrischen Nierentransplantationspatienten (im Alter von 1 bis 18 Jahren), denen oral zweimal täglich 600 mg/m2 bis zu 1 g/m2 Mycophenolatmofetil verabreicht wurde, wurden die pharmakokinetischen Parameter ausgewertet. Mit dieser Dosis wurden ähnliche MPA-AUC-Werte erreicht wie bei erwachsenen Nierentransplantationspatienten, welche gemäß nachfolgender Tabelle 4 Mycophenolatmofetil in einer Dosis von zweimal täglich 1 g in der frühen und späten Posttransplantationsphase erhielten. Die MPA-AUC-Werte waren in der frühen und späten Posttransplantationsphase in allen Altersgruppen ähnlich.
An einer offenen Studie zur Sicherheit, Verträglichkeit und Pharmakokinetik von Mycophenolatmofetil zum Einnehmen bei Kindern und Jugendlichen mit Lebertransplantation, die gleichzeitig mit Ciclosporin und Corticosteroiden behandelt wurden, nahmen 7 auswertbare Patienten teil. Es wurde die Dosis geschätzt, mit der voraussichtlich eine Exposition von 58 hmg/l in der stabilen Phase nach der Transplantation erreicht werden kann. Die mittlere ± SD (standard deviation – Standardabweichung) AUC0-12 (angepasst an eine Dosis von 600 mg/m2) betrug 47,0 ± 21,8 hmg/l, die angepasste Cmax betrug 14,5 ± 4,21 mg/l, bei einer medianen Zeit bis zur maximalen Konzentration von 0,75 h. Um die Ziel-AUC0-12 von 58 hmg/l in der späten Posttransplantationsphase zu erreichen, wäre daher in der Studienpopulation eine Dosis im Bereich von 740 – 806 mg/m2 zweimal täglich erforderlich gewesen.
Ein Vergleich der dosisnormalisierten (auf 600 mg/m2) MPA-AUC-Werte von 12 pädiatrischen Nierentransplantationspatienten im Alter von unter 6 Jahren 9 Monate nach der Transplantation mit den Werten von 7 pädiatrischen Lebertransplantationspatienten [medianes Alter 17 Monate (Bereich: 10 – 60 Monate bei Aufnahme)] 6 und mehr Monate nach der Transplantation ergab, dass bei gleicher Dosis die AUC-Werte bei den pädiatrischen Leberpatienten im Durchschnitt 23 % niedriger waren als bei den pädiatrischen Nierenpatienten. Dies steht im Einklang mit der Notwendigkeit einer höheren Dosierung bei erwachsenen Lebertransplantationspatienten im Vergleich zu erwachsenen Nierentransplantationspatienten, um die gleiche Exposition zu erreichen.
Bei erwachsenen Transplantationspatienten, denen die gleiche Dosis Mycophenolatmofetil verabreicht wird, ist die MPA-Exposition bei Nierentransplantations- und Herztransplantationspatienten vergleichbar. Entsprechend der festgestellten Vergleichbarkeit der MPA-Exposition bei pädiatrischen Nierentransplantationspatienten und erwachsenen Nierentransplantationspatienten bei den jeweils zugelassenen Dosen konnte gezeigt werden, dass die MPA-Exposition bei der empfohlenen Dosierung bei pädiatrischen Herztransplantationspatienten und erwachsenen Herztransplantationspatienten vergleichbar sein wird.
Tabelle 4: Mittlere berechnete MPA-PK-Parameter nach Alter und Zeit nach der Transplantation (Niere)
Altersgruppe (n) |
Angepasste Cmax mg/lA |
Angepasste AUC0-12 hmg/l |
|
Tag 7 |
(17) |
13,2 ± 7,16 |
27,4 ± 9,54 (22,8 ‑ 31,9) |
6 ‑ < 12 J |
(16) |
13,1 ± 6,30 |
33,2 ± 12,1 (27,3 ‑ 39,2) |
12 ‑ 18 J |
(21) |
11,7 ± 10,7 |
26,3 ± 9,14 (22,3 ‑ 30,3)D |
p-WertB |
- |
- |
|
< 2 JC |
(6) |
10,3 ± 5,80 |
22,5 ± 6,68 (17,2 ‑ 27,8) |
> 18 J |
(141) |
27,2 ± 11,6 |
|
Monat 3 |
(15) |
22,7 ± 10,1 |
49,7 ± 18,2 |
6 ‑ < 12 J |
(14)E |
27,8 ± 14,3 |
61,9 ± 19,6 |
12 ‑ 18 J |
(17) |
17,9 ± 9,57 |
53,6 ± 20,2F |
p‑WertB |
- |
- |
|
< 2 JC |
(4) |
23,8 ± 13,4 |
47,4 ± 14,7 |
> 18 J |
(104) |
50,3 ± 23,1 |
|
Monat 9 |
(12) |
30,4 ± 9,16 |
60,9 ± 10,7 |
6 ‑ < 12 J |
(11) |
29,2 ± 12,6 |
66,8 ± 21,2 |
12 ‑ 18 J |
(14) |
18,1 ± 7,29 |
56,7 ± 14,0 |
p‑WertB |
0,004 |
- |
|
< 2 JC |
(4) |
25,6 ± 4,25 |
55,8 ± 11,6 |
> 18 J |
(70) |
53,5 ± 18,3 |
|
AUC0‑12h = Fläche unter der Konzentrations-Zeit-Kurve (Area under the concentration-time curve) vom Zeitpunkt null bis 12 h; KI = Konfidenzintervall; Cmax = maximale Konzentration; MPA = Mycophenolsäure; SD = Standardabweichung (standard deviation); n = Anzahl der Patienten; J = Jahr.
A In den pädiatrischen Altersgruppen sind Cmax und AUC0‑12h an eine Dosis von 600 mg/m2 (95‑%‑Konfidenzintervalle (Kls) nur für AUC0‑12h Tag 7) angepasst, in der Gruppe der Erwachsenen ist AUC0‑12h an eine Dosis von 1 g angepasst.
B p‑Wert stellt den kombinierten p-Wert für die drei wichtigsten pädiatrischen Altersgruppen dar und wird nur angegeben, wenn er signifikant ist (p < 0,05).
C Die < 2‑J-Gruppe stellt eine Untergruppe der < 6‑J-Gruppe dar: es wurden keine statistischen Vergleiche gemacht.
D n = 20.
E Die Daten eines Patienten waren aufgrund eines Probenahmefehlers nicht verfügbar.
F n = 16.
Ältere Menschen
In der Pharmakokinetik von Mycophenolatmofetil und dessen Metaboliten wurde bei älteren Patienten (≥ 65 Jahre) im Vergleich zu jüngeren Patienten keine Veränderung festgestellt.
Patienten, die orale Kontrazeptiva einnehmen
Eine Studie, in der gleichzeitig Mycophenolatmofetil (zweimal täglich 1 g) und orale Kontrazeptiva, welche Ethinylestradiol (0,02 mg bis 0,04 mg) und Levonorgestrel (0,05 mg bis 0,20 mg), Desogestrel (0,15 mg) oder Gestoden (0,05 mg bis 0,10 mg) enthalten, verabreicht wurden und welche bei 18 Frauen ohne Transplantat (die keine anderen Immunsuppressiva einnahmen) während 3 aufeinanderfolgenden Menstruationszyklen durchgeführt wurde, zeigte keinen klinisch relevanten Einfluss von Mycophenolatmofetil auf die ovulationshemmende Wirkung von oralen Kontrazeptiva. Die Serumspiegel von LH, FSH und Progesteron wurden nicht signifikant beeinflusst. Die Pharmakokinetik oraler Kontrazeptiva wurde durch gleichzeitige Anwendung von Mycophenolatmofetil nicht in einem klinisch relevanten Ausmaß beeinflusst (siehe Abschnitt 4.5).
In experimentellen Modellen war Mycophenolatmofetil nicht tumorerzeugend. Die höchste Dosis, die in den Tierstudien zur Kanzerogenität geprüft wurde, ergab ungefähr die 2‑ bis 3‑fache systemische Verfügbarkeit (AUC oder Cmax) dessen, was bei Nierentransplantationspatienten nach Gabe der empfohlenen klinischen Dosis von 2 g/Tag bzw. die 1,3‑ bis 2‑fache systemische Verfügbarkeit (AUC oder Cmax) dessen, was bei Herztransplantationspatienten nach Gabe der empfohlenen klinischen Dosis von 3 g/Tag gefunden wurde.
Zwei Genotoxizitätsuntersuchungen (der In-vitro-Maus-Lymphom-Test und der In-vivo-Maus-Knochenmark-Mikronucleustest) deuteten darauf hin, dass Mycophenolatmofetil ein Potenzial aufweist, chromosomale Aberrationen zu bewirken. Diese Effekte können mit der pharmakodynamischen Wirkungsweise in Verbindung gebracht werden, d. h. mit der Inhibition der Nucleotidsynthese in sensitiven Zellen. Andere In-vitro-Untersuchungen zur Detektion von Genmutationen ergaben keinen Hinweis auf Genotoxizität.
In teratologischen Studien an Ratten und Kaninchen kam es mit 6 mg/kg/Tag bei Ratten bzw. 90 mg/kg/Tag bei Kaninchen zu fetaler Resorption und zu Missbildungen (einschließlich Anophthalmie, Agnathie und Hydrocephalus [bei Ratten] bzw. kardiovaskulären und renalen Anomalien, wie z. B. Ektopie des Herzens und der Nieren, Hernia diaphragmatica und Hernia umbilicalis [bei Kaninchen]), ohne dass beim Muttertier toxische Symptome auftraten. Die systemische Verfügbarkeit dieser Dosen entspricht ungefähr dem 0,5-Fachen oder weniger der empfohlenen klinischen Dosis von 2 g/Tag für Nierentransplantationspatienten und ungefähr dem 0,3‑Fachen der empfohlenen klinischen Dosis von 3 g/Tag für Herztransplantationspatienten (siehe Abschnitt 4.6).
Das blutbildende System und das Lymphsystem waren die Organe, die in den toxikologischen Studien mit Mycophenolatmofetil bei Ratten, Mäusen, Hunden und Affen in erster Linie betroffen waren. Diese Erscheinungen traten bei einer systemischen Verfügbarkeit auf, die der empfohlenen klinischen Dosis von 2 g/Tag für Nierentransplantationspatienten entsprach oder niedriger war. Gastrointestinale Nebenwirkungen wurden bei Hunden bei einer systemischen Verfügbarkeit beobachtet, die der empfohlenen klinischen Dosis entsprach bzw. niedriger war. Gastrointestinale und renale Nebenwirkungen in Verbindung mit Dehydratation wurden auch bei Affen bei der höchsten Dosis beobachtet (die systemische Verfügbarkeit entsprach der nach Gabe der klinischen Dosis bzw. war größer). Das präklinische Toxizitätsprofil von Mycophenolatmofetil scheint mit den Nebenwirkungen übereinzustimmen, die bei klinischen Studien beim Menschen beobachtet wurden. Dadurch liegen nun für die Patienten maßgebliche Ergebnisse zur Sicherheit vor (siehe Abschnitt 4.8).
Beurteilung der Risiken für die Umwelt (Environmental risk assessment [ERA])
Studien zur Beurteilung der Risiken für de Umwelt haben gezeigt, dass der Wirkstoff MPA durch Uferfiltration ein Risiko für das Grundwasser darstellen kann.
CellCept 1 g/5 ml Pulver zur Herstellung einer Suspension zum Einnehmen
Sorbitol
Hochdisperses Siliciumdioxid
Natriumcitrat
Entölte Phospholipide aus Sojabohnen
Gemischtes Fruchtaroma
Xanthangummi
Aspartam* (E951)
Methyl‑4‑hydroxybenzoat (E218)
Citronensäure
* enthält Phenylalanin entsprechend 2,78 mg/5 ml Suspension.
Das Arzneimittel darf, außer mit den unter Abschnitt 6.6 aufgeführten, nicht mit anderen Arzneimitteln gemischt werden.
Das Pulver zur Herstellung einer Suspension zum Einnehmen ist 2 Jahre haltbar.
Nach Zubereitung ist die Suspension zum Einnehmen 2 Monate haltbar.
Pulver zur Herstellung einer Suspension zum Einnehmen und zubereitete Suspension: Nicht über 30 °C lagern.
Jede Flasche enthält 35 g Mycophenolatmofetil in 110 g Pulver zur Herstellung einer Suspension zum Einnehmen. Nach Zubereitung beträgt das Volumen der Suspension 175 ml, das entnehmbare Volumen beträgt 160 ml ‑ 165 ml. 5 ml der rekonstituierten Suspension enthalten 1 g Mycophenolatmofetil.
Ein Adapter sowie 2 Dispenser für Zubereitungen zum Einnehmen sind ebenfalls beigelegt.
Es wird empfohlen, CellCept 1 g/5 ml Pulver zur Herstellung einer Suspension zum Einnehmen vor Abgabe an den Patienten von einem Apotheker zubereiten zu lassen. Das Tragen von Einmalhandschuhen bei der Zubereitung der Suspension sowie beim Abwischen der Flasche/Verschlusskappe und der Arbeitsfläche nach der Zubereitung wird empfohlen.
Herstellung der Suspension
Schütteln Sie die verschlossene Flasche mehrmals zur Auflockerung des Pulvers.
Messen Sie 94 ml gereinigtes Wasser in einen Messzylinder ab.
Füllen Sie ungefähr die Hälfte des gereinigten Wassers in die Flasche. Verschließen Sie die Flasche und schütteln Sie sorgfältig ca. 1 Minute.
Füllen Sie die Flasche mit der Restmenge des Wassers auf und schütteln Sie die verschlossene Flasche erneut ca. 1 Minute.
Entfernen Sie die kindergesicherte Verschlusskappe. Setzen Sie den Flaschenadapter in den Flaschenhals ein.
Verschließen Sie die Flasche wieder fest mit der kindergesicherten Verschlusskappe. Dadurch wird der richtige Sitz des Flaschenadapters in der Flasche sowie die Kindersicherung der Verschlusskappe gewährleistet.
Schreiben Sie das Verfalldatum der zubereiteten Suspension auf das Flaschenetikett. (Nach Zubereitung ist die Suspension 2 Monate haltbar.)
Dieses Arzneimittel kann ein Risiko für die Umwelt darstellen (siehe Abschnitt 5.3). Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu beseitigen.
Roche Registration GmbH
Emil-Barell-Straße 1
79639 Grenzach-Wyhlen
Deutschland
EU/1/96/005/006 CellCept (1 Flasche zu 110 g)
Datum der Erteilung der Zulassung: 14. Februar 1996
Datum der letzten Verlängerung der Zulassung: 13. März 2006
März 2026
Verschreibungspflichtig
Roche Pharma AG
Emil-Barell-Straße 1
79639 Grenzach-Wyhlen
Telefon (07624) 14-0
Telefax (07624) 1019
Ausführliche Informationen zu diesem Arzneimittel sind auf den Internetseiten der Europäischen Arzneimittel-Agentur https://www.ema.europa.eu verfügbar.