SPIRIVA® 18 Mikrogramm
Hartkapseln mit Pulver zur Inhalation
Jede Kapsel enthält 22,5 Mikrogramm Tiotropiumbromid 1 H2O entsprechend 18 Mikrogramm Tiotropium.
Die aus dem Mundstück des HandiHaler® Inhalators abgegebene Dosis beträgt 10 Mikrogramm Tiotropium.
Sonstiger Bestandteil mit bekannter Wirkung: Jede Kapsel enthält 5,5 mg Lactose-Monohydrat.
Vollständige Auflistung der sonstigen Bestandteile: siehe Abschnitt 6.1.
Hartkapsel mit Pulver zur Inhalation.
Hellgrüne Hartkapseln, gefüllt mit Pulver zur Inhalation, auf denen der Präparatecode „TI 01“ und das Firmenlogo aufgedruckt sind.
SPIRIVA ist indiziert als dauerhaft einzusetzender Bronchodilatator zur Befreiung von Symptomen bei chronischer obstruktiver Lungenerkrankung (COPD).
Dosierung
Das Arzneimittel ist nur zur Inhalation bestimmt.
Die empfohlene Dosis von Tiotropiumbromid ist: 1 x täglich den Inhalt von 1 Kapsel mit dem HandiHaler zur jeweils gleichen Tageszeit inhalieren.
Die empfohlene Dosis soll nicht überschritten werden.
SPIRIVA Kapseln sind nur zur Inhalation vorgesehen, nicht zum Einnehmen.
SPIRIVA Kapseln dürfen nicht geschluckt werden.
SPIRIVA Kapseln dürfen nur mit dem HandiHaler inhaliert werden.
Besondere Patientengruppen
Ältere Patienten können Tiotropiumbromid in der empfohlenen Dosis anwenden.
Patienten mit eingeschränkter Nierenfunktion können Tiotropiumbromid in der empfohlenen Dosis anwenden. Für Patienten mit mittlerer bis schwerer Nierenfunktionsstörung (Creatinin-Clearance ≤ 50 ml/min) siehe Abschnitte 4.4 und 5.2.
Patienten mit eingeschränkter Leberfunktion können Tiotropiumbromid in der empfohlenen Dosis anwenden (siehe Abschnitt 5.2).
Kinder und Jugendliche
COPD
Es gibt im Anwendungsgebiet laut Abschnitt 4.1 keinen relevanten Nutzen von SPIRIVA 18 Mikrogramm bei Kindern und Jugendlichen (unter 18 Jahren).
Zystische Fibrose (Mukoviszidose)
Die Sicherheit und Wirksamkeit von SPIRIVA 18 Mikrogramm bei Kindern und Jugendlichen ist nicht erwiesen. Es liegen keine Daten vor.
Art der Anwendung
Der HandiHaler Inhalator wurde speziell entwickelt, um Patienten das Inhalieren des in SPIRIVA 18 Mikrogramm Kapseln enthaltenen Arzneimittels zu ermöglichen. Der HandiHaler darf nicht zur Anwendung von anderen Arzneimitteln verwendet werden. Er ist zur mehrmaligen Anwendung für einen einzelnen Patienten vorgesehen.
Um die richtige Anwendung des Arzneimittels sicherzustellen, sollten die Patienten vom Arzt oder anderen Fachkräften des Gesundheitswesens in die korrekte Handhabung des Inhalators HandiHaler eingewiesen werden.
Gebrauchsanweisung für den HandiHaler Inhalator
Die Patienten sollen zur Anwendung des HandiHalers wie nachfolgend beschrieben vorgehen.
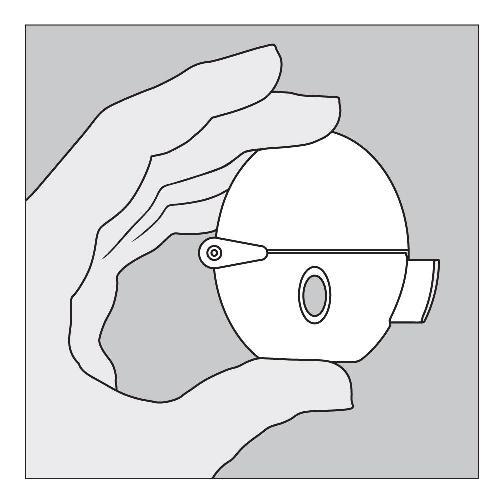 |
Bitte folgen Sie den Anweisungen Ihres Arztes zur Anwendung von SPIRIVA 18 Mikrogramm sehr sorgfältig. Nach der ersten Anwendung können Sie Ihren HandiHaler bis zu einem Jahr lang zur Inhalation von SPIRIVA 18 Mikrogramm verwenden. |
|
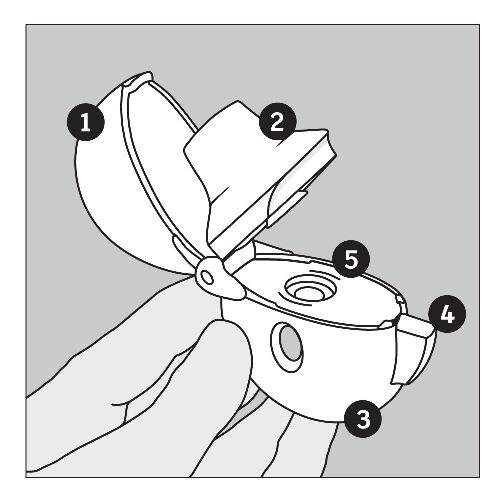 |
Der HandiHaler besteht aus: |
|
1 |
Schutzkappe |
|
2 |
Mundstück |
|
3 |
Geräteunterteil |
|
4 |
Anstechknopf |
|
5 |
Kapselkammer |
|
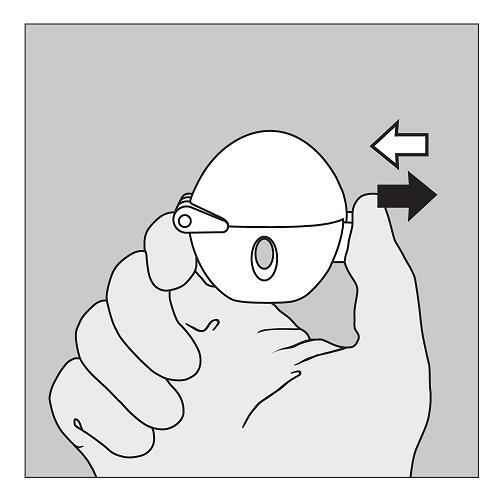 |
1. Zum Öffnen der Schutzkappe drücken Sie den Knopf vollständig ein und lassen ihn wieder los. |
|
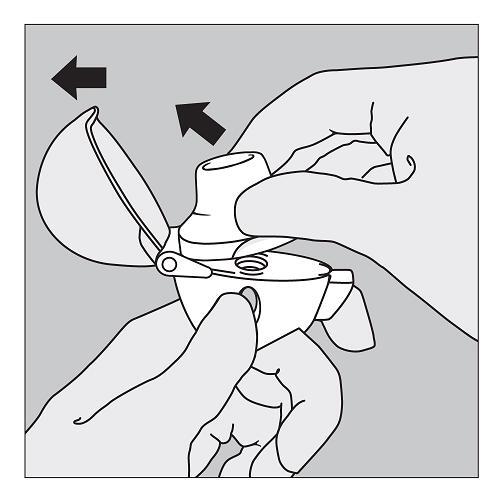 |
2. Öffnen Sie die Schutzkappe durch Hochziehen vollständig. Öffnen Sie dann das Mundstück durch Hochziehen. |
|
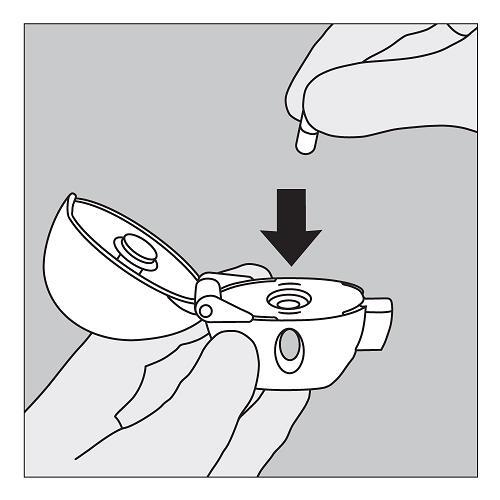 |
3. Entnehmen Sie dem Blister eine SPIRIVA Kapsel (unmittelbar vor der Anwendung) und legen Sie diese wie abgebildet in die Kapselkammer (5) ein. Es ist unerheblich, welches Ende der Kapsel nach oben oder nach unten zeigt. |
|
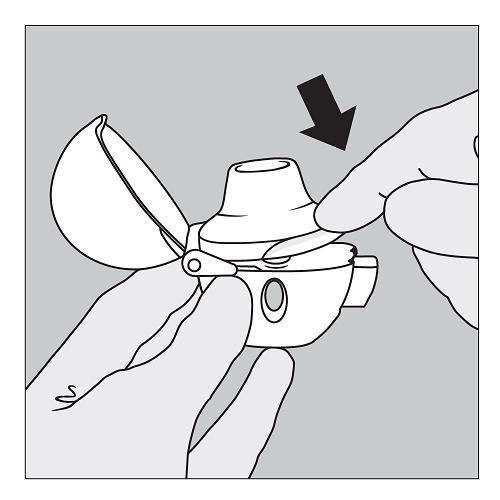 |
4. Klappen Sie das Mundstück fest zu, bis Sie einen Klick hören. Lassen Sie dabei die Schutzkappe aufgeklappt. |
|
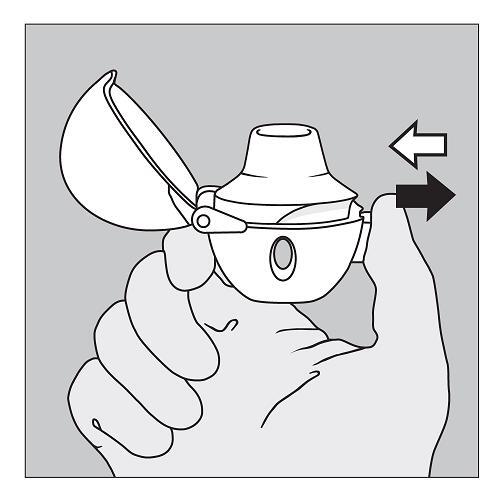 |
5. Halten Sie den HandiHaler mit dem Mundstück nach oben. Drücken Sie den grünen Anstechknopf nur einmal bis zum Anschlag ein und lassen Sie ihn danach wieder los. Die Kapsel wird damit angestochen und das Arzneimittel ist für die Inhalation verfügbar. |
|
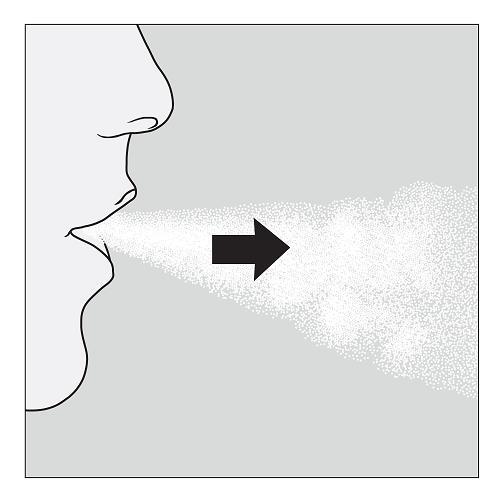 |
6. Atmen Sie zunächst ohne Gerät tief aus. |
|
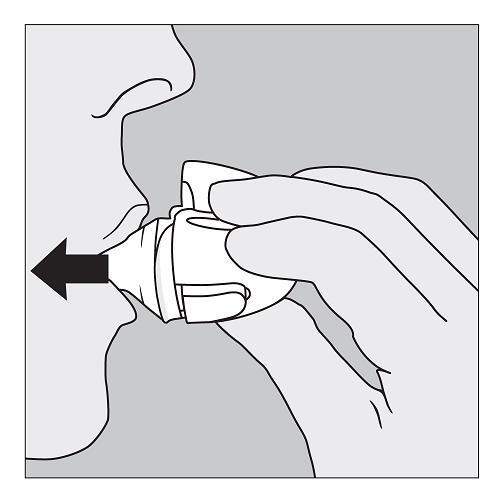 |
7. Führen Sie anschließend den HandiHaler an den Mund und umschließen Sie das Mundstück fest mit den Lippen. Halten Sie den Kopf aufrecht. Atmen Sie langsam und tief ein, aber stark genug, bis Sie hören oder fühlen, dass die Kapsel vibriert. Inhalieren Sie, bis Ihre Lungen gefüllt sind. Anschließend halten Sie Ihren Atem so lange wie möglich an, ohne dass es unangenehm wird. Setzen Sie dabei den HandiHaler ab. Atmen Sie nun normal weiter. Wiederholen Sie Schritt 6 und 7 einmal, um die Kapsel vollständig zu entleeren. |
|
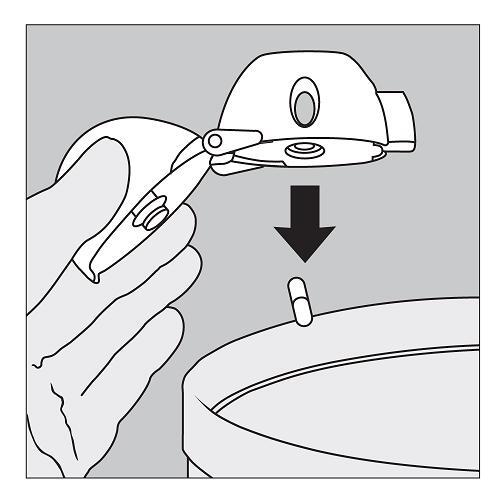 |
8. Zum Entfernen und Entsorgen der leeren Kapsel klappen Sie das Mundstück wieder auf und lassen die Kapsel aus dem HandiHaler fallen. Zur Aufbewahrung Ihres HandiHaler verschließen Sie Mundstück und Schutzkappe wieder. |
|
Reinigung des HandiHalers
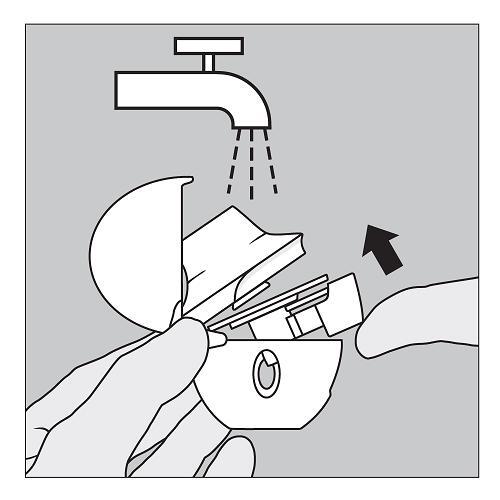 |
Reinigen Sie den HandiHaler einmal pro Monat. Klappen Sie Schutzkappe und Mundstück nacheinander auf. Öffnen Sie anschließend das Geräteunterteil durch Hochheben des Anstechknopfes. Zur Entfernung von Pulverresten spülen Sie den kompletten HandiHaler mit warmem Wasser. Trocknen Sie den HandiHaler sorgfältig, indem Sie das restliche Wasser auf ein Papierhandtuch schütten. Lassen Sie ihn anschließend mit geöffneter Schutzkappe, Mundstück und Geräteunterteil an der Luft trocknen. Da der Trockenvorgang 24 Stunden dauert, reinigen Sie den HandiHaler unmittelbar nach Gebrauch, sodass er für Ihre nächste Dosis bereit ist. Die Außenseite des Mundstücks können Sie nach Bedarf mit einem feuchten, jedoch nicht nassen Tuch reinigen. |
Blister-Handhabung
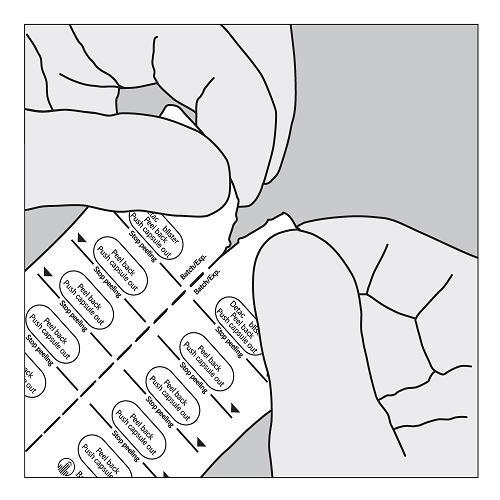 |
A. Trennen Sie die SPIRIVA Blisterstreifen entlang der Perforation. |
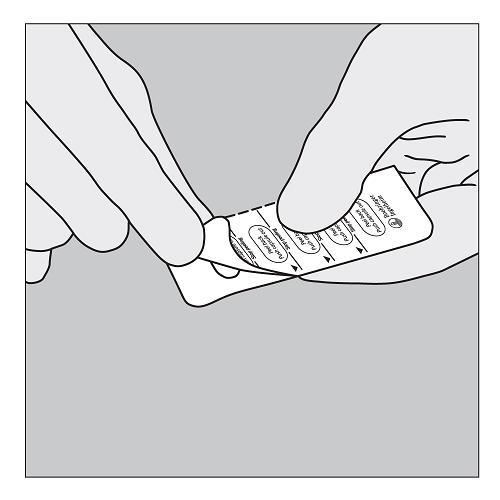 |
B. Öffnen Sie die Folie erst unmittelbar vor Gebrauch mit Hilfe der Lasche soweit, dass eine ganze Kapsel komplett sichtbar wird. Falls dabei versehentlich eine zweite Kapsel der Luft ausgesetzt wird, muss diese verworfen werden. |
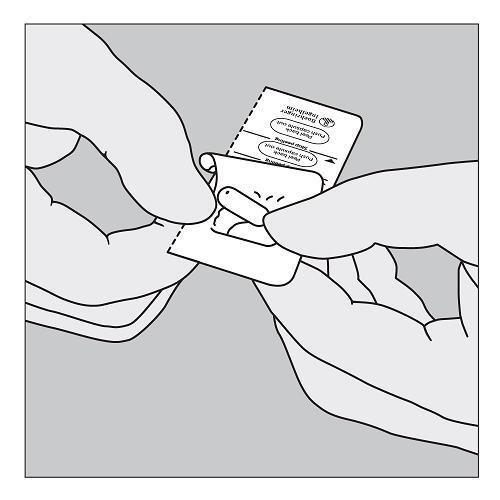 |
C. Entnehmen Sie die Kapsel. |
SPIRIVA Kapseln enthalten nur eine kleine Menge Pulver, so dass die Kapseln nur teilweise gefüllt sind.
Überempfindlichkeit gegen den Wirkstoff oder den in Abschnitt 6.1 genannten sonstigen Bestandteil Lactose-Monohydrat (kann geringe Mengen an Milchproteinen enthalten), oder gegen Atropin oder eines seiner Derivate, wie z. B. Ipratropium oder Oxitropium.
Als Bronchodilatator zur Dauerbehandlung mit einmal täglicher Anwendung sollte Tiotropiumbromid nicht zur Erstbehandlung akuter Bronchospasmen, d. h. nicht als Notfallmedikament, eingesetzt werden.
Nach der Anwendung von Tiotropiumbromid Pulver zur Inhalation sind Immunreaktionen vom Soforttyp möglich.
Da Tiotropiumbromid eine anticholinerge Substanz ist, sollte sie bei Patienten mit Engwinkelglaukom, Prostatahyperplasie oder Harnblasenhalsverengung nur mit Vorsicht angewendet werden (siehe Abschnitt 4.8).
Inhalative Arzneimittel können zu inhalationsbedingten Bronchospasmen führen.
Tiotropium sollte mit Vorsicht angewendet werden bei Patienten mit einem Myokardinfarkt innerhalb der letzten 6 Monate; mit instabilen oder lebensbedrohlichen Herzrhythmusstörungen oder Herzrhythmusstörungen, die eine Intervention oder eine Umstellung der medikamentösen Therapie erforderten, innerhalb der letzten 12 Monate; Hospitalisierung wegen Herzinsuffizienz (NYHA Grad III oder IV) innerhalb der letzten 12 Monate. Solche Patienten waren von den klinischen Prüfungen ausgeschlossen, und die genannten Erkrankungen können von der anticholinergen Wirkungsweise betroffen sein.
Da die Plasmakonzentration mit nachlassender Nierenfunktion bei Patienten mit mittlerer bis schwerer Nierenfunktionsstörung (Creatinin-Clearance ≤ 50 ml/min) ansteigt, sollte Tiotropiumbromid nur dann angewendet werden, wenn der zu erwartende Nutzen ein potenzielles Risiko überwiegt. Langzeiterfahrungen bei Patienten mit schwerer Nierenfunktionsstörung liegen nicht vor (siehe Abschnitt 5.2).
Patienten sollten angewiesen werden, darauf zu achten, dass das Pulver zur Inhalation nicht in die Augen gelangt. Sie sind darüber zu informieren, dass dies zum Auftreten oder zur Verschlimmerung eines Engwinkelglaukoms, Augenschmerzen oder Missempfinden, vorübergehend verschwommenem Sehen, Augenhalos oder unwirklichem Farbempfinden in Verbindung mit geröteten Augen durch Blutstauungen in der Bindehaut und Hornhautödem führen kann. Wenn zwei oder mehrere dieser Symptome gleichzeitig auftreten, sollte die Anwendung von Tiotropiumbromid abgebrochen und unverzüglich ein Augenarzt aufgesucht werden.
Mundtrockenheit, wie sie unter Therapie mit Anticholinergika beobachtet wurde, könnte bei längerer Dauer zum Auftreten von Karies führen.
Tiotropiumbromid sollte nicht häufiger als einmal täglich angewendet werden (siehe Abschnitt 4.9).
SPIRIVA Kapseln enthalten 5,5 mg Lactose-Monohydrat. Diese Menge verursacht normalerweise keine Probleme bei Patienten mit Lactose-Intoleranz. Patienten mit der seltenen hereditären Galactose-Intoleranz, Lactase-Mangel oder Glucose-Galactose-Malabsorption sollten dieses Arzneimittel nicht anwenden. Lactose-Monohydrat kann geringe Mengen an Milchproteinen enthalten, welche allergische Reaktionen auslösen können.
Obwohl keine gezielten Untersuchungen zu Wechselwirkungen mit Arzneimitteln durchgeführt wurden, wurde Tiotropiumbromid zusammen mit anderen Arzneimitteln ohne Anzeichen von Arzneimittel-Wechselwirkungen angewendet. Bei diesen Arzneimitteln handelt es sich u. a. um sympathomimetische Bronchodilatatoren, Methylxanthine, orale und inhalative Steroide, die üblicherweise bei der Behandlung der COPD angewendet werden.
Die Anwendung von LABA oder ICS ändert die Exposition gegenüber Tiotropium nicht.
Die gleichzeitige Anwendung von Tiotropiumbromid und anderen Anticholinergika wurde nicht untersucht und wird daher nicht empfohlen.
Schwangerschaft
Es liegen nur sehr begrenzte Daten zur Anwendung von Tiotropium bei Schwangeren vor. Tierexperimentelle Studien ergaben keine Hinweise auf direkte oder indirekte gesundheitsschädliche Wirkungen in Bezug auf eine Reproduktionstoxizität in klinisch relevanten Dosen (siehe Abschnitt 5.3). Aus Vorsichtsgründen soll eine Anwendung von SPIRIVA während der Schwangerschaft vermieden werden.
Stillzeit
Es ist nicht bekannt, ob Tiotropiumbromid beim Menschen in die Muttermilch ausgeschieden wird. Obwohl Studien mit Nagetieren gezeigt haben, dass Tiotropiumbromid nur in geringer Menge in die Muttermilch ausgeschieden wird, wird die Anwendung von SPIRIVA während der Stillzeit nicht empfohlen. Tiotropiumbromid ist eine langwirksame Substanz. Eine Entscheidung, ob das Stillen fortgesetzt/beendet oder ob die Behandlung mit SPIRIVA fortgesetzt/beendet werden soll, sollte unter Berücksichtigung der Vorteile des Stillens für das Kind und der Behandlung mit SPIRIVA für die Stillende getroffen werden.
Fertilität
Für Tiotropium sind keine klinischen Daten zur Fertilität verfügbar. Eine nichtklinische Studie, die mit Tiotropium durchgeführt wurde, ergab keinen Hinweis auf unerwünschte Effekte auf die Fertilität (siehe Abschnitt 5.3).
Es wurden keine Untersuchungen über die Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen durchgeführt. Beim Auftreten von Schwindel, verschwommenem Sehen oder Kopfschmerzen kann die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen beeinträchtigt sein.
Zusammenfassung des Sicherheitsprofils
Viele der aufgeführten Nebenwirkungen können auf die anticholinergen Eigenschaften von SPIRIVA zurückgeführt werden.
Tabellarische Zusammenfassung der Nebenwirkungen
Die Häufigkeiten der unten aufgelisteten Nebenwirkungen basieren auf der Anzahl der unerwünschten Arzneimittelwirkungen in den Tiotropium-Gruppen (9.647 Patienten) von 28 gepoolten, Placebo-kontrollierten klinischen Studien mit Behandlungsphasen zwischen vier Wochen und vier Jahren.
Bei den Häufigkeitsangaben zu Nebenwirkungen werden folgende Kategorien zugrunde gelegt:
Sehr häufig (≥ 1/10); Häufig (≥ 1/100 bis < 1/10); Gelegentlich (≥ 1/1.000 bis < 1/100); Selten (≥ 1/10.000 bis < 1/1.000); Sehr selten (< 1/10.000); Nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar)
System-Organ-Klasse / MedDRA‑Terminologie |
Häufigkeit |
Stoffwechsel- und Ernährungsstörungen | |
Dehydration |
Nicht bekannt |
Erkrankungen des Nervensystems | |
Schwindel |
Gelegentlich |
Kopfschmerz |
Gelegentlich |
Geschmacksstörungen |
Gelegentlich |
Insomnie |
Selten |
Augenerkrankungen | |
Verschwommenes Sehen |
Gelegentlich |
Glaukom |
Selten |
Erhöhter Augeninnendruck |
Selten |
Herzerkrankungen | |
Vorhofflimmern |
Gelegentlich |
Supraventrikuläre Tachykardie |
Selten |
Tachykardie |
Selten |
Palpitationen |
Selten |
Erkrankungen der Atemwege, des Brustraums und des Mediastinums | |
Pharyngitis |
Gelegentlich |
Dysphonie |
Gelegentlich |
Husten |
Gelegentlich |
Bronchospasmus |
Selten |
Epistaxis |
Selten |
Laryngitis |
Selten |
Sinusitis |
Selten |
Erkrankungen des Gastrointestinaltrakts | |
Trockener Mund |
Häufig |
Gastroösophagealer Reflux |
Gelegentlich |
Obstipation |
Gelegentlich |
Oropharyngeale Candidose |
Gelegentlich |
Intestinale Obstruktion, inklusive |
Selten |
Gingivitis |
Selten |
Glossitis |
Selten |
Dysphagie |
Selten |
Stomatitis |
Selten |
Übelkeit |
Selten |
Karies |
Nicht bekannt |
Erkrankungen der Haut und des Unterhautzellgewebes; Störungen des Immunsystems | |
Hautausschlag |
Gelegentlich |
Urtikaria |
Selten |
Juckreiz |
Selten |
Überempfindlichkeitsreaktionen |
Selten |
Angioödem |
Selten |
Anaphylaktische Reaktion |
Nicht bekannt |
Hautinfektion, Hautulkus |
Nicht bekannt |
Trockene Haut |
Nicht bekannt |
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen | |
Gelenkschwellung |
Nicht bekannt |
Erkrankungen der Nieren und Harnwege | |
Dysurie |
Gelegentlich |
Harnverhalt |
Gelegentlich |
Harnwegsinfekte |
Selten |
Angaben zu ausgewählten Nebenwirkungen
In kontrollierten klinischen Prüfungen wurden unter den Nebenwirkungen am häufigsten anticholinerge Effekte beobachtet, wie z. B. Mundtrockenheit (bei ca. 4 % der Patienten). In 28 klinischen Studien brachen 18 von 9.647 mit Tiotropium behandelten Patienten (0,2 %) die Studie wegen Mundtrockenheit ab.
Zu schwerwiegenden Nebenwirkungen aufgrund des anticholinergen Effektes gehören Glaukom, Verstopfung und Darmobstruktion einschließlich paralytischem Ileus, sowie Harnverhalt.
Besondere Patientengruppen
Mit fortgeschrittenem Alter ist eine Zunahme der anticholinergen Effekte möglich.
Dieses Arzneimittel enthält Lactose-Monohydrat. Lactose-Monohydrat kann geringe Mengen an Milchproteinen enthalten und deshalb allergische Reaktionen hervorrufen.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem
Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt‑Georg‑Kiesinger‑Allee 3, 53175 Bonn, Webseite: www.bfarm.de anzuzeigen.
In hohen Dosen kann Tiotropiumbromid zu anticholinergen Symptomen führen.
Bei gesunden Probanden traten jedoch keine systemischen anticholinergen Nebenwirkungen nach der Inhalation einer Einzeldosis von bis zu 340 Mikrogramm Tiotropiumbromid auf. Auch nach Dosierungen von bis zu 170 Mikrogramm Tiotropiumbromid über 7 Tage wurden bei gesunden Probanden abgesehen von Mundtrockenheit keine klinisch relevanten Nebenwirkungen beobachtet. In einer Studie mit Mehrfachdosierung mit einer täglichen Höchstdosis von 43 Mikrogramm Tiotropiumbromid über 4 Wochen bei COPD-Patienten wurden keine signifikanten Nebenwirkungen beobachtet.
Akute Intoxikation nach versehentlicher oraler Einnahme von Tiotropiumbromid ist unwahrscheinlich, da Tiotropiumbromid nur eine geringe orale Bioverfügbarkeit besitzt.
Pharmakotherapeutische Gruppe: Andere inhalative Mittel bei obstruktiven Atemwegserkrankungen, Anticholinergika
ATC‑Code: R03BB04
Wirkmechanismus
Tiotropiumbromid ist ein langwirksamer, spezifischer Muskarinrezeptor-Antagonist, der im medizinischen Sprachgebrauch häufig als Anticholinergikum bezeichnet wird. Durch die Bindung an die Muskarinrezeptoren der glatten Bronchialmuskulatur hemmt Tiotropiumbromid die cholinergen (bronchokonstriktiven) Effekte von Acetylcholin, das aus den parasympathischen Nervenendigungen freigesetzt wird. Es weist eine ähnliche Affinität zu den Muskarinrezeptor-Subtypen M1 bis M5 auf. In den Luftwegen wirkt Tiotropiumbromid kompetitiv und reversibel antagonistisch an den M3‑Rezeptoren, was zu einer Relaxation führt. Die Wirkung war dosisabhängig und hielt länger als 24 Stunden an. Die lange Wirkungsdauer ist wahrscheinlich auf die sehr langsame Dissoziation von den M3‑Rezeptoren zurückzuführen. Sie zeigen eine signifikant längere Dissoziations-Halbwertszeit als bei Ipratropium. Als N‑quartäres Anticholinergikum ist Tiotropiumbromid nach inhalativer Applikation topisch (broncho-)selektiv und zeigt eine akzeptable therapeutische Breite, ehe es zu systemischen anticholinergen Wirkungen kommt.
Pharmakodynamische Wirkungen
Bei der Bronchodilatation handelt es sich primär um eine lokale Wirkung (in den Atemwegen) und nicht um eine systemische Wirkung. Die Dissoziation vom M2‑Rezeptor ist schneller als die vom M3‑Rezeptor, was sich in in‑vitro-Studien funktionell als kinetisch kontrollierte Rezeptorselektivität von M3 gegenüber M2 zeigte. Die hohe Wirkstärke und langsame Rezeptordissoziation korreliert klinisch mit signifikanter und lang wirkender Bronchodilatation bei Patienten mit COPD.
Kardiale Elektrophysiologie
In einer speziellen QT‑Studie mit 53 gesunden Probanden verlängerten über 12 Tage weder SPIRIVA 18 Mikrogramm noch 54 Mikrogramm (das 3fache der therapeutischen Dosis) die QT‑Intervalle im EKG signifikant.
Klinische Wirksamkeit und Sicherheit
Das klinische Entwicklungsprogramm umfasste vier 1‑jährige und zwei 6‑monatige randomisierte, doppelblinde Studien an 2.663 Patienten (von denen 1.308 Tiotropiumbromid erhielten). Das 1‑Jahres-Programm bestand aus zwei Placebo-kontrollierten Studien sowie zwei Studien mit aktiver Kontrolle (Ipratropiumbromid). Die beiden 6‑Monats-Studien waren sowohl Salmeterol- als auch Placebo-kontrolliert. Untersucht wurden Lungenfunktion und Entwicklung von Dyspnoe, Exazerbationen und gesundheitsbezogener Lebensqualität.
Lungenfunktion
Die einmal tägliche Anwendung von Tiotropiumbromid führte innerhalb von 30 Minuten nach der ersten Dosis zu einer signifikanten Verbesserung der Lungenfunktion (forcierte exspiratorische Einsekundenkapazität [FEV1] und forcierte Vitalkapazität [FVC]), die für die Dauer von 24 Stunden anhielt. Der pharmakodynamische Steady State wurde innerhalb von einer Woche erreicht, wobei die maximale Bronchodilatation im Wesentlichen am dritten Tag beobachtet wurde. Tiotropiumbromid verbesserte signifikant den morgendlichen und abendlichen PEFR (Peak Flow Wert) gemäß den täglichen Aufzeichnungen der Patienten. Die bronchodilatorische Wirkung von Tiotropiumbromid blieb ohne Anzeichen einer Toleranzentwicklung über die 1‑jährige Anwendungsdauer bestehen.
Eine randomisierte, Placebo-kontrollierte klinische Studie an 105 COPD-Patienten zeigte, dass die Bronchodilatation im Vergleich zu Placebo über das 24‑stündige Anwendungsintervall beibehalten wurde, unabhängig davon, ob das Arzneimittel morgens oder abends angewendet wurde.
Klinische Studien (bis zu 12 Monaten)
Dyspnoe, Belastungstoleranz
Tiotropiumbromid verbesserte signifikant die Dyspnoe (ausgewertet mittels Transition Dyspnoea Index). Diese Verbesserung blieb während des gesamten Behandlungszeitraums bestehen.
Der Einfluss von Verbesserungen der Dyspnoe auf die Belastungstoleranz wurde in zwei doppelblinden, randomisierten, Placebo-kontrollierten Studien mit 433 Patienten mit mittlerer bis schwerer COPD untersucht. In diesen Studien verbesserte die 6‑wöchige Behandlung mit SPIRIVA 18 Mikrogramm signifikant die durch Symptome begrenzte Belastungsausdauer während eines Fahrradergometertests mit 75 % der maximalen Arbeitslast um 19,7 % (Studie A) und um 28,3 % (Studie B), verglichen mit Placebo.
Gesundheitsbezogene Lebensqualität
In einer randomisierten, doppelblinden, Placebo-kontrollierten 9‑monatigen klinischen Studie mit 492 Patienten verbesserte SPIRIVA die gesundheitsbezogene Lebensqualität der Patienten signifikant, wie anhand des Gesamtwertes des St. George’s Respiratory Questionnaire (SGRQ) ermittelt wurde. Der Anteil der Patienten, der eine klinisch bedeutsame Verbesserung der Lebensqualität aufwies (d. h. > 4 Einheiten im Gesamtwert des SGRQ), war in der SPIRIVA -Gruppe im Vergleich zur Kontroll-Gruppe um 10,9 Prozentpunkte höher (59,1 % in der SPIRIVA-Gruppe im Vergleich zu 48,2 % in der Kontroll-Gruppe; p = 0,029). Der durchschnittliche Unterschied zwischen den Gruppen war 4,19 Einheiten (p = 0,001; Konfidenzintervall: 1,69‑6,68). Die Verbesserungen in den Subskalen des SGRQ‑Scores betrugen 8,19 Einheiten für „Symptome“, 3,91 Einheiten für „Aktivität“ und 3,61 Einheiten für „Auswirkung auf den Alltag“. Die Verbesserungen in allen diesen Subskalen waren statistisch signifikant.
COPD-Exazerbationen
In einer randomisierten, doppelblinden, Placebo-kontrollierten Studie mit 1.829 Patienten mit mäßiger bis sehr schwerer COPD reduzierte Tiotropiumbromid den Anteil der Patienten mit COPD-Exazerbationen statistisch signifikant (32,2 % vs. 27,8 %). Weiterhin wurde die Anzahl der Exazerbationen um 19 % statistisch signifikant (1,05 vs. 0,85 Exazerbationen pro Patientenjahr) reduziert. Krankenhauseinweisungen aufgrund von COPD-Exazerbationen erfolgten in der Tiotropiumgruppe bei 7,0 % der Patienten und bei 9,5 % der Patienten in der Placebogruppe (p = 0,056); die Anzahl der Krankenhauseinweisungen wegen COPD wurde um 30 % (0,25 vs. 0,18 Ereignisse pro Patientenjahr) verringert.
In einer 1‑jährigen randomisierten, doppelblinden, double-dummy, Parallelgruppen-Studie wurde der Effekt einer Behandlung mit SPIRIVA 18 Mikrogramm einmal täglich mit der Gabe von 50 Mikrogramm Salmeterol (HFA‑Dosieraerosol) zweimal täglich auf die Inzidenz von mittelschweren und schweren Exazerbationen bei 7.376 COPD-Patienten verglichen, die eine Exazerbationsanamnese im vorangegangenen Jahr hatten.
Tabelle 1: Zusammenfassung von Exazerbations-Endpunkten
Endpunkt |
SPIRIVA 18 Mikrogramm (HandiHaler) |
Salmeterol 50 Mikrogramm (HFA-Dosieraerosol) |
Ratio |
p‑Wert |
Zeit (Tage) bis zur ersten Exazerbation † |
187 |
145 |
0,83 |
< 0,001 |
Zeit bis zur ersten schweren (krankenhauspflichtigen) Exazerbation § |
-- |
-- |
0,72 |
< 0,001 |
Patienten mit ≥ 1 Exazerbation, n (%) * |
1.277 (34,4) |
1.414 (38,5) |
0,90 |
< 0,001 |
Patienten mit ≥ 1 schweren (krankenhauspflichtigen) Exazerbation, n (%) * |
262 (7,1) |
336 (9,2) |
0,77 |
< 0,001 |
† Zeit (Tage) bezieht sich auf das 1. Quartil der Patienten. Die „Time to Event“-Analyse wurde mittels des Cox-Proportional-Hazard-Modells mit Zentrum (gepoolt) und Behandlung als Kovariablen durchgeführt; Ratio bezieht sich auf das Hazard Ratio.
§ Die „Time to Event“-Analyse wurde mittels des Cox-Proportional-Hazard-Modells mit Zentrum (gepoolt) und Behandlung als Kovariablen durchgeführt; Ratio bezieht sich auf das Hazard Ratio. Die Zeit (Tage) für das 1. Quartil der Patienten kann nicht berechnet werden, weil der Anteil an Patienten mit schwerer Exazerbation zu gering ist.
* Der Endpunkt „Anzahl der Patienten mit Ereignis“ wurde mittels Cochran-Mantel-Haenszel-Test, stratifiziert nach gepooltem Zentrum, analysiert; Ratio bezieht sich auf das Risk Ratio.
Im Vergleich zu Salmeterol verlängerte SPIRIVA die Zeit bis zur ersten Exazerbation (187 Tage vs. 145 Tage), dies entspricht einer 17 %‑igen Risikoreduktion (Hazard Ratio: 0,83; 95 % Konfidenzintervall (KI): 0,77‑0,90; p < 0,001). SPIRIVA verlängerte auch die Zeit bis zur ersten schweren (krankenhauspflichtigen) Exazerbation (Hazard Ratio: 0,72; 95 % KI: 0,61‑0,85; p < 0,001).
Klinische Langzeitstudien (mehr als 1 Jahr, bis zu 4 Jahren)
In einer randomisierten, doppelblinden, Placebo-kontrollierten 4‑Jahres-Studie mit 5.993 randomisierten Patienten (3.006 mit Placebo und 2.987 mit SPIRIVA behandelt) blieb die aus der Behandlung mit SPIRIVA resultierende Verbesserung des FEV1‑Wertes gegenüber Placebo über die Studiendauer konstant. In der SPIRIVA-Gruppe nahmen anteilig mehr Patienten mindestens 45 Monate lang an der Behandlung teil als in der Placebo-Gruppe (63,8 % vs. 55,4 %; p < 0,001). Der jährliche Abfall des FEV1 war unter Placebo und SPIRIVA vergleichbar. Während der Behandlung mit SPIRIVA verminderte sich das Sterberisiko um 16 %. Todesfälle traten mit einer Inzidenzrate von 4,79 pro 100 Patientenjahre in der Placebo-Gruppe und 4,10 pro 100 Patientenjahre in der Tiotropium-Gruppe auf (Hazard Ratio Tiotropium/Placebo = 0,84; 95 % KI: 0,73‑0,97). Die Behandlung mit Tiotropium verringerte das Risiko eines respiratorischen Versagens (ermittelt aus den unerwünschten Ereignissen) um 19 % (2,09 gegenüber 1,68 Fällen pro 100 Patientenjahren, relatives Risiko Tiotropium/Placebo: 0,81; 95 % KI: 0,65‑0,999).
Aktiv-kontrollierte Tiotropium-Studie
Zum Vergleich der Wirksamkeit und Sicherheit von SPIRIVA HandiHaler und SPIRIVA Respimat wurde eine große randomisierte, doppelblinde, aktiv-kontrollierte Langzeitstudie mit einer Beobachtungsdauer bis zu 3 Jahren durchgeführt. 5.694 Patienten erhielten SPIRIVA HandiHaler, 5.711 Patienten erhielten SPIRIVA Respimat. Die primären Endpunkte waren: Zeit bis zur ersten COPD-Exazerbation, Zeit bis zum Tod (beliebiger Ursache), sowie in einer Substudie mit 906 Patienten die FEV1‑Tiefstwerte vor der nächsten Anwendung.
Die Zeit bis zur ersten COPD-Exazerbation war unter SPIRIVA HandiHaler und unter SPIRIVA Respimat numerisch vergleichbar (Hazard Ratio SPIRIVA HandiHaler/SPIRIVA Respimat: 1,02; 95 % KI: 0,97‑1,08). Die mediane Anzahl der Tage bis zur ersten COPD-Exazerbation betrug bei SPIRIVA HandiHaler 719 Tage und bei SPIRIVA Respimat 756 Tage.
Die bronchodilatatorische Wirkung von SPIRIVA HandiHaler hielt über 120 Wochen an, vergleichbar zum SPIRIVA Respimat. Der mittlere Unterschied im FEV1‑Tiefstwert von SPIRIVA HandiHaler versus SPIRIVA Respimat betrug 0,010 l (95 % KI: ‑0,018 bis +0,038 l).
In der Post-Marketing-Studie TIOSPIR zum Vergleich von SPIRIVA Respimat und SPIRIVA HandiHaler war die Gesamtmortalität, einschließlich Nachverfolgung des Vitalstatus, unter SPIRIVA HandiHaler und unter SPIRIVA Respimat vergleichbar (Hazard Ratio SPIRIVA HandiHaler/SPIRIVA Respimat: 1,04; 95 % KI: 0,91‑1,19).
Kinder und Jugendliche
Die Europäische Arzneimittel-Agentur hat für SPIRIVA eine Freistellung von der Verpflichtung zur Vorlage von Ergebnissen zu Studien in allen pädiatrischen Altersklassen bei COPD und Zystischer Fibrose gewährt (siehe Abschnitt 4.2 bzgl. Informationen zur Anwendung bei Kindern und Jugendlichen).
a) Allgemeine Einleitung
Tiotropiumbromid ist eine nicht-chirale quartäre Ammonium-Verbindung und in Wasser nur schwer löslich. Tiotropiumbromid wird als Pulverinhalation angewendet. Im Allgemeinen wird bei der inhalativen Anwendung der Großteil der abgegebenen Dosis im Verdauungstrakt deponiert und nur in geringerem Maße im Zielorgan Lunge. Ein Großteil der unten beschriebenen pharmakokinetischen Ergebnisse wurde mit Dosen erzielt, die über der empfohlenen therapeutischen Dosis liegen.
b) Allgemeine Charakteristika des Wirkstoffs nach Anwendung des Arzneimittels
Resorption: Die nach Pulverinhalation bei jungen gesunden Probanden gemessene absolute Bioverfügbarkeit von 19,5 % weist auf eine hohe Bioverfügbarkeit des in die Lunge gelangten Anteils hin. Orale Tiotropium-Lösungen weisen eine Bioverfügbarkeit von 2‑3 % auf.
Die maximale Tiotropium-Plasmakonzentration wurde 5‑7 Minuten nach Inhalation beobachtet. Im Steady State betrug der Spitzen-Plasmaspiegel von Tiotropium bei COPD-Patienten 12,9 pg/ml und fiel einem Multikompartiment-Modell folgend schnell ab. Die tiefste Plasmakonzentration im Steady State betrug 1,71 pg/ml.
Die systemische Exposition nach Tiotropium-Inhalation mit dem HandiHaler Inhalator oder mit dem Respimat Inhalator ist vergleichbar.
Verteilung: Die Plasmaproteinbindung von Tiotropium beträgt 72 %, das Verteilungsvolumen 32 l/kg. Örtliche Konzentrationen in der Lunge sind nicht bekannt, jedoch lässt die Anwendungsart wesentlich höhere Werte in der Lunge erwarten. Untersuchungen an Ratten zeigten, dass Tiotropiumbromid die Blut-Hirn-Schranke nicht in einem bedeutenden Maße passiert.
Biotransformation: Das Ausmaß der Metabolisierung ist gering. Dies zeigt sich in der Tatsache, dass 74 % einer intravenösen Dosis bei jungen gesunden Probanden unverändert renal ausgeschieden wird. Der Ester Tiotropiumbromid wird nicht-enzymatisch zu Alkohol (N‑Methylscopin) und Säureverbindung (Dithienylglycolsäure) gespalten, die beide an den Muskarinrezeptoren inaktiv sind. In‑vitro-Untersuchungen an humanen Lebermikrosomen und humanen Hepatozyten weisen darauf hin, dass ein weiterer Teil des Arzneimittels (< 20 % der Dosis nach intravenöser Anwendung) durch Cytochrom-P450 (CYP)-abhängige Oxidation und anschließende Glutathion-Konjugation zu einer Reihe von Phase‑II-Metaboliten metabolisiert wird.
In‑vitro-Untersuchungen an Lebermikrosomen zeigen, dass sich der enzymatische Abbauweg durch die CYP 2D6 (und 3A4)-Inhibitoren Chinidin, Ketoconazol und Gestoden hemmen lässt. Somit sind CYP 2D6 und 3A4 an einem Metabolisierungsweg beteiligt, der für die Eliminierung eines geringeren Teils der Dosis verantwortlich ist. Tiotropiumbromid hemmt auch in übertherapeutischen Dosen CYP 1A1, 1A2, 2B6, 2C9, 2C19, 2D6, 2E1 oder 3A in humanen Lebermikrosomen nicht.
Elimination: Bei COPD-Patienten liegt die effektive Halbwertszeit von Tiotropium zwischen 27 und 45 Stunden. Die Gesamt-Clearance betrug nach intravenöser Anwendung bei jungen gesunden Probanden 880 ml/min. Nach intravenöser Anwendung wird Tiotropium hauptsächlich unverändert mit dem Urin ausgeschieden (74 %). Nach Pulverinhalation bis zum Steady State liegt die Urinausscheidung bei COPD-Patienten in 24 Stunden bei 7 % (1,3 µg) der unveränderten Substanz, der Rest besteht hauptsächlich aus nicht resorbierter Substanz im Darm und wird fäkal ausgeschieden. Die Nierenclearance von Tiotropium liegt über der Creatinin-Clearance, was auf eine Ausscheidung in den Urin hinweist. Nach chronischer einmal täglicher Anwendung bei COPD-Patienten wurde der pharmakokinetische Steady State spätestens nach 7 Tagen erreicht, ohne dass es danach zur Akkumulation kam.
Linearität / Nicht-Linearität: Unabhängig von der Darreichungsform zeigt Tiotropium im therapeutischen Bereich eine lineare Pharmakokinetik.
c) Charakteristika bei Patienten
Ältere Patienten: Wie für alle überwiegend renal ausgeschiedenen Arzneimittel zu erwarten, ging ein fortschreitendes Alter mit einer Abnahme der renalen Tiotropium-Clearance (365 ml/min bei COPD-Patienten < 65 Jahre bis 271 ml/min bei COPD-Patienten ≥ 65 Jahre) einher. Dies führte jedoch nicht zu einem entsprechenden Anstieg der AUC0-6,ss- oder Cmax,ss-Werte.
Patienten mit eingeschränkter Nierenfunktion: Die einmal tägliche Inhalation von Tiotropium bis zum Steady State führte bei COPD-Patienten mit leichter Nierenfunktionsstörung (Creatinin-Clearance 50‑80 ml/min) zu leicht erhöhten AUC0-6,ss-Werten (1,8‑30 % höher) und ähnlichen Cmax,ss-Werten, verglichen mit COPD-Patienten mit normaler Nierenfunktion (Creatinin-Clearance > 80 ml/min).
Bei COPD-Patienten mit mittlerer bis schwerer Nierenfunktionsstörung (Creatinin-Clearance < 50 ml/min) verdoppelte sich die Gesamtexposition nach intravenöser Applikation von Tiotropium (82 % höhere AUC0‑4h und 52 % höhere Cmax), verglichen mit COPD-Patienten mit normaler Nierenfunktion. Dies wurde durch die Plasmakonzentrationen nach Pulverinhalation bestätigt.
Patienten mit eingeschränkter Leberfunktion: Ein relevanter Einfluss auf die Pharmakokinetik von Tiotropium im Fall einer Leberfunktionsstörung ist nicht zu erwarten. Tiotropium wird hauptsächlich renal ausgeschieden (74 % bei jungen gesunden Probanden) und durch eine einfache nicht-enzymatische Esterspaltung zu pharmakologisch inaktiven Produkten abgebaut.
Japanische COPD-Patienten: In einem Studienquervergleich war die mittlere Spitzen-Plasmakonzentration von Tiotropium, 10 Minuten nach Inhalation, im Steady State bei japanischen COPD-Patienten 20‑70 % höher als bei COPD-Patienten kaukasischer Herkunft. Es gab jedoch keine Anzeichen für eine höhere Mortalität oder ein höheres kardiales Risiko bei japanischen Patienten, verglichen mit Patienten kaukasischer Herkunft. Für andere ethnische Gruppen sind die pharmakokinetischen Daten unzureichend.
Kinder und Jugendliche: Siehe Abschnitt 4.2.
d) Pharmakokinetische/pharmakodynamische Zusammenhänge
Es gibt keinen direkten Zusammenhang zwischen Pharmakokinetik und Pharmakodynamik.
Zahlreiche, in konventionellen Studien zur Sicherheitspharmakologie, zur Toxizität bei wiederholter Anwendung und zur Reproduktionstoxizität beobachtete Wirkungen lassen sich durch die anticholinergen Eigenschaften von Tiotropiumbromid erklären. Bei Tieren wurden typischerweise reduzierte Futteraufnahme, gehemmte Gewichtszunahme, trockener Mund und Nase, verminderte Tränen- und Speichelsekretion, Mydriasis und Zunahme der Herzfrequenz beobachtet. Weitere relevante Wirkungen, die in Studien zur Toxizität bei wiederholter Anwendung beobachtet wurden, waren: leichte Reizung der Atemwege bei Ratten und Mäusen, die sich in Rhinitis und Epitheländerungen der Nasenhöhle und des Kehlkopfes zeigte, sowie Prostatitis mit proteinreichen Ablagerungen und Lithiasis in der Blase bei Ratten.
Schädigungen hinsichtlich Schwangerschaft, embryonaler/fetaler Entwicklung, Geburt oder postnataler Entwicklung konnten nur für maternal toxische Dosisbereiche nachgewiesen werden. Tiotropiumbromid zeigte bei Ratten oder Kaninchen keine teratogenen Wirkungen.
In einer Studie zur allgemeinen Reproduktion und Fertilität an Ratten ergaben sich bei keiner Dosierung Hinweise auf unerwünschte Effekte auf die Fertilität oder das Paarungsverhalten, weder bei den behandelten Elterntieren noch bei ihren Nachkommen.
Die respiratorischen (Reizungen) und urogenitalen (Prostatitis) Veränderungen sowie die Reproduktionstoxizität wurden nach lokalen oder systemischen Expositionen beobachtet, die mehr als das 5‑fache der therapeutischen Exposition beim Menschen betrugen. Untersuchungen zur Genotoxizität und zum kanzerogenen Potenzial ließen keine besonderen Gefahren für den Menschen erkennen.
Lactose-Monohydrat (kann geringe Mengen an Milchproteinen enthalten)
Nicht zutreffend.
2 Jahre
Kapseln nach dem ersten Öffnen der Blisterpackung in den folgenden 9 Tagen anwenden.
Entsorgen Sie bitte den HandiHaler Inhalator 12 Monate nach dem ersten Gebrauch.
Nicht über 25 °C lagern.
Nicht einfrieren.
Abziehbare Aluminium/PVC/Aluminium-Blisterpackungen mit jeweils 10 Kapseln.
Der HandiHaler ist ein Pulverinhalator zur Inhalation von Einzeldosen, der aus Acrylnitril-Butadien-Styrol (ABS) Kunststoff und rostfreiem Stahl besteht. Die Kapselkammer besteht aus Methylmethacrylat-Acrylnitril-Butadien-Styrol (MABS) oder Polycarbonat (PC) Kunststoff.
Packungsgrößen:
Faltschachtel mit 30 Kapseln (3 Blisterpackungen)
Faltschachtel mit 60 Kapseln (6 Blisterpackungen)
Faltschachtel mit 90 Kapseln (9 Blisterpackungen)
Kombinationspackung mit 30 Kapseln (3 Blisterpackungen) und 1 HandiHaler Inhalator
Klinikpackung: Bündelpackung mit 5 Faltschachteln zu je 60 Kapseln
Der HandiHaler Inhalator ist auch einzeln verpackt in einer Faltschachtel erhältlich.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu beseitigen.
Boehringer Ingelheim International GmbH
Binger Str. 173
55216 Ingelheim am Rhein
Deutschland
Örtlicher Vertreter
Boehringer Ingelheim Pharma GmbH & Co. KG
Binger Str. 173
55216 Ingelheim am Rhein
Tel.: 0 800 / 77 90 900
Fax: 0 61 32 / 72 99 99
E‑Mail: info@boehringer-ingelheim.de
52523.00.00
Datum der Erteilung der Zulassung: 21.05.2002
Datum der letzten Verlängerung der Zulassung: 17.01.2017
November 2025
Verschreibungspflichtig