Zelboraf® 240 mg Filmtabletten
Jede Tablette enthält 240 mg Vemurafenib (als Kopräzipitat von Vemurafenib und Hypromelloseacetatsuccinat).
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
Filmtablette (Tablette).
Hellrosa bis hellorange, ovale, bikonvexe, ca. 19 mm lange Filmtabletten mit der Prägung „VEM“ auf einer Seite.
Vemurafenib ist angezeigt als Monotherapie zur Behandlung von erwachsenen Patienten mit BRAF‑V600 Mutation‑positivem nicht resezierbarem oder metastasiertem Melanom (siehe Abschnitt 5.1).
Die Behandlung mit Vemurafenib soll von einem qualifizierten, in der Anwendung von antineoplastischen Arzneimitteln erfahrenen Arzt eingeleitet und überwacht werden.
Vor der Einnahme von Vemurafenib muss bei Patienten ein BRAF‑V600 Mutation‑positiver Tumorstatus durch einen validierten Test nachgewiesen worden sein (siehe Abschnitte 4.4 und 5.1).
Dosierung
Die empfohlene Dosis von Vemurafenib beträgt 960 mg (4 Tabletten à 240 mg) zweimal täglich (entsprechend einer Tagesgesamtdosis von 1 920 mg). Vemurafenib kann mit oder ohne Nahrung eingenommen werden, aber eine dauerhafte Einnahme beider täglicher Dosen auf leeren Magen sollte vermieden werden (siehe Abschnitt 5.2).
Dauer der Behandlung
Die Behandlung mit Vemurafenib soll bis zur Krankheitsprogression oder bis zum Auftreten inakzeptabler Toxizitäten fortgeführt werden (siehe Tabellen 1 und 2).
Vergessene Dosen
Eine vergessene Dosis kann bis zu 4 Stunden vor der nächsten Dosis eingenommen werden, um das zweimal tägliche Einnahmeschema beizubehalten. Beide Dosen sollen nicht zeitgleich eingenommen werden.
Erbrechen
Bei Erbrechen nach Gabe von Vemurafenib soll der Patient keine zusätzliche Dosis des Arzneimittels einnehmen, sondern die Behandlung wie gewohnt fortsetzen.
Dosisanpassungen
Die Behandlung von Nebenwirkungen oder einer QTc-Verlängerung kann eine Dosisreduktion, eine vorübergehende Unterbrechung und/oder einen Behandlungsabbruch erforderlich machen (siehe Tabellen 1 und 2). Dosisanpassungen auf eine Dosis von weniger als 480 mg zweimal täglich werden nicht empfohlen.
Für den Fall, dass der Patient ein kutanes Plattenepithelkarzinom (cuSCC) entwickelt, wird empfohlen, die Behandlung ohne Veränderung der Vemurafenib‑Dosis fortzuführen (siehe Abschnitte 4.4 und 4.8).
Tabelle 1: Schema für die Dosisanpassung, basierend auf dem Grad der Nebenwirkungen
Grad (CTC-AE) (a) |
Empfohlene Dosisanpassung |
Grad 1 oder Grad 2 (tolerierbar) |
Vemurafenib-Dosierung von 960 mg zweimal täglich beibehalten. |
Grad 2 (nicht tolerierbar) oder Grad 3 |
|
Erstes Auftreten von Grad-2- oder |
Unterbrechung der Behandlung, bis Grad 0 – 1 vorliegt. Wiederaufnahme der Dosierung mit 720 mg zweimal täglich (oder 480 mg zweimal täglich, wenn die Dosis bereits reduziert wurde). |
Zweites Auftreten von Grad-2- |
Unterbrechung der Behandlung bis Grad 0 – 1 vorliegt. Wiederaufnahme der Dosierung mit 480 mg zweimal täglich (oder dauerhaftes Abbrechen, wenn die Dosis bereits auf 480 mg zweimal täglich reduziert wurde). |
Drittes Auftreten von Grad-2- |
Behandlung dauerhaft abbrechen. |
Grad 4 |
|
Erstes Auftreten von Grad-4-Nebenwirkungen |
Behandlung dauerhaft abbrechen oder unterbrechen, bis Grad 0 – 1 vorliegt. |
Zweites Auftreten von Grad-4-Nebenwirkungen oder Fortbestehen von Grad-4-Nebenwirkungen nach der ersten Dosisreduktion |
Behandlung dauerhaft abbrechen. |
(a) Die Intensität klinischer Nebenwirkungen klassifiziert durch die Common Terminology Criteria for Adverse Events v4.0 (CTC-AE).
Eine expositionsabhängige QTc-Verlängerung wurde in einer unkontrollierten, offenen Phase-II-Studie bei vorbehandelten Patienten mit metastasiertem Melanom beobachtet. Die Behandlung einer QTc-Verlängerung kann bestimmte Überwachungsmaßnahmen erfordern (siehe Abschnitt 4.4).
Tabelle 2: Schema für die Dosisanpassung, basierend auf dem QT-Intervall
QTc‑Wert |
Empfohlene Dosisanpassung |
QTc > 500 ms (Ausgangswert) |
Behandlung nicht empfohlen. |
Anstieg der QTc einerseits auf > 500 ms und andererseits Abweichung von > 60 ms zu den Werten vor der Behandlung |
Behandlung dauerhaft abbrechen. |
Erstes Auftreten von QTc > 500 ms während der Behandlung und Fortbestehen der Abweichung von < 60 ms zu den Werten vor der Behandlung |
Vorübergehende Unterbrechung der Behandlung, bis QTc unter 500 ms sinkt. |
Zweites Auftreten von QTc > 500 ms während der Behandlung und Fortbestehen der Abweichung von < 60 ms zu den Werten vor der Behandlung |
Vorübergehende Unterbrechung der Behandlung, bis QTc unter 500 ms sinkt. |
Drittes Auftreten von QTc > 500 ms während der Behandlung und Fortbestehen der Abweichung von < 60 ms zu den Werten vor der Behandlung |
Behandlung dauerhaft abbrechen. |
Besondere Patientengruppen
Ältere Patienten
Bei Patienten im Alter von > 65 Jahren ist keine spezielle Dosisanpassung erforderlich.
Nierenfunktionsstörungen
Bei Patienten mit Nierenfunktionsstörungen liegen begrenzte Daten vor. Bei Patienten mit schweren Nierenfunktionsstörungen kann das Risiko einer erhöhten Exposition nicht ausgeschlossen werden. Patienten mit schwerer Nierenfunktionsstörung sollen engmaschig überwacht werden (siehe Abschnitte 4.4 und 5.2).
Leberfunktionsstörungen
Bei Patienten mit Leberfunktionsstörungen liegen begrenzte Daten vor. Da Vemurafenib über die Leber ausgeschieden wird, können Patienten mit mittleren bis schweren Leberfunktionsstörungen eine erhöhte Exposition haben und sollen engmaschig überwacht werden (siehe Abschnitte 4.4 und 5.2).
Kinder und Jugendliche
Die Sicherheit und Wirksamkeit von Vemurafenib bei Kindern und Jugendlichen unter 18 Jahren ist bisher nicht erwiesen. Zurzeit vorliegende Daten werden in den Abschnitten 4.8, 5.1 und 5.2 beschrieben; eine Dosierungsempfehlung kann jedoch nicht gegeben werden.
Nicht-kaukasische Patienten
Die Sicherheit und Wirksamkeit von Vemurafenib bei nicht-kaukasischen Patienten ist nicht erwiesen. Es liegen keine Daten vor.
Art der Anwendung
Vemurafenib ist zum Einnehmen. Die Tabletten müssen als Ganzes und mit Wasser geschluckt werden. Sie dürfen nicht zerkaut oder zerdrückt werden.
Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
Bevor mit der Anwendung von Vemurafenib begonnen wird, muss für die Patienten ein durch einen validierten Test bestätigter BRAF‑V600 Mutation‑positiver Tumorstatus vorliegen. Die Wirksamkeit und Sicherheit von Vemurafenib wurden bei Patienten mit Tumoren, die seltene BRAF‑V600 Mutationen, andere als V600E und V600K, exprimieren, nicht ausreichend untersucht (siehe Abschnitt 5.1). Vemurafenib soll bei Patienten mit malignem Melanom vom BRAF‑Wildtyp nicht angewendet werden.
Überempfindlichkeitsreaktionen
Schwerwiegende Überempfindlichkeitsreaktionen, darunter Anaphylaxie, sind in Verbindung mit Vemurafenib berichtet worden (siehe Abschnitte 4.3 und 4.8). Schwere Überempfindlichkeitsreaktionen können Stevens‑Johnson‑Syndrom, generalisierten Ausschlag, Erythem oder Hypotonie mit einschließen. Bei Patienten mit schweren Überempfindlichkeitsreaktionen soll die Behandlung mit Vemurafenib dauerhaft abgebrochen werden.
Dermatologische Reaktionen
In der klinischen Pivotalstudie wurden bei Patienten unter Vemurafenib‑Behandlung schwere dermatologische Reaktionen berichtet, einschließlich seltener Fälle des Stevens‑Johnson‑Syndroms und toxische epidermale Nekrolyse. Nach der Markteinführung wurden unter der Anwendung von Vemurafenib Fälle von Arzneimittelausschlag mit Eosinophilie und systemischen Symptomen (DRESS-Syndrom) berichtet (siehe Abschnitt 4.8). Bei Patienten, bei denen eine schwere dermatologische Nebenwirkung auftritt, soll die Behandlung mit Vemurafenib dauerhaft abgebrochen werden.
Potenzierung von Strahlenschäden
Bei Patienten, die vor, während oder unmittelbar nach der Behandlung mit Vemurafenib eine Strahlentherapie erhielten, wurden Fälle von Radiation-Recall und Strahlensensibilisierung berichtet. Die meisten Fälle betrafen die Haut, aber einige Fälle mit Beteiligung viszeraler Organe hatten einen tödlichen Verlauf (siehe Abschnitte 4.5 und 4.8).
Vemurafenib sollte bei gleichzeitiger oder sequenzieller Strahlentherapie mit Vorsicht angewendet werden.
QT-Verlängerung
In einer unkontrollierten, offenen Phase‑II-Studie mit zuvor behandelten Patienten mit metastasiertem Melanom sind expositionsabhängige QT‑Verlängerungen beobachtet worden (siehe Abschnitt 4.8). Eine QT‑Verlängerung kann zu einem erhöhten Risiko ventrikulärer Arrhythmien, einschließlich Torsade de pointes, führen. Eine Behandlung mit Vemurafenib wird nicht empfohlen bei Patienten mit nicht behebbaren Störungen des Elektrolythaushalts (einschließlich Magnesium), Long‑QT‑Syndrom oder bei Patienten, die Arzneimittel einnehmen, die bekanntermaßen das QT‑Intervall verlängern.
Vor einer Behandlung mit Vemurafenib, nach einem Monat der Behandlung und nach einer Dosisänderung müssen bei allen Patienten das Elektrokardiogramm (EKG) und die Elektrolyte (einschließlich Magnesium) überwacht werden. Während der ersten drei Behandlungsmonate werden, insbesondere bei Patienten mit mittlerer bis schwerer Leberfunktionsstörung, weitere Überwachungen monatlich empfohlen, danach alle drei Monate oder, je nach klinischer Indikation, öfter. Bei Patienten mit einer QTc > 500 Millisekunden (ms) wird ein Behandlungsbeginn mit Vemurafenib nicht empfohlen. Falls die QTc während der Behandlung 500 ms übersteigt, soll die Behandlung mit Vemurafenib vorübergehend unterbrochen, Störungen des Elektrolythaushalts (einschließlich Magnesium) korrigiert und kardiale Risikofaktoren für eine QT‑Verlängerung (wie z. B. kongestive Herzinsuffizienz, Bradyarrhythmien) kontrolliert werden. Sobald die QTc unter 500 ms sinkt, soll die Behandlung mit einer niedrigeren Dosis, wie in Tabelle 2 beschrieben, wieder aufgenommen werden. Ein dauerhafter Abbruch der Vemurafenib-Behandlung wird empfohlen, wenn die QTc sowohl auf Werte > 500 ms steigt als auch > 60 ms von den Werten vor der Behandlung abweicht.
Ophthalmologische Reaktionen
Schwere ophthalmologische Reaktionen, einschließlich Uveitis, Iritis und retinaler Venenverschluss, sind berichtet worden. Die Patienten sollen routinemäßig auf ophthalmologische Reaktionen überwacht werden.
Kutanes Plattenepithelkarzinom (cuSCC)
Bei mit Vemurafenib behandelten Patienten sind Fälle von cuSCC berichtet worden (darunter solche, die als Keratoakanthom oder gemischter Keratoakanthom-Subtyp klassifiziert werden) (siehe Abschnitt 4.8).
Es wird empfohlen, bei allen Patienten vor Beginn der Therapie eine dermatologische Untersuchung durchzuführen und sie im Verlauf der Behandlung routinemäßig zu überwachen. Jede verdächtige Hautläsion soll operativ entfernt, zur dermatopathologischen Untersuchung eingeschickt und nach lokalem Pflegestandard behandelt werden. Der verschreibende Arzt soll den Patienten während und bis zu 6 Monate nach der Behandlung monatlich auf cuSCC untersuchen. Bei Patienten, die cuSCC entwickeln, wird empfohlen, die Behandlung ohne Dosisanpassung fortzuführen. Die Überwachung soll nach Beendigung der Behandlung mit Vemurafenib noch 6 Monate oder bis zur Einleitung einer anderen antineoplastischen Therapie fortgeführt werden. Die Patienten sollen angewiesen werden, ihre Ärzte über das Auftreten jeglicher Hautveränderungen zu informieren.
Nicht‑kutanes Plattenepithelkarzinom (nicht‑cuSCC)
Fälle von nicht-cuSCC sind in klinischen Studien berichtet worden, in denen Patienten Vemurafenib erhalten haben. Patienten sollen vor Behandlungsbeginn und alle 3 Monate im Verlauf der Behandlung einer Kopf- und Halsuntersuchung unterzogen werden, die mindestens eine visuelle Überprüfung der Mundschleimhaut und das Abtasten der Lymphknoten beinhaltet. Außerdem soll bei den Patienten vor der Behandlung und alle 6 Monate im Verlauf der Behandlung eine Computertomographie (CT) des Thorax durchgeführt werden.
Anale Untersuchungen und Untersuchungen des Beckens (bei Frauen) werden vor und bei Beendigung der Behandlung oder wenn klinisch indiziert empfohlen.
Nach Beendigung der Behandlung mit Vemurafenib soll die Überwachung auf nicht‑cuSCC bis zu 6 Monate oder bis zur Einleitung einer anderen antineoplastischen Therapie fortgesetzt werden. Abnorme Befunde sollen gemäß klinischer Praxis behandelt werden.
Neue primäre Melanome
In klinischen Studien wurden neue Fälle von primären Melanomen berichtet. Diese Fälle wurden durch Exzision behandelt und die Patienten setzten die Behandlung ohne Dosisanpassung fort. Eine Überwachung auf Hautläsionen soll, wie weiter oben für das kutane Plattenepithelkarzinom beschrieben, erfolgen.
Andere Tumore
Vemurafenib kann aufgrund seines Wirkmechanismus eine Progression von Krebserkrankungen verursachen, die mit RAS-Mutationen in Verbindung stehen (siehe Abschnitt 4.8). Bei Patienten mit einer vorherigen oder gleichzeitig bestehenden Krebserkrankung, die mit einer RAS-Mutation in Verbindung steht, müssen Nutzen und Risiken vor der Anwendung von Vemurafenib sorgfältig abgewogen werden.
Pankreatitis
Bei mit Vemurafenib behandelten Patienten wurde von Pankreatitis berichtet. Ungeklärte Abdominalschmerzen sollten daher umgehend untersucht werden (einschließlich Messung von Amylase und Lipase im Serum). Patienten, die die Behandlung mit Vemurafenib nach einer Pankreatitis wieder aufnehmen, sollten engmaschig überwacht werden.
Leberschädigung
Unter der Behandlung mit Vemurafenib wurden Leberschäden, darunter Fälle von schweren Leberschäden, berichtet (siehe Abschnitt 4.8). Leberenzyme (Transaminasen und alkalische Phosphatase) und Bilirubin sollen vor Behandlungsbeginn gemessen und während der Behandlung jeden Monat, oder je nach klinischer Indikation, überwacht werden. Auffällige Laborwerte sollen durch Dosisreduktion, Behandlungsunterbrechung oder Behandlungsabbruch behandelt werden (siehe Abschnitte 4.2 und 4.8).
Nierenschäden
Unter der Anwendung von Vemurafenib wurden Nierenschäden berichtet, die von Erhöhungen der Serum-Kreatininwerte bis zu akuter interstitieller Nephritis und akuter tubulärer Nekrose reichten. Die Serum-Kreatininwerte sollen vor Behandlungsbeginn gemessen und während der Behandlung, je nach klinischer Indikation, überwacht werden (siehe Abschnitte 4.2 und 4.8).
Leberfunktionsstörung
Bei Patienten mit Leberfunktionsstörung ist keine Anpassung der Anfangsdosis notwendig. Patienten mit durch Lebermetastasen bedingter leichter Leberfunktionsstörung ohne Hyperbilirubinämie können nach den allgemeinen Empfehlungen überwacht werden. Bei Patienten mit mäßiger bis schwerer Leberfunktionsstörung liegen nur sehr begrenzte Daten vor. Patienten mit mäßiger bis schwerer Leberfunktionsstörung können eine erhöhte Exposition haben (siehe Abschnitt 5.2). Eine engmaschige Überwachung ist daher insbesondere nach den ersten Behandlungswochen erforderlich, da eine Akkumulation über einen verlängerten Zeitraum (mehrere Wochen) auftreten kann. Zusätzlich wird während der ersten drei Monate empfohlen, jeden Monat eine Überwachung mittels EKG durchzuführen.
Nierenfunktionsstörung
Bei Patienten mit leichter oder mäßiger Nierenfunktionsstörung ist keine Anpassung der Anfangsdosis notwendig. Bei Patienten mit schwerer Nierenfunktionsstörung liegen nur begrenzte Daten vor (siehe Abschnitt 5.2). Vemurafenib soll bei Patienten mit schweren Nierenfunktionsstörungen nur mit Vorsicht angewendet werden und die Patienten sollen engmaschig überwacht werden.
Lichtempfindlichkeit
Bei Patienten, die Vemurafenib in klinischen Studien erhielten, wurde leichte bis schwere Lichtempfindlichkeit berichtet (siehe Abschnitt 4.8). Alle Patienten sollen angewiesen werden, während der Einnahme von Vemurafenib Sonnenexposition zu vermeiden. Während der Einnahme des Arzneimittels sollen Patienten dazu angehalten werden, schützende Kleidung zu tragen und eine Sonnencreme mit hohem UVA/UVB-Lichtschutzfaktor sowie einen Lippenschutz (Lichtschutzfaktor ≥ 30) zu verwenden, um sich im Freien gegen Sonnenbrand zu schützen.
Bei Grad 2 (nicht tolerierbarer) oder höherer Lichtempfindlichkeit werden Dosisanpassungen empfohlen (siehe Abschnitt 4.2).
Dupuytren-Kontraktur und Fibromatose der Plantarfaszie (Morbus Ledderhose)
Unter Anwendung von Vemurafenib wurde das Auftreten von Dupuytren-Kontraktur und Fibromatose der Plantarfaszie (Morbus Ledderhose) berichtet. Dabei handelte es sich mehrheitlich um leichte bis mittelschwere Fälle, jedoch wurden auch schwere, bis hin zur Behinderung führende Verlaufsformen der Dupuytren-Kontraktur berichtet (siehe Abschnitt 4.8).
Die Ereignisse sind durch Dosisreduktion, Therapieunterbrechung oder Absetzen der Therapie zu behandeln (siehe Abschnitt 4.2).
Wirkungen von Vemurafenib auf andere Arzneimittel
Vemurafenib kann die Plasmaverfügbarkeit von vorwiegend über CYP1A2 metabolisierten Arzneimitteln erhöhen und die Plasmaverfügbarkeit von vorwiegend über CYP3A4 metabolisierten Arzneimitteln verringern. Die gleichzeitige Anwendung von Vemurafenib und Wirkstoffen, die über CYP1A2 und CYP3A4 metabolisiert werden und eine geringe therapeutische Breite aufweisen, wird nicht empfohlen. Dosisanpassungen für vorwiegend über CYP1A2 oder CYP3A4 metabolisierte Arzneimittel sollen auf Grundlage der jeweiligen therapeutischen Fenster vor der gleichzeitigen Behandlung mit Vemurafenib in Betracht gezogen werden (siehe Abschnitte 4.5 und 4.6).
Bei gleichzeitiger Gabe von Vemurafenib und Warfarin ist Vorsicht geboten und ein zusätzliches INR (International Normalized Ratio)-Monitoring zu erwägen.
Vemurafenib kann die Plasmaverfügbarkeit von Arzneimitteln erhöhen, die zu den P-gp-Substraten gehören. Vorsicht ist daher geboten, wenn Vemurafenib gleichzeitig mit P-gp-Substraten angewendet wird. Eine Dosisreduktion und/oder eine zusätzliche Überwachung der Blutspiegel von Arzneimitteln, die P-gp-Substrate mit einem niedrigen therapeutischen Index (NTI) sind (z. B. Digoxin, Dabigatranetexilat, Aliskiren), sollte in Erwägung gezogen werden, wenn diese Arzneimittel gleichzeitig mit Vemurafenib angewendet werden (siehe Abschnitt 4.5).
Wirkung anderer Arzneimittel auf Vemurafenib
Die gleichzeitige Gabe von potenten Induktoren von CYP3A4, P-gp und einer Glucuronidierung (z. B. Rifampicin, Rifabutin, Carbamazepin, Phenytoin oder Johanniskraut [Hypericin]) könnte zu einer verminderten Exposition von Vemurafenib führen und sollte nach Möglichkeit vermieden werden (siehe Abschnitt 4.5). Eine alternative Behandlung mit weniger induzierendem Potenzial sollte zur Erhaltung der Wirksamkeit von Vemurafenib in Betracht gezogen werden. Bei der gleichzeitigen Gabe von Vemurafenib und potenten CYP3A4- bzw. P-gp-Inhibitoren ist Vorsicht geboten. Es muss eine sorgfältige Sicherheitsüberwachung der Patienten erfolgen und, wenn klinisch indiziert, die Dosis angepasst werden (siehe Tabelle 1 in Abschnitt 4.2).
Gleichzeitige Anwendung mit Ipilimumab
In einer Phase-I-Studie wurden bei gleichzeitiger Anwendung von Ipilimumab (3 mg/kg) und Vemurafenib (960 mg zweimal täglich oder 720 mg zweimal täglich) asymptomatische Erhöhungen 3. Grades von Transaminasen (ALT/AST > 5 x ULN) und Bilirubin (Gesamtbilirubin > 3 x ULN) berichtet. Basierend auf diesen vorläufigen Daten wird die gleichzeitige Anwendung von Ipilimumab und Vemurafenib nicht empfohlen.
Wirkungen von Vemurafenib auf Wirkstoff-metabolisierende Enzyme
Die Ergebnisse einer in vivo durchgeführten Arzneimittel-Interaktionsstudie bei Patienten mit metastasiertem Melanom zeigten, dass Vemurafenib ein moderater CYP1A2-Inhibitor und CYP3A4-Induktor ist.
Die gleichzeitige Anwendung von Vemurafenib und Wirkstoffen, die über CYP1A2 metabolisiert werden und die eine geringe therapeutische Breite aufweisen (z. B. Agomelatin, Alosetron, Duloxetin, Melatonin, Ramelteon, Tacrin, Tizanidin, Theophyllin), wird nicht empfohlen. Kann eine gleichzeitige Anwendung nicht vermieden werden, sollte mit Vorsicht vorgegangen werden, da Vemurafenib die Plasmaexposition von Wirkstoffen, die CYP1A2-Substrate sind, erhöhen kann. Falls klinisch indiziert, kann eine Dosisreduktion bei der begleitenden Behandlung mit dem CYP1A2-Substrat-Arzneimittel in Betracht gezogen werden. Die gleichzeitige Anwendung von Vemurafenib erhöhte die Plasmaexposition (AUC) von Koffein (CYP1A2-Substrat) um das 2,6-Fache. In einer weiteren klinischen Studie führte Vemurafenib nach einer 2-mg-Einzeldosis Tizanidin (ein CYP1A2-Substrat) zu einem ungefähr 2,2‑fachen bzw. 4,7‑fachen Anstieg der Cmax und der AUC von Tizanidin.
Die gleichzeitige Anwendung von Vemurafenib und Wirkstoffen, die über CYP3A4 metabolisiert werden und eine geringe therapeutische Breite aufweisen, wird nicht empfohlen. Kann eine gleichzeitige Gabe nicht vermieden werden, muss berücksichtigt werden, dass Vemurafenib die Plasmakonzentration von CYP3A4-Substraten verringern und dadurch deren Wirksamkeit beeinträchtigen kann. Aus diesem Grund könnte die Wirksamkeit von Kontrazeptiva, die über CYP3A4 metabolisiert und gleichzeitig mit Vemurafenib angewendet werden, verringert sein. Dosisanpassungen von CYP3A4-Substraten mit engem therapeutischen Fenster können in Betracht gezogen werden, sofern klinisch indiziert (siehe Abschnitte 4.4 und 4.6). In einer klinischen Studie verringerte die gleichzeitige Gabe von Vemurafenib die AUC von Midazolam (CYP3A4-Substrat) um durchschnittlich 39 % (maximaler Abfall bis zu 80 %).
In vitro wurde bei einer Vemurafenib-Konzentration von 10 µM eine leichte Induktion von CYP2B6 beobachtet. Derzeit ist nicht bekannt, ob Vemurafenib bei einem Plasmaspiegel von 100 µM, der bei Patienten im Steady State (ungefähr 50 µg/ml) beobachtet wurde, möglicherweise die Plasmakonzentrationen von gleichzeitig angewendeten CYP2B6-Substraten, wie z. B. Bupropion, verringert.
Die gleichzeitige Gabe von Vemurafenib führte zu einer 18%igen Erhöhung der AUC von S-Warfarin (CYP2C9-Substrat). Bei gleichzeitiger Gabe von Vemurafenib und Warfarin ist Vorsicht geboten und eine zusätzliche INR (international normalized ratio)-Überwachung zu erwägen (siehe Abschnitt 4.4).
Vemurafenib bewirkte in vitro eine moderate CYP2C8-Inhibition. Die in-vivo-Relevanz dieses Ergebnisses ist nicht bekannt, aber ein Risiko für eine klinisch relevante Wirkung auf gleichzeitig verabreichte Substrate von CYP2C8 kann nicht ausgeschlossen werden. Bei gleichzeitiger Anwendung von CYP2C8-Substraten mit geringer therapeutischer Breite ist Vorsicht geboten, da Vemurafenib deren Plasmakonzentrationen erhöhen kann.
Da Vemurafenib eine lange Halbwertszeit hat, kann die komplette inhibitorische Wirkung auf ein gleichzeitig angewendetes Arzneimittel möglicherweise erst nach einer 8-tägigen Behandlung mit Vemurafenib beobachtet werden.
Nach Beendigung der Behandlung mit Vemurafenib kann eine Auswaschzeit von mindestens 8 Tagen nötig sein, um Wechselwirkungen mit einer nachfolgenden Behandlung zu vermeiden.
Strahlentherapie
Bei Patienten, die mit Vemurafenib behandelt wurden, wurde eine Potenzierung von Strahlentherapieschäden berichtet (siehe Abschnitte 4.4 und 4.8). In den meisten Fällen erhielten die Patienten Strahlentherapie-Dosen größer oder gleich 2 Gy/Tag (hypofraktionierte Schemata).
Wirkungen von Vemurafenib auf Wirkstoff‑Transportsysteme
In in vitro‑Studien wurde nachgewiesen, dass Vemurafenib ein Inhibitor der Efflux-Transporter P‑Glykoprotein (P‑gp) und Breast Cancer Resistance Protein (BCRP) ist.
Eine klinische Wechselwirkungsstudie zeigte, dass mehrfach oral verabreichte Dosen von Vemurafenib (960 mg zweimal täglich) die Exposition einer oralen Einzeldosis des P‑gp‑Substrats Digoxin erhöhten. AUClast und Cmax von Digoxin waren ca. 1,8- bzw. 1,5‑fach erhöht.
Vemurafenib sollte in Kombination mit P‑gp‑Substraten (z. B. Aliskiren, Ambrisentan, Colchicin, Dabigatranetexilat, Digoxin, Everolimus, Fexofenadin, Lapatinib, Maraviroc, Nilotinib, Posaconazol, Ranolazin, Sirolimus, Sitagliptin, Talinolol, Topotecan) mit Vorsicht angewendet werden und eine Dosisreduktion des begleitenden Arzneimittels kann erwogen werden, sofern dies klinisch indiziert ist. Eine zusätzliche Überwachung der Blutspiegel sollte für P‑gp‑Substrate mit einem niedrigen therapeutischen Index (NTI) in Erwägung gezogen werden (z. B. Digoxin, Dabigatranetexilat, Aliskiren) (siehe Abschnitt 4.4).
Die Wirkungen von Vemurafenib auf Arzneimittel, die BCRP-Substrate sind, sind unbekannt. Es kann nicht ausgeschlossen werden, dass Vemurafenib die Exposition von Wirkstoffen erhöhen kann, die über BCRP transportiert werden (z. B. Methotrexat, Mitoxantron, Rosuvastatin). Viele Arzneimittel gegen Krebs sind BCRP-Substrate und daher besteht ein theoretisches Risiko für eine Wechselwirkung mit Vemurafenib.
Die mögliche Wirkung von Vemurafenib auf andere Transporter ist zurzeit nicht bekannt.
Wirkungen gleichzeitig angewendeter Arzneimittel auf Vemurafenib
In vitro‑Studien deuten darauf hin, dass der CYP3A4‑Metabolismus und die Glucuronidierung für die Metabolisierung von Vemurafenib verantwortlich sind. Die biliäre Exkretion scheint ein weiterer wesentlicher Eliminierungsweg zu sein. In vitro‑Studien haben gezeigt, dass Vemurafenib ein Substrat der Efflux-Transporter P-gp und BCRP ist. Es ist derzeit nicht bekannt, ob Vemurafenib auch ein Substrat anderer Transportproteine ist. Die gleichzeitige Gabe starker CYP3A4-Inhibitoren oder
-Induktoren oder Inhibitoren/Induktoren der Transportprotein-Aktivität kann die Plasmakonzentrationen von Vemurafenib verändern.
Die gleichzeitige Anwendung von Itraconazol, einem potenten CYP3A4- bzw. Pgp-Inhibitor, erhöhte die AUC von Vemurafenib im Steady State um etwa 40 %. Vemurafenib soll in Kombination mit starken CYP3A4‑Inhibitoren, Glucuronidierung und/oder Transportproteinen (z. B. Ritonavir, Saquinavir, Telithromycin, Ketoconazol, Itraconazol, Voriconazol, Posaconazol, Nefazodon, Atazanavir) mit Vorsicht angewendet werden. Bei Patienten, die gleichzeitig mit diesen Wirkstoffen behandelt werden, muss eine sorgfältige Sicherheitsüberwachung erfolgen und, wenn klinisch indiziert, die Dosis angepasst werden (siehe Tabelle 1 in Abschnitt 4.2).
In einer klinischen Studie verringerte die gleichzeitige Gabe einer Einzeldosis Vemurafenib 960 mg und Rifampicin die Plasmaverfügbarkeit von Vemurafenib signifikant um etwa 40 %.
Die gleichzeitige Gabe starker Induktoren von P‑Glykoprotein (P‑gp), der Glucuronidierung und/oder CYP3A4 (z. B. Rifampicin, Rifabutin, Carbamazepin, Phenytoin oder Johanniskraut [Hypericum perforatum]) kann zu einer suboptimalen Exposition von Vemurafenib führen und soll vermieden werden.
Die Wirkungen von P‑gp‑ und BCRP‑ Inhibitoren, die nicht auch potente CYP3A4-Inhibitoren sind, sind nicht bekannt. Es kann nicht ausgeschlossen werden, dass die Pharmakokinetik von Vemurafenib durch solche Arzneimittel über den Einfluss auf P-gp beeinträchtigt wird (z. B. Verapamil, Cyclosporin, Chinidin) oder BCRP (z. B. Cyclosporin, Gefitinib).
Frauen im gebärfähigen Alter/Verhütung bei Frauen
Frauen im gebärfähigen Alter müssen während der Behandlung und für mindestens 6 Monate nach der Behandlung eine effektive Kontrazeption anwenden.
Vemurafenib kann die Wirksamkeit hormonaler Kontrazeptiva verringern (siehe Abschnitt 4.5).
Schwangerschaft
Es liegen keine Daten zur Anwendung von Vemurafenib bei Schwangeren vor.
Vemurafenib zeigte an Rattenembryonen/-föten oder an Kaninchenembryonen/-föten keinen Hinweis für Teratogenität (siehe Abschnitt 5.3). In tierexperimentellen Studien wurde eine Plazentagängigkeit von Vemurafenib nachgewiesen. Aufgrund seines Wirkmechanismus könnte Vemurafenib eine fruchtschädigende Wirkung haben, wenn es bei einer schwangeren Frau angewendet wird. Vemurafenib soll von schwangeren Frauen nicht angewendet werden, es sei denn, der mögliche Nutzen für die Mutter wiegt das mögliche Risiko für den Fötus auf.
Stillzeit
Es ist nicht bekannt, ob Vemurafenib in die Muttermilch übergeht. Ein Risiko für das Neugeborene/den Säugling kann nicht ausgeschlossen werden. Unter Berücksichtigung des Nutzens des Stillens für das Kind und des Nutzens der Behandlung für die Mutter muss die Entscheidung getroffen werden, entweder das Stillen oder die Behandlung mit Vemurafenib abzubrechen.
Fertilität
Es wurden keine spezifischen tierexperimentellen Studien zur Bewertung der Wirkung von Vemurafenib auf die Fertilität durchgeführt. In Toxizitätsstudien mit wiederholter Gabe an Ratten und Hunden wurden jedoch keine histopathologischen Befunde der Reproduktionsorgane an männlichen und weiblichen Tieren festgestellt (siehe Abschnitt 5.3).
Vemurafenib hat geringen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen. Die Patienten sollen darauf hingewiesen werden, dass möglicherweise Abgeschlagenheit oder Augenprobleme auftreten können, wodurch die Fahrtüchtigkeit nicht mehr gewährleistet ist.
Zusammenfassung des Sicherheitsprofils
Die häufigsten bei der Anwendung von Vemurafenib berichteten Nebenwirkungen aller Schweregrade (> 30 %) beinhalten Arthralgie, Abgeschlagenheit, Ausschlag, Lichtempfindlichkeitsreaktionen, Alopezie, Übelkeit, Diarrhö, Kopfschmerzen, Pruritus, Erbrechen, Hautpapillome und Hyperkeratose. Die häufigsten (≥ 5 %) Nebenwirkungen vom Grad 3 waren kutane Plattenepithelkarzinome (cutanous squamous cell carcionoma, cuSCC), Keratoakanthome, Ausschlag, Arthralgie und erhöhte GGT-Werte (Gamma-Glutamyltransferase). CuSCC wurden in den meisten Fällen durch lokale Exzision behandelt.
Tabellarische Auflistung der Nebenwirkungen
Nebenwirkungen, die bei Patienten mit Melanom berichtet wurden, sind nachfolgend gemäß MedDRA nach Systemorganklasse, Häufigkeit und Schweregrad aufgelistet. Die folgende Konvention wurde zur Klassifizierung der Häufigkeit angewendet:
Sehr häufig ≥ 1/10
Häufig ≥ 1/100, < 1/10
Gelegentlich ≥ 1/1 000, < 1/100
Selten ≥ 1/10 000, < 1/1 000
Sehr selten < 1/10 000
Die in diesem Abschnitt aufgeführten Nebenwirkungen basieren auf Ergebnissen von 468 Patienten einer randomisierten, offenen Phase‑III‑Studie an erwachsenen Patienten mit BRAF‑V600 Mutation‑positivem nicht resezierbarem oder Stadium IV Melanom sowie einer einarmigen Phase‑II‑Studie an Patienten mit BRAF‑V600 Mutation-positivem Stadium IV Melanom, die im Vorfeld auf mindestens eine vorherige systemische Therapie nicht angesprochen haben (siehe Abschnitt 5.1). Des Weiteren sind Nebenwirkungen aufgeführt, die aus Sicherheitsberichten von allen klinischen Studien und aus Erfahrungen nach der Markteinführung stammen. Alle aufgeführten Nebenwirkungen basieren auf dem höchsten Prozentsatz, der in den klinischen Phase‑II- und ‑III‑Studien beobachtet wurde. Innerhalb jeder Häufigkeitsklasse werden Nebenwirkungen nach absteigendem Schweregrad aufgelistet und wurden unter Anwendung der NCI‑CTCAE v4.0 (Common Toxicity Criteria) zur Bewertung der Toxizität berichtet.
Tabelle 3: Nebenwirkungen, die bei Patienten auftraten, die in den Phase-II- oder -III-Studien mit Vemurafenib behandelt wurden, und Ereignisse, die aus Sicherheitsberichten von allen klinischen Studien(1) und aus Erfahrungen nach der Markteinführung stammen(2)
Systemorganklasse |
Sehr häufig |
Häufig |
Gelegentlich |
Selten |
Infektionen und parasitäre Erkrankungen |
Follikulitis |
|||
Gutartige, bösartige und nicht spezifizierte Neubildungen (einschl. Zysten und Polypen) |
Plattenepithel-karzinom der Haut(d), Keratoakanthom, seborrhoische Keratose, Hautpapillom |
Basalzellkarzi-nom, neue primäre Melanome(3) |
nicht-cuSCC(1)(3) |
Chronische myelomonozytäre Leukämie(2)(4), Adenokarzinom des Pankreas(5) |
Erkrankungen des Blutes und des Lymphsystems |
Neutropenie, Thrombozytopenie(6) |
|||
Erkrankungen des Immunsystems |
Sarkoidose(1)(2)(j) |
|||
Stoffwechsel- und Ernährungsstörungen |
Verminderter Appetit |
|||
Erkrankungen des Nervensystems |
Kopfschmerzen, Dysgeusie, Schwindelgefühl |
Lähmung des Nervus facialis, periphere Neuropathie |
||
Augenerkrankungen |
Uveitis |
retinaler Venen-verschluss, Iridozyklitis |
||
Gefäßerkrankungen |
Vaskulitis |
|||
Erkrankungen der Atemwege, des Brustraums und Mediastinums |
Husten |
|||
Erkrankungen des Gastrointestinaltrakts |
Diarrhö, Erbrechen, Übelkeit, Obstipation |
Stomatitis |
Pankreatitis(2) |
|
Leber- und Gallenerkrankungen |
Leberschaden(1)(2)(g) |
|||
Erkrankungen der Haut und des Unterhautgewebes |
Lichtempfindlich-keitsreaktionen, aktinische Keratose, Ausschlag, makulo-papulöser Ausschlag, Pruritus, Hyperkeratose, Erythem, palmar-plantares Erythrodysästhe-siesyndrom, Alopezie, trockene Haut, Sonnenbrand |
Papulöser Ausschlag, Pannikulitis (einschließl. Erythema nodosum), Keratosis pilaris |
Toxische epidermale Nekrolyse(e), Stevens-Johnson-Syndrom(f) |
Medikamenten-ausschlag mit Eosinophilie und systemischen Symptomen(1)(2) |
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen |
Arthralgie, Myalgie, Schmerzen in den Extremitäten, Schmerzen des Muskel- und Skelettsystems, Rückenschmerzen |
Arthritis |
Fibromatose der Plantarfaszie (Morbus Ledderhose)(1)(2), Dupuytren-Kontraktur(1)(2) |
|
Erkrankungen der Nieren und Harnwege |
Akute interstitielle Nephritis(1)(2)(h), akute Nierentubulusnekrose(1)(2)(h) |
|||
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort |
Abgeschlagenheit, Pyrexie, periphere Ödeme, Asthenie |
|||
Untersuchungen |
Anstieg der ALT(c), Anstieg der alkalischen Phosphatase(c), Anstieg der AST(c), Anstieg des Bilirubins(c), γ‑GT‑Anstieg(c), Gewichtsab-nahme, QT-Verlängerung im Elektrokardio-gramm, erhöhte Kreatininwerte im Blut(1)(2)(h) |
|||
Verletzung, Vergiftung und durch Eingriffe bedingte Komplikationen |
Potenzierung von Strahlenschäden(1)(2)(i) |
(1) Ereignisse, die aus Sicherheitsberichten von allen klinischen Studien stammen.
(2) Ereignisse, die aus Erfahrungen nach der Markteinführung stammen.
(3) Ein kausaler Zusammenhang zwischen dem Arzneimittel und dem unerwünschten Ereignis ist zumindest eine denkbare Möglichkeit.
(4) Fortschreiten einer vorbestehenden chronischen myelomonozytären Leukämie mit NRAS-Mutation.
(5) Fortschreiten eines vorbestehenden Adenokarzinoms des Pankreas mit KRAS Mutation.
(6) Berechnet auf der Basis von Phase-II- und Phase-III-Studien.
Beschreibung ausgewählter Nebenwirkungen
Anstieg der Leberenzyme(c)
Leberenzymabweichungen, die in der klinischen Phase‑III‑Studie berichtet wurden, sind nachfolgend als Anteil der Patienten, bei denen eine Veränderung der Leberenzyme vom Ausgangswert auf eine Grad-3- oder -4-Abweichung aufgetreten ist, aufgeführt:
• Sehr häufig: γ‑GT
• Häufig: ALT, alkalische Phosphatase, Bilirubin
• Gelegentlich: AST
Es gab keine Erhöhungen auf Grad 4 bei ALT, alkalischer Phosphatase oder Bilirubin.
Leberschaden(g)
Basierend auf den Kriterien für durch Arzneimittel verursachte Leberschäden, die von einer internationalen Expertenarbeitsgruppe bestehend aus Klinikern und Wissenschaftlern entwickelt wurden, wurde ein Leberschaden als eine der folgenden Abweichungen der Laborwerte definiert:
• ≥ 5 x ULN ALT
• ≥ 2 x ULN ALP (ohne eine andere Ursache für eine ALP-Erhöhung)
• ≥ 3 x ULN ALT mit gleichzeitiger Erhöhung der Bilirubinkonzentration > 2 x ULN
Kutanes Plattenepithelkarzinom(d) (cuSCC)
Fälle von cuSCC sind bei mit Vemurafenib behandelten Patienten berichtet worden. Die Häufigkeit des Auftretens von cuSCC bei mit Vemurafenib behandelten Patienten lag studienübergreifend bei ungefähr 20 %. Die Mehrzahl der operativ entfernten Läsionen, die von einem unabhängigen zentralen dermatopathologischen Labor untersucht wurden, wurde als SCC-Keratoakanthom-Subtyp oder mit gemischten Keratoakanthom-Merkmalen (52 %) klassifiziert. Die meisten als „Sonstige“ (43 %) klassifizierten Läsionen waren gutartige Hautläsionen (z. B. Verucca vulgaris, aktinische Keratose, benigne Keratose, Zyste/gutartige Zyste). Das cuSCC trat gewöhnlich früh im Behandlungszyklus auf, im Median mit einer Zeit von 7 bis 8 Wochen bis zum ersten Auftreten. Von den Patienten, bei denen cuSCC auftrat, kam es bei ungefähr 33 % zu einem mehr als einmaligen Auftreten, mit einem medianen Zeitraum von 6 Wochen zwischen den Ereignissen. Fälle von cuSCC wurden im Normalfall durch einfache Exzision behandelt und die Patienten führten ihre Behandlung in der Regel ohne Dosisanpassung fort (siehe Abschnitte 4.2 und 4.4).
Nicht‑kutanes Plattenepithelkarzinom (nicht‑cuSCC)
Fälle von nicht‑cuSCC sind bei mit Vemurafenib behandelten Patienten berichtet worden, die in klinische Studien eingeschlossen waren. Die Überwachung auf nicht‑cuSCC sollte wie in Abschnitt 4.4 beschrieben erfolgen.
Neue primäre Melanome
In klinischen Studien wurden neue primäre Melanome berichtet. Die Fälle wurden durch Exzision behandelt und die Patienten setzten die Behandlung ohne Dosisanpassung fort. Eine Überwachung auf Hautläsionen soll, wie in Abschnitt 4.4 beschrieben, erfolgen.
Potenzierung von Strahlenschäden(i)
Fälle, die berichtet wurden, beinhalten Recall-Phänomene, Hautschädigung durch Strahlen, strahlenbedingte Pneumonitis, Strahlenösophagitis, strahlenbedingte Proktitis, strahlenbedingte Hepatitis, Strahlenzystitis und Strahlennekrose.
In einer klinischen Phase-III-Studie (MO25515, n = 3.219) wurde eine höhere Inzidenz der Potenzierung von Strahlenschäden berichtet, wenn Patienten vor und während der Behandlung mit Vemurafenib eine Strahlentherapie erhielten (9,1 %), verglichen mit Patienten, die während der Behandlung mit Vemurafenib eine Strahlentherapie erhielten (5,2 %) oder Patienten, die vor der Behandlung mit Vemurafenib eine Strahlentherapie erhielten (1,5 %).
Überempfindlichkeitsreaktionen(e)
Schwerwiegende Überempfindlichkeitsreaktionen, einschließlich Anaphylaxie, sind in Verbindung mit Vemurafenib berichtet worden. Schwere Überempfindlichkeitsreaktionen können Stevens‑Johnson‑Syndrom, generalisierten Ausschlag, Erythem oder Hypotonie mit einschließen. Bei Patienten mit schweren Überempfindlichkeitsreaktionen soll die Behandlung mit Vemurafenib dauerhaft abgebrochen werden (siehe Abschnitt 4.4).
Dermatologische Reaktionen(f)
In der klinischen Pivotalstudie wurden bei Patienten unter Vemurafenib-Behandlung schwere dermatologische Reaktionen berichtet, einschließlich seltener Fälle des Stevens‑Johnson‑Syndroms und toxische epidermale Nekrolyse. Bei Patienten, bei denen eine schwere dermatologische Nebenwirkung auftritt, soll die Behandlung dauerhaft abgebrochen werden.
QT‑Verlängerung
Eine Analyse zentralisierter EKG‑Daten aus einer offenen, unkontrollierten Phase II QT‑Substudie mit 132 Patienten, die eine Dosis von 960 mg Vemurafenib zweimal täglich erhielten (NP22657), zeigte eine expositionsabhängige QTc‑Verlängerung. Die mittlere QTc‑Wirkung blieb über den ersten Behandlungsmonat hinaus stabil bei 12 ms ‑ 15 ms, wobei die größte mittlere QTc‑Verlängerung (15,1 ms; oberes 95-%-KI: 17,7 ms) innerhalb der ersten 6 Monate beobachtet wurde (n = 90 Patienten). Bei zwei Patienten (1,5 %) traten behandlungsbedingt absolute QTc‑Werte > 500 ms (CTC‑Grad 3) auf, und nur bei einem Patienten (0,8 %) trat eine QTc‑Veränderung von > 60 ms gegenüber dem Ausgangswert auf (siehe Abschnitt 4.4).
Akute Nierenschäden(h)
Unter Anwendung von Vemurafenib wurden Fälle von Nierenschäden berichtet, die von einer Erhöhung der Kreatininwerte bis zu akuter interstitieller Nephritis und akuter tubulärer Nekrose reichten. Einige Fälle traten in Zusammenhang mit Dehydratation auf. Die Erhöhung der Serum-Kreatininwerte war meistens leicht (> 1 ‑ 1,5 x ULN) bis mäßig (> 1,5 – 3 x ULN) und eine Reversibilität wurde beobachtet (siehe Tabelle 4).
Tabelle 4: Veränderungen der Kreatininwerte zum Ausgangswert in der Phase-III-Studie
Vemurafenib (%) |
Dacarbazin (%) |
|
Veränderung ≥ 1 Grad zum Ausgangswert (alle Grade) |
27,9 |
6,1 |
Veränderung ≥ 1 Grad zum Ausgangswert bis Grad 3 oder höher |
1,2 |
1,1 |
• bis Grad 3 |
0,3 |
0,4 |
• bis Grad 4 |
0,9 |
0,8 |
Tabelle 5: Fälle akuter Nierenschäden in der Phase-III-Studie
Vemurafenib (%) |
Dacarbazin (%) |
|
Fälle akuter Nierenschäden* |
10,0 |
1,4 |
Fälle akuter Nierenschäden in Zusammenhang mit Dehydratation |
5,5 |
1,0 |
Dosisanpassung bei akuten Nierenschäden |
2,1 |
0 |
Alle Prozentzahlen stellen die Fallzahl bezogen auf die Gesamtanzahl an Patienten dar, die dem jeweiligen Arzneimittel ausgesetzt waren.
* Schließt akute Nierenschäden, Nierenfunktionsstörung und Änderungen der Laborwerte ein, die mit akuten Nierenschäden übereinstimmen.
Sarkoidose(j)
Bei Patienten, die mit Vemurafenib behandelt wurden, wurden Fälle von Sarkoidose berichtet, die hauptsächlich die Haut, die Lunge und die Augen betrafen. In der Mehrzahl der Fälle wurde Vemurafenib weiterhin eingenommen, wobei sich die Sarkoidose entweder zurückbildete oder persistierte.
Besondere Patientengruppen
Ältere Patienten
In der Phase-III‑Studie waren 94 (28 %) der 336 mit Vemurafenib behandelten Patienten mit nicht resezierbarem oder metastasiertem Melanom ≥ 65 Jahre. Bei älteren Patienten (≥ 65 Jahre) können häufiger Nebenwirkungen, einschließlich cuSCC, vermindertem Appetit und kardialen Störungen auftreten.
Geschlecht
Grad‑3‑Nebenwirkungen, die in klinischen Studien mit Vemurafenib häufiger bei Frauen als bei Männern berichtet wurden, waren Ausschlag, Arthralgie und Lichtempfindlichkeit.
Kinder und Jugendliche
Die Sicherheit von Vemurafenib bei Kindern und Jugendlichen ist nicht erwiesen. In einer klinischen Studie mit sechs jugendlichen Patienten wurden keine neuen Beobachtungen bezüglich der Sicherheit gemacht.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem
Bundesinstitut für Arzneimittel und Medizinprodukte
Abt. Pharmakovigilanz
Kurt-Georg-Kiesinger-Allee 3
53175 Bonn
Website: http://www.bfarm.de
anzuzeigen.
Es gibt kein spezifisches Antidot bei Überdosierung mit Vemurafenib. Patienten, bei denen Nebenwirkungen auftreten, sollen eine angemessene symptomatische Behandlung erhalten. In klinischen Studien wurden keine Fälle von Überdosierung mit Vemurafenib beobachtet. Im Falle einer vermuteten Überdosierung soll Vemurafenib vorerst nicht eingenommen und eine unterstützende Behandlung eingeleitet werden.
Pharmakotherapeutische Gruppe: Antineoplastische Mittel, Proteinkinase‑Inhibitoren, ATC‑Code: L01EC01
Wirkmechanismus und pharmakodynamische Wirkungen
Vemurafenib ist ein Inhibitor der BRAF‑Serin‑Threonin‑Kinase. Mutationen des BRAF‑Gens führen zu einer konstitutiven Aktivierung von BRAF‑Proteinen, was die Zellproliferation ohne die Anwesenheit assoziierter Wachstumsfaktoren auslösen kann.
Präklinische Daten aus biochemischen Versuchen haben gezeigt, dass Vemurafenib ein potenter Inhibitor der BRAF‑Kinasen mit aktivierenden Mutationen im Kodon 600 ist (Tabelle 6).
Tabelle 6: Kinaseinhibitorische Aktivität von Vemurafenib gegen verschiedene BRAF‑Kinasen
Kinase |
Antizipierte Häufigkeit bei V600 Mutation‑positivem Melanom (t) |
Inhibitorische Konzentration 50 (nM) |
BRAFV600E |
87,3 % |
10 |
BRAFV600K |
7,9 % |
7 |
BRAFV600R |
1 % |
9 |
BRAFV600D |
< 0,2 % |
7 |
BRAFV600G |
< 0,1 % |
8 |
BRAFV600M |
< 0,1 % |
7 |
BRAFV600A |
< 0,1 % |
14 |
BRAFWT |
nicht anwendbar |
39 |
(t) Schätzung anhand von 16 403 Melanomen mit identifizierten BRAF Kodon 600‑Mutationen in der öffentlichen COSMIC Datenbank, Veröffentlichung 71 (November 2014).
Diese inhibitorische Wirkung wurde durch ERK-Phosphorylierung und zelluläre Anti‑Proliferations‑Versuche in vorhandenen Melanom‑Zelllinien, die das V600‑mutierte BRAF aufweisen, bestätigt. In zellulären Anti‑Proliferations‑Versuchen reichte die inhibitorische Konzentration 50 (IC50) gegen die V600‑mutierten Zelllinien (V600E, V600R, V600D und V600K mutierte Zelllinien) von 0,016 µM bis 1,131 µM, wobei die IC50 gegen BRAF‑Zelllinien vom Wildtyp bei 12,06 µM bzw. 14,32 µM lag.
Bestimmung des BRAF‑Mutationsstatus
Vor der Einnahme von Vemurafenib muss bei Patienten ein BRAF‑V600 Mutation‑positiver Tumorstatus durch einen validierten Test nachgewiesen worden sein. In den klinischen Phase‑II- und ‑III‑Studien wurden geeignete Patienten über einen real‑time Polymerase-Kettenreaktions-Assay (den cobas 4800 BRAF-V600 Mutation-Test) identifiziert. Dieser Test ist CE‑zertifiziert und wird zur Bestimmung des BRAF‑Mutationsstatus von DNA verwendet, die aus formalinfixiertem, in Paraffin eingebettetem (FFPE) Tumorgewebe isoliert wurde. Dieser hochsensitive Test (bis zu 5 % V600E- Sequenz vor dem Hintergrund einer Wildtyp-Sequenz aus FFPE-gewonnener DNA) wurde zum Nachweis einer prädominanten BRAF‑V600E Mutation entwickelt. Nicht-klinische und klinische Studien mit retrospektiven Sequenzierungsanalysen haben gezeigt, dass der Test auch die weniger häufigen BRAF‑V600D und V600K Mutationen mit niedrigerer Sensitivität nachweist. Von den aus nicht‑klinischen und klinischen Studien verfügbaren Proben (n = 920), die laut cobas‑Test Mutation‑positiv waren und zusätzlich durch Sequenzierung analysiert wurden, wurde mittels Sanger- und 454‑Sequenzierung keine Probe als Wildtyp identifiziert.
Klinische Wirksamkeit und Sicherheit
Die Wirksamkeit von Vemurafenib wurde bei 336 Patienten in einer klinischen Phase‑III-Studie (NO25026) und bei 278 Patienten in zwei klinischen Phase‑II-Studien (NP22657 und MO25743) bewertet. Alle Patienten mussten gemäß cobas 4800 BRAF-V600 Mutation-Test fortgeschrittene Melanome mit BRAF‑V600 Mutation aufweisen.
Ergebnisse der Phase‑III‑Studie (NO25026) an nicht vorbehandelten Patienten
Eine offene, multizentrische, internationale, randomisierte Phase‑III‑Studie unterstützt die Anwendung von Vemurafenib bei nicht vorbehandelten Patienten mit BRAF‑V600E Mutation‑positivem nicht resezierbarem oder metastasiertem Melanom. Die Patienten wurden entweder einer Behandlung mit Vemurafenib (960 mg zweimal täglich) oder mit Dacarbazin (1.000 mg/m2 alle drei Wochen am Tag 1) randomisiert zugeteilt.
Insgesamt wurden 675 Patienten auf Vemurafenib (n = 337) oder Dacarbazin (n = 338) randomisiert. Der Großteil der Patienten war männlich (56 %) und kaukasisch (99 %), das mediane Alter lag bei 54 Jahren (24 % waren ≥ 65 Jahre), alle Patienten hatten einen ECOG‑Performance‑Status von 0 oder 1 und die Mehrheit der Patienten befand sich im M1c-Status der Krankheit (65 %). Die co-primären Wirksamkeits-Endpunkte der Studie waren Gesamtüberleben (OS) und progressionsfreies Überleben (PFS).
Bei der vorher festgelegten Interimsanalyse mit dem 30. Dezember 2010 als Stichtag für die Datenerhebung wurden signifikante Verbesserungen in den co-primären Endpunkten Gesamtüberleben (OS) (p < 0,0001) und progressionsfreies Überleben (PFS) (p < 0,0001) (nicht stratifizierter Log-Rank-Test) beobachtet. Nach Empfehlung des Data Safety Monitoring Board (DSMB) wurden diese Ergebnisse im Januar 2011 veröffentlicht und die Studie wurde so angepasst, dass Dacarbazin-Patienten in den Vemurafenib-Arm wechseln konnten. Danach wurden Post-hoc-Analysen zum Überleben durchgeführt, wie in Tabelle 7 beschrieben.
Tabelle 7: Gesamtüberleben nicht vorbehandelter Patienten mit BRAF-V600 Mutation‑positivem Melanom zum Stichtag der Studie (n = 338 Dacarbazin, n = 337 Vemurafenib)
Stichtage |
Behandlung |
Anzahl der Todesfälle (%) |
Hazard Ratio |
Anzahl der Patienten, die gewechselt haben (%) |
30. Dezember 2010 |
Dacarbazin |
75 (22) |
0,37 (0,26; 0,55) |
0 (nicht anwendbar) |
Vemurafenib |
43 (13) |
|||
31. März 2011 |
Dacarbazin |
122 (36) |
0,44 (0,33; 0,59)(w) |
50 (15 %) |
Vemurafenib |
78 (23) |
|||
3. Oktober 2011 |
Dacarbazin |
175 (52) |
0,62 (0,49; 0,77)(w) |
81 (24 %) |
Vemurafenib |
159 (47) |
|||
1. Februar 2012 |
Dacarbazin |
200 (59) |
0,70 (0,57; 0,87)(w) |
83 (25 %) |
Vemurafenib |
199 (59) |
|||
20. Dezember 2012 |
Dacarbazin |
236 (70) |
0,78 (0,64; 0,94)(w) |
84 (25 %) |
Vemurafenib |
242 (72) |
(w) Zensierte Ergebnisse zum Zeitpunkt des Wechsels
Nicht zensierte Ergebnisse zum Zeitpunkt des Wechsels: 31. März 2011: HR (95-%-KI) = 0,47 (0,35; 0,62); 3. Oktober 2011: HR (95-%-KI) = 0,67 (0,54; 0,84); 1. Februar 2012: HR (95-%-KI) = 0,76 (0,63; 0,93); 20. Dezember 2012: HR (95-%-KI) = 0,79 (0,66; 0,95)
Bild 1: Kaplan‑Meier‑Kurven des Gesamtüberlebens - zuvor nicht behandelte Patienten (Stichtag 20. Dezember 2012)
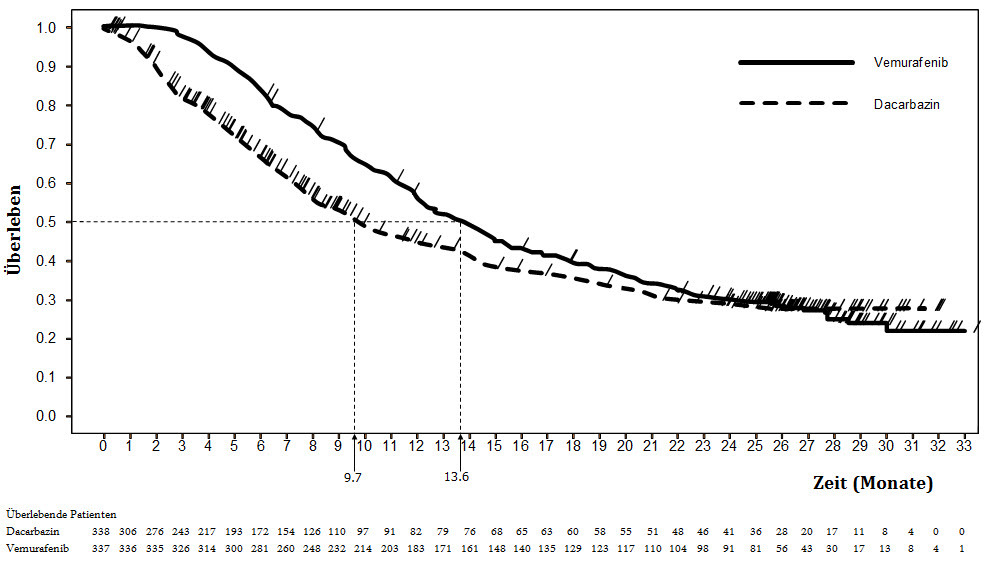
Tabelle 8 zeigt den Behandlungserfolg für alle spezifizierten Stratifizierungsvariablen, die als Prognosefaktoren etabliert sind.
Tabelle 8: Gesamtüberleben nicht vorbehandelter Patienten mit BRAF‑V600 Mutation‑positivem Melanom angegeben nach LDH, Tumorstadium und ECOG‑Status (Post-hoc-Analyse mit Stichtag 20. Dezember 2012, zensierte Ergebnisse zum Zeitpunkt des Wechsels)
Stratifizierungsvariable |
n |
Hazard Ratio |
95-%-Konfidenzintervall |
LDH normal |
391 |
0,88 |
0,67; 1,16 |
LDH > ULN |
284 |
0,57 |
0,44; 0,76 |
Stadium IIIc/M1A/M1B |
234 |
1,05 |
0,73; 1,52 |
Stadium MIC |
441 |
0,64 |
0,51; 0,81 |
ECOG PS = 0 |
459 |
0,86 |
0,67; 1,10 |
ECOG PS = 1 |
216 |
0,58 |
0,42; 0,9 |
LDH: Lactatdehydrogenase, ECOG PS: Eastern Cooperative Oncology Group Performance Status
Tabelle 9 zeigt die Gesamtansprechrate und progressionsfreies Überleben nicht vorbehandelter Patienten mit BRAF‑V600 Mutation‑positivem Melanom.
Tabelle 9: Gesamtansprechrate und progressionsfreies Überleben nicht vorbehandelter Patienten mit BRAF‑V600 Mutation‑positivem Melanom
Vemurafenib |
Dacarbazin |
p-Wert(x) |
||
Stichtag 30. Dezember 2010(y) | ||||
Gesamtansprechrate |
48,4 % |
5,5 % |
< 0,0001 |
|
Progressionsfreies Überleben |
0,26 |
< 0,0001 |
||
Anzahl der Ereignisse (%) |
104 (38 %) |
182 (66 %) |
||
Medianes PFS (Monate) |
5,32 |
1,61 |
||
Stichtag 1. Februar 2012(z) | ||||
Progressionsfreies Überleben |
0,38 |
< 0,0001 |
||
Anzahl der Ereignisse (%) |
277 (82 %) |
273 (81 %) |
||
Medianes PFS (Monate) |
6,87 |
1,64 |
||
(x) Nicht stratifizierter Log-Rank-Test für PFS und Chi-Quadrat-Test der Gesamtansprechrate.
(y) Am 30. Dezember 2010 waren insgesamt 549 Patienten für eine Auswertung zum PFS und 439 für eine Auswertung zur Gesamtansprechrate bewertbar.
(z) Am 1. Februar 2012 waren insgesamt 675 Patienten für die Post-hoc-Analyse zur PFS-Aktualisierung bewertbar.
Bei insgesamt 57 von 673 Patienten der Studie NO25026, deren Tumoren retrospektiv durch Sequenzierung analysiert wurden, wurden BRAF‑V600K Mutation-positive Melanome berichtet. Obwohl durch die niedrige Patientenanzahl begrenzt, legen Wirksamkeitsanalysen bei diesen Patienten mit V600K‑positiven Tumoren einen ähnlichen Behandlungsnutzen von Vemurafenib bezüglich OS, PFS und bestätigtem Gesamtansprechen dar. Für Patienten mit anderen seltenen BRAF‑V600 mutierten Melanomen, welche nicht die Mutation V600E bzw. V600K aufweisen, liegen keine Daten vor.
Ergebnisse der Phase‑II‑Studie (NP22657) an Patienten, die auf mindestens eine vorherige Behandlung nicht angesprochen haben
Eine einarmige, multizentrische, multinationale Phase‑II‑Studie wurde an 132 Patienten durchgeführt, die gemäß cobas 4800 BRAF‑V600 Mutation-Test ein BRAF‑V600E Mutation‑positives metastasiertes Melanom aufgewiesen und mindestens eine vorherige Behandlung erhalten hatten. Das mediane Alter lag bei 52 Jahren, wobei 19 % der Patienten älter als 65 Jahre waren. Die Mehrheit der Patienten war männlich (61 %), kaukasisch (99 %) und hatte Stadium M1c der Krankheit (61 %). 49 % der Patienten hatten auf ≥ 2 vorherige Behandlungen nicht angesprochen.
Der primäre Endpunkt der bestätigten besten Gesamtansprechrate (Complete Response + Partial Response), durch ein unabhängiges Prüfungskomitee bewertet, lag nach einer medianen Nachbeobachtung von 12,9 Monaten (Bereich: 0,6 bis 20,1) bei 53 % (95-%-KI: 44 %, 62 %). Das mediane Gesamtüberleben lag bei 15,9 Monaten (95-%-KI: 11,6; 18,3). Die Gesamtüberlebensrate nach 6 Monaten lag bei 77 % (95-%-KI: 70 %, 85 %) und nach 12 Monaten bei 58 % (95-%-KI: 49 %; 67 %).
Neun der 132 Patienten, die in die Studie NP22657 aufgenommen wurden, hatten, nach retrospektiver Sanger‑Sequenzierung, V600K Mutation‑positive Tumoren. Von diesen Patienten kam es bei 3 zu einem partiellen Ansprechen, bei 3 zu einer stabilen Erkrankung, bei 2 zu einer progressiven Erkrankung und ein Patient konnte nicht bewertet werden.
Ergebnisse der Phase‑II‑Studie (MO25743) bei Patienten mit Hirnmetastasen
Eine einarmige, multizentrische Studie (n = 146) mit Vemurafenib wurde mit erwachsenen Patienten mit histologisch bestätigtem metastasiertem Melanom durchgeführt, die eine BRAF‑V600 Mutation (laut cobas 4800 BRAF‑V600 Mutation-Test) und Hirnmetastasen aufwiesen. Die Studie bestand aus zwei Kohorten, in die simultan Patienten eingeschlossen wurden:
Kohorte 1 mit vorher unbehandelten Patienten (n = 90): Patienten, die keine vorherige Behandlung ihrer Hirnmetastasen erhalten hatten; eine vorherige systemische Behandlung eines metastasierten Melanoms war zulässig, BRAF- und MEK-Inhibitoren ausgeschlossen.
Kohorte 2 mit zuvor behandelten Patienten (n = 56): Patienten, die eine vorherige Behandlung ihrer Hirnmetastasen erhalten hatten und nach dieser Behandlung progredient wurden. Bei Patienten, die mit stereotaktischer Strahlentherapie (SRT) behandelt wurden oder bei denen eine Operation durchgeführt wurde, musste sich nach der vorherigen Behandlung eine neue, nach RECIST bewertbare Läsion im Gehirn entwickelt haben.
Insgesamt wurden 146 Patienten eingeschlossen. Die Mehrheit der Patienten war männlich (61,6 %) und kaukasisch (92,5 %) und das mediane Alter betrug 54 Jahre (Bereich: 26 bis 83 Jahre), bei ähnlicher Verteilung in den beiden Kohorten. Bei Studienbeginn lag die mediane Anzahl an Zielläsionen im Gehirn in beiden Kohorten bei 2 (Bereich: 1 bis 5).
Der primäre Wirksamkeitsendpunkt der Studie war die beste Gesamtansprechrate (BORR) im Gehirn von Patienten mit metastasiertem Melanom mit vorher unbehandelten Hirnmetastasen, bewertet durch ein unabhängiges Review-Komitee (IRC).
Sekundäre Endpunkte schlossen eine Bewertung der Wirksamkeit von Vemurafenib unter Berücksichtigung der BORR im Gehirn von vorher behandelten Patienten, der Dauer des Ansprechens (DOR), des progressionsfreien Überlebens (PFS) und des Gesamtüberlebens (OS) bei Patienten mit Melanom mit Hirnmetastasen ein (siehe Tabelle 10).
Tabelle 10: Wirksamkeit von Vemurafenib bei Patienten mit Hirnmetastasen
Kohorte 1 |
Kohorte 2 |
Gesamt n = 146 |
|
BORRa bei Patienten mit Hirnmetastasen und Ansprechen n (%) |
16 (17,8 %) |
10 (17,9 %) |
26 (17,8 %) |
DORc im Gehirn (n) |
(n = 16) |
(n = 10) |
(n = 26) |
BORR extrakraniell n (%)a |
26 (32,9 %) |
9 (22,5 %) |
35 (29,4 %) |
PFS - gesamt |
3,7 |
3,7 |
3,7 |
PFS – nur Gehirn |
3,7 |
4,0 |
3,7 |
OS |
8,9 |
9,6 |
9,6 |
a Beste bestätigte Gesamtansprechrate, bewertet durch ein unabhängiges Review-Komitee, Anzahl an Patienten mit Ansprechen, n (%)
b Zweiseitiges 95‑%‑Clopper-Pearson Konfidenzintervall (KI)
c Dauer des Ansprechens, bewertet durch ein unabhängiges Review-Komitee
d Kaplan-Meier-Schätzung
e Prüfarzt-bewertet
Kinder und Jugendliche
Ergebnisse der Phase-I-Studie (NO25390) bei Kindern und Jugendlichen
Eine Dosisfindungsstudie der Phase I wurde zur Bewertung der Anwendung von Vemurafenib bei sechs jugendlichen Patienten mit BRAF-V600-Mutation-positivem Melanom im Stadium IIIC oder IV durchgeführt. Alle behandelten Patienten waren mindestens 15 Jahre alt und hatten ein Körpergewicht von mindestens 45 kg. Drei Patienten wurden mit Vemurafenib 720 mg zweimal täglich und drei Patienten mit Vemurafenib 960 mg zweimal täglich behandelt. Die maximal verträgliche Dosis konnte nicht bestimmt werden. Obwohl vorübergehende Tumorregressionen beobachtet wurden, lag die beste Gesamtansprechrate (BORR) auf Basis des bestätigten Ansprechens bei 0 % (95-%-KI: 0 %, 46 %). Die Studie wurde aufgrund geringer Rekrutierung eingestellt. Siehe Abschnitt 4.2 bzgl. Informationen zur Anwendung bei Kindern und Jugendlichen.
Nach den Kriterien aus dem biopharmazeutischen Klassifizierungssystem ist Vemurafenib ein Arzneimittel der Klasse IV (geringe Lösbarkeit und Permeabilität). Die pharmakokinetischen Parameter von Vemurafenib wurden in einer Phase‑I- und ‑III‑Studie durch eine Nicht-Kompartiment-Analyse bestimmt (20 Patienten nach 15 Tagen mit einer Dosierung von 960 mg zweimal täglich und 204 Patienten im Steady State am Tag 22) sowie durch eine Populations-PK-Analyse, bei der gepoolte Daten von 458 Patienten verwendet wurden. Von diesen Patienten waren 457 Kaukasier.
Resorption
In einer Phase-I-Studie unter unkontrollierten Bedingungen bezüglich des Einflusses von Nahrung bei 4 Patienten mit BRAF-V600-positiven Malignomen betrug die Bioverfügbarkeit im Steady State relativ zu einer intravenösen Mikrodosis 32 - 115 % (Mittelwert 64 %).
Nach einer Einzeldosis von 960 mg (vier Tabletten à 240 mg) wird Vemurafenib mit einer medianen Tmax von ungefähr 4 Stunden resorbiert. Vemurafenib zeigt starke Schwankungen zwischen den Patienten. In der Phase‑II-Studie lagen AUC0-8 und Cmax am Tag 1 bei 22,1 µg•h/ml ± 12,7 µg•h/ml und 4,1 µg/ml ± 2,3 µg/ml. Eine Akkumulierung erfolgt nach multipler zweimal täglicher Anwendung von Vemurafenib. In der Nicht‑Kompartiment‑Analyse lag das Tag 15/Tag 1-Verhältnis nach einer Dosierung von 960 mg Vemurafenib zweimal täglich bei einem 15- bis 17‑Fachen der AUC und einem 13- bis 14‑Fachen von Cmax, die unter Steady State Bedingungen eine AUC0-8h und Cmax von 380,2 µg•h/ml ± 143,6 µg•h/ml bzw. 56,7 µg/ml ± 21,8 µg/ml ergaben.
Nahrung (fettreiche Mahlzeit) erhöht die relative Bioverfügbarkeit einer einzelnen 960 mg Dosis von Vemurafenib. Das Verhältnis der geometrischen Mittel von nüchternem und nicht nüchternem Zustand war für Cmax und AUC 2,5- bzw. 4,6- bis 5,1‑fach. Die mediane Tmax erhöhte sich von 4 auf 7,5 Stunden, wenn eine einzelne Dosis von Vemurafenib zusammen mit Nahrung eingenommen wurde.
Die Wirkung von Nahrung auf die Steady State Verfügbarkeit von Vemurafenib ist zurzeit nicht bekannt. Die regelmäßige Einnahme von Vemurafenib auf leeren Magen kann zu einer signifikant niedrigeren Steady State Verfügbarkeit führen verglichen mit der regelmäßigen Einnahme von Vemurafenib mit oder kurz nach einer Mahlzeit. Aufgrund der hohen Anreicherung von Vemurafenib im Steady State wird erwartet, dass eine gelegentliche Einnahme von Vemurafenib auf leeren Magen einen begrenzten Einfluss auf die Steady State Verfügbarkeit hat. Sicherheits- und Wirksamkeitsdaten aus den pivotalen Studien wurden von Patienten gesammelt, die Vemurafenib mit oder ohne Nahrung eingenommen haben.
Die Variabilität der Exposition kann auch durch Unterschiede im Gehalt der gastrointestinalen Flüssigkeit, der Volumina, des pH-Wertes, der Motilität, der Übergangszeit und der Gallenflüssigkeit entstehen.
Im Steady State ist die mittlere Plasmaverfügbarkeit von Vemurafenib während des 24-Stunden- Intervalls stabil, wie durch das mittlere Verhältnis von 1,13 zwischen den Plasmakonzentrationen vor und 2 – 4 Stunden nach der morgendlichen Dosis angezeigt. Nach der Einnahme wird die Resorptionsrate in der Population der Patienten mit metastasiertem Melanom konstant auf 0,19 hr-1 geschätzt (mit 101 % Variabilität zwischen den Patienten).
Verteilung
Das scheinbare Verteilungsvolumen von Vemurafenib in der Patientenpopulation mit metastasiertem Melanom wird auf 91 l geschätzt (mit einer Variabilität von 64,8 % zwischen den Patienten). In vitro bindet es stark an menschliche Plasmaproteine (> 99 %).
Biotransformation
Die relativen Anteile von Vemurafenib und seiner Metabolite wurden in einer Massenbilanz‑Studie am Menschen charakterisiert mit einer oral angewendeten Einzeldosis von 14C‑markiertem Vemurafenib. CYP3A4 ist in vitro das für den Metabolismus von Vemurafenib primär verantwortliche Enzym. Konjugationsmetabolite (Glucuronidierung und Glycosylierung) wurden auch beim Menschen identifiziert. Trotzdem war die ursprüngliche Verbindung der Hauptbestandteil (95 %) im Plasma. Obwohl der Metabolismus scheinbar nicht zu einer relevanten Menge an Metaboliten im Plasma führt, kann die Wichtigkeit des Metabolismus für die Ausscheidung nicht ausgeschlossen werden.
Elimination
Die scheinbare Clearance von Vemurafenib in der Patientenpopulation mit metastasiertem Melanom wird auf 29,3 l/Tag geschätzt (mit einer Variabilität zwischen den Patienten von 31,9 %). Die anhand der populationspharmakokinetischen Analyse geschätzte Populations-Eliminationshalbwertszeit von Vemurafenib beträgt 51,6 Stunden (das 5. und das 95. Perzentil der geschätzten individuellen Halbwertszeit liegen im Bereich von 29,8 ‑ 119,5 Stunden).
In der Massenbilanz‑Studie am Menschen mit oral angewendetem Vemurafenib wurden im Durchschnitt 95 % der Dosis innerhalb von 18 Tagen ausgeschieden. Der Hauptteil der zu Vemurafenib gehörenden Substanzen (94 %) wurde über die Fäzes und < 1 % wurde über den Urin ausgeschieden. Die renale Elimination scheint bei der Vemurafenib-Ausscheidung keine Rolle zu spielen, während die biliäre Exkretion unveränderter Substanz möglicherweise ein wichtiger Eliminationsweg ist. Vemurafenib ist in vitro sowohl Substrat als auch Inhibitor von P‑gp.
Besondere Patientengruppen
Ältere Patienten
Auf Grundlage der Populations‑PK‑Analyse hat das Alter keine statistisch signifikante Wirkung auf die Pharmakokinetik von Vemurafenib.
Geschlecht
Die populationspharmakokinetische Analyse ergab eine 17 % höhere scheinbare Clearance (CL/F) und ein 48 % größeres scheinbares Verteilungsvolumen (V/F) bei Männern als bei Frauen. Es ist nicht klar, ob es sich hierbei um eine geschlechts- oder körpergrößenspezifische Wirkung handelt. Die Unterschiede in der Exposition sind jedoch nicht ausreichend groß, um eine Dosisanpassung nach Geschlecht oder Körpergröße zu rechtfertigen.
Nierenfunktionsstörungen
In der populationspharmakokinetischen Analyse, unter Verwendung von Daten aus klinischen Studien bei Patienten mit metastasiertem Melanom, beeinflusste eine leichte bis mäßige Nierenfunktionsstörung die scheinbare Vemurafenib-Clearance nicht (Kreatinin-Clearance > 40 ml/min). Für Patienten mit schwerer Nierenfunktionsstörung liegen keine Daten vor (siehe Abschnitte 4.2 und 4.4).
Leberfunktionsstörungen
Auf der Grundlage präklinischer Daten und der Massenbilanz-Studie am Menschen wird der größte Teil von Vemurafenib über die Leber eliminiert. In der populationspharmakokinetischen Analyse, unter Verwendung von Daten aus klinischen Studien mit Patienten mit metastasiertem Melanom, beeinflussten erhöhte AST- und ALT‑Werte von bis zum 3‑Fachen des oberen Normalwertes die scheinbare Vemurafenib-Clearance nicht. Die Daten reichen nicht aus, um die Wirkung metabolischer oder exkretorischer Leberfunktionsstörung auf die Vemurafenib-Pharmakokinetik zu bestimmen (siehe Abschnitte 4.2 und 4.4).
Kinder und Jugendliche
Begrenzte pharmakokinetische Daten von sechs jugendlichen Patienten im Alter zwischen 15 und 17 Jahren mit BRAF-V600-Mutation-positivem Melanom im Stadium IIIC oder IV lassen vermuten, dass die pharmakokinetischen Eigenschaften von Vemurafenib bei Jugendlichen im Allgemeinen ähnlich sind wie bei Erwachsenen. Siehe Abschnitt 4.2 bzgl. Informationen zur Anwendung bei Kindern und Jugendlichen.
Das präklinische Sicherheitsprofil von Vemurafenib wurde an Ratten, Hunden und Kaninchen bestimmt.
In Studien zur Toxizität bei wiederholter Gabe wurden beim Hund die Leber und das Knochenmark als Zielorgane identifiziert. Reversible toxische Wirkungen (hepatozelluläre Nekrose und Degeneration) in der Leber wurden bei Expositionen, die unter der zu erwartenden klinischen Belastung lagen (basierend auf AUC‑Vergleichen), in der 13‑wöchigen Studie an Hunden festgestellt. Eine fokale Knochenmarksnekrose wurde in einer frühzeitig beendeten 39‑wöchigen Studie an Hunden unter Expositionen ähnlich der erwarteten klinischen Belastung (basierend auf AUC‑Vergleichen) bei einem Hund festgestellt. In einer in vitro-Knochenmarks-Zytotoxizitäts-Studie wurde in einigen lympho‑hämatopoetischen Zellpopulationen von Ratte, Hund und Mensch in klinisch relevanten Konzentrationen eine leichte Zytotoxizität beobachtet.
Es wurde gezeigt, dass Vemurafenib in vitro auf kultivierten murinen Fibroblasten nach UVA-Bestrahlung phototoxisch wirkt, jedoch nicht in vivo in einer Rattenstudie in Dosen von bis zu 450 mg/kg/Tag (bei Expositionen unter der erwarteten klinischen Exposition [basierend auf AUC‑Vergleichen]). Es wurden keine spezifischen Studien an Tieren durchgeführt, um die Wirkung von Vemurafenib auf die Fertilität zu bewerten. In Studien zur Toxizität bei wiederholter Gabe wurden jedoch bei männlichen und weiblichen Ratten und bei Hunden bei Dosierungen von bis zu 450 mg/kg/Tag (bei Expositionen unter der erwarteten klinischen Exposition am Menschen [basierend auf AUC-Vergleichen]) keine histopathologischen Befunde in Bezug auf die Fortpflanzungsorgane festgestellt. In embryofötalen Entwicklungsstudien an Ratten und Kaninchen, bei Dosen entsprechend bis zu jeweils 250 mg/kg/Tag und 450 mg/kg/Tag, die zu Expositionen unter der erwarteten klinischen Exposition führten (basierend auf AUC‑Vergleichen), wurde keine Teratogenität beobachtet. Jedoch waren die Expositionen in den embryofötalen Entwicklungsstudien unter der klinischen Exposition basierend auf AUC‑Vergleichen. Deswegen ist es schwierig zu definieren, in welchem Ausmaß diese Ergebnisse auf Menschen extrapoliert werden können. Daher kann eine Wirkung von Vemurafenib auf den Fötus nicht ausgeschlossen werden. Im Hinblick auf die prä- und postnatale Entwicklung wurden keine Studien durchgeführt.
Weder über in vitro-Untersuchungen (Genmutationstest an Bakterien [AMES], Chromosomenaberrationstest an menschlichen Lymphozyten) noch über den in-vivo-Mikronukleustest an Rattenknochenmark, die mit Vemurafenib durchgeführt wurden, wurden Anzeichen für Genotoxizität festgestellt.
Es wurden keine Karzinogenitätsstudien mit Vemurafenib durchgeführt.
Tablettenkern
Croscarmellose-Natrium
Hochdisperses Siliciumdioxid
Magnesiumstearat
Hyprolose
Filmüberzug
Poly(vinylalkohol)
Titandioxid (E 171)
Macrogol 3350
Talkum
Eisen(III)‑oxid (E 172)
Nicht zutreffend.
3 Jahre
In der Originalverpackung aufbewahren, um den Inhalt vor Feuchtigkeit zu schützen.
Perforierte Blisterpackung zur Abgabe von Einzeldosen aus Aluminium/Aluminium.
Packungsgröße: 56 x 1 Filmtabletten (7 Blisterpackungen zu je 8 x 1 Tablette)
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu beseitigen.
Roche Registration GmbH
Emil-Barell-Straße 1
79639 Grenzach-Wyhlen
Deutschland
EU/1/12/751/001
Datum der Erteilung der Zulassung: 17. Februar 2012
Datum der letzten Verlängerung der Zulassung: 22. September 2016
März 2024
Verschreibungspflichtig
Roche Pharma AG
Emil-Barell-Str. 1
79639 Grenzach-Wyhlen
Telefon (07624) 14-0
Telefax (07624) 1019
Ausführliche Informationen zu diesem Arzneimittel sind auf den Internetseiten der Europäischen Arzneimittel-Agentur http://www.ema.europa.eu verfügbar.