ADCETRIS 50 mg Pulver für ein Konzentrat zur Herstellung einer Infusionslösung.
Jede Durchstechflasche enthält 50 mg Brentuximab vedotin.
Nach Rekonstitution (siehe Abschnitt 6.6) enthält jeder ml 5 mg Brentuximab vedotin.
ADCETRIS ist ein Antikörper‑Wirkstoff‑Konjugat. Es besteht aus einem auf CD30 gerichteten monoklonalen Antikörper (rekombinantes chimäres Immunglobulin G1 [IgG1], das durch rekombinante DNA‑Technologie in Ovarialzellen des Chinesischen Hamsters produziert wird) und dem Antimikrotubuli‑Wirkstoff Monomethyl‑Auristatin E (MMAE), der kovalent daran gebunden ist.
Sonstige Bestandteile mit bekannter Wirkung:
Jede Durchstechflasche enthält etwa 13,2 mg Natrium.
Jede Durchstechflasche enthält etwa 2 mg Polysorbat 80.
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
Pulver für ein Konzentrat zur Herstellung einer Infusionslösung.
Weißer bis cremefarbener Kuchen oder Pulver.
Hodgkin‑Lymphom
ADCETRIS wird angewendet bei erwachsenen Patienten mit bislang unbehandeltem CD30+ Hodgkin‑Lymphom (HL) im Stadium III oder IV in Kombination mit Doxorubicin, Vinblastin und Dacarbazin (AVD) (siehe Abschnitte 4.2 und 5.1).
ADCETRIS wird angewendet bei erwachsenen Patienten mit bislang unbehandeltem CD30+ HL im Stadium IIB mit Risikofaktoren, im Stadium III oder im Stadium IV in Kombination mit Etoposid, Cyclophosphamid, Doxorubicin, Dacarbazin, Dexamethason (BrECADD) (siehe Abschnitte 4.2 und 5.1).
ADCETRIS wird angewendet zur Behandlung von erwachsenen Patienten mit CD30+ HL mit erhöhtem Rezidiv‑ oder Progressionsrisiko nach einer autologen Stammzelltransplantation (ASCT) (siehe Abschnitt 5.1).
ADCETRIS wird angewendet bei der Behandlung von erwachsenen Patienten mit rezidiviertem oder refraktärem CD30+ Hodgkin‑Lymphom (HL):
nach einer ASCT, oder
nach mindestens zwei vorangegangenen Therapien, wenn eine ASCT oder eine Kombinationschemotherapie nicht als Behandlungsoption in Frage kommt.
Systemisches anaplastisches großzelliges Lymphom
ADCETRIS wird in Kombination mit Cyclophosphamid, Doxorubicin und Prednison (CHP) bei erwachsenen Patienten mit bislang unbehandeltem systemischem anaplastischem großzelligem Lymphom (systemic anaplastic large cell lymphoma, sALCL) angewendet (siehe Abschnitt 5.1).
ADCETRIS wird angewendet bei der Behandlung von erwachsenen Patienten mit rezidiviertem oder refraktärem sALCL.
Kutanes T‑Zell‑Lymphom
ADCETRIS wird angewendet zur Behandlung erwachsener Patienten mit CD30+ kutanem T‑Zell‑Lymphom (cutaneous t‑cell lymphoma, CTCL) nach mindestens einer vorangegangenen systemischen Behandlung (siehe Abschnitt 5.1).
Die Anwendung von ADCETRIS sollte unter der Aufsicht eines in der Anwendung von Krebsmedikamenten erfahrenen Arztes erfolgen.
Dosierung
Bislang unbehandeltes HL
ADCETRIS + AVD
Die empfohlene Dosis in Kombination mit einer Chemotherapie (Doxorubicin [A], Vinblastin [V] und Dacarbazin [D] [AVD]) beträgt 1,2 mg/kg als intravenöse Infusion über 30 Minuten am 1. und 15. Tag jedes 28‑Tage‑Zyklus über 6 Zyklen (siehe Abschnitt 5.1).
Bei allen erwachsenen Patienten mit bislang unbehandeltem HL, die eine Kombinationstherapie erhalten, wird ab der ersten Dosis eine Primärprophylaxe mit Wachstumsfaktoren (granulocyte‑colony stimulating factor, G‑CSF) empfohlen (siehe Abschnitt 4.4).
Siehe Zusammenfassung der Merkmale des Arzneimittels (Fachinformationen) der Chemotherapeutika, die in Kombination mit ADCETRIS zur Behandlung von bislang unbehandelten Patienten mit HL verabreicht werden.
BrECADD
Die empfohlene Dosis in Kombination mit einer Chemotherapie (Etoposid (E), Cyclophosphamid (C), Doxorubicin (A), Dacarbazin (D), Dexamethason (D) [BrECADD]) beträgt 1,8 mg/kg als intravenöse Infusion über 30 Minuten und wird alle 3 Wochen über bis zu 6 Zyklen verabreicht (siehe Abschnitt 5.1).
Eine Primärprophylaxe mit Wachstumsfaktorunterstützung (G‑CSF) muss ab dem 5. Tag jedes Zyklus bei allen erwachsenen Patienten mit zuvor unbehandeltem HL, die eine Kombinationstherapie erhalten, durchgeführt werden (siehe Abschnitt 4.4). Eine Vorbehandlung mit Dexamethason über 4 Tage vor dem ersten Chemotherapiezyklus wird für Patienten > 40 Jahre oder nach Ermessen des Arztes empfohlen.
Während der gesamten Dauer der Chemotherapie muss dreimal wöchentlich eine Antibiotikaprophylaxe erfolgen.
Empfehlungen zur Dosierung von Chemotherapeutika, die in Kombination mit ADCETRIS bei Patienten mit zuvor unbehandeltem HL verabreicht werden, siehe Tabelle 4.
HL mit erhöhtem Risiko für Rezidiv oder Progression
Die empfohlene Dosis beträgt 1,8 mg/kg, als intravenöse Infusion über 30 Minuten alle 3 Wochen verabreicht.
Die Behandlung mit ADCETRIS sollte gemäß klinischer Beurteilung nach der Erholung von der ASCT einsetzen. Die Patienten sollten bis zu 16 Zyklen erhalten (siehe Abschnitt 5.1).
Rezidiviertes oder refraktäres HL
Die empfohlene Dosierung beträgt 1,8 mg/kg, die als intravenöse Infusion über 30 Minuten alle 3 Wochen verabreicht wird.
Die empfohlene Anfangsdosierung für die Wiederholungsbehandlung von Patienten, die zuvor schon auf die Behandlung mit ADCETRIS angesprochen haben, beträgt 1,8 mg/kg, die als intravenöse Infusion über 30 Minuten alle 3 Wochen verabreicht wird. Alternativ kann die Behandlung mit der zuletzt tolerierten Dosierung begonnen werden (siehe Abschnitt 5.1).
Die Behandlung sollte bis zur Krankheitsprogression oder bis zum Auftreten inakzeptabler Toxizität fortgesetzt werden (siehe Abschnitt 4.4).
Patienten, bei denen eine Stabilisierung oder Besserung der Erkrankung erreicht wird, sollten mindestens 8 Zyklen und bis zu maximal 16 Zyklen (ca. 1 Jahr) erhalten (siehe Abschnitt 5.1).
Bislang unbehandeltes sALCL
Die empfohlene Dosis in Kombination mit einer Chemotherapie (Cyclophosphamid [C], Doxorubicin [H] und Prednison [P]; [CHP]) beträgt 1,8 mg/kg und wird als intravenöse Infusion über 30 Minuten alle 3 Wochen für 6 bis 8 Zyklen verabreicht (siehe Abschnitt 5.1).
Bei allen erwachsenen Patienten mit bislang unbehandeltem sALCL, die eine Kombinationstherapie erhalten, wird ab der ersten Dosis eine Primärprophylaxe mit G‑CSF empfohlen (siehe Abschnitt 4.4).
Siehe die Zusammenfassung der Merkmale des Arzneimittels (Fachinformationen) der Chemotherapeutika, die in Kombination mit ADCETRIS zur Behandlung von bislang unbehandelten Patienten mit sALCL verabreicht werden.
Rezidiviertes oder refraktäres sALCL
Die empfohlene Dosierung beträgt 1,8 mg/kg, die als intravenöse Infusion über 30 Minuten alle 3 Wochen verabreicht wird.
Die empfohlene Anfangsdosierung für die Wiederholungsbehandlung von Patienten, die zuvor schon auf die Behandlung mit ADCETRIS angesprochen hatten, beträgt 1,8 mg/kg, die als intravenöse Infusion über 30 Minuten alle 3 Wochen verabreicht wird. Alternativ kann die Behandlung mit der zuletzt vertragenen Dosierung eingeleitet werden (siehe Abschnitt 5.1).
Die Behandlung sollte bis zur Krankheitsprogression oder bis zum Auftreten inakzeptabler Toxizität fortgesetzt werden (siehe Abschnitt 4.4).
Patienten, bei denen eine Stabilisierung oder Besserung der Erkrankung erreicht wird, sollten mindestens 8 Zyklen und bis zu maximal 16 Zyklen (ca. 1 Jahr) erhalten (siehe Abschnitt 5.1).
CTCL
Die empfohlene Dosis beträgt 1,8 mg/kg, als intravenöse Infusion über 30 Minuten alle 3 Wochen verabreicht.
Patienten mit CTCL sollten bis zu 16 Zyklen erhalten (siehe Abschnitt 5.1).
Allgemein
Wenn das Gewicht des Patienten mehr als 100 kg beträgt, sollte für die Dosisberechnung der Wert von 100 kg verwendet werden (siehe Abschnitt 6.6).
Vor der Verabreichung jeder Dosis dieses Arzneimittels sollte ein komplettes Blutbild durchgeführt werden (siehe Abschnitt 4.4).
Die Patienten sollten während und nach der Infusion (siehe Abschnitt 4.4) überwacht werden.
Anpassung der Dosierung
Neutropenie
Wenn sich während der Behandlung eine Neutropenie entwickelt, sollte die Gabe der nächsten Dosis verzögert werden oder bei nachfolgenden Zyklen eine Dosisanpassung vorgenommen werden. Siehe Tabelle 1, Tabelle 2, Tabelle 3 und Tabelle 4 für entsprechende Dosierungsempfehlungen für die Monotherapie bzw. Kombinationstherapie (siehe auch Abschnitt 4.4).
Tabelle 1: Dosierungsempfehlungen für die Monotherapie bei Neutropenie
Schweregrad der Neutropenie |
Änderung des Dosierungsschemas |
|
Grad 1 |
(< LLN ‑ 1500/mm3 |
Dosis und Behandlungsintervalle beibehalten. |
< LLN ‑ 1,5 x 109/l) oder |
||
Grad 2 |
(< 1500 ‑ 1000/mm3 |
|
< 1,5 ‑ 1,0 x 109/l) |
||
Grad 3 |
(< 1000 ‑ 500/mm3 |
Die Verabreichung der Dosis verzögern, bis die Toxizität wieder auf ≤ Grad 2 oder den Ausgangswert zurückgegangen ist, danach die Behandlung in unveränderter Dosierung und unveränderten Behandlungsintervallen fortführenb. Bei Patienten, die eine Neutropenie Grad 3 oder Grad 4 entwickeln, können in den folgenden Zyklen G‑CSF oder GM‑CSF in Betracht gezogen werden. |
Grad 4 |
(< 500/mm3< 0,5 x 109/l) |
|
a. Die Einteilung basiert auf den Common Terminology Criteria for Adverse Events (CTCAE) V3.0 des National Cancer Institute (NCI), siehe Neutrophile/Granulozyten; LLN = unterer Grenzwert des Normbereichs (lower limit of normal). | ||
Tabelle 2: Dosierungsempfehlungen bei Neutropenie während einer AVD/CHP‑Kombinationstherapie
Schweregrad der Neutropenie |
Änderung des Dosierungsschemas |
|
Grad 1 |
(< LLN ‑ 1500/mm3 |
Bei allen erwachsenen Patienten, die eine Kombinationstherapie erhalten, wird ab der ersten Dosis eine Primärprophylaxe mit G‑CSF empfohlen. Dosis und Behandlungsintervalle beibehalten. |
< LLN ‑ 1,5 x 109/l) oder |
||
Grad 2 |
(< 1500 ‑ 1000/mm3 |
|
< 1,5 ‑ 1,0 x 109/l) oder |
||
Grad 3 |
(< 1000 ‑ 500/mm3 |
|
< 1,0 ‑ 0,5 x 109/l) oder |
||
Grad 4 |
(< 500/mm3 |
|
< 0,5 x 109/l) |
||
| ||
Tabelle 3: Dosierungsempfehlungen für Brentuximab vedotin bei Hämotoxizitäten während einer BrECADD‑Kombinationstherapie
Schweregrad |
Änderung des Dosierungsschemas |
|
Leukozyten |
≥ 2500/mm3 |
Dosis und Behandlungsintervalle beibehalten. |
Neutrophile |
≥ 1500/mm3 |
|
UND |
||
Thrombozyten |
≥ 80 000/mm3 |
|
Leukozyten |
< 2000-1000/mm3 |
Die Behandlung aussetzen bis die Toxizität wieder auf den Ausgangswert zurückgegangen ist; wenn sich die Werte bis zum 28. Tag des Zyklus nicht erholen, kann eine Dosisverringerung von Brentuximab vedotin von 1,2 mg/kg bis zu einem Maximum von 120 mg alle 3 Wochen in Betracht gezogen werden. |
Neutrophile |
< 1000-500/mm3 |
|
UND |
||
Thrombozyten |
< 50 000-25 000/mm3 |
|
Leukozyten |
< 1000/mm3 |
Die Behandlung aussetzen bis die Toxizität wieder auf den Ausgangswert zurückgegangen ist, dann die Behandlung mit Brentuximab vedotin mit einer verringerten Dosis von 1,2 mg/kg bis zu einem Maximum von 120 mg alle 3 Wochen fortsetzen. |
Neutrophile |
< 500/mm3 |
|
UND |
||
Thrombozyten |
< 25 000/mm3 |
|
a. Die Einteilung basiert auf den Common Terminology Criteria for Adverse Events (CTCAE) V4.0 des National Cancer Institute (NCI), siehe Neutrophile/Granulozyten; LLN = unterer Grenzwert des Normbereichs. | ||
Bei Patienten, die nach dem BrECADD‑Schema behandelt werden, wird die Dosis bei Auftreten eines oder mehrerer Ereignisse in einem bestimmten Zyklus auf den unten angegebenen Wert gesenkt und über die nächsten Zyklen beibehalten.
Treten Ereignisse in zwei aufeinanderfolgenden Zyklen auf, wird die Dosis auf den Ausgangswert gesenkt (siehe Tabelle 4). Zu den Ereignissen gehören Leukopenie über mehr als 4 Tage, Thrombozytopenie an einem oder mehreren Tagen, Infektion CTCAE Grad 4, andere CTCAE‑Grad 4‑Toxizitäten und eine Behandlungsverzögerung von mehr als 2 Wochen aufgrund einer unzureichenden Erholung der Blutwerte.
Tabelle 4: Anfangsdosierung und Dosisverringerungsstufen für das BrECADD‑Behandlungsschema
Dosis |
Cyclophosphamid (C) |
Doxorubicin (A) |
Etoposid (E) |
Dacarbazin (D) |
Dexamethason (D) |
4 (Anfangsdosierung) |
1250 mg/m2 |
40 mg/m2 |
150 mg/m2 |
250 mg/m2 |
40 mg |
3 |
1100 mg/m2 |
40 mg/m2 |
125 mg/m2 |
250 mg/m2 |
40 mg |
2 |
950 mg/m2 |
40 mg/m2 |
100 mg/m2 |
250 mg/m2 |
40 mg |
1 |
800 mg/m2 |
40 mg/m2 |
100 mg/m2 |
250 mg/m2 |
40 mg |
Ausgangswert |
650 mg/m2 |
35 mg/m2 |
100 mg/m2 |
250 mg/m2 |
40 mg |
Periphere Neuropathie
Tabelle 5 bzw. Tabelle 6 enthalten Dosierungsempfehlungen für die Monotherapie bzw. die Kombinationstherapie für den Fall, dass sich während der Behandlung eine periphere sensorische oder motorische Neuropathie entwickelt oder verschlechtert (siehe Abschnitt 4.4).
Tabelle 5: Dosierungsempfehlungen für die Monotherapie für den Fall, dass sich eine periphere sensorische oder motorische Neuropathie entwickelt oder verschlechtert
Schweregrad der peripheren sensorischen oder motorischen Neuropathie |
Änderung der Dosis und des Zeitplans |
|
Grad 1 |
(Parästhesie und/oder |
Dosis und Behandlungsintervalle beibehalten. |
Grad 2 |
(Beeinträchtigung der |
Die Verabreichung der Dosis verzögern, bis die Toxizität wieder auf ≤ Grad 1 oder den Ausgangswert zurückgegangen ist, danach die Behandlung mit einer reduzierten Dosierung von 1,2 mg/kg bis höchstens 120 mg alle 3 Wochen fortsetzen. |
Grad 3 |
(Beeinträchtigung der |
Die Verabreichung der Dosis verzögern, bis die Toxizität wieder auf ≤ Grad 1 oder den Ausgangswert zurückgegangen ist, danach die Behandlung mit einer reduzierten Dosierung von 1,2 mg/kg bis höchstens 120 mg alle 3 Wochen fortsetzen. |
Grad 4 |
(sensorische Neuropathie, |
Behandlung abbrechen. |
a. Die Einteilung basiert auf den Common Terminology Criteria for Adverse Events (CTCAE) V3.0 des National Cancer Institute (NCI), siehe Neuropathie: motorisch; Neuropathie: sensorisch; und neuropathische Schmerzen. | ||
Tabelle 6: Dosierungsempfehlungen für die Kombinationstherapie für den Fall, dass sich eine periphere sensorische oder motorische Neuropathie entwickelt oder verschlechtert
Kombinationstherapie mit |
Kombinationstherapie mit |
Kombinationstherapie mit |
||
Schweregrad der peripheren sensorischen oder motorischen Neuropathie |
Änderung der Dosis und des Zeitplans |
Änderung der Dosis und des Zeitplans |
Änderung der Dosis und des Zeitplans |
|
Grad 1 |
(Parästhesie und/oder verminderte Reflexe, ohne Funktionsverlust) |
Dosis und Behandlungsintervalle |
Dosis und Behandlungsintervalle |
Dosis und Behandlungsintervalle |
Grad 2 |
(Beeinträchtigung der Funktion, jedoch keine Beeinträchtigung der Alltagsaktivitäten) |
Dosis auf 0,9 mg/kg bis höchstens 90 mg alle 2 Wochen verringern. |
Sensorische Neuropathie: Behandlung mit der gleichen Dosis fortsetzen. Motorische Neuropathie: Dosis auf 1,2 mg/kg bis höchstens 120 mg alle 3 Wochen verringern. |
Die Behandlung aussetzen bis die Symptome auf Werte ≤ Grad 1 oder den Ausgangswert zurückgegangen sind, dann die Behandlung mit Brentuximab vedotin mit einer verringerten Dosis von 1,2 mg/kg bis zu einem Maximum von 120 mg alle 3 Wochen wieder aufnehmen. |
Grad 3 |
(Beeinträchtigung der Alltagsaktivitäten) |
Behandlung mit ADCETRIS aussetzen bis Toxizität ≤ Grad 2, dann Behandlung mit einer niedrigeren Dosis von 0,9 mg/kg bis höchstens 90 mg alle 2 Wochen wieder aufnehmen. |
Sensorische Neuropathie: Dosis auf 1,2 mg/kg bis höchstens 120 mg alle 3 Wochen verringern. Motorische Neuropathie: Behandlung abbrechen. |
|
Grad 4 |
(sensorische Neuropathie, die stark behindernd ist, oder motorische Neuropathie, die lebensbedrohlich ist oder zu einer Lähmung führt) |
Behandlung abbrechen. |
Behandlung abbrechen. |
Behandlung abbrechen. |
a. Die Einteilung basiert auf den Common Terminology Criteria for Adverse Events (CTCAE) V4.03 des National Cancer Institute (NCI), siehe Neuropathie: motorisch; Neuropathie: sensorisch; und neuropathische Schmerzen. | ||||
Besondere Patientengruppen
Patienten mit Beeinträchtigung der Leber oder Nierenfunktionsbeeinträchtigung
Kombinationstherapie
Patienten mit eingeschränkter Nierenfunktion sollten engmaschig auf unerwünschte Ereignisse überwacht werden. Es gibt keine Erfahrungswerte aus klinischen Studien mit ADCETRIS in Kombination mit einer Chemotherapie bei Patienten mit eingeschränkter Nierenfunktion, bei denen das Serumkreatinin ≥ 2,0 mg/dl und/oder die Kreatinin‑Clearance oder die errechnete Kreatinin‑Clearance ≤ 40 ml/min beträgt. Der Einsatz von ADCETRIS in Kombination mit einer Chemotherapie sollte bei Patienten mit schwerer Nierenfunktionsstörung vermieden werden.
Patienten mit eingeschränkter Leberfunktion sollten engmaschig auf unerwünschte Ereignisse überwacht werden. Die empfohlene Startdosis bei Patienten mit leichter Leberfunktionsstörung, die ADCETRIS in Kombination mit AVD erhalten, beträgt 0,9 mg/kg, die als intravenöse Infusion über 30 Minuten alle 2 Wochen verabreicht wird. Die empfohlene Startdosis bei Patienten mit leichter Leberfunktionsstörung, die ADCETRIS in Kombination mit CHP erhalten, beträgt 1,2 mg/kg, die als intravenöse Infusion über 30 Minuten alle 3 Wochen verabreicht wird. Es gibt keine Erfahrungswerte aus klinischen Studien mit ADCETRIS in Kombination mit einer Chemotherapie bei Patienten mit eingeschränkter Leberfunktion, bei denen der Bilirubinwert die Obere Normalgrenze (ON) > 1,5‑fach übersteigt (ausgenommen sind Patienten mit Gilbert Syndrom), oder wenn der Alanin‑Aminotransferase(ALT)‑ oder der Aspartat‑Aminotransferase(AST)‑Wert die ON > 3‑fach übersteigt, oder > 5‑fach, wenn es gute Gründe gibt, diese Erhöhung auf Leber‑lokalisiertes HL zurückzuführen. Der Einsatz von ADCETRIS in Kombination mit einer Chemotherapie sollte bei Patienten mit mittelgradiger und schwerer Leberfunktionsstörung vermieden werden.
Monotherapie
Die empfohlene Startdosis bei Patienten mit schwerer Nierenfunktionsstörung beträgt 1,2 mg/kg, die als intravenöse Infusion über 30 Minuten alle 3 Wochen verabreicht wird. Patienten mit eingeschränkter Nierenfunktion sollten hinsichtlich auftretender Nebenwirkungen engmaschig überwacht werden (siehe Abschnitt 5.2).
Die empfohlene Startdosis bei Patienten mit eingeschränkter Leberfunktion beträgt 1,2 mg/kg, die als intravenöse Infusion über 30 Minuten alle 3 Wochen verabreicht wird. Patienten mit eingeschränkter Leberfunktion sollten hinsichtlich auftretender Nebenwirkungen engmaschig überwacht werden (siehe Abschnitt 5.2).
Ältere Patienten
Die Dosierungsempfehlungen für Patienten ab 65 Jahren sind dieselben wie bei Erwachsenen. Die derzeit verfügbaren Daten werden in den Abschnitten 4.8, 5.1 und 5.2 beschrieben.
Die Sicherheit und Wirksamkeit von ADCETRIS als Teil des BrECADD‑Schemas bei Patienten ab 60 Jahren ist nicht nachgewiesen.
Kinder und Jugendliche
Die Sicherheit und Wirksamkeit von ADCETRIS bei Kindern (unter 18 Jahren) sind nicht erwiesen. Die derzeit verfügbaren Daten werden in den Abschnitten 4.8, 5.1 und 5.2 beschrieben, es können jedoch keine Dosierungsempfehlungen gegeben werden.
Art der Anwendung
Die empfohlene Dosis ADCETRIS wird über 30 Minuten infundiert.
Für Hinweise zur Rekonstitution und Verdünnung des Arzneimittels vor der Anwendung siehe Abschnitt 6.6.
ADCETRIS darf nicht als intravenöse Stoßtherapie oder als Bolus verabreicht werden. ADCETRIS muss durch eine dafür reservierte intravenöse Leitung verabreicht werden und darf nicht mit anderen Arzneimitteln gemischt werden (siehe Abschnitt 6.2).
Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
Die kombinierte Anwendung von Bleomycin und ADCETRIS verursacht pulmonale Toxizität (siehe Abschnitt 4.5).
Rückverfolgbarkeit
Um die Rückverfolgbarkeit biologischer Arzneimittel zu verbessern, müssen die Bezeichnung des Arzneimittels und die Chargenbezeichnung des angewendeten Arzneimittels eindeutig dokumentiert werden.
Progressive multifokale Leukenzephalopathie
Bei mit ADCETRIS behandelten Patienten kann eine Reaktivierung des John Cunningham Virus (JCV) auftreten, die zu einer progressiven multifokalen Leukenzephalopathie (PML) und zum Tod führen kann. PML wurde bei Patienten berichtet, die diese Behandlung erhielten, nachdem sie zuvor mehrere andere Chemotherapien erhalten hatten. PML ist eine seltene demyelinisierende Erkrankung des zentralen Nervensystems, die durch die Reaktivierung von latentem JCV verursacht wird und oft tödlich verläuft.
Die Patienten sollten genau auf neue oder sich verschlechternde neurologische und kognitive Anzeichen oder Symptome für Verhaltensveränderungen, die möglicherweise auf eine PML hinweisen, überwacht werden. Die Verabreichung von ADCETRIS sollte bei jedem Verdacht auf PML unterbrochen werden. Möglichkeiten zur Abklärung des PML‑Verdachts schließen neurologische Untersuchung, Gadolinium‑Kontrast‑MRT des Gehirns und Liquor‑PCR‑Untersuchung auf JCV‑DNA oder Gehirn‑Biopsie mit Nachweis von JCV ein. Eine negative JCV‑PCR schließt PML nicht aus. Zusätzliche Nachuntersuchungen können gerechtfertigt sein, wenn keine alternative Diagnose gestellt werden kann. Die Verabreichung von ADCETRIS Dosen muss dauerhaft eingestellt werden, wenn die Diagnose von PML bestätigt wird.
Der Arzt sollte insbesondere auf Symptome achten, die auf eine PML hinweisen, und die der Patient möglicherweise nicht bemerkt (z. B. kognitive, neurologische oder psychiatrische Symptome).
Pankreatitis
Bei Patienten, die mit ADCETRIS behandelt wurden, wurde akute Pankreatitis beobachtet. Über Fälle mit tödlichem Ausgang wurde berichtet.
Patienten sollen engmaschig hinsichtlich neu auftretender oder sich verschlimmernder Schmerzen im Abdomen kontrolliert werden. Diese Schmerzen könnten auf eine akute Pankreatitis hindeuten. Für die Abklärung am Patienten sollten körperliche Untersuchungen, Laboruntersuchungen auf Serumamylase und Serumlipase, und bildgebende Verfahren des Abdomens, solche wie Ultraschall und andere geeignete Untersuchungsmethoden, herangezogen werden. Bei Verdacht auf akute Pankreatitis sollte die Gabe von ADCETRIS ausgesetzt werden. Wenn sich die Diagnose einer akuten Pankreatitis bestätigt, muss ADCETRIS abgesetzt werden.
Pulmonale Toxizität
Es wurden Fälle von pulmonaler Toxizität, einschließlich Pneumonie, interstitieller Lungenerkrankung und akutem Atemnot‑Syndrom (acute respiratory distress syndrome, ARDS), einige mit tödlichem Verlauf, bei Patienten berichtet, die mit ADCETRIS behandelt wurden. Obwohl ein kausaler Zusammenhang mit ADCETRIS nicht gesichert ist, kann das Risiko für eine pulmonale Toxizität nicht ausgeschlossen werden. Im Fall von neu auftretenden oder sich verstärkenden pulmonalen Symptomen (z. B. Husten, Dyspnoe), sollte umgehend eine diagnostische Einschätzung vorgenommen sowie eine angemessene Behandlung von Patienten eingeleitet werden. Es sollte erwogen werden die Dosierung von ADCETRIS während der Auswertung und bis zur symptomatischen Verbesserung beizubehalten.
Schwere Infektionen und opportunistische Infektionen
Bei Patienten, die mit ADCETRIS behandelt wurden, wurden schwere Infektionen wie Lungenentzündung, Staphylokokken‑Bakteriämie, Sepsis/septischer Schock (inklusive tödlichen Ausgängen), Herpes zoster und Zytomegalovirus (CMV) (Reaktivierung) sowie opportunistische Infektionen wie Pneumocystis‑jiroverci Pneumonie und orale Candidose berichtet. Die Patienten sollten während der Behandlung sorgfältig dahingehend überwacht werden, ob sich eine mögliche schwere und opportunistische Infektion entwickelt.
Reaktionen im Zusammenhang mit einer Infusion
Es wurden Fälle von Sofort und Spät-Reaktionen im Zusammenhang mit einer Infusion (infusion-related reactions (IRR)) sowie anaphylaktische Reaktionen berichtet.
Die Patienten sollten während und nach der Infusion sorgfältig überwacht werden. Wenn eine anaphylaktische Reaktion auftritt, muss die Gabe von ADCETRIS sofort und endgültig abgebrochen und eine geeignete medizinische Behandlung eingeleitet werden.
Wenn eine IRR auftritt, muss die Infusion unterbrochen werden und geeignete medizinische Maßnahmen eingeleitet werden. Die Infusion kann nach Abklingen der Symptome wieder mit einer langsameren Geschwindigkeit begonnen werden. Patienten, bei denen bereits eine IRR aufgetreten war, sollten für die nachfolgenden Infusionen entsprechend prämediziert werden. Die Prämedikation kann Paracetamol, ein Antihistaminikum und ein Corticosteroid enthalten.
Bei Patienten mit Antikörper gegen Brentuximab vedotin treten IRR häufiger und in schwererer Ausprägung auf (siehe Abschnitt 4.8).
Tumorlyse‑Syndrom
Unter Behandlung mit ADCETRIS wurden Fälle von Tumorlyse‑Syndrom (TLS) berichtet. Bei Patienten mit rasch proliferierenden Tumoren und hoher Tumorlast besteht das Risiko eines Tumorlyse‑Syndroms. Diese Patienten sollten engmaschig überwacht und entsprechend medizinisch behandelt werden. Die Behandlung von TLS kann eine forcierte Hydrierung, Überwachung der Nierenfunktion, Korrektur von Elektrolytstörungen, anti‑hyperurikämische Therapie und eine unterstützende Behandlung umfassen.
Periphere Neuropathie
ADCETRIS kann sowohl sensorische als auch motorische periphere Neuropathie verursachen. Eine durch ADCETRIS ausgelöste periphere Neuropathie ist typischerweise eine Folge kumulativer Exposition zu diesem Arzneimittel und ist in den meisten Fällen reversibel. In den klinischen Studien zeigte sich bei einem Großteil der Patienten ein vollständiges Abklingen oder eine Verbesserung der Symptome (siehe Abschnitt 4.8). Die Patienten sollten auf Anzeichen einer Neuropathie, wie Hypästhesie, Hyperästhesie, Parästhesie, Unwohlsein, ein brennendes Gefühl, neuropathische Schmerzen oder Schwäche überwacht werden. Bei Patienten mit neu auftretender oder sich verschlechternder peripherer Neuropathie kann ein Aufschub der Verabreichung und eine Dosisreduktion von ADCETRIS oder ein Absetzen der Behandlung erforderlich werden (siehe Abschnitt 4.2).
Hämatologische Toxizität
Unter ADCETRIS können Grad 3 oder Grad 4 Anämie, Thrombozytopenie und anhaltende (≥ 1 Woche) Grad 3 oder Grad 4 Neutropenie auftreten. Vor der Verabreichung jeder Dosis sollte ein komplettes Blutbild erstellt werden. Wenn sich eine Grad 3 oder Grad 4 Neutropenie entwickelt, siehe Abschnitt 4.2.
Febrile Neutropenie
Unter Behandlung mit ADCETRIS wurden Fälle von febriler Neutropenie (Fieber unbekannter Ursache, ohne klinisch oder mikrobiologisch dokumentierte Infektion mit < 1,0 x 109/l neutrophile Granulozyten, Fieber ≥ 38,5 °C; Ref. CTCAE v3) berichtet. Vor der Verabreichung jeder Dosis sollte ein komplettes Blutbild erstellt werden. Die Patienten sollten engmaschig auf Fieber überwacht werden und wenn sich eine febrile Neutropenie entwickelt, entsprechend dem besten medizinischen Verfahren behandelt werden.
Bei einer Kombinationsbehandlung mit AVD, CHP oder als BrECADD‑Schema war ein fortgeschrittenes Alter ein Risikofaktor für febrile Neutropenie.
Wenn ADCETRIS in Kombination mit AVD oder CHP gegeben wird, wird bei allen erwachsenen Patienten unabhängig von deren Alter ab der ersten Dosis eine vorhergehende Prophylaxe mit G‑CSF empfohlen.
Wenn ADCETRIS in Kombination als Teil des BrECADD‑Schemas gegeben wird, muss allen erwachsenen Patienten unabhängig von deren Alter ab dem 5. Tag jedes Zyklus eine Primärprophylaxe mit G‑CSF verabreicht werden.
Schwere Hautreaktionen (Severe Cutaneous Adverse Reactions, SCARs)
Unter Behandlung mit ADCETRIS wurden Fälle schwerer Hautreaktionen (SCARs), einschließlich Stevens‑Johnson‑Syndrom (SJS), Epidermolysis acuta toxica (TEN) sowie Arzneimittelwirkung mit Eosinophilie und systemischen Symptomen (drug reaction with eosinophilia and systemic symptoms, DRESS) gemeldet. Über tödliche Ausgänge von SJS und TEN wurde berichtet. Wenn ein SJS, TEN oder DRESS auftritt, muss ADCETRIS abgebrochen und eine geeignete medizinische Behandlung eingeleitet werden.
Gastrointestinale Komplikationen
Gastrointestinale (GI) Komplikationen einschließlich gastrointestinaler Obstruktion, Ileus, Enterokolitis, neutropenische Kolitis, Erosionen, Geschwüre, Perforationen und Hämorrhagie, einige mit Todesfolge, wurden bei Patienten, die mit ADCETRIS behandelt wurden, berichtet. Bei dem Auftreten von neuen oder sich verschlechternden GI‑Symptomen sollte umgehend eine diagnostische Auswertung und eine entsprechende Behandlung durchgeführt werden.
Hepatotoxizität
Im Zusammenhang mit ADCETRIS wurde von einer Hepatotoxizität in Form von erhöhten Alanin‑Aminotransferase‑ (ALT) und Aspartat‑Aminotransferase‑ (AST) Werten berichtet. Es sind auch schwerwiegende Fälle von Hepatotoxizität, einschließlich Todesfällen, aufgetreten. Vorbestehende Lebererkrankungen, Komorbiditäten und begleitende medikamentöse Behandlung können das Risiko ebenfalls erhöhen. Die Leberfunktion sollte vor dem Beginn einer Behandlung untersucht und bei Patienten, die ADCETRIS erhalten, regelmäßig überprüft werden. Patienten, bei denen eine Hepatotoxizität auftritt, benötigen eventuell eine Verzögerung der Behandlung, eine Änderung der Dosierung oder einen Abbruch der Behandlung mit ADCETRIS.
Hyperglykämie
In klinischen Studien wurde bei Patienten mit erhöhtem Body Mass Index (BMI) mit oder ohne Diabetes mellitus in der Anamnese über Fälle von Hyperglykämie berichtet. Allerdings sollten bei jedem Patienten, bei dem ein hyperglykämisches Ereignis auftritt, die Glukosewerte im Serum eng überwacht werden. Bei Bedarf sollte eine antidiabetische Behandlung verabreicht werden.
Paravasation an der Infusionsstelle
Es ist zu einem Paravasat während intravenösen Infusionen gekommen. Angesichts der Möglichkeit eines Paravasats wird empfohlen, die Infusionsstelle während der Arzneimittelverabreichung genau auf eine mögliche Infiltration zu überwachen.
Eingeschränkte Nieren‑ und Leberfunktion
Es liegen nur begrenzte Erfahrungen bei Patienten mit eingeschränkter Nieren‑ und Leberfunktion vor. Verfügbare Daten ergeben, dass die MMAE‑Clearance möglicherweise bei schweren Nierenfunktionsstörungen, Leberfunktionsstörungen und durch niedrige Serum‑Albumin‑Konzentrationen beeinträchtigt werden könnte (siehe Abschnitt 5.2).
CD30+ CTCL
Das Ausmaß der Behandlungsauswirkungen bei anderen CD30+ CTCL‑Subtypen außer Mycosis fungoides (MF) und primär kutanem anaplastischem großzelligem Lymphom (pcALCL) ist aufgrund fehlender belastbarer Nachweise nicht klar. In zwei einarmigen Phase‑2‑Studien mit ADCETRIS konnte die Krankheitsaktivität in den Subtypen Sézary‑Syndrom (SS), lymphomatoide Papulose (LyP) und gemischte CTCL‑Histologie nachgewiesen werden. Diese Daten legen nahe, dass die Wirksamkeit und Sicherheit auf andere CTCL CD30+ ‑Subtypen extrapoliert werden können. Dennoch sollte ADCETRIS erst nach sorgfältiger Abwägung des potenziellen Nutzen‑Risiko‑Verhältnisses im Einzelfall und mit Vorsicht bei anderen CD30+ CTCL‑Patienten eingesetzt werden (siehe Abschnitt 5.1).
Natriumgehalt der sonstigen Bestandteile
Dieses Arzneimittel enthält 13,2 mg Natrium pro Durchstechflasche, entsprechend 0,7 % der von der WHO für einen Erwachsenen empfohlenen maximalen täglichen Natriumaufnahme mit der Nahrung von 2 g.
Polysorbatgehalt der sonstigen Bestandteile
Dieses Arzneimittel enthält 2 mg Polysorbat 80 pro Durchstechflasche entsprechend 0,2 mg/ml. Polysorbate können allergische Reaktionen hervorrufen.
Wechselwirkungen mit Arzneimitteln, die über den CYP3A4‑Stoffwechselweg (CYP3A4‑Inhibitoren/Induktoren) metabolisiert werden
Die gleichzeitige Gabe von Brentuximab vedotin mit Ketoconazol, einem starken CYP3A4‑ und P‑gp‑Inhibitor, erhöhte die Exposition von dem Antimikrotubuli‑Wirkstoff MMAE um rund 73 % und beeinflusste die Plasma‑Exposition von Brentuximab vedotin nicht. Daher kann die gleichzeitige Gabe von Brentuximab vedotin zusammen mit starken CYP3A4‑und P‑gp‑Inhibitoren dazu führen, dass die Häufigkeit von Neutropenie zunimmt. Wenn sich eine Neutropenie entwickelt, siehe Tabelle 1 und Tabelle 2 für Dosierungsempfehlungen bei Neutropenie (siehe Abschnitt 4.2).
Die gleichzeitige Gabe von Brentuximab vedotin mit Rifampicin, einem starken CYP3A4‑Induktor, veränderte die Plasma‑Exposition von Brentuximab vedotin nicht. Obwohl die PK‑Daten nur begrenzt sind, scheint die gleichzeitige Gabe von Rifampicin zu einer reduzierten Plasma‑Konzentration von nachweisbaren MMAE‑Metaboliten zu führen.
Die gleichzeitige Gabe von Midazolam, einem CYP3A4‑Substrat, zusammen mit Brentuximab vedotin beeinflusste den Metabolismus von Midazolam nicht. Daher ist nicht zu erwarten, dass Brentuximab vedotin die Exposition von Arzneimitteln, die über CYP3A4‑Enzyme metabolisiert werden, beeinflusst.
Doxorubicin, Vinblastin und Dacarbazin (AVD)
Die pharmakokinetischen Eigenschaften des Antikörper‑Wirkstoff‑Konjugats (antibody drug conjugate, ADC) und von MMAE im Serum bzw. Plasma nach einer Verabreichung von Brentuximab vedotin in Kombination mit AVD ähnelten denen bei der Monotherapie.
Die gleichzeitige Anwendung von Brentuximab vedotin hatte keinen Einfluss auf die Plasmaexposition von AVD.
Cyclophosphamid, Doxorubicin und Prednison (CHP)
Die pharmakokinetischen Eigenschaften des ADC und von MMAE im Serum bzw. Plasma nach einer Verabreichung von Brentuximab vedotin in Kombination mit CHP ähnelten denen der Monotherapie.
Es wird nicht erwartet, dass die gleichzeitige Anwendung von Brentuximab vedotin Einfluss auf die Exposition von CHP hat.
Bleomycin
Es wurden keine formellen Arzneimittelwechselwirkungsstudien mit Brentuximab vedotin und Bleomycin (B) durchgeführt. In einer Phase‑1‑Dosisfindungs‑ und Sicherheitsstudie (SGN35‑009) wurde bei 11 von 25 Patienten (44 %), die mit Brentuximab vedotin plus ABVD behandelt wurden, eine nicht akzeptable pulmonale Toxizität (einschließlich 2 tödlicher Ereignisse) festgestellt. Bei Brentuximab vedotin + AVD wurden keine pulmonale Toxizität oder tödliche Ereignisse gemeldet. Deshalb ist die gleichzeitige Anwendung von ADCETRIS und Bleomycin kontraindiziert (siehe Abschnitt 4.3).
Etoposid, Cyclophosphamid, Doxorubicin, Dacarbazin, Dexamethason (BrECADD‑Schema)
Die Pharmakokinetik von ADC und MMAE wurde im Rahmen von BrECADD nicht untersucht. Es wird nicht erwartet, dass die Exposition gegenüber Brentuximab vedotin und die gleichzeitige Chemotherapie im BrECADD‑Schema beeinträchtigt werden.
Frauen in gebärfähigem Alter
Frauen im gebärfähigen Alter sollen während und bis zu 6 Monate nach der Behandlung mit ADCETRIS zwei zuverlässige Verhütungsmethoden anwenden.
Schwangerschaft
Bisher liegen keine Erfahrungen mit der Anwendung von ADCETRIS bei Schwangeren vor. Tierexperimentelle Studien haben eine Reproduktionstoxizität gezeigt (siehe Abschnitt 5.3).
ADCETRIS darf während der Schwangerschaft nicht angewendet werden, es sei denn, der potentielle Nutzen für die Mutter ist deutlich größer als das mögliche Risiko für den Fötus. Wenn eine schwangere Frau behandelt werden muss, muss sie deutlich über das potenzielle Risiko für den Fötus hingewiesen werden.
Der Abschnitt Fertilität weiter unten enthält Hinweise zur Beratung von Frauen, deren männliche Partner mit ADCETRIS behandelt werden.
Stillzeit
Es gibt nur ungenügende Informationen darüber, ob Brentuximab vedotin oder seine Metabolite in die Muttermilch übergehen.
Ein Risiko für das Neugeborene/Kind kann nicht ausgeschlossen werden.
Es sollte eine Entscheidung darüber getroffen werden, ob das Stillen zu unterbrechen ist oder ob auf die Behandlung verzichtet werden soll/die Behandlung zu unterbrechen ist. Dabei ist sowohl das potentielle Risiko des Stillens für das Kind als auch der Nutzen der Therapie für die Frau zu berücksichtigen.
Fertilität
In präklinischen Studien verursachte die Behandlung mit Brentuximab vedotin Hodentoxizität und kann möglicherweise die männliche Fertilität verändern. Es hat sich gezeigt, dass MMAE aneugenische Eigenschaften besitzt (siehe Abschnitt 5.3). Männern, die mit diesem Arzneimittel behandelt werden, wird empfohlen, vor der Behandlung Sperma‑Proben einfrieren zu lassen. Männern, die mit diesem Arzneimittel behandelt werden, wird empfohlen, während der Behandlung und bis zu 6 Monate nach der letzten Dosis kein Kind zu zeugen.
ADCETRIS kann einen mäßigen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen (z.B. Schwindelgefühl) haben, siehe Abschnitt 4.8.
Zusammenfassung des Sicherheitsprofils
Das Sicherheitsprofil von ADCETRIS basiert auf den verfügbaren Daten klinischer Studien, dem Named Patient Programm (NPP) und bisherigen Erfahrungen nach der Markteinführung. Die Häufigkeiten der unten und in Tabelle 7 beschriebenen Nebenwirkungen wurden auf Basis der Daten von klinischen Studien bestimmt.
Monotherapie
Im gepoolten Datensatz von ADCETRIS als Monotherapie in den HL‑, sALCL‑ und CTCL‑Studien (SG035‑0003, SG035‑0004, SGN35‑005, SGN35‑006, C25001, C25006 und C25007, siehe Abschnitt 5.1) waren die häufigsten Nebenwirkungen (≥ 10 %) Infektionen, periphere sensorische Neuropathie, Übelkeit, Ermüdung/Fatigue, Diarrhö, Fieber, Neutropenie, Infektionen der oberen Atemwege, Arthralgie, Ausschlag, Husten, Erbrechen, Pruritus, periphere motorische Neuropathie, Reaktionen im Zusammenhang mit einer Infusion, Obstipation, Dyspnoe, Myalgie, erniedrigtes Gewicht und Abdominalschmerz.
Schwerwiegende Nebenwirkungen traten bei 12 % der Patienten auf. Die Häufigkeit von einmaligen, schwerwiegenden Nebenwirkungen lag bei ≤ 1 %.
Unerwünschte Ereignisse führten bei 24 % der Patienten, die ADCETRIS erhielten, zum Abbruch der Behandlung.
Die Sicherheitsdaten bei Patienten, die erneut mit ADCETRIS (SGN35‑006, siehe Abschnitt 5.1) behandelt wurden, entsprachen denen, die in den kombinierten Phase‑2‑Zulassungsstudien beobachtet wurden, mit Ausnahme der peripheren motorischen Neuropathie, die eine höhere Inzidenz aufwies (28 % gegenüber 9 % in den Phase‑2‑Zulassungsstudien) und hauptsächlich Grad 2 war. Patienten hatten auch eine höhere Inzidenz von Arthralgie, Anämie Grad 3 und Rückenschmerzen im Vergleich zu den in den kombinierten Phase‑2‑Zulassungsstudien beobachteten Patienten.
Die Sicherheitsdaten bei Patienten mit rezidiviertem oder refraktärem HL ohne vorausgegangene Stammzelltransplantation und mit einer Behandlung in der empfohlenen Dosierung von 1,8 mg/kg alle drei Wochen in einer einarmigen Phase‑4‑Studie (n = 60), in der Phase 1 in Dosis‑Eskalations‑ und klinisch‑pharmakologischen Studien (n = 15 Patienten) sowie bei dem NPP (n = 26 Patienten) (siehe Abschnitt 5.1) entsprachen dem Sicherheitsprofil der zulassungsrelevanten klinischen Studien.
Kombinationstherapie (AVD/CHP)
Informationen zur Sicherheit von Chemotherapeutika, die in Kombination mit ADCETRIS (Doxorubicin, Vinblastin und Dacarbazin (AVD) oder Cyclophosphamid, Doxorubicin und Prednison (CHP)) verabreicht werden, finden sich in der jeweiligen Zusammenfassung der Merkmale des Arzneimittels (Fachinformation).
In den Studien zu ADCETRIS als Kombinationstherapie bei 662 Patienten mit fortgeschrittenem, bislang unbehandeltem HL (C25003) und 223 Patienten mit bislang unbehandeltem CD30+ Peripheres T‑Zell‑Lymphom ohne weitere Spezifizierung (PTCL) (SGN35‑014), waren die häufigsten Nebenwirkungen (≥ 10 %): Infektionen, Neutropenie, periphere sensorische Neuropathie, Übelkeit, Obstipation, Erbrechen, Diarrhö, Ermüdung, Fieber, Alopezie, Anämie, erniedrigtes Gewicht, Stomatitis, febrile Neutropenie, Abdominalschmerz, verminderter Appetit, Schlaflosigkeit, Knochenschmerzen, Ausschlag, Husten, Dyspnoe, Arthralgie, Myalgie, Rückenschmerzen, periphere motorische Neuropathie, Infektionen der oberen Atemwege und Schwindelgefühl.
Bei Patienten, die eine ADCETRIS‑Kombinationstherapie erhielten, traten bei 34 % der Patienten schwerwiegende Nebenwirkungen auf. Schwerwiegende Nebenwirkungen, die bei mindestens 3 % der Patienten auftraten, waren febrile Neutropenie (15 %), Fieber (5 %) und Neutropenie (3 %).
Unerwünschte Ereignisse führten bei 10 % der Patienten zum Abbruch der Behandlung. Zu den unerwünschten Ereignissen, die bei ≥ 2 % der Patienten zum Abbruch der Behandlung führten, gehörten periphere sensorische Neuropathie und periphere Neuropathie.
Tabellarische Auflistung der Nebenwirkungen
Die Nebenwirkungen von ADCETRIS sind gemäß MedDRA‑System nach Organklassen und dem bevorzugten Terminus aufgelistet (siehe Tabelle 7). Innerhalb der Systemorganklassen wird die Häufigkeit der Nebenwirkungen wie folgt klassifiziert: sehr häufig (≥ 1/10); häufig (≥ 1/100, < 1/10); gelegentlich (≥ 1/1 000, < 1/100); selten (≥ 1/10 000, < 1/1 000); sehr selten (< 1/10 000); nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar). Innerhalb jeder Häufigkeitsgruppe werden die Nebenwirkungen nach abnehmendem Schweregrad angegeben.
Tabelle 7: Nebenwirkungen von ADCETRIS
Organklasse |
Nebenwirkungen |
Nebenwirkungen (Kombinationstherapie) |
Infektionen und parasitäre Erkrankungen | ||
Sehr häufig |
Infektiona, Infektion der oberen Atemwege |
Infektiona, Infektion der oberen Atemwege |
Häufig |
Herpes zoster, Pneumonie, Herpes simplex, orale Candidose |
Pneumonie, orale Candidose, Sepsis/ septischer Schock, Herpes zoster |
Gelegentlich |
Pneumocystis jirovecii-Pneumonie, Staphylokokken‑Bakteriämie, Zytomegalovirusinfektion oder Reaktivierung dieser Infektion, Sepsis/septischer Schock |
Herpes simplex, Pneumocystis jirovecii-Pneumonie |
Nicht bekannt |
Progressive multifokale Leukoenzephalopathie |
|
Erkrankungen des Blutes und des Lymphsystems | ||
Sehr häufig |
Neutropenie |
Neutropeniea, Anaemie, febrile Neutropenie |
Häufig |
Anämie, Thrombozytopenie |
Thrombozytopenie |
Gelegentlich |
Febrile Neutropenie |
|
Erkrankungen des Immunsystems | ||
Gelegentlich |
Anaphylaktische Reaktionen |
Anaphylaktische Reaktionen |
Stoffwechsel‑ und Ernährungsstörungen | ||
Sehr häufig |
Appetit vermindert |
|
Häufig |
Hyperglykämie |
Hyperglykämie |
Gelegentlich |
Tumorlyse‑Syndrom |
Tumorlyse‑Syndrom |
Psychiatrische Erkrankungen | ||
Sehr häufig |
Schlaflosigkeit |
|
Erkrankungen des Nervensystems | ||
Sehr häufig |
Periphere sensorische Neuropathie, periphere motorische Neuropathie |
Periphere sensorische Neuropathiea, periphere motorische Neuropathiea, Schwindelgefühl |
Häufig |
Schwindelgefühl |
|
Gelegentlich |
Demyelinisierende Polyneuropathie |
|
Erkrankungen der Atemwege, des Brustraums und des Mediastinums | ||
Sehr häufig |
Husten, Dyspnoe |
Husten, Dyspnoe |
Erkrankungen des Gastrointestinaltrakts | ||
Sehr häufig |
Übelkeit, Diarrhö, Erbrechen, Obstipation, Abdominalschmerz |
Übelkeit, Obstipation, Erbrechen, Diarrhö, Abdominalschmerz, Stomatitis |
Gelegentlich |
Akute Pankreatitis |
Akute Pankreatitis |
Leber‑ und Gallenerkrankungen | ||
Häufig |
Erhöhte Alanin-Aminotransferase/Aspartat-Aminotransferase (ALT/AST) |
Erhöhte Alanin-Aminotransferase/Aspartat-Aminotransferase (ALT/AST) |
Erkrankungen der Haut und des Unterhautgewebes | ||
Sehr häufig |
Ausschlaga, Pruritus |
Alopezie, Ausschlaga |
Häufig |
Alopezie |
Pruritus |
Gelegentlich |
Stevens‑Johnson‑Syndrom/ Epidermolysis acuta toxica |
Stevens‑Johnson‑Syndromb |
Nicht bekannt |
Arzneimittelwirkung mit Eosinophilie und systemischen Symptomen (DRESS) |
|
Skelettmuskulatur‑, Bindegewebs‑ und Knochenerkrankungen | ||
Sehr häufig |
Arthralgie, Myalgie |
Knochenschmerzen, Arthralgie, Myalgie, Rückenschmerzen |
Häufig |
Rückenschmerzen |
|
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort | ||
Sehr häufig |
Ermüdung/Fatigue, Fieber, Reaktion im Zusammenhang mit einer Infusiona |
Ermüdung/Fatigue, Fieber |
Häufig |
Schüttelfrost |
Reaktion im Zusammenhang mit einer Infusion a, Schüttelfrost |
Nicht bekannt |
Extravasation an der Infusionsstellec |
|
Untersuchungen | ||
Sehr häufig |
Gewicht erniedrigt |
Gewicht erniedrigt |
a. Entspricht der Zusammenfassung der bevorzugten Begriffe. | ||
Kombinationstherapie (BrECADD‑Schema)
Für Informationen zur Sicherheit von Chemotherapeutika, die in Kombination mit ADCETRIS (Etoposid, Cyclophosphamid, Doxorubicin, Dacarbazin, Dexamethason [BrECADD]) verabreicht werden, wird auf die jeweiligen Zusammenfassungen der Merkmale des Arzneimittels (Fachinformationen) verwiesen.
In der HD21‑Studie erhielten 747 Patienten BrECADD und 741 Patienten eBEACOPP (eskaliertes Regime aus Bleomycin [B], Etoposid [E], Doxorubicin [A], Cyclophosphamid [C], Vincristin [O], Procarbazin [P] und Prednison [P]). Das Sicherheitsprofil von ADCETRIS bei Patienten, die BrECADD erhielten, entsprach dem anderer Kombinationstherapien (AVD/CHP).
Schwerwiegende Nebenwirkungen traten bei 39,4 % der mit BrECADD behandelten Patienten auf sowie bei 36,4 % der Patienten, die eBEACOPP erhielten. Die häufigsten schwerwiegenden Nebenwirkungen bei Patienten, die BrECADD erhielten (> 3 %), waren febrile Neutropenie (19,3 %), Fieber (3,9 %) und Neutropenie (3,2 %).
Schwerwiegende kardiale Nebenwirkungen traten bei 2,7 % der Patienten, die BrECADD erhielten, und bei 1,1 % der Patienten, die eBEACOPP erhielten, auf. Die häufigste schwerwiegende kardiale Nebenwirkung bei Patienten, die BrECADD erhielten (> 0,5 %), war Tachykardie (0,9 %).
Schwerwiegende unerwünschte Ereignisse führten bei 2 % der Patienten in den BrECADD- und eBEACOPP-Armen zum Abbruch der Behandlung. Die häufigsten schwerwiegenden unerwünschten Ereignisse, die im BrECADD-Arm zum Abbruch führten, waren febrile Neutropenie (0,3 %) und Herzinsuffizienz (0,3 %).
Beschreibung ausgewählter Nebenwirkungen
Neutropenie und febrile Neutropenie
Monotherapie
Neutropenie führte in klinischen Studien bei 13 % der Patienten zu Dosisverzögerungen. Neutropenie vom Grad 3 wurde bei 13 % und Neutropenie vom Grad 4 bei 5 % der Patienten berichtet. Bei einem Patienten musste wegen Neutropenie die Dosis verringert und bei einem weiteren Patienten die Behandlung aufgrund von Neutropenie abgebrochen werden.
Unter dieser Behandlung kann sich eine schwere und länger anhaltende (≥ 1 Woche) Neutropenie entwickeln, wodurch sich das Risiko der Patienten für schwerwiegende Infektionen erhöhen kann. Febrile Neutropenie wurde bei weniger als 1 % der Patienten berichtet (siehe Abschnitt 4.2).
Bei Patienten in den Phase‑2‑Zulassungsstudien (SG035‑0003 und SG035‑0004) war die mittlere Dauer der Grad 3 oder Grad 4 Neutropenie beschränkt (1 Woche); 2 % der Patienten hatten eine Grad 4‑Neutropenie, die ≥ 7 Tage dauerte. Weniger als die Hälfte der Patienten in der pivotalen Phase‑2‑Population mit Grad 3 oder Grad 4 Neutropenie wies zeitlich assoziierte Infektionen auf und die Mehrheit der zeitlich assoziierten Infektionen hatte einen Schweregrad von 1 oder 2.
Kombinationstherapie
In den klinischen Studien C25003 (ADCETRIS + AVD) und SGN35-014 (ADCETRIS + CHP) mit ADCETRIS als Kombinationstherapie führte Neutropenie bei 19 % der Patienten zum Aussetzen der Behandlung. Eine Neutropenie Grad 3 wurde bei 17 % und eine Neutropenie Grad 4 bei 41 % der Patienten gemeldet. Zwei Prozent der Patienten benötigten eine Dosisverringerung und < 1 % setzten eines oder mehrere der Studienarzneimittel aufgrund von Neutropenie ab.
Eine febrile Neutropenie wurde bei 20 % der Patienten gemeldet, die vorab keine Prophylaxe mit G‑CSF erhalten hatten (siehe Abschnitt 4.2). Die Häufigkeit febriler Neutropenie betrug bei den Patienten, die vorab eine Prophylaxe mit G‑CSF erhalten hatten, 13 %.
In der klinischen Studie HD21 (BrECADD) zu ADCETRIS als Kombinationstherapie führte Neutropenie bei 0,5 % der Patienten zu einer Verzögerung der Behandlung. Neutropenie von Grad 3 wurde bei 0,5 % und Neutropenie von Grad 4 bei 9 % der Patienten gemeldet. Bei 1,1 % der Patienten war eine Dosisverringerung erforderlich; es gab keine Behandlungsabbrüche aufgrund einer schweren Neutropenie. Alle Patienten erhielten eine Primärprophylaxe mit G-CSF (siehe Abschnitt 4.2). Die Häufigkeit von febriler Neutropenie betrug 26,5 % bei Patienten, die BrECADD erhielten.
Schwere Infektionen und opportunistische Infektionen
Monotherapie
Schwere Infektionen und opportunistische Infektionen traten in klinischen Studien bei 10 % der Patienten auf, Sepsis und septischer Schock traten bei < 1 % der Patienten auf. Die am häufigsten berichteten opportunistischen Infektionen waren Herpes zoster und Herpes simplex.
Kombinationstherapie
In den klinischen Studien (C25003 [ADCETRIS + AVD] und SGN35-014 [ADCETRIS + CHP]) zu ADCETRIS als Kombinationstherapie traten bei 15 % der Patienten schwerwiegende Infektionen einschließlich opportunistischer Infektionen auf; Sepsis, neutropenische Sepsis, septischer Schock oder Bakteriämie traten bei 4 % der Patienten auf. Die am häufigsten gemeldeten opportunistischen Infektionen waren Herpesvirusinfektionen.
In der klinischen Studie (HD21 [BrECADD]) zu ADCETRIS als Kombinationstherapie traten bei 14,3 % der Patienten schwere Infektionen und parasitäre Erkrankungen auf. Die am häufigsten gemeldeten Ereignisse waren Infektionen (2 %), Lungenentzündung (1,7 %) und neutropenische Infektionen (1,2 %).
Periphere Neuropathie
Monotherapie
In klinischen Studien trat bei 57 % der Patienten eine behandlungsbedingte Neuropathie auf, eine periphere motorische Neuropathie trat bei 13 % der Patienten auf. Die periphere Neuropathie führte bei 15 % zu einem Abbruch der Behandlung, bei 15 % zu einer Dosisverringerung und bei 16 % zu Dosisverzögerungen. Bei Patienten, bei denen eine periphere Neuropathie auftrat, betrug die mediane Zeit bis zum Auftreten der peripheren Neuropathie 12 Wochen. Die mediane Dauer der Behandlung von Patienten, die die Behandlung aufgrund einer peripheren Neuropathie abbrachen, betrug 11 Zyklen.
Bei denjenigen Patienten, bei denen in den Phase‑2‑Zulassungsstudien (SG035‑0003 und SG035‑0004) und in den randomisierten Phase‑3‑Monotherapiestudien (SGN35‑005 und C25001) eine periphere Neuropathie auftrat, reichte die mediane Nachverfolgungszeit ab dem Ende der Behandlung bis zur letzten Untersuchung von 48,9 bis zu 98 Wochen. Zum Zeitpunkt der letzten Untersuchung waren bei den meisten Patienten (82 – 85 %), bei denen eine periphere Neuropathie aufgetreten war, die Symptome der peripheren Neuropathie abgeklungen bzw. hatten sich gebessert. Insgesamt betrug die mediane Dauer bis zum Abklingen bzw. bis zur Verbesserung der peripheren Neuropathiesymptome 16 bis 23,4 Wochen.
Bei Patienten mit rezidiviertem oder refraktärem HL oder sALCL, die erneut mit ADCETRIS (SGN35‑006) behandelt wurden, zeigte sich bei einem Großteil der Patienten (80 %) zum Zeitpunkt der letzten Untersuchung ebenfalls eine Verbesserung bzw. ein völliges Abklingen der Symptome der peripheren Neuropathie.
Kombinationstherapie
In der klinischen Studie zu ADCETRIS als Kombinationstherapie mit AVD trat bei 67 % der Patienten eine behandlungsbedingte Neuropathie auf; eine periphere motorische Neuropathie trat bei 11 % der Patienten auf. Die periphere Neuropathie führte bei 7 % zu einem Abbruch der Behandlung, bei 21 % zu einer Dosisverringerung und bei 1 % der Patienten zu einem Aussetzen der Behandlung. Bei den Patienten, bei denen eine periphere Neuropathie auftrat, betrug die mediane Zeit bis zum Auftreten der peripheren Neuropathie 8 Wochen. Patienten, die die Behandlung aufgrund einer peripheren Neuropathie abbrachen, erhielten im Median 8 Dosen ADCETRIS + AVD bevor die Behandlung mit einem oder mehreren Wirkstoffen abgebrochen wurde.
Bei den Patienten, bei denen eine periphere Neuropathie auftrat, lag die mediane Nachverfolgungszeit vom Ende der Behandlung bis zur letzten Untersuchung bei ca. 286 Wochen. Zum Zeitpunkt der letzten Untersuchung waren bei den meisten Patienten (86 %), bei denen eine periphere Neuropathie aufgetreten war, die Symptome der peripheren Neuropathie abgeklungen bzw. hatten sich gebessert. Insgesamt betrug die mediane Dauer bis zum Abklingen bzw. bis zur Verbesserung der Symptome einer peripheren Neuropathie17 Wochen (Bereich von 0 Wochen bis 283 Wochen).
In der klinischen Studie mit ADCETRIS als Kombinationstherapie mit CHP trat bei 52 % der Patienten eine behandlungsbedingte Neuropathie auf; eine periphere motorische Neuropathie trat bei 9 % der Patienten auf. Eine periphere Neuropathie führte bei 1 % zu einem Abbruch der Behandlung, bei 7 % zu einer Dosisverringerung und bei < 1 % der Patienten zu einem Aussetzen der Behandlung. Bei den Patienten, bei denen eine periphere Neuropathie auftrat, betrug die mediane Zeit bis zum Auftreten der peripheren Neuropathie 9,1 Wochen. Patienten, die die Behandlung aufgrund einer peripheren Neuropathie abbrachen, erhielten im Median 5 Dosen A+CHP, bevor die Behandlung mit einem oder mehreren Wirkstoffen abgebrochen wurde.
Bei denjenigen Patienten, bei denen eine periphere Neuropathie auftrat, lag die mediane Nachverfolgungszeit vom Ende der Behandlung bis zur letzten Untersuchung bei ca. 177 Wochen. Zum Zeitpunkt der letzten Untersuchung waren bei 64 % der Patienten, bei denen eine periphere Neuropathie aufgetreten war, die Symptome der peripheren Neuropathie abgeklungen bzw. hatten sich gebessert. Insgesamt betrug die mediane Dauer bis zum Abklingen bzw. bis zur Verbesserung der peripheren Neuropathiesymptome 19 Wochen (Bereich von 0 Wochen bis 205 Wochen).
In der klinischen Studie (HD21 [BrECADD]) zu ADCETRIS als Kombinationstherapie trat bei 38,8 % der Patienten eine behandlungsbedingte periphere sensorische Neuropathie auf; eine periphere motorische Neuropathie trat bei 3,6 % der Patienten auf. Periphere sensorische Neuropathie als schwerwiegendes unerwünschtes Ereignis führte bei keinem Patienten zum Abbruch der Behandlung, bei 4,7 % zu einer Dosisverringerung und bei 1,5 % zu einer Verzögerung der Behandlung. Periphere motorische Neuropathie als schwerwiegendes unerwünschtes Ereignis führte bei keinem Patienten zum Abbruch der Behandlung, bei 0,7 % zu einer Dosisreduktion und bei 0,1 % zu einer Verzögerung der Behandlung.
Reaktionen im Zusammenhang mit einer Infusion (IRR)
Monotherapie
IRR wie Kopfschmerzen, Ausschlag, Rückenschmerzen, Erbrechen, Schüttelfrost, Übelkeit, Atemnot, Pruritus und Husten wurden von 12 % der Patienten berichtet. Anaphylaktische Reaktionen wurden berichtet (siehe Abschnitt 4.4). Die Symptome einer anaphylaktischen Reaktion können unter anderem Urtikaria, Angioödem, Hypotonie und Bronchospasmus umfassen, müssen sich aber nicht darauf beschränken.
Kombinationstherapie
In den klinischen Studien (C25003 [ADCETRIS + AVD] und SGN35-014 [ADCETRIS + CHP]), IRRs, wie Kopfschmerzen, Ausschlag, Rückenschmerzen, Erbrechen, Schüttelfrost, Übelkeit, Dyspnoe, Pruritus, Husten, Schmerzen an der Infusionsstelle und Fieber wurden bei 8 % der Patienten berichtet. Anaphylaktische Reaktionen wurden berichtet (siehe Abschnitt 4.4). Symptome einer anaphylaktischen Reaktion können unter anderem Urtikaria, Angioödem, Hypotonie und Bronchospasmus sein.
Immunogenität
In klinischen Studien wurden die Patienten in regelmäßigen Abständen mit einem empfindlichen elektrochemisch lumineszierenden Immunoassay auf Antikörper gegen Brentuximab vedotin untersucht. Bei Patienten mit Antikörpern gegen Brentuximab vedotin wurde eine höhere Inzidenz von Reaktionen im Zusammenhang mit einer Infusion beobachtet als bei Patienten, die als temporär positiv oder negativ getestet wurden.
Das Vorhandensein von Antikörpern gegen Brentuximab vedotin korrelierte nicht mit einem klinisch relevanten Rückgang der Brentuximab vedotin Serumspiegel und führte nicht zu einer Verminderung der Wirksamkeit von Brentuximab vedotin. Obwohl das Vorhandensein von Antikörpern gegen Brentuximab vedotin nicht zwangsläufig die Entwicklung einer IRR prognostiziert, gab es eine höhere Inzidenz von IRR bei Patienten, die anhaltend Anti-Wirkstoff-Antikörper‑positiv (antidrug antibody, ADA) waren im Vergleich zu Patienten, die temporär ADA‑positiv bzw. niemals ADA‑positiv waren.
Monotherapie‑Studie C25002
Bei den pädiatrischen Patienten, die als ADA‑positiv bestätigt wurden, gab es einen Trend zu einer erhöhten Brentuximab‑vedotin‑Clearance. Es wurden keine Patienten im Alter unter 12 Jahren (0 von 11) und 2 Patienten im Alter ab 12 Jahren (2 von 23) anhaltend ADA‑positiv.
Studie zur kombinierten Anwendung C25004
Der Anteil an ADA‑Positivität war in der Studie C25004 gering; 4 Patienten (im Alter von ≥ 12 Jahren) von 59 Patienten wurden vorübergehend ADA‑positiv, und kein Patient wurde anhaltend ADA‑positiv. Aufgrund der geringen Anzahl von vorübergehend ADA‑positiven Patienten ist die Auswirkung von ADA auf die Wirksamkeit uneindeutig.
Kinder und Jugendliche
Monotherapie‑Studie C25002
Die Sicherheit wurde in einer Phase‑1/2‑Studie an pädiatrischen Patienten im Alter von 7‑17 Jahren (n = 36) mit rezidiviertem oder refraktärem (r/r) HL und sALCL untersucht (siehe Abschnitt 5.1). Im Rahmen dieser Studie an 36 Patienten wurden keine neuen Sicherheitsbedenken gemeldet.
Studie zur kombinierten Anwendung C25004
Die Sicherheit wurde in einer offenen, multizentrischen Studie an 59 pädiatrischen Patienten im Alter von 6 bis 17 Jahren mit zuvor unbehandelter klassischer CD30+ HL‑Erkrankung im fortgeschrittenen Stadium in Kombination mit einer Chemotherapie untersucht (siehe Abschnitt 5.1). In dieser Studie wurden keine neuen Sicherheitsbedenken gemeldet. Die in dieser Studie am häufigsten gemeldete schwerwiegende Nebenwirkung war febrile Neutropenie (17 %). Eine G‑CSF‑Prophylaxe wurde in das Ermessen des Arztes gestellt. In dieser Studie wurden bei 24 % der pädiatrischen Patienten Periphere Neuropathie‑Ereignisse (gemäß standardisierter MedDRA‑Abfrage) gemeldet.
Ältere Patienten
Monotherapie
Das Sicherheitsprofil bei älteren Patienten entspricht im Wesentlichen dem von erwachsenen Patienten. Allerdings sind ältere Patienten möglicherweise anfälliger für Ereignisse wie Pneumonie, Neutropenie und febrile Neutropenie.
Kombinationstherapie
Bei älteren Patienten aus den Studien C25003 (ADCETRIS + AVD) und SGN35-014 (ADCETRIS + CHP) (≥ 60 Jahre; n = 186 [21 %]) war die Inzidenz unerwünschter Ereignisse in allen Behandlungsarmen ähnlich. Bei älteren Patienten wurden mehr schwerwiegende unerwünschte Ereignisse und Dosisveränderungen (einschließlich Aussetzen der Verabreichung, Dosisreduktionen und Behandlungsabbrüche) im Vergleich zur Gesamtpopulation der Studie berichtet. Das fortgeschrittene Alter stellte bei den Patienten in beiden Armen einen Risikofaktor für febrile Neutropenie dar. Bei älteren Patienten, die eine G‑CSF‑Primärprophylaxe erhalten hatten, lag die Inzidenz von Neutropenie und febriler Neutropenie unter der derjenigen, die keine G‑CSF‑Primärprophylaxe erhalten hatten.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen‑Risiko‑Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung über das Bundesinstitut für Impfstoffe und biomedizinische Arzneimittel - Paul-Ehrlich-Institut - Paul-Ehrlich-Str. 51-59, 63225 Langen, Tel.: +49 6103 77 0, Fax: +49 6103 77 1234, Website: www.pei.de anzuzeigen.
Es gibt kein bekanntes Antidot bei einer Überdosierung mit ADCETRIS. Im Falle einer Überdosierung sollte der Patient engmaschig auf Nebenwirkungen, vor allem Neutropenie, überwacht werden und eine unterstützende Behandlung eingeleitet werden (siehe Abschnitt 4.4).
Pharmakotherapeutische Gruppe: Antineoplastische Mittel; monoklonale Antikörper und Antikörper‑Wirkstoff‑Konjugate; ATC‑Code: L01FX05
Wirkmechanismus
Brentuximab vedotin ist ein Antikörper‑Wirkstoff‑Konjugat (ADC), das ein Zytostatikum freisetzt, und selektiv bei CD30‑tragenden Tumorzellen eine Apoptose auslöst. Präklinische Daten deuten darauf hin, dass die biologische Aktivität von Brentuximab vedotin auf einem mehrstufigen Prozess beruht. Durch Bindung des ADC an CD30 auf der Zellenoberfläche wird die Internalisierung des ADC‑CD30‑Komplexes ausgelöst, der dann in das lysosomale Kompartiment eingeschleust wird. Innerhalb der Zelle wird durch eine proteolytische Spaltung ein klar definierter aktiver Bestandteil, MMAE, freigesetzt. Die Bindung von MMAE an Tubulin stört das Mikrotubuli‑Netzwerk innerhalb der Zelle, wodurch der Zellzyklus unterbrochen und ein programmierter Zelltod der CD30‑exprimierenden Tumorzelle ausgelöst wird.
Bei klassischem HL, sALCL und CTCL‑Subtypen (einschließlich MF und pcALCL) ist CD30 als Antigen auf der Oberfläche der malignen Zellen exprimiert. Diese Expression ist unabhängig vom Krankheitsstadium, der Therapielinie oder dem Transplantationsstatus. Diese Eigenschaften machen aus CD30 ein Ziel für eine therapeutische Intervention. Durch den auf CD30 gerichteten Wirkmechanismus ist Brentuximab vedotin in der Lage, Chemotherapie‑Resistenzen zu überwinden, da CD30 gleichbleibend bei Patienten exprimiert wird, die refraktär auf Kombinationschemotherapien sind, ungeachtet dem vorherigen Transplantationsstatus. Der auf CD30 gerichtete Wirkmechanismus von Brentuximab vedotin, die fortgesetzte Expression von CD30 im Verlauf einer klassischen HL‑, sALCL‑ bzw. CD30+ CTCL‑Erkrankung und bei unterschiedlichen Vortherapien sowie die klinische Evidenz für eine Wirkung in CD30‑positiven malignen Erkrankungen nach verschiedenen vorausgegangenen Therapielinien bilden eine biologische Begründung für die Verwendung bei Patienten mit rezidiviertem oder refraktärem klassischem HL und sALCL mit und ohne vorausgegangener autologen Stammzelltransplantation und CD30+ CTCL nach mindestens 1 vorangegangenen systemischen Behandlung.
Die Beteiligung von anderen Antikörper‑assoziierten Funktionen am Wirkmechanismus wurde nicht ausgeschlossen.
Pharmakodynamische Wirkungen
Kardiale Elektrophysiologie
Von 52 Patienten, die alle 3 Wochen 1,8 mg/kg Brentuximab vedotin in einer einarmigen, offenen, multizentrischen Phase‑1‑Studie zur kardiologischen Verträglichkeit erhielten, waren 46 Patienten mit CD30‑exprimierenden malignen hämatologischen Erkrankungen auswertbar. Das primäre Ziel bestand darin, die Wirkung von Brentuximab vedotin auf die kardiale ventrikuläre Repolarisation zu beurteilen. Die vorher festgelegte primäre Analyse war die QTc‑Veränderung vom Ausgangswert gemessen zu mehreren Zeitpunkten in Zyklus 1.
Das obere 90-%‑Konfidenzintervall (KI) um die mittlere Wirkung auf QTc betrug zu jedem Messzeitpunkt nach Beginn der Studie in Zyklus 1 und Zyklus 3 < 10 ms. Diese Daten deuten darauf hin, dass Brentuximab vedotin in einer Dosierung von 1,8 mg/kg alle 3 Wochen bei Patienten mit CD30‑exprimierenden Tumoren keine klinisch relevante QT‑Verlängerung verursacht.
Klinische Wirksamkeit und Sicherheit
Hodgkin‑Lymphom
Studie C25003
Die Wirksamkeit und Sicherheit von ADCETRIS wurden in einer randomisierten, offenen, zweiarmigen, multizentrischen Studie an 1334 Patienten mit fortgeschrittenem, bislang unbehandeltem HL in Kombination mit einer Chemotherapie (Doxorubicin [A], Vinblastin [V] und Dacarbazin [D] [AVD]) untersucht. Patienten mit lymphozytenprädominantem nodulärem HL (NLPHL) wurden nicht in die Studie aufgenommen. Alle Patienten hatten eine histologisch bestätigte CD30‑exprimierende Erkrankung. Bei 62 % der Patienten lag ein extranodaler Befall vor. Von den 1334 Patienten wurden 664 Patienten in den ADCETRIS + AVD‑Arm (A+AVD) und 670 Patienten in den ABVD‑Arm (Doxorubicin [A], Bleomycin [B], Vinblastin [V] und Dacarbazin [D]) randomisiert und nach der Anzahl der Risikofaktoren gemäß dem International Prognostic Factor Project (IPFP) und nach der geografischen Region stratifiziert. Die Patienten wurden jeweils am 1. und am 15. Tag eines 28‑tägigen Zyklus mit 1,2 mg/kg ADCETRIS als intravenöse Infusion über 30 Minuten + 25 mg/m² Doxorubicin, 6 mg/m² Vinblastin und 375 mg/m² Dacarbazin behandelt. Die mediane Anzahl der erhaltenen Zyklen lag bei 6 (Bereich 1 bis 6 Zyklen). Tabelle 8 enthält eine Zusammenfassung der Patienten‑ und Krankheitsmerkmale am Ausgangspunkt. Zwischen den beiden Studienarmen gab es keine relevanten Unterschiede bei den Patienten‑ und Krankheitsmerkmalen.
Tabelle 8: Zusammenfassung der Patienten‑ und Krankheitsmerkmale am Ausgangspunkt der Phase‑3‑HL‑Studie mit bislang unbehandelten Patienten
Patientenmerkmale |
ADCETRIS + AVD |
ABVD |
Mittleres Alter (Bereich) |
35 Jahre (18‑82) |
37 Jahre (18‑83) |
Patienten ≥ 65 Jahre n (%) |
60 (9) |
62 (9) |
Geschlecht, n (%) |
378M (57) |
398M (59) |
ECOG (Eastern Cooperative Oncology Group) Status, n (%) |
||
0 |
376 (57) |
378 (57) |
1 |
260 (39) |
263 (39) |
2 |
28 (4) |
27 (4) |
Fehlend |
0 |
2 |
Krankheitsmerkmale |
||
Mittlere Zeit von der Diagnose HL bis zur ersten Verabreichung (Bereich) |
0,92 Mo (0,1‑21,4) |
0,89 Mo (0,0‑81,4) |
Krankheitsstadiuma bei der Diagnose HL, n (%) |
||
III |
237 (36) |
246 (37) |
IV |
425 (64) |
421 (63) |
nicht zutreffend |
1 (< 1) |
1 (< 1) |
Fehlend |
0 |
2 (< 1) |
Extranodaler Befall zum Zeitpunkt der Diagnose, n (%) |
411 (62) |
416 (62) |
IPFPb‑Risikofaktoren, n (%) |
||
0‑1 |
141 (21) |
141 (21) |
2‑3 |
354 (53) |
351 (52) |
4‑7 |
169 (25) |
178 (27) |
Knochenmarkbeteiligung zum Zeitpunkt der Diagnose bzw. der Aufnahme in die Studie, n (%) |
147(22) |
151 (23) |
B‑Symptomea n (%) |
400 (60) |
381 (57) |
a Gemäß der Ann Arbor Stadieneinteilung. | ||
Der primäre Endpunkt in Studie C25003 war das modifizierte progressionsfreie Überleben (modified progression‑free survival, mPFS) durch ein unabhängiges Gutachterkomitee (independent review facility, IRF), definiert als Zeitpunkt von der Randomisierung bis zum Fortschreiten der Krankheit, Tod oder bis zum Erhalt einer anschließenden Krebsbehandlung falls nach Durchführung der Erstlinienbehandlung gemäß IRF keine komplette Remission (non‑complete response [non‑CR]) erreicht wurde. Der Zeitpunkt des modifizierten Ereignisses war das Datum der ersten PET (positron emission tomography)‑Untersuchung nach Beendigung der Erstlinienbehandlung, die das Fehlen einer kompletten Remission (CR), definiert als Deauville‑Score ≥ 3, zeigte. Das mediane modifizierte PFS gemäß IRF‑Beurteilung wurde in keinem Behandlungsarm erreicht. Die Ergebnisse in der Intent‑to‑treat (ITT)‑Population zeigten bei ADCETRIS + AVD eine statistisch signifikante Verbesserung des modifizierten progressionsfreien Überlebens mit einer stratifizierten Hazard Ratio (HR) von 0,770 (95‑%‑KI, 0,603; 0,983, p = 0,035), was einer 23 %igen Verringerung des Risikos von modifizierten PFS‑Ereignissen für ADCETRIS + AVD im Vergleich zu ABVD entspricht.
Tabelle 9 zeigt die Wirksamkeitsergebnisse in Bezug auf modifiziertes progressionsfreies Überleben (mPFS) und Gesamtüberleben (overall survival, OS) in der ITT‑Population.
Tabelle 9: Wirksamkeitsergebnisse bei bislang unbehandelten HL‑Patienten die mit 1,2 mg/kg ADCETRIS + AVD am jeweils 1. und 15. Tag eines 28‑tägigen Behandlungszyklus (ITT) behandelt wurden
Intent to Treat (ITT) Population |
|||
ADCETRIS + AVD |
ABVD |
Stratifizierte Hazard Ratio und p‑Wert |
|
Anzahl Ereignisse (%) |
117 (18) |
146 (22) |
0,77 |
Geschätztes mPFSa gem. IRF nach 2 Jahren (%) |
82,1 |
77,2 |
|
Gesamtüberlebenb Anzahl Todesfälle (%) |
28 (4) |
39 (6) |
0,73 |
a Zum Zeitpunkt der Untersuchung betrug die mediane modifizierte PFS‑Nachverfolgungszeit für beide Arme 24,6 Monate. | |||
Abbildung 1: Modifiziertes progressionsfreies Überleben gemäß IRF in der ITT‑Population (ADCETRIS + AVD im Vergleich zu ABVD)
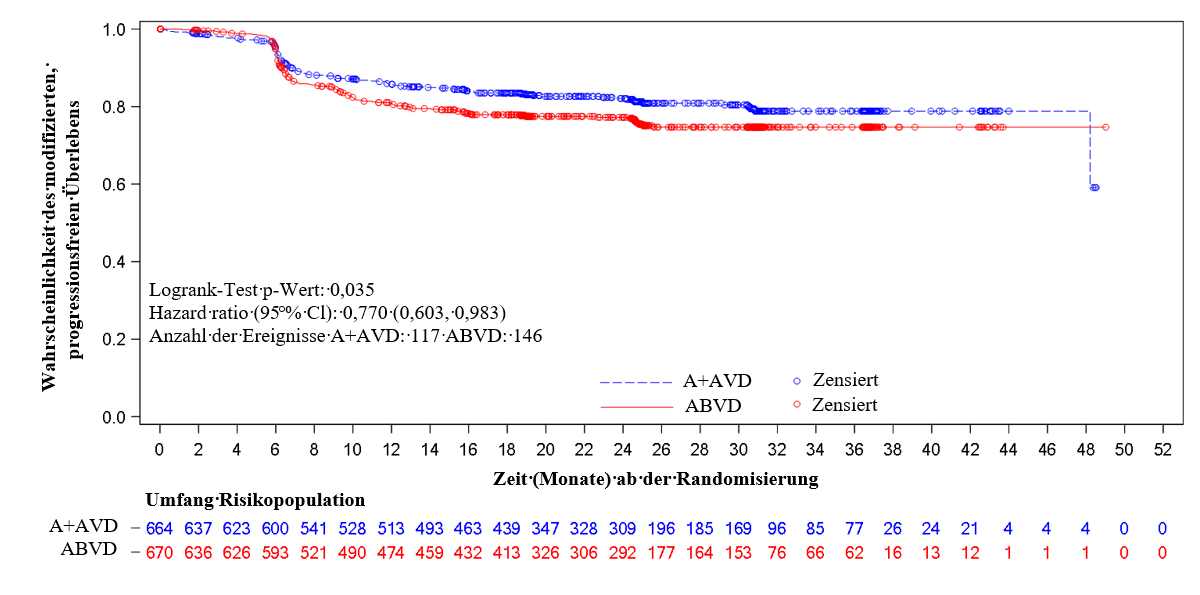
Weitere sekundäre Wirksamkeitsendpunkte, einschließlich CR‑Rate und ORR (objective response rate) zum Ende des randomisierten Behandlungsplans, CR‑Rate am Ende der Erstlinienbehandlung und Rate der PET‑Negativität am Ende des 2. Zyklus, Dauer des Ansprechens (duration of response, DOR), Dauer der vollständigen Remission (duration of complete remission, DOCR), krankheitsfreies Überleben (disease‑free survival, DFS) sowie ereignisfreies Überleben (event‑free survival, EFS) tendierten alle zugunsten von ADCETRIS + AVD in der ITT‑Population.
Vorab festgelegte Subgruppenanalysen des modifizierten PFS nach IRF zeigten keinen klinisch bedeutsamen Unterschied zwischen den beiden Armen bei älteren Patienten (Alter der Patienten ≥ 60 Jahre [n = 186] [HR = 1,00, 95‑%‑KI (0,58, 1,72)] und Alter ≥ 65 Jahre [n = 122] [HR = 1,01, 95 %] KI (0,53, 1,94)] und Patienten ohne extranodale Lokalisation (n = 445) (HR = 1,04, 95‑%‑KI [0,67, 1,62]).
Eine abschließende Analyse des Gesamtüberlebens wurde anhand von Daten mit einer medianen Nachbeobachtungszeit von über 7 Jahren für das Gesamtüberleben durchgeführt. In der ITT-Population war ein geringerer Anteil der zu ADCETRIS + AVD randomisierten Patienten gestorben (46 Todesfälle, 7 %) als bei den zu ABVD randomisierten Patienten (69 Todesfälle, 10 %; HR = 0,62, 95-%-KI [0,423, 0,899]), s. Abbildung 2. Der Anteil der verstorbenen Patienten in Stadium III, die ADCETRIS + AVD (20 Todesfälle, 8 %) und ABVD (20 Todesfälle, 8 %) erhielten, war ähnlich hoch (HR = 1,01, 95-%-KI [0,542, 1,874]). Ein geringerer Anteil der Patienten im Stadium IV, die zu A + AVD randomisiert worden waren (26 Todesfälle, 6 %), war im Vergleich zu den Patienten, die zu ABVD randomisiert worden waren, gestorben (48 Todesfälle, 11 %; HR = 0,49, 95-%-KI [0,303, 0,790]). Eine Subgruppenanalyse des Gesamtüberlebens zeigte keinen klinisch bedeutsamen Unterschied zwischen den beiden Behandlungsarmen bei Patienten ohne extranodalen Befall (n = 445) (HR = 1,28, 95 % KI [0,710, 2,303]).
Abbildung 2: Endgültige Analyse Gesamtüberleben (ADCETRIS + AVD vs. ABVD) (ITT, >7 Jahre mediane Nachverfolgungszeit)
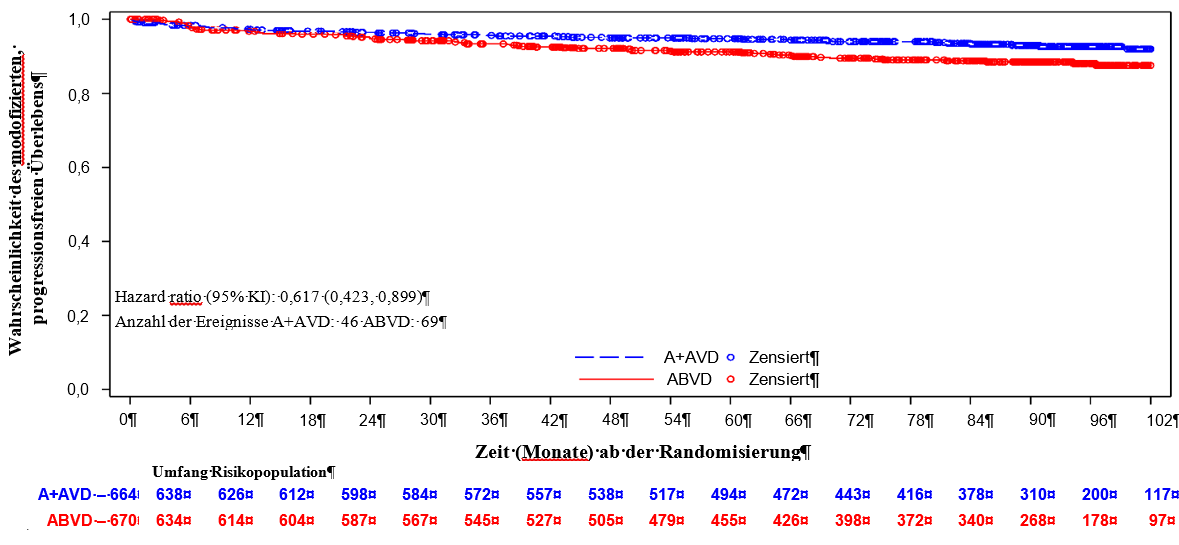
Im Rahmen der primären Analyse der ITT‑Population erhielten 33 % weniger Patienten, die in der ITT‑Population mit ADCETRIS + AVD behandelt worden waren, eine anschließende Salvage‑Chemotherapie (n = 66) und eine Hochdosis‑Chemotherapie und Transplantation (n = 36) verglichen mit denen, die mit ABVD behandelt worden waren (n = 99 und n = 54). Von den Patienten mit Stadium IV erhielten 35 % weniger Patienten, die mit ADCETRIS + AVD behandelt worden waren, eine anschließende Salvage‑Chemotherapie (n = 45) im Vergleich zu denen mit ABVD (n = 69) und 22 % weniger der mit ADCETRIS + AVD behandelten Patienten erhielten eine Hochdosis‑Chemotherapie und Transplantation (n = 29) verglichen mit denen, die mit ABVD behandelt worden waren (n = 37).
Studie HD21
Die Sicherheit und Wirksamkeit von ADCETRIS (Brentuximab vedotin [Br]) wurde in einer offenen, prospektiven, multizentrischen Phase-3-Studie an 1500 Patienten mit zuvor unbehandeltem HL im Stadium IIB mit großem Mediastinaltumor und/oder extranodalen Läsionen, HL im Stadium III oder IV in Kombination mit Chemotherapie (Etoposid [E], Cyclophosphamid [C], Doxorubicin [A], Dacarbazin [D], Dexamethason [D] [BrECADD]) untersucht. Von den 1500 Patienten wurden 751 Patienten zum BrECADD-Arm und 749 Patienten zum eBEACOPP-Arm (eskaliertes Bleomycin [B], Etoposid [E], Doxorubicin [A], Cyclophosphamid [C], Vincristin [O], Procarbazin [P] und Prednison [P]) randomisiert und nach Region der Aufnahme, Alter, Geschlecht und International Prognostic Score (IPS) stratifiziert. Patienten im BrECADD-Arm wurden am ersten Tag jedes 21-tägigen Zyklus mit 1,8 mg/kg ADCETRIS behandelt, das als intravenöse Infusion über 30 Minuten verabreicht wurde. Die Patienten erhielten außerdem eine Chemotherapie mit 1250 mg/m2 Cyclophosphamid, 40 mg/m2 Doxorubicin, 150 mg/m2 Etoposid oder Etoposidphosphat, 250 mg/m2 Dacarbazin und 40 mg Dexamethason (siehe Abschnitt 4.2).
Alle behandelten Patienten erhielten eine Primärprophylaxe mit G-CSF (siehe Abschnitt 4.2). Nach zwei Behandlungszyklen wurde eine erneute Untersuchung mittels PET (Restaging) durchgeführt, wobei PET-negative Patienteninsgesamt 4 Zyklenund PET-positive Patienteninsgesamt 6 Zyklen erhalten sollten. Die mediane Anzahl der in beiden Armen verabreichten Zyklen betrug 4 (Bereich: 1 bis 6 Zyklen).
Tabelle 10 enthält eine Zusammenfassung der Ausgangsmerkmale von Patienten und Krankheit. Es gab keine relevanten Unterschiede der Patienten- und Krankheitsmerkmale zwischen beiden Armen.
Tabelle 10: Zusammenfassung der Patienten‑ und Krankheitsmerkmale am Ausgangspunkt der Phase‑3‑HL‑Studie mit bislang unbehandelten Patienten
Patientenmerkmale |
BrECADD |
eBEACOPP |
Medianes Alter (Bereich) |
31 Jahre (18-60) |
31 Jahre (18-60) |
Patienten < 45 Jahre n (%) |
590 (79) |
584 (78) |
Patienten im Alter von 45 bis 60 Jahren, n (%) |
161 (21) |
165 (22) |
Geschlecht, n (%) |
419M (56) |
419M (56) |
ECOG (Eastern Cooperative Oncology Group) Status, n (%) |
||
0 |
514 (68) |
521 (70) |
1 |
223 (30) |
205 (27) |
2 |
11 (1) |
18 (2) |
Fehlend |
3 (< 1) |
5 (< 1) |
Krankheitsmerkmale |
||
Mediane Zeit von der HL- Diagnose zur Randomisierung (Bereich) |
0,6 Mo (0,12) |
0,6 Mo (0,10) |
Krankheitsstadiuma bei der Erstdiagnose HL, n (%) |
||
II |
118 (16) |
117 (16) |
III |
298 (40) |
293 (39) |
IV |
332 (44) |
334 (45) |
Fehlend |
3 (< 1) |
5 (< 1) |
IPSb-Gruppen, n (%) |
||
0-2 |
394 (52) |
403 (54) |
3-7 |
357 (48) |
346 (46) |
B-Symptomea n (%) |
517 (69) |
501 (67) |
a Gemäß der Ann Arbor Stadieneinteilung. | ||
Die Studie HD21 wurde mit zwei koprimären Endpunkten (behandlungsbedingte Morbidität [TRMB] und progressionsfreies Überleben [PFS] [gemäß Prüfarzt mit zentraler Bestätigung]) konzipiert. Das erste koprimäre Ziel der Studie bestand im Nachweis der geringeren Toxizität von BrECADD im Vergleich zu eBEACOPP, gemessen anhand der TRMB. Wenn durch den Überlegenheitstest eine geringere Toxizität nachgewiesen wurde, bestand das zweite koprimäre Ziel im weiteren Nachweis der nicht unterlegenen Wirksamkeit von BrECADD im Vergleich zu eBEACOPP in Bezug auf das PFS.
TRMB wurde als jegliche Organtoxizität von Grad 3 oder 4 gemäß den Common Terminology Criteria for Adverse Events (CTCAE) oder hämatologische Toxizität von Grad 4 während der primären Chemotherapie definiert, einschließlich des Zeitraums von bis zu 30 Tagen nach der letzten Chemotherapiedosis.
Zum Zeitpunkt der Primäranalyse wurde die Überlegenheit von BrECADD in Bezug auf TRMB mit einer absoluten Risikoreduktion von -16,7 Prozentpunkten und einer statistisch signifikanten Reduktion des relativen Risikos nachgewiesen. Der co-primäre Endpunkt PFS, unabhängig von versäumten Besuchen und unabhängig von der Einleitung einer neuen Krebstherapie, erfüllte die Nichtunterlegenheit im BrECADD-Behandlungsarm im Vergleich zu eBEACOPP mit einer statistisch signifikanten Risikoreduktion (nicht stratifiziertes HR = 0,62 [multiplizitätsbereinigtes 95%-KI, 0,369, 1,040]) (Datenstichdatum - 31. Dezember 2022).
Die Inzidenz von TRMB im BrECADD-Arm (42 %) war im Vergleich zu eBEACOPP (58,7 %) nachweislich geringer. Dies lag hauptsächlich an der Verringerung der hämatologischen Toxizitäten von Grad 4 (31,2 % bei BrECADD und 52,1 % bei eBEACOPP).
Die TRMB nach Behandlungsarm ist in Tabelle 11 aufgeführt. Die Wirksamkeitsergebnisse aus der aktualisierten PFS- und Gesamtüberlebensanalyse (OS) sind in Tabelle 12 aufgeführt (Datenstichtag: 31. Oktober 2023).
Tabelle 11: Behandlungsbedingte Morbidität (TRMB) nach Behandlungsarm (Sicherheitspopulation)
BrECADD |
eBEACOPP |
|||
Anzahl Patienten mit TRMB |
314 (42) |
435 (59) |
||
Akute hämatologische Toxizität von Grad 4 |
233 (31) |
386 (52) |
||
Anämie |
3 (< 1) |
3 (< 1) |
||
Thrombozytopenie |
227 (30) |
383 (52) |
||
Infektion |
13 (2) |
10 (1) |
||
Akute Organtoxizität; Grad 3 oder Grad 4 |
139 (19) |
129 (17) |
||
Herzerkrankungen |
18 (2) |
10 (1) |
||
Erkrankungen des |
58 (8) |
32 (4) |
||
Leber- und |
37 (5) |
22 (3) |
||
Erkrankungen des |
20 (3) |
40 (5) |
||
Periphere sensorische |
9 (1) |
17 (2) |
||
Periphere motorische |
2 (< 1) |
1 (< 1) |
||
Erkrankungen des |
11 (2) |
24 (3) |
||
Erkrankungen der Nieren |
7 (< 1) |
10 (1) |
||
Erkrankungen der |
25 (3) |
35 (5) |
||
Prozentuale Differenz (BrECADD - eBEACOPP) |
-16,7 |
|||
Genaues 95-%-KI |
-21,7, -11,5 |
|||
Tabelle 12: Wirksamkeitsergebnisse bei bislang unbehandelten HL‑Patienten, die mit 1,8 mg/kg BrECADD über einen 21-tägigen Zyklus behandelt wurden (aktualisierte PFSa-Analyse Datenstichtag – 31. Oktober 2023)
Intent to Treat (ITT) Population |
||
BrECADD |
eBEACOPP |
|
Anzahl PFS-Ereignisse (%) |
44 (5,9) |
65 (8,7) |
PFS-Hazard-Ratio (95 % KI) |
0,664 (0,453, 0,973) |
|
Geschätztes PFSb,c (95 % KI) |
||
Nach 3 Jahren |
95,2 |
92,4 |
Nach 5 Jahren |
92,8 |
90,2 |
Gesamtüberlebend Anzahl Todesfälle (%) |
12 (1,6) |
13 (1,7) |
OS-Hazard-Ratio (95 % KI) |
0,919 |
|
Geschätzte OS-Rate (95 % KI) |
||
Nach 3 Jahren |
98,9 |
98,9 |
Nach 5 Jahren |
98,1 |
97,9 |
a. Bei der PFS-Analyse wurden keine zwischenzeitlich auftretenden Ereignisse berücksichtigt, wie versäumte Besuche oder der Beginn einer neuen Krebstherapie. | ||
Die Dauer der Komplettremission (CR) zeigte in der ITT-Population im BrECADD-Arm einen klinisch bedeutsamen Nutzen im Vergleich zum eBEACOPP-Arm, wohingegen andere sekundäre Wirksamkeitsendpunkte, einschließlich ORR und CR-Rate am Ende der Chemotherapie, in beiden Armen einen vergleichbaren Nutzen zeigten.
Studie SGN35‑005
Die Wirksamkeit und Sicherheit von ADCETRIS wurde in einer randomisierten, doppelblinden, placebokontrollierten, zweiarmigen, multizentrischen Studie bei 329 Patienten mit HL und erhöhtem Rezidiv‑ und Progressionsrisiko nach einer ASCT untersucht. Patienten mit bekannter zerebraler/meningealer Erkrankung, einschließlich PML in der Vorgeschichte, waren von der Studienteilnahme ausgeschlossen. Die Merkmale der Patientenpopulation sind in Tabelle 13 aufgeführt. Von den 329 Patienten wurden per Randomisierung 165 Patienten dem Verum‑ und 164 dem Placeboarm zugeteilt. In der Studie erhielten die Patienten planmäßig ihre erste Dosis nach der Erholung von der ASCT (30 ‑ 45 Tage nach der ASCT). Die Patienten erhielten 1,8 mg/kg ADCETRIS oder entsprechendes Placebo intravenös über 30 Minuten alle 3 Wochen für bis zu 16 Zyklen.
Um die Teilnahmevoraussetzungen zu erfüllen, musste bei den Patienten mindestens einer der folgenden Risikofaktoren vorliegen:
HL refraktär gegenüber der Erstlinientherapie.
HL‑Rezidiv oder –Progression < 12 Monate nach dem Ende der Erstlinientherapie.
Extranodaler Befall zum Zeitpunkt des Rezidivs vor der ASCT, einschließlich extranodaler Ausbreitung nodaler Neoplasie in benachbarte lebenswichtige Organe.
Tabelle 13: Zusammenfassung der Patienten‑ und Krankheitsmerkmale zu Beginn der Phase‑3‑Studie zu HL nach ASCT
Patientenmerkmale |
ADCETRIS |
Placebo |
|||||
Medianes Alter, Jahre (Bereich) |
33 Jahre (18 ‑ 71) |
32 Jahre (18 ‑ 76) |
|||||
Geschlecht |
76 M (46 %)/89 W (54 %) |
97 M (59 %)/67 W (41 %) |
|||||
ECOG‑Status |
|||||||
0 |
87 (53 %) |
97 (59 %) |
|||||
1 |
77 (47 %) |
67 (41 %) |
|||||
2 |
1 (1 %) |
0 |
|||||
Krankheitsmerkmale |
|||||||
Mediane Anzahl vorausgegangener Chemotherapien (Bereich) |
2 (2 ‑ 8) |
2 (2 ‑ 7) |
|||||
Mediane Dauer von der HL‑Diagnose bis zur ersten Dosis (Bereich) |
18,7 Mo. (6,1 ‑ 204,0) |
18,8 Mo. (7,4 ‑ 180,8) |
|||||
HL-Stadium bei Erstdiagnose |
|||||||
Stadium I |
1 (1 %) |
5 (3 %) |
|||||
Stadium II |
73 (44 %) |
61 (37 %) |
|||||
Stadium III |
48 (29 %) |
45 (27 %) |
|||||
Stadium IV |
43 (26 %) |
51 (31 %) |
|||||
Unbekannt |
0 |
2 (1 %) |
|||||
PET‑Scan‑Status vor ASCT |
|||||||
FDG‑AVID |
64 (39 %) |
51 (31 %) |
|||||
FDG‑NEGATIV |
56 (34 %) |
57 (35 %) |
|||||
NICHT ERMITTELT |
45 (27 %) |
56 (34 %) |
|||||
Extranodaler Befall zum Zeitpunkt der Rezidivierung vor der ASCT |
54 (33 %) |
53 (32 %) |
|||||
B‑Symptomea |
47 (28 %) |
40 (24 %) |
|||||
Bestes Ansprechen auf Salvage‑Therapie vor der ASCTb |
|||||||
Komplette Remission |
61 (37 %) |
62 (38 %) |
|||||
Partielle Remission |
57 (35 %) |
56 (34 %) |
|||||
Stabile Erkrankung |
47 (28 %) |
46 (28 %) |
|||||
HL‑Status am Ende der vorhergehenden Standard‑Chemotherapieb |
|||||||
Refraktär |
99 (60 %) |
97 (59 %) |
|||||
Rezidivierung nach < 12 Monaten |
53 (32 %) |
54 (33 %) |
|||||
Rezidivierung nach ≥ 12 Monaten |
13 (8 %) |
13 (8 %) |
|||||
a. Bei refraktärer Erkrankung oder bei Progression oder Rezidivierung nach vorhergehender Therapie. | |||||||
Die Wirksamkeitsergebnisse gemäß der primären Analyse des primären Endpunkts sind in Tabelle 14 aufgeführt. Der primäre Endpunkt des PFS nach IRF wurde erreicht. Hier bestand ein Unterschied im medianen PFS von 18,8 Monaten zugunsten des Verum‑Behandlungsarms.
Tabelle 14: Ergebnisse zur Wirksamkeit bei HL‑Patienten mit erhöhtem Rezidiv‑ und Progressionsrisiko nach einer ASCT, die alle 3 Wochen mit 1,8 mg/kg ADCETRIS behandelt wurden (ITT, primäre Analyse)
ADCETRIS |
Placebo |
Stratifizierte Hazard Ratio |
||
Progressionsfreies |
Median nach IRF |
|||
42,9 Monate |
24,1 Monate |
0,57 |
||
Median nach Prüfarzt |
||||
Nicht erreicht |
15,8 Monate |
0,5 |
||
Gesamtüberleben |
Zahl der Todesfälle (%) |
|||
28 (17) |
25 (15) |
1,15 |
||
a. Zum Zeitpunkt der primären Analyse betrug die mediane Nachverfolgungszeit für beide Studienarme 30 Monate (Bereich 0 – 50). | ||||
Vorab festgelegte Subgruppenanalysen des PFS nach IRF erfolgten im Hinblick auf bestes Ansprechen auf Salvage‑Therapie vor der ASCT, HL‑Status nach Erstlinientherapie, Lebensalter, Geschlecht, Körpergewicht bei Studienbeginn, ECOG‑Performance‑Status bei Studienbeginn, Zahl der vorhergehenden Therapien vor der ASCT, geografische Region, PET‑Status vor der ASCT, B‑Symptomatik‑Status nach Versagen vorhergehender Therapien sowie extranodaler Beteiligungsstatus vor der ASCT. Die Analysen ergaben einen durchgängigen Trend zugunsten der Patienten, die mit ADCETRIS behandelt wurden, im Vergleich zu den Patienten die Placebo erhielten, mit Ausnahme der Altersgruppe ≥ 65 Jahre (n = 8).
Im Hinblick auf die Lebensqualität wurden keine Unterschiede zwischen Verum‑ und Placeboarm festgestellt. Die Auswertung der Inanspruchnahme medizinischer Ressourcen (MRU) ergab, dass stationäre und ambulante Behandlungen sowie Fehlzeiten z. B. am Arbeitsplatz von Patienten und Betreuungspersonen unter ADCETRIS bei HL mit erhöhtem Rezidivrisiko geringer waren als unter Placebo.
Eine aktualisierte Analyse nach 3‑jähriger Nachverfolgung ergab einen anhaltenden Vorteil beim PFS nach IRF (HR = 0,58 [95‑%‑KI (0,41; 0,81)]).
Zum Ende der Studie, etwa 10 Jahre nach der Aufnahme des ersten Patienten, zeigte das PFS nach Prüfarzt weiterhin einen Nutzen (HR = 0,51 [95‑%‑KI (0,37, 0,71)]). Die Ergebnisse zum Gesamtüberleben passten zu denen, die zum Zeitpunkt der primären Analyse berichtet wurden (HR = 1,11 [95‑%‑KI (0,72, 1,70)]).
Abbildung 3 zeigt das PFS nach Prüfarzt in der ITT‑Population zum Zeitpunkt des Studienendes.
Abbildung 3: Kaplan‑Meier‑Kurve des PFS nach Prüfarzt (ITT, Studienende)
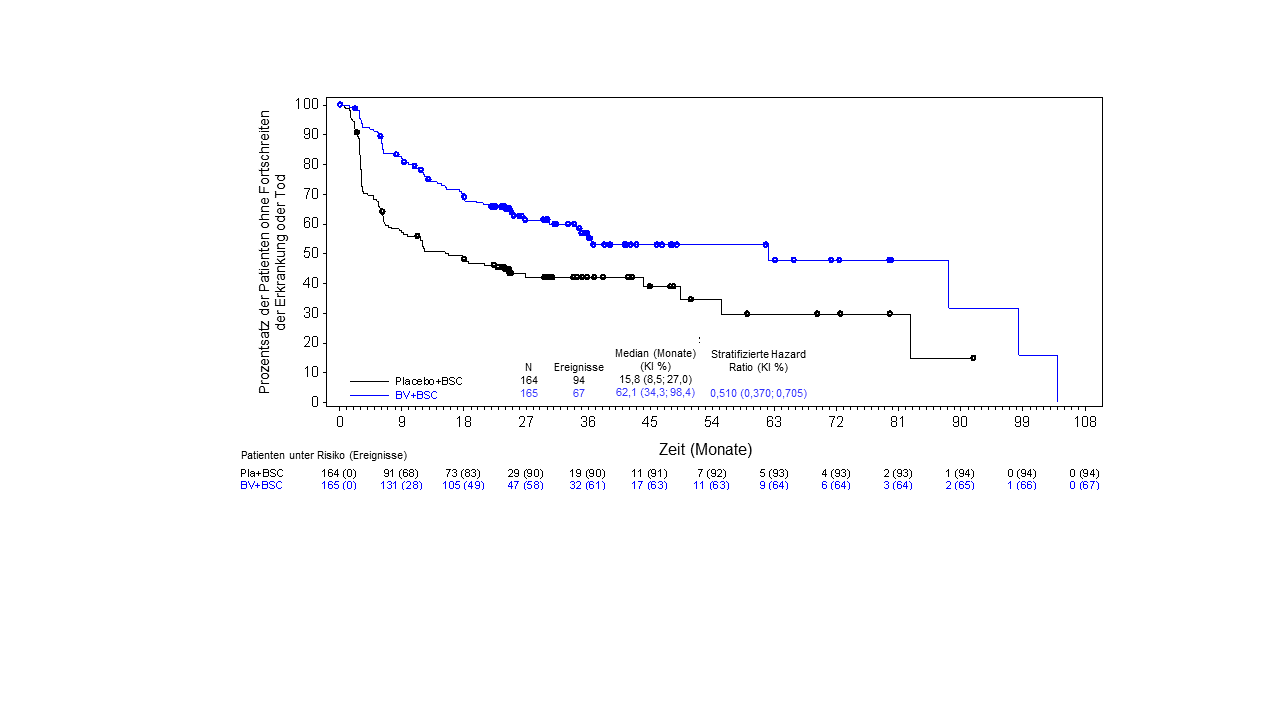
Post‑hoc‑ Risikofaktoranalysen
In Post‑hoc‑Analysen wurden anhand der primären Analyse des primären Endpunkts die Auswirkungen eines erhöhten Risikos (Zahl der Risikofaktoren) auf den klinischen Nutzen untersucht (Tabelle 15). Die repräsentativen Risikofaktoren für diese Analyse waren:
Auftreten des HL < 12 Monate nach oder HL refraktär gegenüber der vorhergehenden Therapie
PR oder Krankheitsstabilisierung als bestes Ansprechen auf die letzte Salvage‑Therapie laut CT‑ und/oder PET‑Scan.
Extranodaler Befall bei Rezidivierung vor der ASCT.
B‑Symptomatik bei Rezidivierung vor der ASCT.
Zwei oder mehr vorausgehende Salvage‑Therapien.
Die Ergebnisse der post‑hoc‑Analysen deuten auf einen größeren klinischen Nutzen bei Patienten mit zwei oder mehr Risikofaktoren hin, wobei zwischen den einzelnen Risikofaktoren keine Unterschiede bestehen. Bei Patienten mit nur einem Risikofaktor für Rezidivierung und Progression war kein Nutzen beim PFS oder OS festzustellen.
Tabelle 15: Zusammenfassung des PFS nach IRF sowie des OS, jeweils nach Zahl der Risikofaktoren, in der Phase‑3‑Studie zu HL nach ASCT (primäre Analyse)
Progressionsfreies Überleben nach IRF | |||||||
Anzahl Risikofaktoren = 1 |
Anzahl Risikofaktoren ≥ 2 |
Anzahl Risikofaktoren ≥ 3 |
|||||
ADCETRIS |
Placebo |
ADCETRIS |
Placebo |
ADCETRIS |
Placebo |
||
Anzahl Patienten mit Progression und Todesfällea (%) |
9 (43) |
7 (25) |
51 (35) |
68 (50) |
32 (39) |
49 (58) |
|
Stratifizierte Hazard Ratio |
1,65 (95-%-KI [0,60; 4,55])b |
0,49 (95-%-KI [0,34; 0,71]) |
0,43 (95-%-KI [0,27; 0,68]) |
||||
Gesamtüberleben | |||||||
Anzahl Risikofaktoren = 1 |
Anzahl Risikofaktoren ≥ 2 |
Anzahl Risikofaktoren ≥ 3 |
|||||
ADCETRIS |
Placebo |
ADCETRIS |
Placebo |
ADCETRIS |
Placebo |
||
Anzahl Todesfällec (%) |
5 (24) |
1 (4) |
23 (16) |
24 (18) |
15 (18) |
16 (19) |
|
Stratifizierte Hazard Ratio |
7,94 (95-%-KI [0,93; 68,06])b |
0,94 (95-%-KI [0,53; 1,67]) |
0,92 (95-%-KI [0,45; 1,88]) |
||||
a. Todesfall ohne vorherige Progression und mit höchstens einem ausgefallenen Untersuchungstermin. | |||||||
Zum Zeitpunkt der aktualisierten Analyse (3 Jahre Nachverfolgungszeit) betrug bei den Patienten mit 2 oder mehr Risikofaktoren die Hazard Ratio des PFS nach IRF 0,49 (95‑%‑KI [0,34; 0,71]) und die Hazard Ratio des PFS nach Prüfarzt 0,41 (95‑%‑KI [0,29; 0,58]) (siehe Abbildungen 4 und 5).
Abbildung 4: Kaplan‑Meier‑Kurve des PFS nach IRF bei Patienten mit ≥ 2 Risikofaktoren (3‑Jahres‑Nachverfolgung)
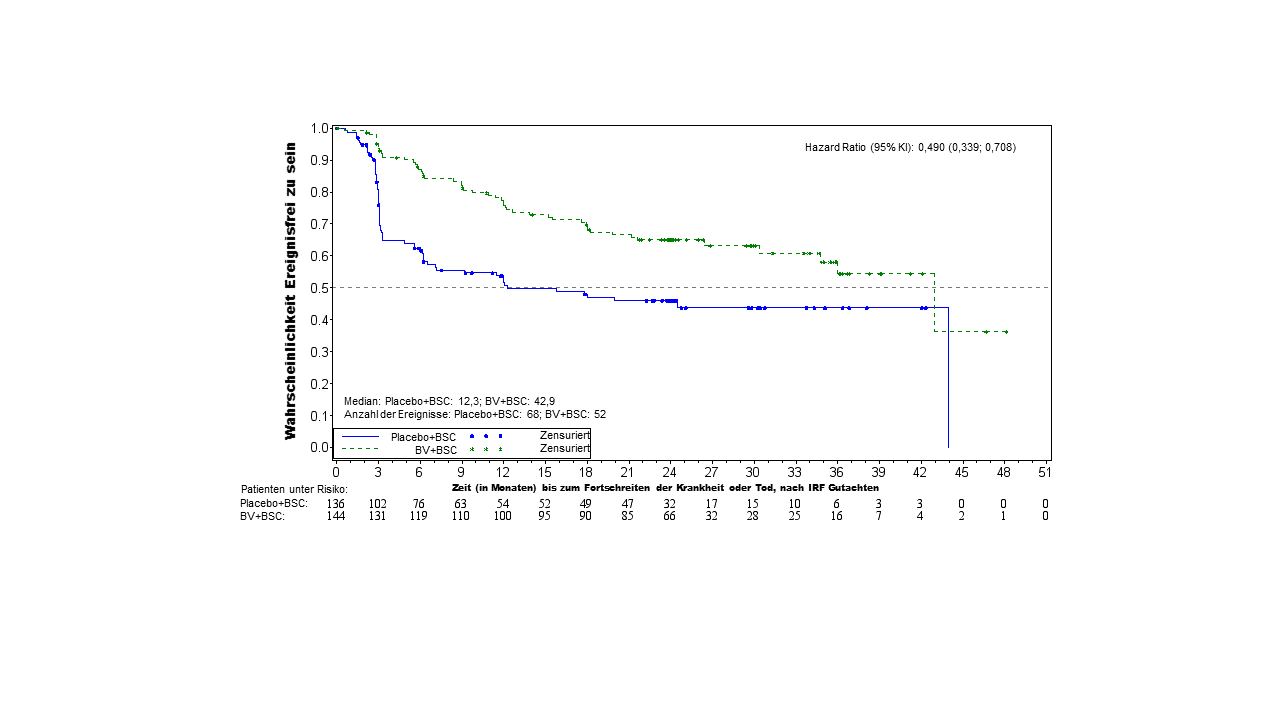
Abbildung 5: Kaplan‑Meier‑Kurve des PFS nach Prüfarzt bei Patienten mit ≥ 2 Risikofaktoren (3‑Jahres‑Nachverfolgung)
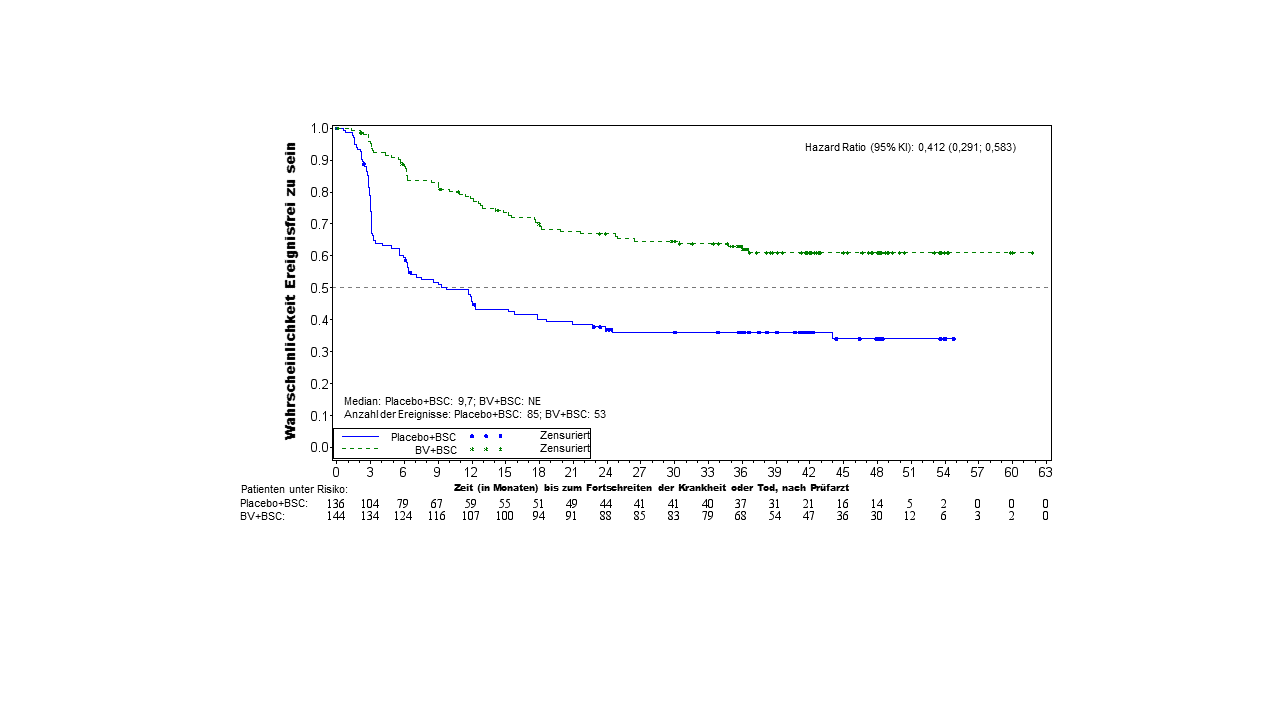
Zum Ende der Studie, etwa 10 Jahre nach der Aufnahme des ersten Patienten, betrug die Hazard Ratio für das PFS nach Prüfarzt bei Patienten mit 2 oder mehr Risikofaktoren 0,41 (95‑%‑KI [0,29, 0,58]). Die Hazard Ratio für das PFS nach Prüfarzt bei Patienten mit 3 oder mehr Risikofaktoren betrug 0,38 (95‑%‑KI [0,25, 0,59]). Die Ergebnisse zum Gesamtüberleben passten weiterhin zu denen, die in der primären Analyse beobachtet wurden.
Studie SG035‑0003
Die Wirksamkeit und Sicherheit von ADCETRIS als Monotherapie wurde in einer zulassungsrelevanten offenen, einarmigen, multizentrischen Studie bei 102 Patienten mit rezidiviertem oder refraktärem HL untersucht. Siehe Tabelle 16 unten für eine Zusammenfassung der Patienten‑ und der Krankheitsmerkmale bei Studienbeginn.
Tabelle 16: Zusammenfassung der Patienten‑ und Krankheitsmerkmale der in der Phase‑2‑Studie eingeschlossenen Patienten mit rezidiviertem oder refraktärem HL
Patientenmerkmale |
n = 102 |
|
Medianes Alter, Jahre (Bereich) |
31 Jahre (15‑77) |
|
Geschlecht |
48 M (47 %) / 54 W (53 %) |
|
ECOG‑Status |
||
0 |
42 (41 %) |
|
1 |
60 (59 %) |
|
Vorangegangene autologe Stammzelltransplantation (ASCT) |
102 (100 %) |
|
Vorausgegangene Chemotherapien |
3,5 (1–13) |
|
Zeit von ASCT bis zum ersten Rezidiv nach der Transplantation |
6,7 Mo (0–131) |
|
Histologisch gesicherte CD30‑exprimierende Krankheit |
102 (100 %) |
|
Krankheitsmerkmale |
||
Primär refraktär nach Erstlinien‑Therapiea |
72 (71 %) |
|
Refraktär nach letzter Therapie |
43 (42 %) |
|
B‑Symptome bei Studienbeginn |
35 (33 %) |
|
Stadium III bei Erstdiagnose |
27 (26 %) |
|
Stadium IV bei Erstdiagnose |
20 (20 %) |
|
a. Eine primär refraktäre HL wird definiert als das Nicht‑Erreichen einer kompletten Remission oder als Fortschreiten der Erkrankung innerhalb von 3 Monaten nach Abschluss der Erstlinien‑Therapie. | ||
18 Patienten (18 %) erhielten 16 Zyklen mit ADCETRIS, der Medianwert der verabreichten Zyklen war 9 (Bereich von 1 bis 16).
Das Ansprechen auf die Behandlung mit ADCETRIS wurde von einem unabhängigen Aufsichtskomitee (IRF) auf Basis der Revised Response Criteria for Malignant Lymphoma (Cheson, 2007) beurteilt. Das Ansprechen auf die Behandlung wurde mittels Spiral‑CT von Thorax, Hals, Abdomen und Becken, mittels PET‑Scans und klinischer Daten beurteilt. Das Ansprechen wurde in den Zyklen 2, 4, 7, 10, 13 und 16 beurteilt, mit PET‑Scans in den Zyklen 4 und 7.
Nach der IRF‑Beurteilung lag die objektive Ansprechrate (ORR) bei 75 % (76 von 102 Patienten in der Intent‑to‑Treat [ITT]‑Population), und in 94 % der Patienten wurde eine Reduktion der Tumor‑Last erreicht. Eine komplette Remission (CR) wurde bei 33 % (34 von 102 Patienten in der ITT‑Gruppe) erzielt. Das mediane Gesamtüberleben (OS) betrug 40,5 Monate (die mittlere Beobachtungszeit [Zeit bis zum Tod oder bis zum letzten Kontakt] ab der ersten Dosis betrug 35,1 Monate [von 1,8 bis 72,9+ Monate]). Das erwartete Gesamtüberleben nach 5 Jahren lag bei 41 % (95‑%‑KI [31 %, 51 %]). Die Beurteilung der Prüfärzte entsprach im Allgemeinen der unabhängigen Überprüfung der Scans. 8 der behandelten Patienten, die auf die Therapie ansprachen, erhielten eine allogene Stammzelltransplantation. Weitere Ergebnisse zur Wirksamkeit siehe Tabelle 17.
Tabelle 17: Die Ergebnisse zur Wirksamkeit bei rezidiviertem oder refraktärem Hodgkin‑Lymphom bei Patienten, die alle 3 Wochen mit 1,8 mg/kg ADCETRIS behandelt wurden
Bestes klinisches Ansprechen (n = 102) |
IRF n (%) |
95-%-KI |
Objektive Ansprechrate (CR + PR) |
76 (75) |
64,9; 82,6 |
Komplette Remission (CR) |
34 (33) |
24,3; 43,4 |
Partielle Remission (PR) |
42 (41) |
Nicht zutreffend |
Gesamtansprechrate (CR + PR + Krankheitsstabilisierung) |
98 (96) |
90,3; 98,9 |
Ansprechdauer |
Median nach IRF |
95-%-KI |
Objektive Ansprechrate (CR + PR)a |
6,7 Monate |
3,6; 14,8 |
Komplette Remission (CR) |
27,9 Monate |
10,8; NAb |
Gesamtüberleben |
95-%-KI |
|
Median |
40,5 Monate |
28,7; 61,9 |
Erwartete 5‑Jahres-Gesamtüberlebensrate |
41 % |
31 %, 51 % |
a. Die Ansprechdauer lag zwischen 1,2+ Monaten bis 43+ Monaten, und die mediane Nachverfolgungszeit ab der ersten Dosis für Patienten, die gemäß IRF ein objektives Ansprechen (OR) erzielten, betrug 9,0 Monate. | ||
Eine explorative intraindividuelle Analyse zeigte, dass ungefähr 64 % der HL‑Patienten, die mit ADCETRIS innerhalb der klinischen Studie SG035‑0003 behandelt wurden, eine klinische Verbesserung in Form von verlängertem progressionsfreiem Überleben (PFS) erfuhren im Vergleich zur direkt vorangegangen Therapie.
Von den 35 Patienten (33 %), die zu Beginn der Studie B‑Symptome aufwiesen, kam es bei 27 Patienten (77 %) in einer mittleren Zeit von 0,7 Monaten nach Behandlungsbeginn mit ADCETRIS zum Verschwinden aller B‑Symptome.
Daten von HL‑Patienten, die nicht für eine Stammzelltransplantation (SCT) infrage kommen
Studie C25007
Eine einarmige Phase‑4‑Studie wurde bei Patienten mit rezidiviertem oder refraktärem HL (n = 60) durchgeführt, die zuvor mindestens eine Chemotherapie erhalten hatten und zum Zeitpunkt der Behandlung mit ADCETRIS nicht für eine Stammzelltransplantation oder Kombinationschemotherapie in Betracht gezogen wurden. Infrage kommende Patienten durften keine Stammzelltransplantation erhalten haben. Die mittlere Anzahl Zyklen lag bei 7 (Bereich 1 – 16 Zyklen). Die Patienten erhielten alle 3 Wochen 1,8 mg/kg ADCETRIS.
Zum Zeitpunkt der primären Analyse des primären Endpunkts nach IRF lag die objektive Ansprechrate (ORR) in der ITT‑Population bei 50 % (95‑%‑KI [37; 63 %]). Das beste Gesamtansprechen, eine komplette Remission, wurde bei 7 Patienten (12 %) berichtet; eine partielle Remission wurde bei 23 Patienten (38 %) berichtet. Bei diesen 30 Patienten lag die mittlere Ansprechzeit, definiert als der Zeitraum von der ersten Dosis bis zur partiellen Remission bzw. bis zur kompletten Remission, je nachdem was als erstes eintritt, bei 6 Wochen (Bereich 5 – 39 Wochen). Die mittlere Zeit bis zum besten Gesamtansprechen, die als die Zeit von der ersten Dosis bis zum besten klinischen Gesamtansprechen in Form einer partiellen bzw. kompletten Remission definiert ist, lag bei 11 Wochen (Bereich 5 – 60 Wochen). 28 Patienten (47 %) erhielten nach der Behandlung mit ADCETRIS mit einer mittleren Anzahl von 7 Zyklen (Bereich 4 – 16 Zyklen) eine Stammzelltransplantation. Die 32 Patienten (53 %), die nachfolgend keine Stammzelltransplantation erhielten, erhielten ebenfalls ADCETRIS mit einer mittleren Anzahl von 7 Zyklen (Bereich 1 ‑ 16 Zyklen).
49 (82 %) der 60 Patienten in der Studie hatten zuvor mehr als eine Krebsbehandlung erhalten und 11 Patienten (18 %) hatten zuvor genau eine Krebsbehandlung erhalten. Nach IRF lag die objektive Ansprechrate (ORR) der Patienten, die zuvor mehr als eine Krebsbehandlung erhalten hatten, bei 51 % (95‑%‑KI [36 %, 66 %]) und bei den Patienten, die zuvor genau eine Krebsbehandlung erhalten hatten, bei 45 % (95‑%‑KI [17 %, 77 %]). Bei den Patienten, die zuvor mehr als eine Krebsbehandlung erhalten hatten, wurde bei 6 Patienten (12 %) das beste Gesamtansprechen mit einer kompletten Remission berichtet; eine teilweise Remission wurde bei 19 Patienten (39 %) berichtet. Bei den Patienten, die zuvor genau eine Krebsbehandlung erhalten hatten, wurde bei einem Patienten (9 %) eine komplette Remission berichtet; eine partielle Remission wurde bei 4 Patienten (36 %) berichtet. 22 der 49 Patienten (45 %), die zuvor mehr als eine Krebsbehandlung erhalten hatten, erhielten nachfolgend eine Stammzelltransplantation; 6 der 11 Patienten (55 %), die zuvor genau eine Krebsbehandlung erhalten hatten, erhielten nachfolgend eine Stammzelltransplantation.
Daten von Patienten mit rezidiviertem oder refraktärem HL, ohne vorherige autologe Stammzelltransplantation, und unter einer Behandlung mit 1,8 mg/kg ADCETRIS alle 3 Wochen wurden ebenfalls von Phase‑1‑Dosis‑Eskalations‑ und klinisch‑pharmakologischen Studien (n = 15) sowie aus einem NPP (n = 26) gewonnen.
Analyse der Patientenmerkmale ergab ein Versagen von mehreren vorangegangenen Chemotherapien (Median 3 in einem Bereich von 1 ‑ 7) vor der ersten Gabe von ADCETRIS. Neunundfünfzig Prozent (59 %) der Patienten befanden sich in einem fortgeschrittenen Krankheitsstadium (Grad III oder IV).
Die Ergebnisse dieser Phase‑1‑Studien und die Erfahrungen aus dem NPP zeigten, dass bei Patienten mit rezidiviertem oder refraktärem HL ohne vorausgegangene autologe Stammzelltransplantation ein klinisch relevantes Ansprechen erreicht werden kann. Dies wurde durch eine von Studienärzten beurteilte objektive Ansprechrate von 54 % und einer kompletten Remission von 22 % nach im Mittel 5 Zyklen von ADCETRIS belegt.
Studie SGN35‑006 (Studie zur Wiederholungsbehandlung)
Die Wirksamkeit der erneuten Behandlung von Patienten, die zuvor auf die Behandlung mit ADCETRIS angesprochen hatten (CR oder PR), wurde in einer offenen, multizentrischen Phase‑2‑Studie untersucht. Zwanzig Patienten mit rezidiviertem oder refraktärem HL erhielten eine Anfangsdosis von 1,8 mg/kg und ein Patient erhielt eine Anfangsdosis von 1,2 mg/kg ADCETRIS, das intravenös über 30 Minuten alle 3 Wochen verabreicht wurde. Die mittlere Anzahl von Zyklen betrug 7 (Bereich 2 ‑ 37 Zyklen). Von den 20 auswertbaren Patienten mit HL, erreichten 6 Patienten (30 %) eine CR und 6 Patienten (30 %) eine PR unter der Wiederholungsbehandlung mit ADCETRIS bei einer ORR von 60 %. Die mittlere Dauer des Ansprechens betrug 9,2 und 9,4 Monate bei Patienten, die eine OR (CR + PR) bzw. CR erreichten.
Systemisches großzelliges anaplastisches Lymphom
Studie SGN35‑014
Die Wirksamkeit und Sicherheit von ADCETRIS wurden in einer randomisierten, doppelblinden, aktiv kontrollierten, multizentrischen Double‑Dummy‑Studie an 452 Patienten mit bislang unbehandeltem CD30+ PTCL in Kombination mit Cyclophosphamid (C), Doxorubicin (H) und Prednison (P) (CHP) untersucht. Für die Aufnahme in die Studie war eine CD30‑Expression von ≥ 10 % pro immunhistochemischem Verfahren erforderlich. Nur Patienten mit CD30+ PTCLs, die für ein (CHOP)‑basiertes Behandlungsschema mit Cyclophosphamid (C), Doxorubicin (H), Vincristin (O) und Prednison (P) infrage kamen, wurden in die Studie aufgenommen. Die Kombination ADCETRIS + CHP wurde nicht für alle PTCL‑Subtypen untersucht. Die in die Studie aufgenommenen PTCL‑Subtypen sind in Tabelle 18 aufgeführt. Von den 452 Patienten wurden 226 zur Behandlung mit ADCETRIS + CHP randomisiert und 226 zur Behandlung mit CHOP. Die Randomisierung wurde nach ALK‑positivem sALCL im Vergleich zu allen anderen Subtypen und nach dem Internationalen Prognostischen Index (IPI) stratifiziert. Die Patienten erhielten 1,8 mg/kg ADCETRIS jeweils an Tag 1 jedes 21‑Tage‑Zyklus als intravenöse Infusion über 30 Minuten + CHP (750 mg/m2 Cyclophosphamid alle 3 Wochen als intravenöse Infusion; 50 mg/m2 Doxorubicin alle 3 Wochen als intravenöse Infusion; und 100 mg orales Prednison an den Tagen 1 bis 5 eines jeden 3‑wöchigen Zyklus) 6 bis 8 Zyklen lang. Die mediane Anzahl der erhaltenen Zyklen lag bei 6 (Bereich 1 bis 8 Zyklen); 70 % der Patienten erhielten 6 Behandlungszyklen und 18 % 8 Behandlungszyklen. Tabelle 18 enthält eine Zusammenfassung der Patienten‑ und Krankheitsmerkmale bei Studienbeginn.
Tabelle 18: Zusammenfassung der Patienten‑ und Krankheitsmerkmale am Ausgangspunkt der Phase‑3‑PTCL‑Studie mit bislang unbehandelten Patienten (ITT und sALCL)
ITTPopulation |
sALCLPopulationb |
||||||
Patientenmerkmale |
ADCETRIS + CHP |
CHOP |
ADCETRIS + CHP |
CHOP |
|||
Medianes Alter (Bereich) |
58,0 (18‑85) |
58,0 (18‑83) |
55,0 (18‑85) |
54,0 (18‑83) |
|||
Patienten ≥ 65 Jahre (%) |
69 (31) |
70 (31) |
38 (23) |
36 (23) |
|||
Männlich, n (%) |
133 (59) |
151 (67) |
95 (59) |
110 (71) |
|||
ECOG‑Status, n (%) |
|||||||
0 |
84 (37) |
93 (41) |
58 (36) |
53 (34) |
|||
1 |
90 (40) |
86 (38) |
62 (38) |
61 (40) |
|||
2 |
51 (23) |
47 (21) |
41 (25) |
40 (26) |
|||
Krankheitsmerkmale |
|||||||
Diagnose, nach lokaler Beurteilung, n (%)a |
|||||||
sALCL |
162 (72) |
154 (68) |
162 (100) |
154 (100) |
|||
ALK‑positiv |
49 (22) |
49 (22) |
49 (30) |
49 (32) |
|||
ALK‑negativ |
113 (50) |
105 (46) |
113 (70) |
105 (68) |
|||
Peripheres T-Zell-Lymphom |
29 (13) |
43 (19) |
n. z. (nicht zutreffend) |
n. z. |
|||
Angioimmunoblastisches T- |
30 (13) |
24 (11) |
n. z. |
n. z. |
|||
Adulte/s T-Zell-Leukämie/- |
4 (2) |
3 (1) |
n. z. |
n. z. |
|||
Enteropathie-assoziiertes T- |
1 (0) |
2 (1) |
n. z. |
n. z. |
|||
Mediane Dauer von der Diagnose bis zur ersten Dosis, in Monaten (Bereich) |
0,8 (0; 19) |
0,9 (0; 10) |
0,8 (0, 19) |
0,9 (0, 10) |
|||
Krankheitsstadium bei der Diagnose von PTCL, n (%) |
|||||||
Stadium I |
12 (5) |
9 (4) |
12 (7) |
7 (5) |
|||
Stadium II |
30 (13) |
37 (16) |
22 (14) |
27 (18) |
|||
Stadium III |
57 (25) |
67 (30) |
29 (18) |
46 (30) |
|||
Stadium IV |
127 (56) |
113 (50) |
99 (61) |
74 (48) |
|||
IPI |
|||||||
0 |
8 (4) |
16 (7) |
7 (4) |
14 (9) |
|||
1 |
45 (20) |
32 (14) |
34 (21) |
18 (12) |
|||
2 |
74 (33) |
78 (35) |
58 (36) |
60 (39) |
|||
3 |
66 (29) |
66 (29) |
37 (23) |
40 (26) |
|||
4 |
29 (13) |
25 (11) |
22 (14) |
16 (10) |
|||
5 |
4 (2) |
9 (4) |
4 (2) |
6 (4) |
|||
Extranodaler Befall zum Zeitpunkt der Diagnose, n (%) |
|||||||
≤ 1 Herd |
142 (63) |
146 (65) |
94 (58) |
95 (62) |
|||
> 1 Herd |
84 (37) |
80 (35) |
68 (42) |
59 (38) |
|||
Mittels Biopsie erkannte Knochenmarkbeteiligung bei Studienbeginn, n (%) |
|||||||
Ja |
30 (13) |
34 (15) |
15 (9) |
13 (8) |
|||
Nein |
196 (87) |
192 (85) |
147 (91) |
141 (92) |
|||
a Gemäß WHO‑Klassifikation von 2008. | |||||||
Der primäre Endpunkt in der Studie SGN35‑014 war das progressionsfreie Überleben (PFS), beurteilt durch ein unabhängiges Gutachterkomitee (IRF), definiert als Zeit ab dem Datum der Randomisierung bis zum Datum des ersten dokumentierten Fortschreitens der Krankheit, bis zum Tod jeglicher Ursache oder bis zum Erhalt einer anschließenden Chemotherapie zur Behandlung der verbleibenden oder fortschreitenden Erkrankung (je nachdem, was zuerst eintritt). Eine konsolidierende Bestrahlung nach der Behandlung, eine Chemotherapie nach der Behandlung zum Zweck der Mobilisierung peripherer Blutstammzellen und eine konsolidierende autologe oder allogene Stammzelltransplantation wurden nicht als Fortschreiten der Krankheit oder als Beginn einer neuen Krebstherapie angesehen.
Die wichtigsten sekundären Endpunkte waren das PFS gemäß Beurteilung des IRF für Patienten mit zentral bestätigtem sALCL, die CR‑Rate gemäß IRF nach Abschluss der Studienbehandlung, das OS und die ORR gemäß IRF nach Abschluss der Studienbehandlung, Die wichtigsten sekundären Endpunkte wurden in einer sequenziellen Analyse hierarchisch statistisch getestet nachdem die statistische Signifikanz des PFS gemäß IRF festgestellt wurde.
Der primäre Endpunkt und die alpha‑geschützten, wichtigsten sekundären Endpunkte, die hierarchisch ausgewertet wurden, wurden erreicht. Das mediane PFS gemäß Beurteilung eines IRF für die ITT‑Population betrug 48,2 Monate in der Gruppe ADCETRIS + CHP gegenüber 20,8 Monaten in der CHOP‑Gruppe. Die stratifizierte Hazard Ratio betrug 0,71 (95‑%‑KI: 0,54; 0,93; p = 0,011), was auf eine 29 %ige Verringerung des Risikos von PFS‑Ereignissen für ADCETRIS + CHP im Vergleich zu CHOP hinweist. Beim Gesamtüberleben betrug die stratifizierte Hazard Ratio 0,66 (95‑%‑KI: 0,46; 0,95, p = 0,024), was auf eine 34 %ige Verringerung des Risikos von OS‑Ereignissen für ADCETRIS + CHP im Vergleich zu CHOP hinweist.
Das PFS gemäß IRF für Patienten mit zentral bestätigtem sALCL war ein vordefinierter sekundärer Endpunkt. Das mediane PFS gemäß IRF betrug 55,7 Monate im ADCETRIS + CHP‑Arm gegenüber 54,2 Monaten im CHOP‑Arm. Die stratifizierte Hazard Ratio betrug 0,59 (95‑%‑KI, 0,42; 0,84), was einer statistisch signifikanten Verringerung des Risikos von PFS‑Ereignissen für ADCETRIS+CHP gegenüber CHOP von 41 % (p‑Wert = 0,003) entspricht, siehe Abbildung 6 und Tabelle 19.
Für Patienten mit lokal diagnostiziertem sALCL wurden Subgruppenanalysen durchgeführt. Beim Gesamtüberleben betrug die stratifizierte Hazard Ratio 0,54 (95‑%‑KI: 0,34; 0,87), was einer 46 %igen Verringerung des Risikos von OS‑Ereignissen für ADCETRIS + CHP im Vergleich zu CHOP entspricht (siehe Abbildung 7). Zum Behandlungsende betrug die CR‑Rate nach IRF‑Bewertung 71,0 % bei Patienten im ADCETRIS+CHP‑Arm im Vergleich zu 53,2 % bei Patienten im CHOP‑Arm mit einer Differenz von 17,7 % (95‑%‑KI: 7,2 %; 28,3 %). Zum Behandlungsende betrug die ORR‑Rate nach IRF‑Bewertung 87,7 % bei Patienten im ADCETRIS+CHP‑Arm im Vergleich zu 70,8 % bei Patienten im CHOP‑Arm mit einer Differenz von 16,9 % (95‑%‑KI: 8,1 %; 25,7 %). In der Subgruppe der Patienten mit ALK+ sALCL bzw. ALK‑ sALCL betrug die stratifizierte Hazard Ratio für PFS gemäß IRF 0,29 (95‑%‑KI: 0,11; 0,79) bzw. 0,65 (95‑%‑KI: 0,44; 0,95).
Tabelle 19: Wirksamkeitsergebnisse bei bislang unbehandelten sALCL‑Patienten, die jeweils an Tag 1 eines 3‑wöchigen Zyklus mit 1,8 mg/kg ADCETRIS behandelt wurden (primäre Analyse)
ADCETRIS + CHP |
CHOP |
||
PFS gemäß IRF | |||
Anzahl der Patienten mit einem PFS- |
56 (34) |
73 (48) |
|
Medianes PFS, in Monaten (95-%-KI) |
55,66 (48,20, NE) |
54,18 (13,44, NE) |
|
Hazard Ratio (95-%-KI )b |
0,59 (0,42, 0,84) |
||
p-Wertc |
0,0031 |
||
Geschätztes PFS (95-%-KI)d zum Zeitpunkt: |
|||
6 Monate |
88,0 % |
68,4 % |
|
12 Monate |
78,7 % |
60,3 % |
|
24 Monate |
68,4 % |
53,9 % |
|
36 Monate |
65,5 % |
50,2 % |
|
OSe | |||
Todesfälle (%) |
29 (18) |
44 (29) |
|
Medianes OS, in Monaten (95-%-KI) |
NE (NE, NE) |
NE (NE, NE) |
|
Hazard Ratio (95-%-KI)b |
0,54 (0,34, 0,87) |
||
p-Wertc,f |
0,0096 |
||
CR-Rateg | |||
% (95-%-KI) |
71 % (63,3 %, 77,8 %) |
53 % (45,0 %, 61,3 %) |
|
p-Wertf,h |
0,0004 |
||
ORRg | |||
% (95-%-KI) |
88 % (81,6 %, 92,3 %) |
71 % (62,9 %, 77,8 %) |
|
p-Wertf,h |
< 0,0001 |
||
|
CR = vollständige Remission; IRF = unabhängiges Gutachterkomitee; NE = not estimable, nicht abschätzbar; ORR = objektive Ansprechrate; PFS = progressionsfreies Überleben.
| |||
Abbildung 6: Progressionsfreies Überleben gemäß IRF in der sALCL‑Population (ADCETRIS + CHP vs. CHOP) (primäre Analyse)
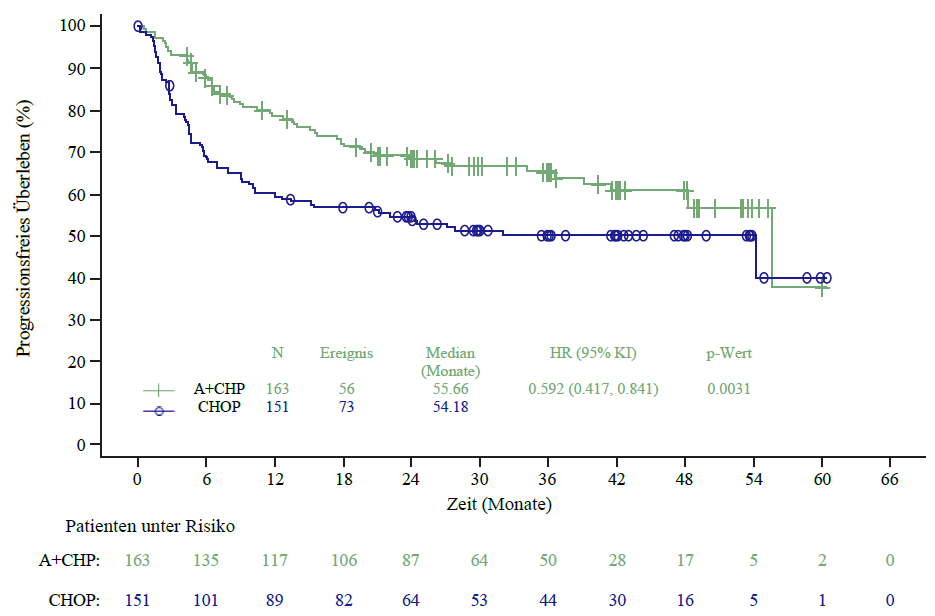
Abbildung 7: Gesamtüberleben in der sALCL‑Population (ADCETRIS + CHP vs. CHOP) (primäre Analyse)
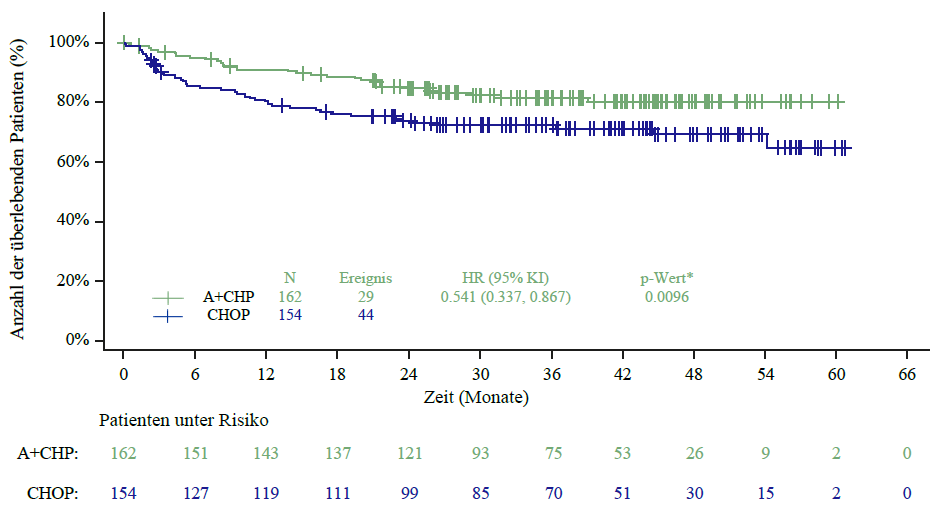
* Der p‑Wert für das Gesamtüberleben wurde nicht auf multiples Testen adjustiert.
Bei Studienende, mehr als 7 Jahre nach der Aufnahme des ersten Patienten, zeigten die PFS‑Ergebnisse nach Prüfarzt in der ITT‑Population eine 30%ige Verringerung des Risikos eines PFS‑Ereignisses im ADCETRIS + CHP‑Arm im Vergleich zu Patienten, die mit CHOP behandelt wurden (HR = 0,70 [95‑%‑KI (0,53, 0,91)]). Die PFS‑Ergebnisse nach Prüfarzt in der sALCL‑Population zeigten eine 45%ige Verringerung des Risikos eines PFS‑Ereignisses im ADCETRIS + CHP‑Arm im Vergleich zu den mit CHOP behandelten Patienten (HR = 0,55 [95‑%‑KI (0,39, 0,79)]).
Bei Studienende zeigten die Ergebnisse zum Gesamtüberleben weiterhin eine Verbesserung und entsprachen denen, die zum Zeitpunkt der primären Analyse berichtet wurden. Die Ergebnisse zum Gesamtüberleben in der ITT‑Population zeigten eine 28%ige Verringerung des Sterberisikos im ADCETRIS + CHP‑Arm im Vergleich zu den mit CHOP behandelten Patienten (HR = 0,72 [95‑%‑KI (0,53 bis 0,99)]). Die Ergebnisse zum Gesamtüberleben in der sALCL‑Population zeigten eine 34%ige Verringerung des Sterberisikos in der ADCETRIS + CHP‑Gruppe im Vergleich zu den mit CHOP behandelten Patienten (HR = 0,66 [95‑%‑KI (0,43, 1,01)]), siehe Abbildung 8.
Abbildung 8: Gesamtüberleben in der sALCL‑Population (ADCETRIS + CHP vs. CHOP) (Studienende)
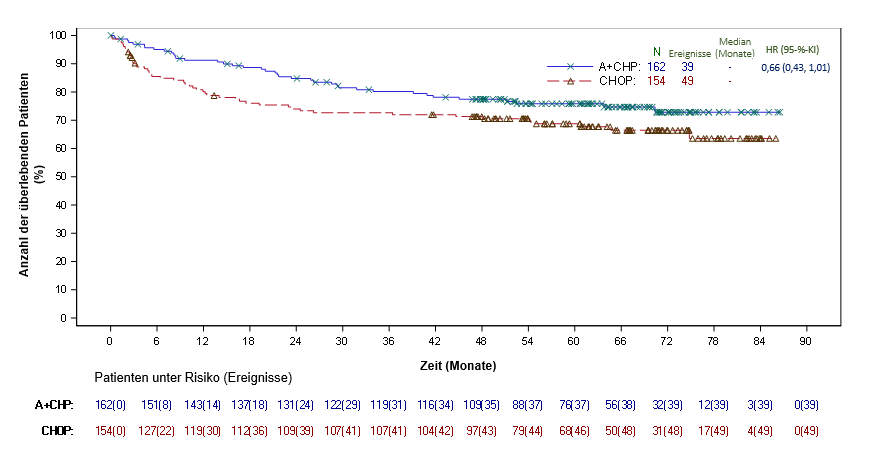
Studie SG035‑0004
Die Wirksamkeit und Sicherheit von ADCETRIS als Monotherapie wurde in einer offenen, einarmigen, multizentrischen Studie bei 58 Patienten mit rezidiviertem oder refraktärem sALCL untersucht. Siehe Tabelle 20 unten für eine Zusammenfassung der Patienten‑ und der Krankheitsmerkmale.
Tabelle 20: Zusammenfassung der Patienten‑ und Krankheitsmerkmale der in der Phase‑2‑Studie eingeschlossenen Patienten mit rezidiviertem oder refraktärem sALCL
Patientenmerkmale |
n = 58 |
|
Medianes Alter, Jahre (Bereich) |
52 Jahre (14‑76) |
|
Geschlecht |
33 M (57 %)/25 W (43 %) |
|
ECOG-Statusa |
||
0 |
19 (33 %) |
|
1 |
38 (66 %) |
|
Vorangegangene ASCT |
15 (26 %) |
|
Vorausgegangene Chemotherapien (Bereich)dd |
2 (1-6) |
|
Histologisch gesicherte CD30-exprimierende Krankheit |
57 (98 %) |
|
Anaplastische Lymphom Kinase (ALK)-negative Erkrankung |
42 (72 %) |
|
Krankheitsmerkmale |
||
Primär refraktär für Erstlinien-Therapieb |
36 (62 %) |
|
Refraktär nach letzter Therapie |
29 (50 %) |
|
Rückfall nach der letzten Therapie |
29 (50 %) |
|
B‑Symptome bei Studienbeginn |
17 (29 %) |
|
Stadium III bei Erstdiagnose |
8 (14 %) |
|
Stadium IV bei Erstdiagnose |
21 (36 %) |
|
| ||
Die mittlere Zeit zwischen der Erstdiagnose von sALCL bis zur ersten Dosis mit ADCETRIS betrug 16,8 Monate.
Zehn (10) Patienten (17 %) erhielten 16 Zyklen mit ADCETRIS, der Medianwert der verabreichten Zyklen war 7 (Bereich von 1 bis 16).
Das Ansprechen auf die Behandlung mit ADCETRIS wurde von einem unabhängigen Aufsichtskomitee (IRF) auf Basis der Revised Response Criteria for Malignant Lymphoma (Cheson, 2007) beurteilt. Das Ansprechen auf die Behandlung wurde mittels Spiral‑CT von Thorax, Hals, Abdomen und Becken, mittels PET‑Scans und klinischer Daten beurteilt. Das Ansprechen wurde in den Zyklen 2, 4, 7, 10, 13 und 16 beurteilt, mit PET‑Scans in den Zyklen 4 und 7.
Die objektive Ansprechrate betrug nach der IRF‑Beurteilung 86 % (50 von 58 Patienten in der ITT‑Gruppe). Bei 59 % (34 von 58 Patienten in der ITT‑Gruppe) wurde eine komplette Remission und bei 97 % der Patienten eine Reduktion (jeglichen Grades) der Tumor‑Last erreicht. Das geschätzte 5 Jahres‑Gesamtüberleben betrug 60 % (95‑%‑KI [47 %,73 %]). Die mittlere Beobachtungszeit (Zeit bis zum Tod oder bis zum letzten Kontakt) ab der ersten Dosis betrug 71,4 Monate. Die Beurteilung der Prüfärzte entsprach im Allgemeinen der unabhängigen Überprüfung der Scans. Von den behandelten Patienten, die auf die Therapie ansprachen, erhielten 9 eine allogene Stammzelltransplantation (SCT) und 9 eine autologe Stammzelltransplantation. Weitere Ergebnisse zur Wirksamkeit siehe Tabelle 21 und Abbildung 9.
Tabelle 21: Die Ergebnisse zur Wirksamkeit bei rezidiviertem oder refraktärem sALCL bei Patienten, die alle 3 Wochen mit 1,8 mg/kg ADCETRIS behandelt wurden
Bestes klinisches Ansprechen (n = 58 ) |
IRF n (%) |
95-%-KI |
Objektive Ansprechrate (CR + PR) |
50 (86) |
74,6; 93,9 |
Komplette Remission (CR) |
34 (59) |
44,9; 71,4 |
Partielle Remission (PR) |
16 (28) |
Nicht zutreffend |
Gesamtansprechrate (CR + PR + Krankheitsstabilisierung) |
52 (90) |
78,8; 96,1 |
Ansprechdauer |
Median nach IRF |
95-%-KI |
Objektive Ansprechrate (CR + PR)a |
13,2 |
5,7; 26,3 |
Komplette Remission (CR) |
26,3 |
13,2; NAb |
Progressionsfreies Überleben |
Median nach IRF |
95-%-KI |
Median |
14,6 |
6,9; 20,6 |
Gesamtüberleben |
Median |
95-%-KI |
Median |
Nicht erreicht |
21,3, NAb |
| ||
Abbildung 9: Kaplan‑Meier‑Kurve des Gesamtüberlebens
Eine explorative intraindividuelle Analyse zeigte, dass ungefähr 69 % der sALCL‑Patienten, die mit ADCETRIS innerhalb der klinischen Studie SG035‑0004 behandelt wurden, eine klinische Verbesserung in Form von verlängertem progressionsfreiem Überleben (PFS) erfuhren im Vergleich zur direkt vorangegangen Therapie.
Von den 17 Patienten (29 %), die zu Beginn der Studie B‑Symptome aufwiesen, kam es bei 14 Patienten (82 %) in einer mittleren Zeit von 0,7 Monaten nach Behandlungsbeginn mit ADCETRIS zum Verschwinden aller B‑Symptome.
Studie C25006
Die Wirksamkeit und Sicherheit von ADCETRIS als Monotherapie wurde auch in einer offenen, einarmigen multizentrischen Phase‑4‑Studie bei 50 Patienten mit rezidiviertem oder refraktärem sALCL untersucht. Die ORR gemäß IRF‑Beurteilung betrug 64 % (32 von 50 Patienten in der ITT‑Gruppe). Die mediane Dauer des Ansprechens (duration of response, DOR) gemäß IRF wurde nicht erreicht (95 % KI 19,71 Monate, NE). Die CR‑Rate lag bei 30 % (15 von 50 Patienten in der ITT‑Gruppe), und bei 93 % der auswertbaren Patienten wurde eine Tumorreduktion (jeglichen Grades) erreicht. Die mediane DOCR gemäß IRF wurde nicht erreicht (95‑%‑KI 10,61 Monate, NE). Im Allgemeinen stimmten die Beurteilungen über das Ansprechen durch IRF und den Prüfarzt überein. Von den behandelten Patienten erhielten 13 anschließend eine hämatopoetische Stammzelltransplantation.
Die gepoolten Daten der Studien C25006 und SG035‑0004 (n = 108) zeigen gemäß IRF eine ORR von 76 % (82 von 108 Patienten in der ITT‑Gruppe). Die mediane DOR gemäß IRF betrug 17,0 Monate (95‑%‑KI 12,62, 32,46). Die CR lag bei 45 % (49 von 108 Patienten in der ITT‑Gruppe), und bei 96 % der auswertbaren Patienten wurde eine Tumorreduktion (jeglichen Grades) erreicht. Die mediane DOCR gemäß IRF betrug 26,3 Monate (95‑%‑KI 16,16, NE). Im Allgemeinen war die Beurteilung über das Ansprechen durch IRF und den Prüfarzt einheitlich.
Studie SGN35‑006 (Studie zur Wiederholungsbehandlung)
Die Wirksamkeit der erneuten Behandlung von Patienten, die zuvor auf die Behandlung mit ADCETRIS angesprochen hatten (CR oder PR), wurde in einer offenen, multizentrischen Phase‑2‑Studie untersucht. Sieben Patienten mit rezidiviertem sALCL erhielten eine Anfangsdosis von 1,8 mg/kg und ein Patient erhielt eine Anfangsdosis von 1,2 mg/kg ADCETRIS, das intravenös über 30 Minuten alle 3 Wochen verabreicht wurde. Die mittlere Anzahl von Zyklen betrug 8,5 (Bereich 2 – 30 Zyklen). Von den 8 sALCL Patienten wurden 3 jeweils zweimal erneut behandelt, in Summe 11 Erfahrungswerte einer Wiederholungsbehandlung. Die erneute Behandlung mit ADCETRIS führte zu 6 CRs (55 %) und 4 PRs (36 %), bei einer OR von 91 %. Die mittlere Dauer des Ansprechens betrug 8,8 und 12,3 Monate bei Patienten, die eine OR (CR + PR) bzw. CR erreichten.
Kutanes T‑Zell‑Lymphom
Studie C25001
Die Wirksamkeit und Sicherheit von ADCETRIS als Monotherapie wurde in einer randomisierten, offenen, multizentrischen Phase‑3‑Zulassungsstudie an 128 Patienten mit histologisch gesichertem CD30+ CTCL untersucht. Die CD30‑Positivität wurde so definiert, dass ≥ 10 % lymphoide Zielzellen ein Membran‑, Zytoplasma‑ und/oder Golgi‑Färbemuster aufweisen basierend auf einem immunhistochemischen Verfahren (Ventana anti‑CD30 [Ber‑H2]). Patienten mit der Diagnose Mycosis fungoides (MF) oder primär kutanes anaplastisches großzelliges Lymphom (pcALCL) wurden als für die Studie geeignet eingestuft. Die Patienten wurden gemäß diesen Krankheitstypen stratifiziert und 1:1 randomisiert und erhielten entweder ADCETRIS oder nach Wahl des Arztes entweder Methotrexat oder Bexaroten. Patienten mit pcALCL erhielten zuvor entweder eine Strahlenbehandlung oder mindestens eine systemische Vorbehandlung, und Patienten mit MF erhielten mindestens 1 systemische Vorbehandlung. Patienten, bei denen gleichzeitig eine systemische ALCL, Sézary‑Syndrom und andere Non‑Hodgkin‑Lymphome (außer lymphomatoide Papulose [LyP]) diagnostiziert wurden, wurden von dieser Studie ausgeschlossen. Die Patienten erhielten alle 3 Wochen 1,8 mg/kg ADCETRIS intravenös über 30 Minuten bis zu 16 Zyklen oder nach Wahl des Arztes bis zu 48 Wochen lang. Die mediane Anzahl der Zyklen betrug im ADCETRIS‑Arm ca. 12 Zyklen. Im Arm nach Wahl des Arztes betrug die mediane Behandlungsdauer (Anzahl der Zyklen) bei den Patienten, die Bexaroten erhielten, etwa 16 Wochen (5,5 Zyklen) und 11 Wochen (3 Zyklen) bei den Patienten, die Methotrexat erhielten. Tabelle 22 enthält eine Zusammenfassung der Patienten‑ und Krankheitsmerkmale am Ausgangspunkt.
Tabelle 22: Zusammenfassung der Patienten‑ und Krankheitsmerkmale am Ausgangspunkt in der Phase‑3‑CTCL‑Studie (ITT‑Population)
Patientenmerkmale |
ADCETRIS |
Wahl des Arztes (Methotrexat oder Bexaroten) |
||
Medianes Alter (Bereich) |
62 Jahre (22‑83) |
58,5 Jahre (22‑83) |
||
Patienten ≥ 65 Jahre n (%) |
28 (44 %) |
24 (38 %) |
||
ECOG‑Status n (%) |
||||
0 |
43 (67) |
46 (72) |
||
1 |
18 (28) |
16 (25) |
||
2 |
3 (5) |
2 (3) |
||
Krankheitsmerkmale |
||||
Mediane Anzahl der vorangegangenen Behandlungen (Bereich) |
4 (0‑13) |
3,5 (1‑15) |
||
Mediane Anzahl der hautbezogenen Behandlungen (Bereich) |
1 (0‑6) |
1 (0‑9) |
||
Mediane Anzahl der systemischen Behandlungen (Bereich) |
2 (0‑11) |
2 (1‑8) |
||
MF, n (%) |
48 (75) |
49 (77) |
||
Frühstadium (IA‑IIA) |
15 (31) |
18 (37) |
||
Fortgeschritten (IIB‑IVBa) |
32 (67) |
30 (61) |
||
pcALCL, n (%) |
16 (25) |
15 (23) |
||
nur Haut |
9 (56) |
11 (73) |
||
Extrakutane Erkrankung |
7 (44) |
4 (27) |
||
| ||||
Die häufigsten vorangegangenen hautbezogenen Behandlungen bei der ITT‑Population waren Strahlenbehandlung (64 %), Phototherapie (48 %) und topische Steroide (17 %). Die häufigsten vorangegangenen systemischen Behandlungen bei der ITT‑Population waren Chemotherapie (71 %), Immuntherapie (43 %) und Bexaroten (38 %).
Der primäre Endpunkt war eine objektive Ansprechrate, die mindestens 4 Monate anhält (ORR4) (Dauer vom ersten bis zum letzten Ansprechen ≥ 4 Monate), ermittelt durch eine unabhängige Überprüfung des Globalen Ansprechwerts (GRS), die aus Hautuntersuchungen (modifiziertes Werkzeug zur Bestimmung des gewichteten Schweregrads, [mSWAT], nach Bewertung des Prüfarztes), der Beurteilung der Lymphknoten und einer viszeral‑röntgenologischen Beurteilung sowie dem Nachweis von zirkulierenden Sézary‑Zellen besteht (Olsen 2011). Tabelle 23 enthält die Ergebnisse für ORR4 und andere wichtige sekundäre Endpunkte.
Tabelle 23: Wirksamkeitsergebnisse bei CTCL‑Patienten, die alle 3 Wochen mit 1,8 mg ADCETRIS/kg (ITT‑Population) behandelt worden waren
ADCETRIS n = 64 |
Wahl des Arztes (Methotrexat oder Bexaroten) |
||
Objektive Ansprechrate von mindestens 4 Monaten (ORR4) nach IRF | |||
n (%) |
36 (56,3) |
8 (12,5) |
|
Prozentualer Unterschied (95-%-KI) |
43,8 (29,1; 58,4) |
||
p‑Wert |
< 0,001 |
||
Gesamtansprechrate (CR) nach IRF | |||
n (%) |
10 (15,6) |
1 (1,6) |
|
Prozentualer Unterschied (95-%- KI) |
14,1 (-4,0; 31,5) |
||
Angepasster p-Werta |
0,0046 |
||
Progressionsfreies Überleben (PFS) nach IRF | |||
Median (Monate) |
16,7 |
3,5 |
|
Risikoquotient |
0,270 |
||
95-%-KI |
(0,17; 0,43) |
||
Angepasster p-Werta |
< 0,001 |
||
a. Mit einem gewichteten Holm‑Verfahren berechnet. | |||
Vorab festgelegte Subgruppenanalysen von ORR4 nach IRF wurden anhand des CTCL‑Subtyps der Patienten, der Behandlung nach Wahl des Arztes, des ECOG‑Ausgangsstatus, des Alters, des Geschlechts und der geografischen Region durchgeführt. Die Analysen zeigten einen durchgängigen Trend in Richtung eines Nutzens für Patienten, die ADCETRIS erhielten, im Vergleich zu Patienten, die ein Arzneimittel nach Wahl des Arztes erhalten hatten. ORR4 betrug im ADCETRIS‑Arm 50 % und 75 % gegenüber 10,2 % und 20 % bei MF bzw. pcALCL im Arm nach Wahl des Arztes.
Es konnten keine signifikanten Unterschiede in der Lebensqualität (bewertet anhand des fünfdimensionalen EuroQol‑Fragebogens [EQ‑5D] und der Fragebögen zur Erfassung der Lebensqualität in der Onkologie [FACT‑G]) zwischen den Behandlungsarmen beobachtet werden.
Die Wirksamkeit und Sicherheit von ADCETRIS wurde in zwei weiteren offenen Studien an 108 Patienten mit rezidivierender CD30+ CTCL (einschließlich Patienten mit MF und pcALCL sowie SS, LyP und gemischter CTCL‑Histologie) unabhängig von der Höhe der CD30‑Expression untersucht. Die Patienten erhielten alle 3 Wochen 1,8 mg/kg ADCETRIS intravenös über 30 Minuten bis zu 16 Zyklen lang. Die Sicherheits‑ und Wirksamkeitsergebnisse dieser Studien entsprachen den Ergebnissen der Studie C25001. Die Ansprechrate für MF betrug 54‑66 %, für pcALCL 67 %, für SS 50 %, für LyP 92 % und für gemischte CTCL‑Histologie 82‑85 %.
Kinder und Jugendliche
Kombinationstherapie
C25004
Die Sicherheit und die Anti‑Tumor‑Aktivität von ADCETRIS wurden in einer offenen, multizentrischen Studie an 59 pädiatrischen Patienten (6 bis 17 Jahre) mit zuvor unbehandelter klassischer CD30+ HL‑Erkrankung im fortgeschrittenen Stadium in Kombination mit einer Chemotherapie (Doxorubicin [A], Vinblastin [V] und Dacarbazin [D] [AVD]) untersucht. Alle Patienten hatten eine histologisch bestätigte CD30‑exprimierende Erkrankung. Bei 59 % der Patienten (n = 35) lag ein extranodaler Befall vor. Alle 59 pädiatrischen Patienten wurden jeweils am 1. und am 15. Tag eines jeden 28‑tägigen Zyklus mit 48 mg/m² ADCETRIS behandelt, verabreicht als intravenöse Infusion über 30 Minuten + 25 mg/m² Doxorubicin, 6 mg/m² Vinblastin und 375 mg/m² Dacarbazin. Die Körperoberflächen‑basierte Dosis von ADCETRIS wurde so gewählt, dass sie den in der Studie C25003 beobachteten pharmakokinetischen Expositionen bei Erwachsenen entspricht. Die maximal verträgliche pädiatrische Dosis (maximum tolerated dose, MTD) wurde nicht erreicht. Die Mehrheit der Patienten (88 %) erreichte ein objektives Ansprechen bis zum Ende der Behandlung gemäß IRF‑Bewertung, wobei 76 % eine komplette Remission erreichten. Kein Patient starb. Insgesamt 13 Patienten (22 %) in der Sicherheitspopulation erhielten Berichten zufolge nach dem 6. Zyklus eine Bestrahlung.
Monotherapie
C25002
Die Sicherheit, Pharmakokinetik und Antitumoraktivität von ADCETRIS bei 36 pädiatrischen Patienten (im Alter von 7‑17 Jahren) mit r/r HL und sALCL (Kinder im Alter von 7–11 Jahren, n = 12 und Jugendliche im Alter von 12 bis 17 Jahren, n = 24) wurden im Rahmen einer offenen, multizentrischen Phase‑1/2‑Dosiseskalationsstudie (C25002) als Monotherapie untersucht. In Phase 1 der Studie wurden das Sicherheitsprofil (siehe Abschnitt 4.8), die maximalverträgliche Dosis (MTD) bei Kindern und Jugendlichen bzw. die empfohlene Phase‑2‑Dosis (RP2D) ermittelt sowie die Pharmakokinetik von ADCETRIS bewertet (siehe Abschnitt 5.2). Phase 1 umfasste 3 r/r HL‑Patienten, die mit 1,4 mg/kg behandelt wurden, und 9 Patienten (7 r/r HL und 2 sALCL), die mit 1,8 mg/kg behandelt wurden. Die MTD wurde nicht erreicht. Als RP2D wurde 1,8 mg/kg bestimmt. Im Verlauf der Studie wurden insgesamt 16 Patienten mit r/r HL und 17 Patienten mit r/r sALCL, von denen sich 10 im ersten Rezidiv befanden, mit 1,8 mg/kg ADCETRIS behandelt. Die Gesamtansprechrate (ORR), bewertet von einem unabhängigen Aufsichtskomitee (IRF), wurde in beiden Studienphasen bei RP2D untersucht. Von 33 Patienten, die die RP2D erhielten, konnte das Ansprechen bei 32 Patienten ausgewertet werden. Die ORR der Patienten mit auswertbarem Ansprechen betrug bei r/r HL‑Patienten 47 %, bei r/r sALCL Patienten 53 % und bei sALCL‑Patienten beim ersten Rezidiv 60 %. 8 HL‑Patienten und 9 sALCL‑Patienten erhielten nach der Behandlung mit ADCETRIS eine Stammzelltransplantation.
Monotherapie
Die Pharmakokinetik von Brentuximab vedotin wurde in Phase‑1‑Studien und in einer populations‑pharmakokinetischen Analyse von 314 Patientendaten untersucht. In allen klinischen Studien wurde Brentuximab vedotin als intravenöse Infusion verabreicht.
Maximale Konzentrationen des Brentuximab vedotin Antikörper‑Wirkstoff‑Konjugates (ADC) wurden in der Regel am Ende der Infusion oder zu dem Zeitpunkt der Probennahme, der dem Ende der Infusion am nächsten lag, beobachtet. Es wurde ein multiexponentieller Abfall der ADC‑Serumkonzentration mit einer terminalen Eliminationshalbwertszeit von etwa 4 bis 6 Tagen beobachtet. Die Exposition war in etwa proportional zur Dosis. Bei der Verabreichung von mehreren 3‑wöchigen Dosen wurde in Übereinstimmung mit der geschätzten Halbwertszeit nur eine minimale bis keine Akkumulation von ADC beobachtet. Typische Cmax‑ und AUC(0‑∞) ‑Werte von ADC nach Gabe einer einzelnen Dosis von 1,8 mg/kg in einer Phase‑1‑Studie betrugen ca. 31,98 μg/ml bzw. 79,41 μg/ml x Tag.
MMAE ist der Hauptmetabolit von Brentuximab vedotin. Die mittleren Werte für Cmax, AUC (0‑∞) und Tmax von MMAE nach Gabe einer einzelnen Dosis von 1,8 mg/kg ADC in einer Phase‑1‑Studie betrugen ca. 4,97 ng/ml, 37,03 ng/ml x Tag bzw. 2,09 Tage. Die MMAE‑Exposition nahm nach mehreren Dosen von Brentuximab vedotin ab, dabei wurden bei nachfolgenden Dosen etwa 50 % bis 80 % der Exposition nach der ersten Dosis beobachtet. MMAE wird weiter zu einem gleichermaßen wirksamen Metaboliten umgewandelt. Die Exposition des Metaboliten ist jedoch um eine Größenordnung geringer als die von MMAE. Daher ist es unwahrscheinlich, dass er einen wesentlichen Einfluss auf den systemischen Effekt von MMAE hat.
Im ersten Zyklus wurde eine höhere MMAE Exposition von einem Rückgang der absoluten Neutrophilenanzahl begleitet.
Kombinationstherapie
Die Pharmakokinetik von ADCETRIS in Kombination mit AVD wurde in einer einzelnen Phase‑3‑Studie an 661 Patienten untersucht. Populationspharmakokinetische Analysen zeigten, dass die Pharmakokinetik von ADCETRIS in Kombination mit AVD mit der der Monotherapie übereinstimmte.
Nach mehrmaliger intravenöser (i.v.‑) Infusion von 1,2 mg/kg Brentuximab vedotin alle zwei Wochen wurden die maximalen Serumkonzentrationen von ADC gegen Ende der Infusion beobachtet und die Elimination zeigte einen mehrfach exponentiellen Abfall mit einer t1/2z von etwa 4 bis 5 Tagen. Die höchsten Plasmakonzentrationen von MMAE wurden ungefähr 2 Tage nach dem Ende der Infusion beobachtet und wiesen einen einfach exponentiellen Abfall mit einem t1/2z von ungefähr 3 bis 4 Tagen auf.
Nach mehrmaliger i.v.‑Infusion von 1,2 mg/kg Brentuximab vedotin alle zwei Wochen wurden im 3. Zyklus stationäre Talkonzentrationen von ADC und MMAE erreicht. Nach dem Erreichen des stationären Zustands schien sich die PK des ADC nicht über den Zeitraum zu ändern. Die ADC‑Akkumulation (über AUC14D zwischen dem 1. und dem 3. Zyklus ermittelt) lag beim 1,27‑Fachen. Die MMAE‑Exposition (über AUC14D zwischen dem 1. und dem 3. Zyklus ermittelt) schien über den Zeitraum um etwa 50 % zu sinken.
Die Pharmakokinetik von ADCETRIS in Kombination mit CHP wurde in einer Phase‑3‑Studie an 223 Patienten (SGN35‑014) untersucht. Nach der intravenösen Infusion mehrerer Dosen von 1,8 mg/kg ADCETRIS alle 3 Wochen war die Pharmakokinetik des ADC und von MMAE mit der Pharmakokinetik der Monotherapie vergleichbar.
Die Pharmakokinetik von ADCETRIS wurde im BrECADD-Schema nicht untersucht.
Verteilung
In vitro wurde MMAE zu 68‑82 % an humane Plasmaproteine gebunden. Es ist unwahrscheinlich, dass MMAE stark proteingebundene Arzneimittel verdrängt oder von diesen aus der Bindung verdrängt wird. In vitro war MMAE ein Substrat von P‑gp und in klinischen Konzentrationen kein Inhibitor von P‑gp.
Beim Menschen lag das mittlere Verteilungsvolumen des ADC im Gleichgewicht bei etwa 6 ‑ 10 l. Basierend auf populationspharmakokinetischen Schätzungen betrug das typische zentrale scheinbare Verteilungsvolumen von MMAE 35,5 l.
Biotransformation
Der Immunglobulinanteil des ADC wird voraussichtlich als Protein abgebaut, und die Aminosäure‑Komponenten werden wiederverwendet oder ausgeschieden.
In‑vivo‑Daten bei Tieren und Menschen weisen darauf hin, dass nur ein Bruchteil des von Brentuximab vedotin freigesetzten MMAE metabolisiert wird. Die Konzentrationen der MMAE‑Metaboliten wurden in humanem Plasma nicht gemessen. Es wurde gezeigt, dass mindestens ein Metabolit von MMAE in vitro aktiv ist.
MMAE ist ein Substrat von CYP3A4 und möglicherweise von CYP2D6. In‑vitro‑Daten deuten darauf hin, dass MMAE hauptsächlich durch Oxidation durch CYP3A4/5 metabolisiert wird. In‑vitro‑Studien mit menschlichen Leber‑Mikrosomen deuten darauf hin, dass MMAE CYP3A4/5 nur in Konzentrationen hemmt, die deutlich über den bei der klinischen Anwendung erzielten Konzentrationen liegen. MMAE hemmt keine anderen Isoformen.
MMAE induzierte in Primärkulturen von menschlichen Hepatozyten keine wichtigen CYP450‑Enzyme.
Elimination
Das ADC wird mit einer geschätzten typischen CL und Halbwertszeit von 1,5 l/Tag bzw. 4‑6 Tagen eliminiert.
Die Elimination von MMAE wird durch seine Freisetzung aus dem ADC limitiert, die geschätzte typische scheinbare CL und Halbwertszeit von MMAE betrug 19,99 l/Tag bzw. 3‑4 Tage.
Bei Patienten, die eine Dosis von 1,8 mg/kg Brentuximab vedotin erhielten, wurde eine Ausscheidungsstudie durchgeführt. Ungefähr 24 % des gesamten MMAE, das als Teil des ADC während einer Brentuximab vedotin‑Infusion zugeführt wird, konnte über einen Zeitraum von 1 Woche im Urin und in den Faeces wiedergefunden werden. Hiervon wurden ungefähr 72 % des MMAE in den Faeces nachgewiesen. Ein geringerer Anteil an MMAE (28 %) wurde im Urin ausgeschieden.
Pharmakokinetik bei besonderen Populationen
Die populationspharmakokinetische Analyse zeigte, dass die Serum‑Albumin‑Konzentration vor der Verabreichung von Brentuximab vedotin eine signifikante Kovariable der MMAE‑Clearance darstellt. Die Analyse ergab, dass die MMAE‑Clearance bei Patienten mit niedrigen Serum‑Albumin‑Konzentrationen < 3,0 g/dl zweimal niedriger war als bei Patienten mit Serum‑Albumin Konzentrationen im Normalbereich.
Eingeschränkte Leberfunktion
In einer Studie wurde die PK von Brentuximab vedotin und MMAE nach Verabreichung von 1,2 mg/kg ADCETRIS an Patienten mit leichter (Child‑Pugh A; n = 1), mittelschwerer (Child‑Pugh B; n = 5) und schwerer (Child‑Pugh C; n = 1) Leberfunktionsstörung untersucht. Verglichen mit Patienten mit normaler Leberfunktion, stieg die MMAE Exposition etwa um das 2,3‑Fache (90‑%‑KI 1,27 ‑ 4,12‑fach) bei Patienten mit Leberfunktionsstörung.
Eingeschränkte Nierenfunktion
In einer Studie wurde die PK von Brentuximab vedotin und MMAE nach Verabreichung von 1,2 mg/kg ADCETRIS an Patienten mit leichter (n = 4), mittelschwerer (n = 3) und schwerer (n = 3) Nierenfunktionsstörung untersucht. Verglichen mit Patienten mit normaler Nierenfunktion, stieg die MMAE Exposition etwa um das 1,9‑Fache (90‑%‑KI 0,85 ‑ 4,21‑fach) bei Patienten mit schwerer Nierenfunktionsstörung (Kreatinin‑Clearance < 30 ml/min). Es wurden keine Effekte bei Patienten mit leichter oder mittelschwerer Nierenfunktionsstörung beobachtet.
Ältere Patienten
Die Populationspharmakokinetik von Brentuximab vedotin aus verschiedenen Studien wurde untersucht, darunter Daten von 380 Patienten bis zu 87 Jahren (34 Patienten ≥ 65 ‑ < 75 und 17 Patienten ≥ 75 Jahre alt). Darüber hinaus wurde die Populationspharmakokinetik von Brentuximab vedotin in Kombination mit AVD untersucht, einschließlich Daten von 661 Patienten bis zum Alter von 82 Jahren (42 Patienten ≥ 65 ‑ < 75 und 17 Patienten ≥ 75 Jahre alt). Der Einfluss des Alters auf die Pharmakokinetik wurde in jeder Analyse untersucht und war keine signifikante Kovariate.
Kinder und Jugendliche
Monotherapie
C25002
Die Pharmakokinetik von Brentuximab vedotin (BV), ADC und MMAE nach einer 30‑minütigen intravenösen Infusion von 1,4 mg BV/kg oder 1,8 mg BV/kg alle 3 Wochen wurde in einer klinischen Phase‑1/2‑Studie an 36 pädiatrischen Patienten (7 ‑ 17 Jahre) mit r/r HL und sALCL untersucht (n = 12 Kinder im Alter von 7 ‑ 11 Jahren und n = 24 Jugendliche im Alter von 12 bis 17 Jahren) (siehe Abschnitt 5.1). Maximale Konzentrationen (Cmax) des ADC wurden in der Regel am Ende der Infusion oder zum Zeitpunkt der Probennahme, der dem Ende der Infusion am nächsten lag, beobachtet. Es wurde ein multiexponentieller Abfall der ADC‑Serumkonzentration mit einer terminalen Eliminationshalbwertszeit von etwa 4 bis 5 Tagen beobachtet. Die Exposition war in etwa proportional zur Dosis, wobei ein Trend zu einer niedrigeren ADC‑Exposition bei niedrigerem Alter/niedrigerem Körpergewicht in der Studienpopulation beobachtet wurde. Die mittleren Werte für ADC AUC bei den Kindern und Jugendlichen in dieser Studie lagen ca. 14 % bzw. 3 % niedriger als der bei erwachsenen Patienten, wohingegen die MMAE‑Exposition um 53 % unter bzw. um 13 % über der von erwachsenen Patienten lag. Die mittleren Werte für Cmax und AUC von ADC nach einer einzelnen Dosis von 1,8 mg/kg betrugen 29,8 µg/ml bzw. 67,9 µg*Tag/ml bei Patienten unter 12 Jahren und 34,4 µg/ml bzw. 77,8 µg* Tag/ml bei Patienten ab 12 Jahren. Die mittleren Werte für Cmax, AUC und Tmax von MMAE nach einer einzelnen Dosis von 1,8 mg/kg betrugen 3,73 ng/ml, 17,3 ng*Tag/ml bzw. 1,92 Tage bei Patienten unter 12 Jahren und 6,33 ng/ml, 42,3 ng*Tag/ml bzw. 1,82 Tage bei Patienten ab 12 Jahren. Bei den pädiatrischen Patienten, die als ADA‑positiv bestätigt wurden, gab es einen Trend zu einer erhöhten Brentuximab‑vedotin‑Clearance. Es wurden keine Patienten im Alter unter 12 Jahren (0 von 11) und 2 Patienten im Alter ab 12 Jahren (2 von 23) anhaltend ADA‑positiv.
Kombinationstherapie
C25004
Die Pharmakokinetik von Brentuximab vedotin, ADC und MMAE nach einer 30‑minütigen intravenösen Infusion von BV, verabreicht in einer Dosierung von 48 mg/m2 alle 2 Wochen in Kombination mit Doxorubicin, Vinblastin und Dacarbazin (AVD), wurden in einer klinischen Phase‑1/2‑Studie an 59 pädiatrischen Patienten (6 bis 17 Jahre) mit neu diagnostiziertem CD30+ klassischem Hodgkin‑Lymphom im fortgeschrittenen Stadium untersucht (Kinder im Alter von 6 bis 11 Jahren, n = 11 und Jugendliche im Alter von 12 bis 17 Jahren, n = 48). Die maximalen Konzentrationen (Cmax) des ADC im Serum traten etwa am Ende der Infusion auf und nahmen multiexponentiell mit einer terminalen Halbwertszeit von etwa 4 Tagen ab. Die Cmax von MMAE im Plasma trat etwa 2 Tage nach der BV‑Verabreichung auf und hatte eine Halbwertszeit von etwa 2 Tagen. Der geometrische Mittelwert von Cmax bzw. AUC von ADC nach einer einzelnen Dosis von 48 mg/m2 betrug 22,5 µg/ml bzw. 46,7 µg*Tag/ml. Der geometrische Mittelwert von Cmax bzw. AUC von MMAE nach einer einzelnen Dosis von 48 mg/m2 betrug 4,9 ng/ml bzw. 27,2 ng*Tag/ml. In den pädiatrischen Altersgruppen (< 12 Jahre, 12‑16 Jahre und > 16 Jahre) wurden nach einer Körperoberflächen‑bezogenen Dosierung von BV von 48 mg/m2 in Kombination mit AVD ähnliche ADC‑Expositionen erreicht.
In einem In‑vivo‑Knochenmark‑Mikrokerntest bei Ratten wurde nachgewiesen, dass MMAE aneugenische Eigenschaften besitzt. Diese Ergebnisse waren konsistent mit der pharmakologischen Wirkung von MMAE auf den mitotischen Spindelapparat (Unterbrechung des Mikrotubuli‑Netzes) in den Zellen.
Die Auswirkungen von Brentuximab vedotin auf die männliche und weibliche Fertilität wurden nicht im Menschen untersucht. Allerdings weisen die Ergebnisse von Toxizitätsstudien an Ratten, denen wiederholt Dosen von Brentuximab vedotin verabreicht wurden, auf eine mögliche Beeinträchtigung der männlichen Fortpflanzungsfähigkeit und Fruchtbarkeit hin. Testikuläre Atrophie und Degeneration waren nach einer 16‑wöchigen behandlungsfreien Phase teilweise reversibel.
Brentuximab vedotin verursachte Embryo‑fetale Letalität bei trächtigen weiblichen Ratten.
In präklinischen Studien wurden lymphoide Depletion und ein verringertes Gewicht des Thymus beobachtet, was durch die pharmakologische Störung der Mikrotubuli verursacht durch das aus Brentuximab vedotin freigesetzte MMAE erklärt werden kann.
Citronensäure‑Monohydrat (zur pH‑Wert‑Einstellung) (E 330)
Natriumcitrat (Ph.Eur.) (zur pH‑Wert‑Einstellung) (E 331)
Trehalose‑Dihydrat (Ph.Eur.)
Polysorbat 80 (E 433)
Da keine Kompatibilitätsstudien durchgeführt wurden, darf dieses Arzneimittel, außer mit den unter Abschnitt 6.6 aufgeführten, nicht mit anderen Arzneimitteln gemischt werden.
4 Jahre.
Nach Rekonstitution/Verdünnung: Aus mikrobiologischer Sicht sollte die gebrauchsfertige Zubereitung sofort verwendet werden. Allerdings wurde die chemische und physikalische Stabilität der rekonstituierten Lösung bei 2 °C ‑ 8 °C für bis zu 24 Stunden nachgewiesen.
Im Kühlschrank lagern (2 °C ‑ 8 °C).
Nicht einfrieren.
Die Durchstechflasche im Umkarton aufbewahren, um den Inhalt vor Licht zu schützen.
Aufbewahrungsbedingungen nach Rekonstitution und Verdünnung des Arzneimittels, siehe Abschnitt 6.3.
Typ‑I‑Glas Durchstechflasche mit Butyl‑Gummistopfen und Aluminium‑Flip‑off‑Verschluss mit Kunststoffkappe, die 50 mg Pulver enthält.
Packung mit 1 Durchstechflasche.
Allgemeine Vorsichtsmaßnahmen
Die Vorschriften für die sachgerechte Handhabung und Entsorgung von Krebsarzneimitteln müssen beachtet werden.
Beim Umgang mit dem Arzneimittel ist eine aseptische Vorgehensweise einzuhalten.
Anleitung zur Rekonstitution
Jede einzelne Durchstechflasche muss mit 10,5 ml Wasser für Injektionszwecke bis auf eine Endkonzentration von 5 mg/ml rekonstituiert werden. Jede Durchstechflasche enthält eine 10 %ige Überfüllung, resultierend in 55 mg ADCETRIS pro Durchstechflasche und einer Gesamtrekonstitutionsmenge von 11 ml.
1. Richten Sie den Flüssigkeitsstrahl gegen die Wand der Durchstechflasche und nicht direkt in den Kuchen oder das Pulver.
2. Schwenken Sie die Durchstechflasche vorsichtig, um das Auflösen zu unterstützen. NICHT SCHÜTTELN.
3. Die rekonstituierte Lösung in der Durchstechflasche ist eine klare bis leicht opalisierende, farblose Lösung mit einem End‑pH von 6,6.
4. Die rekonstituierte Lösung muss visuell auf ungelöste Partikel und Verfärbungen überprüft werden. Sollte eines von beiden festgestellt werden, muss das Arzneimittel verworfen werden.
Zubereitung der Infusionslösung
Die entsprechende Menge an rekonstituiertem ADCETRIS muss aus der/den Durchstechflasche(n) entnommen und in einen Infusionsbeutel mit physiologischer Kochsalzlösung (0,9 %, Natriumchlorid 9 mg/ml) zur Injektion gegeben werden, um eine Endkonzentration von 0,4‑1,2 mg/ml ADCETRIS zu erreichen. Das empfohlene Volumen des Verdünnungsmittels beträgt 150 ml. Bereits rekonstituiertes ADCETRIS kann auch in 5 %‑Dextrose zur Injektion oder in Ringer‑Laktat‑Injektionslösung verdünnt werden.
Den Beutel vorsichtig umdrehen, um die ADCETRIS‑Lösung zu mischen. NICHT SCHÜTTELN.
Nach der Entnahme der zu verdünnenden Menge muss der nicht verwendete Inhalt der Durchstechflasche entsprechend den nationalen Richtlinien entsorgt werden.
Zu der vorbereiteten ADCETRIS‑Infusionslösung oder dem intravenösen Infusionsset dürfen keine anderen Arzneimittel hinzugefügt werden. Die Infusionsleitung muss nach der Verabreichung mit physiologischer Kochsalzlösung (0,9 %, Natriumchlorid 9 mg/ml) zur Injektion, 5 %‑Dextrose‑Injektionslösung oder Ringer‑Laktat‑Injektionslösung gespült werden.
Nach dem Verdünnen sollte die ADCETRIS‑Lösung sofort mit der empfohlenen Infusionsgeschwindigkeit infundiert werden.
Die Zeitspanne zwischen der Rekonstitution bis zur Infusion darf 24 Stunden nicht überschreiten.
Bestimmung der Dosis:
Berechnung der gesamten ADCETRIS‑Dosis (ml), die weiter verdünnt werden muss (siehe Abschnitt 4.2):
ADCETRIS‑Dosis (mg/kg) x Körpergewicht des Patienten (kg) |
= |
ADCETRIS‑Gesamtdosis (ml), die weiter verdünnt werden muss |
Konzentration in der rekonstituierten Durchstechflasche (5 mg/ml) |
Hinweis: Wenn das Gewicht des Patienten über 100 kg beträgt, sollte der Wert 100 kg für die Dosisberechnung verwendet werden. Die maximale empfohlene Dosis beträgt 180 mg.
Berechnung der Zahl der benötigten ADCETRIS Durchstechflaschen:
ADCETRIS‑Gesamtdosis (ml), die verabreicht werden soll |
= |
Anzahl der benötigten Durchstechflaschen |
Gesamtvolumen pro Durchstechflasche (10 ml/Durchstechflasche) |
Tabelle 24: Beispielberechnungen für Patienten mit einem Gewicht von 60 kg bis 120 kg, die die empfohlene Dosis von 1,8 mg/kg, 1,2 mg/kg oder 0,9 mg/kg ADCETRIS erhaltena, b
Empfohlene |
Gewicht des Patienten (kg) |
Gesamtdosis = |
Zu verdünnendes Gesamtvolumenc = Gesamtdosis geteilt durch die Konzentration in der rekonstituierten Durchstechflasche [5 mg/ml] |
Anzahl der benötigten Durchstechflaschen = Zu verdünnendes Gesamtvolumen geteilt durch das Gesamtvolumen pro Durchstechflasche [10 ml/Durchstech-flasche] |
1,8 mg/kg (bis höchstens 180 mg) |
60 kg |
108 mg |
21,6 ml |
2,16 Durchstech-flaschen |
80 kg |
144 mg |
28,8 ml |
2,88 Durchstech-flaschen |
|
100 kg |
180 mg |
36 ml |
3,6 Durchstechflaschen |
|
120 kgd |
180 mg |
36 ml |
3,6 Durchstechflaschen |
|
1,2 mg/kg (bis höchstens 120 mg) |
60 kg |
72 mg |
14,4 ml |
1,44 Durchstech-flaschen |
80 kg |
96 mg |
19,2 ml |
1,92 Durchstech-flaschen |
|
100 kg |
120 mg |
24 ml |
2,4 Durchstechflaschen |
|
120 kgd |
120 mg |
24 ml |
2,4 Durchstechflaschen |
|
0.9 mg/kg (bis höchstens 90 mg) |
60 kg |
54 mg |
10,8 ml |
1,08 Durchstech-flaschen |
80 kg |
72 mg |
14,4 ml |
1,44 Durchstech-flaschen |
|
100 kg |
90 mg |
18 ml |
1,8 Durchstechflaschen |
|
120 kgd |
90 mg |
18 ml |
1,8 Durchstechflaschen |
|
a. Diese Tabelle enthält Berechnungsbeispiele für erwachsene Patienten. | ||||
Entsorgung
ADCETRIS ist nur zum Einmalgebrauch bestimmt.
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Richtlinien zu entsorgen.
Takeda Pharma A/S
Delta Park 45
2665 Vallensbaek Strand
Dänemark
medinfoEMEA@takeda.com
EU/1/12/794/001
Datum der Erteilung der Zulassung: 25. Oktober 2012
Datum der letzten Verlängerung der Zulassung: 16. September 2021
02.2026
Ausführliche Informationen zu diesem Arzneimittel sind auf den Internetseiten der Europäischen Arzneimittel‑Agentur https://www.ema.europa.eu verfügbar.
Verschreibungspflichtig
Takeda GmbH
Telefon: 0800 8253325
E-Mail: medinfoEMEA@takeda.com
Artikelnummer 1107103882