▼Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung zu melden. Hinweise zur Meldung von Nebenwirkungen, siehe Abschnitt 4.8 .
Xofigo® 1100 kBq/ml Injektionslösung
Jeder ml Lösung enthält 1100 kBq (223Ra) Radiumchlorid (Radium‑223‑dichlorid, radium Ra 223 dichloride), entsprechend 0,58 ng Radium‑223 am Referenzdatum. Das Radium liegt in der Lösung als freies Ion vor.
Jede Durchstechflasche enthält 6 ml Lösung (6,6 MBq Radium‑223‑dichlorid am Referenzdatum).
Radium‑223 ist ein Alphastrahler und hat eine Halbwertszeit von 11,4 Tagen. Die spezifische Aktivität von Radium‑223 beträgt 1,9 MBq/ng.
Der sechsstufige Zerfall von Radium‑223 zu Blei‑207 erfolgt über kurzlebige Tochternuklide und wird von einer Reihe an Alpha‑, Beta‑ und Gammastrahlungen mit unterschiedlichen Energien und Emissionswahrscheinlichkeiten begleitet. Der von Radium‑223 und dessen Tochternukliden als Alphateilchen abgegebene Energieanteil beträgt 95,3 % (Energiebereich von 5,0 – 7,5 MeV). Der als Betateilchen abgegebene Energieanteil beträgt 3,6 % (mittlere Energien von 0,445 MeV und 0,492 MeV), und der als Gammastrahlung abgegebene Energieanteil beträgt 1,1 % (Energiebereich von 0,01 – 1,27 MeV).
Abbildung 1: Zerfallsreihe von Radium‑223 mit physikalischen Halbwertszeiten und Zerfallsart:
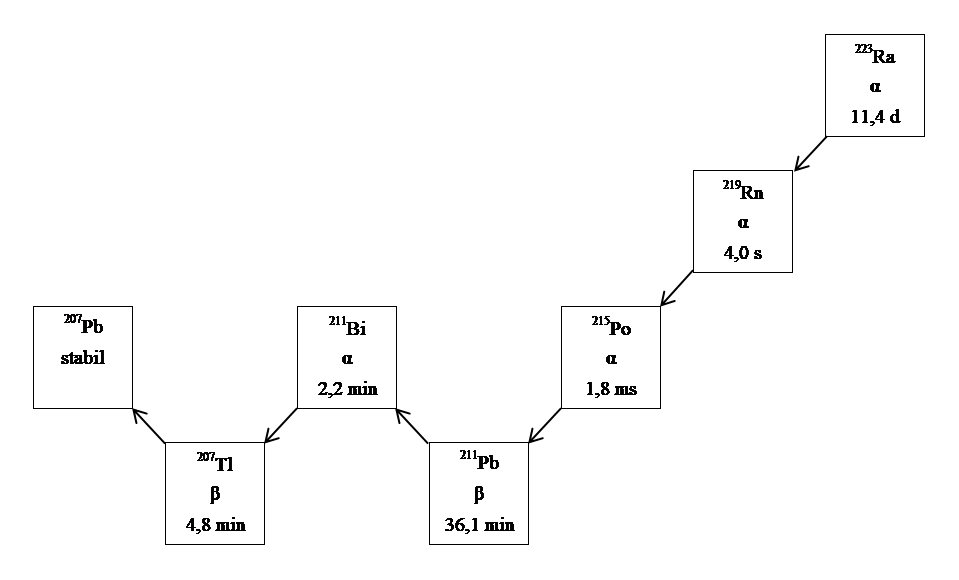
Sonstige Bestandteile mit bekannter Wirkung
Jeder ml Lösung enthält 0,194 mmol (entsprechend 4,5 mg) Natrium.
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
Injektionslösung.
Klare, farblose isotonische Lösung mit einem pH zwischen 6,0 und 8,0.
Xofigo wird als Monotherapie oder in Kombination mit einem LHRH-Analogon (LHRH: Luteinisierendes-Hormon-freisetzendes Hormon) zur Behandlung von erwachsenen Patienten mit metastasiertem kastrationsresistentem Prostatakarzinom (mCRPC) und symptomatischen Knochenmetastasen ohne bekannte viszerale Metastasen angewendet, bei denen die Erkrankung nach Erhalt von mindestens zwei vorausgehenden systemischen Therapielinien zur Behandlung des mCRPC (außer LHRH-Analoga) fortschreitet, oder für die keine andere verfügbare systemische mCRPC‑Therapie geeignet ist (siehe Abschnitt 4.4).
Xofigo darf nur von Personen, die für den Umgang mit radioaktiven Arzneimitteln autorisiert sind, in einem dafür vorgesehenen klinischen Bereich (siehe Abschnitt 6.6) und nach der Beurteilung des Patienten durch einen qualifizierten Arzt angewendet werden.
Dosierung
Das Behandlungsschema für Xofigo umfasst eine Aktivität von 55 kBq pro kg Körpergewicht, die in 4‑wöchigem Abstand sechsmal injiziert werden.
Die Sicherheit und Wirksamkeit von Xofigo bei Anwendung von mehr als 6 Injektionen wurden nicht untersucht.
Einzelheiten zur Berechnung des anzuwendenden Volumens, siehe Abschnitt 12.
Spezielle Populationen
Ältere Patienten
Insgesamt wurden keine Unterschiede in Bezug auf die Sicherheit und Wirksamkeit zwischen älteren (≥ 65 Jahre) und jüngeren (< 65 Jahre) Patienten in der Phase‑III‑Studie festgestellt.
Bei älteren Patienten wird eine Dosisanpassung nicht für erforderlich gehalten.
Leberfunktionsstörung
Die Sicherheit und Wirksamkeit von Xofigo wurden bei Patienten mit Leberfunktionsstörung nicht untersucht.
Da Radium‑223 weder in der Leber abgebaut noch über die Galle ausgeschieden wird, ist nicht zu erwarten, dass eine Leberfunktionsstörung die Pharmakokinetik von Radium‑223‑dichlorid beeinflusst.
Bei Patienten mit Leberfunktionsstörung wird eine Dosisanpassung nicht für erforderlich gehalten.
Nierenfunktionsstörung
In der klinischen Phase‑III‑Studie wurden zwischen Patienten mit leichter Nierenfunktionsstörung (Creatinin‑Clearance [CLCR]: 50 bis 80 ml/min) und normaler Nierenfunktion keine relevanten Unterschiede in Bezug auf die Sicherheit oder Wirksamkeit beobachtet. Zu Patienten mit mäßig schwerer (CLCR: 30 bis 50 ml/min) Nierenfunktionsstörung liegen nur begrenzt Daten vor. Zu Patienten mit schwerer (CLCR < 30 ml/min) Nierenfunktionsstörung oder terminaler Niereninsuffizienz liegen keine Daten vor.
Da die Ausscheidung über den Urin jedoch nur minimal ist und der größte Teil der Elimination mit dem Stuhl erfolgt, ist nicht zu erwarten, dass eine Nierenfunktionsstörung die Pharmakokinetik von Radium‑223‑dichlorid beeinflusst.
Bei Patienten mit Nierenfunktionsstörung wird eine Dosisanpassung nicht für erforderlich gehalten.
Kinder und Jugendliche
Es gibt im Anwendungsgebiet Prostatakarzinom keinen relevanten Nutzen von Xofigo bei Kindern und Jugendlichen.
Art der Anwendung
Xofigo ist zur intravenösen Anwendung. Es muss langsam injiziert werden (im Allgemeinen bis zu 1 Minute).
Der intravenöse Zugang oder die Kanüle müssen vor und nach der Injektion von Xofigo mit einer isotonischen Natriumchloridlösung für Injektionszwecke gespült werden.
Weitere Hinweise zur Anwendung des Arzneimittels, siehe Abschnitte 6.6 und 12.
Xofigo ist in der Kombination mit Abirateronacetat und Prednison/Prednisolon kontraindiziert (siehe Abschnitt 4.4).
Kombination mit Abirateron und Prednison/Prednisolon oder mit anderen systemischen Tumortherapien außer LHRH-Analoga
Eine Zwischenanalyse einer klinischen Studie bei Chemotherapie-naiven Patienten mit asymptomatischem oder leicht symptomatischem kastrationsresistentem Prostatakarzinom und Krankheitsprogression mit Knochenmetastasen zeigte ein erhöhtes Risiko für Frakturen und einen Trend zu erhöhter Mortalität bei Patienten, die Xofigo in Kombination mit Abirateronacetat und Prednison/Prednisolon erhielten, im Vergleich zu den Patienten, die Placebo in Kombination mit Abirateronacetat und Prednison/Prednisolon erhielten (siehe Abschnitt 5.1).
Daher ist Xofigo in Kombination mit Abirateronacetat und Prednison/Prednisolon kontraindiziert (siehe Abschnitt 4.3).
Die Sicherheit und Wirksamkeit von Xofigo in Kombination mit anderen Tumortherapien außer LHRH‑Analoga sind nicht nachgewiesen; ein erhöhtes Mortalitäts‑ und Frakturrisiko ist möglich. Die Kombination von Radium-223 mit anderen systemischen Tumortherapien außer LHRH-Analoga wird daher nicht empfohlen.
Es liegen nur begrenzt Daten dazu vor, wieviel Zeit nach einer Behandlung mit Abirateronacetat plus Prednison/Prednisolon vergehen muss, bevor Xofigo sicher angewendet werden kann bzw. umgekehrt. Ausgehend von den Halbwertszeiten von Xofigo und Abirateron wird empfohlen, eine nachfolgende Behandlung mit Xofigo frühestens 5 Tage nach der letzten Gabe von Abirateronacetat in Kombination mit Prednison/Prednisolon zu beginnen. Eine nachfolgende systemische Krebstherapie sollte frühestens 30 Tage nach der letzten Gabe von Xofigo eingeleitet werden.
Behandlung von Patienten mit asymptomatischen oder leicht symptomatischen Knochenmetastasen
Ein erhöhtes Sterbe‑ und Frakturrisiko wurde in einer klinischen Studie beobachtet, in der Xofigo zusätzlich zu Abirateronacetat plus Prednison/Prednisolon bei Patienten mit asymptomatischem oder leicht symptomatischem kastrationsresistentem Prostatakarzinom angewendet wurde.
Der Nutzen einer Therapie mit Xofigo bei Erwachsenen mit kastrationsresistentem Prostatakarzinom und nur asymptomatischen Knochenmetastasen wurde bisher nicht nachgewiesen. Die Anwendung von Xofigo bei Erwachsenen mit kastrationsresistentem Prostatakarzinom und nur asymptomatischen Knochenmetastasen wird daher nicht empfohlen. Bei Erwachsenen mit kastrationsresistentem Prostatakarzinom und leicht symptomatischen Knochenmetastasen ist der Therapienutzen sorgfältig gegen die Risiken abzuwägen, da wahrscheinlich eine hohe osteoblastische Aktivität erforderlich ist, um einen Therapienutzen zu erzielen (siehe Abschnitt 5.1).
Patienten mit einer geringen Anzahl von osteoblastischen Knochenmetastasen
In klinischen Studien zeigten Patienten mit weniger als 6 Knochenmetastasen ein erhöhtes Risiko für Knochenfrakturen und hatten keinen statistisch signifikanten Überlebensvorteil. Eine vorab geplante Subgruppenanalyse ergab außerdem, dass das Gesamtüberleben bei Patienten mit Gesamt‑ALP < 220 U/l nicht signifikant verbessert war. Deshalb wird die Behandlung mit Radium-223 bei Patienten mit einer geringen Menge an osteoblastischen Knochenmetastasen nicht empfohlen (siehe Abschnitt 5.1).
Knochenmarksuppression
Bei Patienten, die Xofigo erhielten, wurde von Knochenmarksuppression, insbesondere Thrombozytopenie, Neutropenie, Leukopenie und Panzytopenie berichtet (siehe Abschnitt 4.8).
Deshalb ist zu Behandlungsbeginn und vor jeder Dosisgabe von Xofigo eine hämatologische Untersuchung der Patienten durchzuführen. Vor der ersten Anwendung sollten die absolute Neutrophilenzahl ≥ 1,5 x 109/l, die Thrombozytenzahl ≥ 100 x 109/l und die Hämoglobinkonzentration ≥ 10,0 g/dl betragen. Vor den nachfolgenden Anwendungen sollten die absolute Neutrophilenzahl ≥ 1,0 x 109/l und die Thrombozytenzahl ≥ 50 x 109/l betragen. Im Falle, dass sich diese Werte trotz angemessener Behandlung entsprechend dem Therapiestandard nicht innerhalb von 6 Wochen nach der letzten Anwendung von Xofigo wieder erholen, darf die Behandlung mit Xofigo nur nach einer sorgfältigen Nutzen-Risiko-Abwägung fortgesetzt werden.
Patienten mit nachweislich eingeschränkter Knochenmarkreserve z. B. nach einer vorherigen zytotoxischen Chemotherapie und/oder externer Strahlentherapie (external beam radiation therapy, EBRT) oder Patienten mit Prostatakarzinom mit fortgeschrittener diffuser Infiltration des Knochens (extent of disease 4, EOD4; „Superscan“) sind mit Vorsicht zu behandeln. Bei diesen Patienten wurde während der Phase‑III‑Studie eine erhöhte Inzidenz hämatologischer Nebenwirkungen wie z. B. Neutropenie und Thrombozytopenie beobachtet (siehe Abschnitt 4.8).
Die Wirksamkeit und Sicherheit zytotoxischer Chemotherapien, die nach einer Behandlung mit Xofigo durchgeführt werden, sind nicht erwiesen. Die begrenzt verfügbaren Daten zeigen, dass Patienten, die eine Chemotherapie nach einer Behandlung mit Xofigo erhielten, ein ähnliches hämatologisches Profil aufwiesen wie Patienten, die eine Chemotherapie nach einer Behandlung mit Placebo erhielten (siehe auch Abschnitt 5.1).
Morbus Crohn und Colitis ulcerosa
Die Sicherheit und Wirksamkeit von Xofigo bei Patienten mit Morbus Crohn oder Colitis ulcerosa wurden nicht untersucht. Aufgrund der Ausscheidung von Xofigo über den Stuhl kann die radioaktive Strahlung zu einer Verschlimmerung akut entzündlicher Darmerkrankungen führen. Xofigo sollte bei Patienten mit akut entzündlichen Darmerkrankungen nur nach einer sorgfältigen Nutzen-Risiko-Bewertung angewendet werden.
Rückenmarkkompression
Bei Patienten mit unbehandelter drohender oder bestehender Rückenmarkkompression ist die Behandlung gemäß dem klinisch indizierten Therapiestandard abzuschließen, bevor die Behandlung mit Xofigo begonnen oder wieder aufgenommen wird.
Knochenfrakturen
Xofigo erhöht das Risiko für Knochenfrakturen. In einer klinischen Studie bewirkte die Gabe von Xofigo zusätzlich zu Abirateronacetat plus Prednison/Prednisolon einen Anstieg der Inzidenz von Frakturen im Xofigo-Arm um etwa das Dreifache (siehe Abschnitt 4.8 und 5.1). Ein erhöhtes Frakturrisiko wurde insbesondere bei Patienten mit vorbestehender Osteoporose sowie bei Patienten mit weniger als 6 Knochenmetastasen festgestellt. Xofigo akkumuliert vermutlich in Bereichen mit hohem Knochenumsatz, wie z. B. an Stellen einer degenerativen Knochenerkrankung (Osteoporose) oder kürzlich aufgetretener (Mikro-)Fraktur, und erhöht dadurch das Risiko für Knochenfrakturen. Weitere Faktoren wie z. B. die gleichzeitige Anwendung von Steroiden können das Frakturrisiko weiter erhöhen.
Vor Behandlungsbeginn mit Radium-223 sind der Knochenstatus (z. B. mittels Szintigraphie, Knochendichtemessung) sowie das Frakturrisiko des Patienten (z. B. Osteoporose, weniger als 6 Knochenmetastasen, das Frakturrisiko erhöhende Behandlung, niedriger Body-Mass-Index) sorgfältig zu untersuchen und für mindestens 24 Monate engmaschig zu beobachten. Präventive Maßnahmen wie die Anwendung von Bisphosphonaten oder Denosumab sind in Betracht zu ziehen, bevor eine Behandlung mit Xofigo begonnen oder wieder aufgenommen wird (siehe Abschnitt 4.8). Bei Patienten mit bereits hohem Frakturrisiko bei Behandlungsbeginn ist der Therapienutzen sorgfältig gegen das Risiko abzuwägen. Bei Patienten mit Knochenfrakturen müssen die Frakturen orthopädisch stabilisiert werden, bevor die Behandlung mit Xofigo begonnen oder wieder aufgenommen wird.
Osteonekrose des Kiefers
Bei Patienten, die mit Bisphosphonaten und Xofigo behandelt werden, kann ein erhöhtes Risiko für die Entwicklung einer Osteonekrose des Kiefers nicht ausgeschlossen werden. In der Phase‑III‑Studie wurden Fälle von Osteonekrose des Kiefers bei 0,67 % der Patienten (4/600) im Xofigo‑Arm verglichen mit 0,33 % der Patienten (1/301) im Placebo‑Arm berichtet. Allerdings waren alle Patienten mit Osteonekrose des Kiefers vorausgehend oder gleichzeitig mit Bisphosphonaten (z. B. Zoledronsäure) und vorheriger Chemotherapie (z. B. Docetaxel) behandelt worden.
Sekundäre maligne Neoplasien
Xofigo trägt zur langfristigen kumulativen Gesamtstrahlenexposition eines Patienten bei. Daher kann die langfristige kumulative Strahlenexposition mit einem erhöhten Risiko für Krebs und Erbgutdefekte verbunden sein. Insbesondere kann das Risiko für Osteosarkome, myelodysplastisches Syndrom und Leukämien erhöht sein. In klinischen Studien wurden bei Nachbeobachtungsphasen von bis zu 3 Jahren bisher keine Fälle einer Xofigo‑bedingten Krebserkrankung berichtet.
Gastrointestinale Toxizität
Xofigo erhöht die Inzidenz von Durchfall, Übelkeit und Erbrechen (siehe Abschnitt 4.8), dies kann zu Dehydrierung führen. Die orale Flüssigkeitsaufnahme sowie der Flüssigkeitsstatus der Patienten sollten sorgfältig überwacht werden. Patienten sollten darauf hingewiesen werden, ärztlichen Rat einzuholen, wenn bei ihnen schwerer oder anhaltender Durchfall, Übelkeit, Erbrechen auftreten.
Patienten, die Anzeichen oder Symptome einer Dehydrierung oder Hypovolämie aufzeigen, sollten unverzüglich behandelt werden.
Verhütung bei Männern
Aufgrund der potenziellen Auswirkungen von radioaktiver Strahlung auf die Spermatogenese sollten Männer angewiesen werden, während und bis zu 6 Monate nach der Behandlung mit Xofigo zuverlässige Verhütungsmethoden anzuwenden (siehe Abschnitt 4.6).
Sonstige Bestandteile
Je nach appliziertem Volumen enthält dieses Arzneimittel bis zu 54 mg (2,35 mmol) Natrium pro Dosis. Dies entspricht 2,7 % der von der WHO für einen Ewachsenen empfohlenen maximalen täglichen Natriumaufnahme mit der Nahrung von 2 g.
Es wurden keine klinischen Studien zur Erfassung von Wechselwirkungen durchgeführt.
Da Wechselwirkungen mit Calcium und Phosphat nicht ausgeschlossen werden können, sollte eine Unterbrechung einer zusätzlichen Zufuhr dieser Substanzen und/oder von Vitamin D einige Tage vor Beginn der Behandlung mit Xofigo in Erwägung gezogen werden.
Eine begleitende Chemotherapie zusammen mit Xofigo kann die Knochenmarksuppression verstärken (siehe Abschnitt 4.4). Die Sicherheit und Wirksamkeit einer begleitenden Chemotherapie zusammen mit Xofigo ist nicht erwiesen.
Verhütung bei Männern
Es wurden keine tierexperimentellen Studien zur Reproduktion mit Xofigo durchgeführt.
Aufgrund der potenziellen Auswirkungen von radioaktiver Strahlung auf die Spermatogenese sollten Männer angewiesen werden, während und bis zu 6 Monate nach der Behandlung mit Xofigo zuverlässige Verhütungsmethoden anzuwenden.
Schwangerschaft und Stillzeit
Xofigo ist bei Frauen nicht indiziert. Xofigo darf nicht bei Frauen angewendet werden, die schwanger sind oder sein könnten oder stillen.
Fertilität
Es liegen keine Daten über die Auswirkungen von Xofigo auf die menschliche Fertilität vor.
Gemäß tierexperimenteller Studien besteht ein potenzielles Risiko, dass die radioaktive Strahlung von Xofigo möglicherweise toxische Auswirkungen auf die männlichen Keimdrüsen und die Spermatogenese hat (siehe Abschnitt 5.3). Männliche Patienten sollten sich vor der Behandlung zur Konservierung von Spermien beraten lassen.
Xofigo hat keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Zusammenfassung des Sicherheitsprofils
Das Gesamtsicherheitsprofil von Xofigo beruht auf Daten von 600 Patienten, die in der Phase‑III‑Studie mit Xofigo behandelt wurden.
Die am häufigsten beobachteten Nebenwirkungen (≥ 10 %) bei mit Xofigo behandelten Patienten waren Diarrhö, Übelkeit, Erbrechen, Thrombozytopenie und Knochenfrakturen.
Die schwerwiegendsten Nebenwirkungen waren Thrombozytopenie und Neutropenie (siehe Abschnitt 4.4 und „Beschreibung ausgewählter Nebenwirkungen“ unten).
Tabellarische Auflistung der Nebenwirkungen
Die unter Xofigo beobachteten Nebenwirkungen sind in der nachstehenden Tabelle (siehe Tabelle 1) nach Systemorganklassen aufgeführt. Um eine bestimmte Reaktion und ihre Synonyme und damit verbundenen Erkrankungen zu beschreiben, wird der am besten geeignete MedDRA-Begriff verwendet.
Nebenwirkungen aus klinischen Studien sind nach ihrer Häufigkeit eingeteilt. Die Häufigkeiten sind wie folgt definiert: sehr häufig (≥1/10), häufig (≥1/100, <1/10), gelegentlich (≥1/1 000, <1/100), selten (≥1/10 000, <1/1 000), sehr selten (< 1/10 000).
Innerhalb jeder Häufigkeitsgruppe sind die Nebenwirkungen nach abnehmendem Schweregrad angeordnet.
Tabelle 1: Nebenwirkungen, die in klinischen Studien von mit Xofigo behandelten Patienten berichtet wurden
Systemorganklasse |
Sehr häufig |
Häufig |
Gelegentlich |
Erkrankungen des Blutes und des Lymphsystems |
Thrombozytopenie |
Neutropenie |
Lymphopenie |
Erkrankungen des Gastrointestinaltrakts |
Diarrhö |
||
Skelettmuskulatur‑, Bindegewebs‑ und Knochenerkrankungen |
Knochenfraktur |
Osteoporose |
|
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort |
Reaktionen an der Injektionsstelle |
Beschreibung ausgewählter Nebenwirkungen
Knochenfrakturen
Xofigo erhöht das Risiko für Knochenfrakturen (siehe Abschnitt 5.1). In klinischen Studien verringerte die gleichzeitige Gabe von Bisphosphonaten oder Denosumab die Inzidenz von Knochenfrakturen bei Patienten unter Radium-223-Monotherapie. Frakturen traten bis zu 24 Monate nach der ersten Dosis Radium-223 auf.
Thrombozytopenie und Neutropenie
Eine Thrombozytopenie (alle Grade) trat bei 11,5 % der mit Xofigo behandelten Patienten und 5,6 % der mit Placebo behandelten Patienten auf. Eine Thrombozytopenie Grad 3 oder 4 wurde bei 6,3 % der mit Xofigo behandelten Patienten und 2 % der mit Placebo behandelten Patienten beobachtet (siehe Abschnitt 4.4). Insgesamt war die Häufigkeit einer Thrombozytopenie Grad 3 oder 4 bei Patienten, die zuvor kein Docetaxel erhalten hatten (2,8 % der mit Xofigo behandelten Patienten verglichen mit 0,8 % der mit Placebo behandelten Patienten), geringer als bei Patienten, die zuvor Docetaxel erhalten hatten (8,9 % der mit Xofigo behandelten Patienten verglichen mit 2,9 % der mit Placebo behandelten Patienten). Bei Patienten mit EOD4 (extent of disease 4; „Superscan“) wurde eine Thrombozytopenie (alle Grade) bei 19,6 % der mit Xofigo behandelten Patienten und 6,7 % der mit Placebo behandelten Patienten berichtet. Eine Thrombozytopenie Grad 3 oder 4 wurde bei 5,9 % der mit Xofigo behandelten Patienten und 6,7 % der mit Placebo behandelten Patienten beobachtet (siehe Abschnitt 4.4).
Eine Neutropenie (alle Grade) wurde von 5 % der mit Xofigo behandelten Patienten und 1 % der mit Placebo behandelten Patienten berichtet. Eine Neutropenie Grad 3 oder 4 wurde bei 2,2 % der mit Xofigo behandelten Patienten und 0,7 % der mit Placebo behandelten Patienten beobachtet. Insgesamt war die Häufigkeit einer Neutropenie Grad 3 oder 4 bei Patienten, die zuvor kein Docetaxel erhalten hatten (0,8 % der mit Xofigo behandelten Patienten verglichen mit 0,8 % der mit Placebo behandelten Patienten), geringer als bei Patienten, die zuvor Docetaxel erhalten hatten (3,2 % der mit Xofigo behandelten Patienten verglichen mit 0,6 % der mit Placebo behandelten Patienten).
In einer Phase‑I‑Studie trat der Nadir der Neutrophilen‑ und Thrombozytenzahlen 2 bis 3 Wochen nach der intravenösen Applikation einer Einzeldosis Xofigo auf.
Reaktionen an der Injektionsstelle
Reaktionen an der Injektionsstelle der Grade 1 und 2 wie Erythem, Schmerzen und Schwellung wurden von 1,2 % der mit Xofigo behandelten Patienten und 0 % der mit Placebo behandelten Patienten berichtet.
Sekundäre maligne Neoplasien
Xofigo trägt zur langfristigen kumulativen Gesamtstrahlenexposition eines Patienten bei. Die langfristige kumulative Strahlenexposition kann mit einem erhöhten Risiko für Krebs und Erbgutdefekten verbunden sein. Insbesondere kann das Risiko für Osteosarkome, myelodysplastisches Syndrom und Leukämien erhöht sein. In klinischen Studien wurden bei Nachbeobachtungsphasen von bis zu 3 Jahren keine Fälle einer Xofigo‑bedingten Krebserkrankung berichtet.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen‑Risiko‑Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung über das Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger-Allee 3, D-53175 Bonn, Website: http://www.bfarm.de anzuzeigen.
Es liegen keine Meldungen über versehentliche Überdosierungen von Xofigo im Rahmen von klinischen Studien vor.
Es gibt kein spezifisches Antidot. Im Falle einer versehentlichen Überdosierung sollten allgemeine unterstützende Maßnahmen einschließlich der Überwachung auf mögliche hämatologische und gastrointestinale Toxizität eingeleitet werden.
In einer klinischen Phase‑I‑Studie wurden Einzeldosen Xofigo, die eine Aktivität von bis zu 276 kBq pro kg Körpergewicht enthielten, untersucht und dabei keine dosislimitierenden Toxizitäten beobachtet.
Pharmakotherapeutische Gruppe: Radiotherapeutika, andere Radiotherapeutika, verschiedene Radiotherapeutika, ATC‑Code: V10XX03
Wirkmechanismus
Xofigo ist ein therapeutisches, Alphateilchen emittierendes Arzneimittel.
Sein aktiver Bestandteil, Radium‑223 (als Radium‑223‑dichlorid), imitiert Calcium und wird selektiv im Knochen und hier insbesondere in Bereichen von Knochenmetastasen eingelagert, indem es Komplexe mit dem Knochenmineral Hydroxylapatit bildet. Der hohe lineare Energietransfer von Alphastrahlern (80 keV/µm) führt in den angrenzenden Tumorzellen zu einer hohen Häufigkeit von Doppelstrangbrüchen der DNA, wodurch ein wirksamer zytotoxischer Effekt erzielt wird. Zusätzliche Auswirkungen auf die Mikroumgebung des Tumors, Osteoblasten und Osteoklasten inbegriffen, tragen ebenfalls zur In-Vivo-Wirksamkeit bei. Die Reichweite der Alphateilchen von Radium‑223 beträgt weniger als 100 µm (weniger als 10 Zelldurchmesser), weshalb die Schädigung des umgebenden normalen Gewebes minimiert wird.
Pharmakodynamische Wirkungen
In einer randomisierten Phase‑II‑Studie gab es im Vergleich zu Placebo bei allen fünf untersuchten Serumbiomarkern für den Knochenumbau einen signifikanten Unterschied zugunsten von Xofigo (Knochenbildungsmarker: knochenspezifische alkalische Phosphatase [ALP], Gesamt‑ALP und Propeptid des Typ‑I‑Prokollagens [procollagen I N propeptide, PINP], Knochenresorptionsmarker: carboxyterminales quervernetzendes Telopeptid des Typ‑I‑Kollagens / Serum carboxyterminales quervernetzendes Telopeptid des Typ-I-Kollagens [S‑CTX‑I] und das quervernetzte Telopeptid des Typ‑I‑Kollagens [ICTP]).
Kardiale Elektrophysiologie / Verlängerung des QT‑Intervalls
Nach intravenöser Injektion von Xofigo wurden in einer Subgruppe von 29 Patienten der Phase‑III‑Studie (ALSYMPCA), im Vergleich zu Placebo, keine signifikanten Verlängerungen des QTc-Intervalls beobachtet.
Klinische Wirksamkeit und Sicherheit
Die klinische Sicherheit und Wirksamkeit von Xofigo wurden in einer doppelblinden, randomisierten, multizentrischen Phase‑III‑Studie mit Mehrfachapplikationen (ALSYMPCA; EudraCT 2007‑006195‑1) bei Patienten mit kastrationsresistentem Prostatakarzinom und symptomatischen Knochenmetastasen untersucht. Patienten mit viszeralen Metastasen und maligner Lymphadenopathie von mehr als 3 cm Größe waren ausgeschlossen.
Der primäre Wirksamkeitsendpunkt war das Gesamtüberleben. Die wichtigsten sekundären Endpunkte beinhalteten die Zeit bis zu symptomatischen skelettbezogenen Ereignissen (SSE), die Zeit bis zur Progression der Gesamt‑alkalischen Phosphatase (ALP), die Zeit bis zur Progression des Prostata‑spezifischen Antigens (PSA), das Ansprechen der Gesamt‑ALP und die Normalisierung der Gesamt‑ALP.
Am Stichtag der vorher geplanten Zwischenanalyse (konfirmatorische Analyse) waren insgesamt 809 Patienten randomisiert, im Verhältnis 2:1 eine Therapie mit Xofigo 55 kBq/kg intravenös alle 4 Wochen über 6 Zyklen (n = 541) plus bestmöglichem Therapiestandard oder einem entsprechenden Placebo plus bestmöglichem Therapiestandard (n = 268) zu erhalten. Der bestmögliche Therapiestandard umfasste z. B. eine lokale externe Strahlentherapie, Bisphosphonate, Corticosteroide, Antiandrogene, Östrogene, Estramustin oder Ketoconazol.
Bei 921 randomisierten Patienten wurde vor dem Crossover (d. h. dem Angebot an die Patienten in der Placebogruppe, auf Xofigo zu wechseln) eine aktualisierte deskriptive Analyse der Sicherheit und des Gesamtüberlebens durchgeführt.
Die demographischen Eigenschaften und die Krankheitsmerkmale zu Studienbeginn (Population der Zwischenanalyse) waren zwischen der Xofigo‑ und der Placebo‑Gruppe ähnlich und sind nachstehend für die Xofigo‑Gruppe angegeben:
das mittlere Alter der Patienten betrug 70 Jahre (Spanne 49 bis 90 Jahre).
87 % der aufgenommenen Patienten wiesen einen ECOG-Status des Allgemeinzustands (performance status, PS) von 0 ‑ 1 auf.
41 % erhielten Bisphosphonate.
42 % der Patienten hatten zuvor kein Docetaxel erhalten, weil sie hierfür ungeeignet waren oder eine Behandlung mit Docetaxel ablehnten.
46 % der Patienten hatten keine Schmerzen oder wurden auf der WHO‑Skala auf einen Wert von 1 (asymptomatisch oder leicht symptomatisch) eingestuft, und 54 % wiesen einen Wert auf der WHO‑Schmerzskala von 2 ‑ 3 auf.
16 % der Patienten hatten < 6 Knochenmetastasen, 44 % der Patienten wiesen zwischen 6 und 20 Knochenmetastasen auf und 40 % der Patienten hatten mehr als 20 Knochenmetastasen oder wiesen einen Superscan auf.
83 % der Patienten erhielten im Behandlungszeitraum gleichzeitig Agonisten des Luteinisierendes‑Hormon‑freisetzenden Hormons (luteinising hormone‑releasing hormone, LHRH) und 21 % der Patienten erhielten gleichzeitig Antiandrogene.
Die Ergebnisse sowohl der Zwischenanalyse als auch der aktualisierten Analyse ergaben, dass das Gesamtüberleben bei Patienten, die Xofigo plus den bestmöglichen Therapiestandard erhielten, im Vergleich zu Patienten, die Placebo plus den bestmöglichen Therapiestandard erhielten, signifikant verlängert war (siehe Tabelle 2 und Abbildung 2). Eine höhere Rate an Todesfällen, die nicht durch Prostatakrebs bedingt waren, wurde in der Placebo‑Gruppe beobachtet (26/541, 4,8 % der Patienten im Xofigo‑Arm verglichen mit 23/268, 8,6 % im Placebo‑Arm).
Tabelle 2: Überlebensergebnisse der Phase‑III‑Studie ALSYMPCA
Xofigo |
Placebo |
|
Zwischenanalyse |
N = 541 |
N = 268 |
Anzahl (%) Todesfälle |
191 (35,3 %) |
123 (45,9 %) |
Medianes Gesamtüberleben (Monate) (95 %‑KI) |
14,0 (12,1 – 15,8) |
11,2 (9,0 – 13,2) |
Hazard Ratiob (95 %‑KI) |
0,695 (0,552 – 0,875) |
|
p‑Werta (2‑seitig) |
0,00185 |
|
Aktualisierte Analyse |
N = 614 |
N = 307 |
Anzahl (%) Todesfälle |
333 (54,2 %) |
195 (63,5 %) |
Medianes Gesamtüberleben (Monate) (95 %‑KI) |
14,9 (13,9 – 16,1) |
11,3 (10,4 – 12,8) |
Hazard Ratiob (95 %‑KI) |
0,695 (0,581 – 0,832) |
|
KI = Konfidenzintervall
a Die Phase‑3‑Studie ALSYMPCA wurde aufgrund erwiesener Wirksamkeit nach der Zwischenanalyse beendet. Da die aktualisierte Analyse nur zu deskriptiven Zwecken dargestellt ist, wird hier kein p‑Wert angegeben.
b Hazard Ratio (Xofigo über Placebo) < 1 favorisiert Xofigo.
Abbildung 2: Gesamtüberlebenskurven nach Kaplan‑Meier (aktualisierte Analyse)
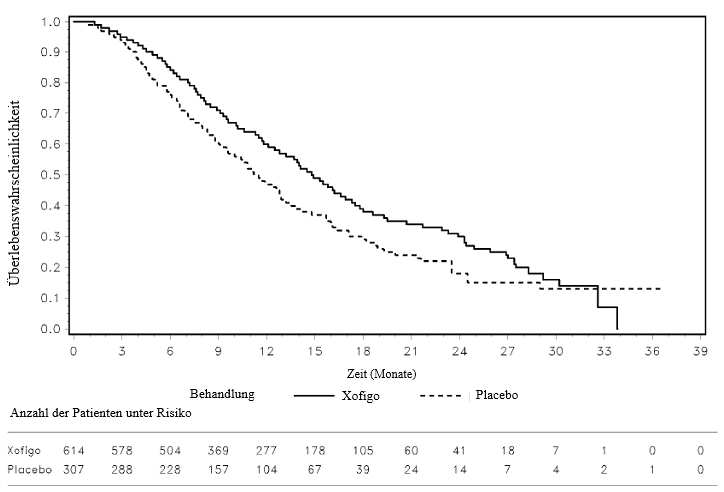
Die Ergebnisse der Zwischenanalyse und der aktualisierten Analyse zeigten im Xofigo‑Arm außerdem bei allen wesentlichen sekundären Endpunkten eine signifikante Verbesserung gegenüber dem Placebo‑Arm (siehe Tabelle 3). Die Daten für die Zeit bis zum Ereignis in Bezug auf die ALP‑Progression wurden durch den statistisch signifikanten Vorteil in Bezug auf die ALP‑Normalisierung und das ALP‑Ansprechen in Woche 12 unterstützt.
Tabelle 3: Sekundäre Wirksamkeitsendpunkte der Phase‑III-Studie ALSYMPCA (Interimsanalyse)
Inzidenz |
Analyse der Zeit bis zum Ereignis (95%‑KI) |
|||||||
[Anz. (%) der Patienten] |
[mediane Anz. d. Monate] |
Hazard |
p-Wert |
|||||
Xofigo |
Placebo |
Xofigo |
Placebo |
|||||
Symptomatisches skelettbezogenes Ereignis (SSE) |
zusammengesetzter SSE‑Endpunkt a |
132 |
82 |
13,5 |
8,4 |
0,610 |
0,00046 |
|
SSE Komponenten |
Externe Bestrahlung zur Schmerzlinderung |
122 |
72 |
17,0 |
10,8 |
0,649 |
0,00375 |
|
Rückenmarkkompression |
17 |
16 |
NE |
NE |
0,443 |
0,01647 |
||
Chirurgischer Eingriff |
9 |
5 |
NE |
NE |
0,801 |
0,69041 |
||
Knochenfrakturen |
20 |
18 |
NE |
NE |
0,450 |
0,01255 |
||
Gesamt‑ALP‑Progression c |
79 |
116 |
NE |
3,7 |
0,162 |
< 0,00001 |
||
PSA‑Progression d |
288 |
141 |
3,6 |
3,4 |
0,671 |
0,00015 |
||
ALP = alkalische Phosphatase; KI = Konfidenzintervall; NE = nicht ermittelbar; PSA = Prostata‑spezifisches Antigen; SSE = symptomatisches skelettbezogenes Ereignis
a Definiert als Auftreten eines der Folgenden: externe Bestrahlung zur Schmerzlinderung oder pathologische Fraktur oder Rückenmarkkompression oder tumorbedingter orthopädischer chirurgischer Eingriff.
b Aufgrund von fehlenden Ereignissen nach dem Median nicht ermittelbar.
c Definiert als ≥ 25 %iger Anstieg im Vergleich zum Ausgangswert/Nadir.
d Definiert als ≥ 25 %iger Anstieg und Anstieg der absoluten Werte um ≥ 2 ng/ml im Vergleich zum Ausgangswert/Nadir.
Überlebensanalyse nach Untergruppen
Die Überlebensanalyse der Untergruppen zeigte unabhängig von der Anwendung von Bisphosphonaten zu Studienbeginn oder der vorherigen Anwendung von Docetaxel einen gleichmäßigen Überlebensvorteil für die Behandlung mit Xofigo.
In der Phase‑III‑Studie ALSYMPCA konnte in der Untergruppe der Patienten mit weniger als 6 Knochenmetastasen (Hazard Ratio [HR] für Radium-223 gegenüber Placebo: 0,901; 95%-KI [0,553 – 1,466]; p = 0,674) oder der Patienten, deren Gesamt‑alkalische Phosphatase (ALP) vor Behandlungsbeginn < 220 U/l war (HR: 0,823; 95 %-KI [0,633 – 1,068]; p = 0,142) kein statistisch signifikanter Therapienutzen beim Gesamtüberleben nachgewiesen werden. Bei Patienten mit geringem Maß an osteoblastischer Aktivität ihrer Knochenmetastasen könnte daher die Wirksamkeit reduziert sein.
Lebensqualität
Die gesundheitsbezogene Lebensqualität wurde in der Phase‑III‑Studie ALSYMPCA mit spezifischen Fragebögen beurteilt: dem EQ‑5D (generisches Instrument) und dem FACT‑P (für das Prostatakarzinom spezifisches Instrument). Beide Gruppen erleiden einen Verlust an Lebensqualität. Verglichen mit Placebo war die Abnahme der Lebensqualität für Xofigo in dem Behandlungszeitraum langsamer gemäß dem EQ‑5D‑Nutzen‑Indexwert (‑0,040 versus ‑0,109; p = 0,001), dem selbst-berichteten EQ‑5D‑Visual‑Analogue‑Health‑Status (VAS) (‑2,661 versus ‑5,860; p = 0,018) und dem FACT‑P‑Gesamtwert (‑3,880 versus ‑7,651; p = 0,006). Die aus Publikationen bekannten minimal bedeutsamen Unterschiede wurden jedoch nicht erreicht. Es gibt limitierte Evidenz dafür, dass die Verzögerung im Verlust der gesundheitsbezogenen Lebensqualität über den Behandlungszeitraum hinaus verlängert wird.
Schmerzlinderung
Die Ergebnisse der Phase‑III‑Studie ALSYMPCA bezüglich der Zeit bis zur externen Strahlentherapie zur Schmerzlinderung und die geringere Anzahl an Patienten, die in der Xofigo‑Gruppe von Knochenschmerzen als Nebenwirkung berichteten, weisen auf einen positiven Effekt auf Knochenschmerzen hin.
Anschließende Behandlung mit zytotoxischen Substanzen
Im Rahmen der im Verhältnis 2:1 randomisierten Studie ALSYMPCA erhielten 93 (15,5 %) der Patienten in der Xofigo‑Gruppe und 54 (17,9 %) der Patienten in der Placebo‑Gruppe zu verschiedenen Zeitpunkten nach der letzten Behandlung eine zytotoxische Chemotherapie. Zwischen den beiden Gruppen waren keine Unterschiede im Hinblick auf die hämatologischen Laborwerte zu erkennen.
Kombination mit Abirateron und Prednison/Prednisolon
Die klinische Wirksamkeit und Sicherheit des gleichzeitigen Beginns der Behandlung mit Xofigo, Abirateronacetat und Prednison/Prednisolon wurden in einer randomisierten, placebokontrollierten multizentrischen Phase‑III‑Studie (ERA-223 Studie) bei 806 Chemotherapie-naiven Patienten mit asymptomatischem oder leicht symptomatischem kastrationsresistentem Prostatakarzinom mit Knochenmetastasen bewertet. Die Studie wurde basierend auf einer Empfehlung eines unabhängigen Gremiums zur Datenüberwachung vorzeitig entblindet. Eine Zwischenanalyse zeigte eine erhöhte Inzidenz von Frakturen (28,6 % vs. 11,4 %) und reduziertes medianes Gesamtüberleben (30,7 Monate versus 33,3 Monate, HR 1,195; 95 %-KI [0,950 – 1,505], p = 0,13) bei Patienten, die Xofigo in Kombination mit Abirateronacetat und Prednison/Prednisolon erhielten, im Vergleich zu Patienten, die Placebo in Kombination mit Abirateronacetat und Prednison/Prednisolon erhielten.
Kinder und Jugendliche
Die Europäische Arzneimittel‑Agentur hat für Xofigo eine Freistellung von der Verpflichtung zur Vorlage von Ergebnissen zu Studien in allen pädiatrischen Altersklassen zur Behandlung aller unter die Kategorie Maligne Neoplasien fallenden Erkrankungen (außer Tumoren des Zentralnervensystems, Neoplasien des blutbildenden und lymphatischen Gewebes) und zur Behandlung des Multiplen Myeloms gewährt (siehe Abschnitt 4.2 bzgl. Informationen zur Anwendung bei Kindern und Jugendlichen).
Allgemeine Einführung
Die Daten der Pharmakokinetik, Biodistribution und Dosimetrie stammen aus drei Phase‑I‑Studien. Die pharmakokinetischen Daten wurden von 25 Patienten gewonnen, die eine Aktivität zwischen 51 und 276 kBq/kg erhalten hatten. Die Daten der Pharmakokinetik, Biodistribution und Dosimetrie stammen von 6 Patienten, die in einem Abstand von 6 Wochen zweimal eine Aktivität von 110 kBq/kg erhalten hatten, sowie von 10 Patienten, die eine Aktivität von 55, 110 oder 221 kBq/kg erhalten hatten.
Resorption
Xofigo wird als intravenöse Injektion appliziert und ist demnach zu 100 % bioverfügbar.
Verteilung und Organaufnahme
Nach intravenöser Injektion wird Radium‑223 rasch aus dem Blut entfernt und vorwiegend in Knochen und Knochenmetastasen eingelagert oder in den Darm ausgeschieden.
Fünfzehn Minuten nach der Injektion verblieben ungefähr 20 % der injizierten Aktivität im Blut. Nach 4 Stunden verblieben ungefähr 4 % der injizierten Aktivität im Blut, ein Wert, der 24 Stunden nach der Injektion auf weniger als 1 % gesunken war. Das Verteilungsvolumen war größer als das Blutvolumen, was auf eine Verteilung in periphere Körpergewebe hinweist.
Zehn Minuten nach der Injektion wurde im Knochen und im Darm Aktivität beobachtet. 4 Stunden nach der Injektion betrug der mittlere prozentuale Anteil der in Knochen und Darm vorhandenen radioaktiven Dosis ungefähr 61 % beziehungsweise 49 %.
In anderen Organen wie Herz, Leber, Nieren, Harnblase und Milz wurde 4 Stunden nach der Injektion keine signifikante Aufnahme festgestellt.
Biotransformation
Radium‑223 ist ein zerfallendes Isotop und wird nicht metabolisiert.
Elimination
Die Ausscheidung aus dem Körper erfolgt überwiegend mit dem Stuhl. Ungefähr 5 % wird über den Harn ausgeschieden, und es gibt keine Hinweise für eine hepatobiliäre Ausscheidung.
Gesamtkörpermessungen 7 Tage nach der Injektion (nach Korrektur für den Zerfall) deuten darauf hin, dass im Median 76 % der angewendeten Aktivität aus dem Körper ausgeschieden wurde. Die Eliminationsrate von Radium‑223‑dichlorid aus dem Gastrointestinaltrakt wird durch stark unterschiedliche Darmpassagen in der Bevölkerung beeinflusst, wobei der normale Bereich von einer einmal täglichen bis einmal wöchentlichen Darmentleerung reicht.
Linearität/Nicht‑Linearität
Die Pharmakokinetik von Radium‑223‑dichlorid war im untersuchten Aktivitätsbereich (51 bis 276 kBq/kg) linear.
Kinder und Jugendliche
Die Sicherheit und Wirksamkeit von Xofigo bei Kindern und Jugendlichen im Alter unter 18 Jahren wurden nicht untersucht.
Systemische Toxizität
In Studien zur Toxizität bei einmaliger und wiederholter Gabe an Ratten waren die Hauptbefunde eine verminderte Gewichtszunahme, hämatologische Veränderungen, verminderte Serumspiegel der alkalischen Phosphatase und mikroskopische Befunde in Knochenmark (Depletion hämatopoetischer Zellen, Fibrose), Milz (sekundäre extramedulläre Hämatopoese) und Knochen (Depletion der Osteozyten, Osteoblasten, Osteoklasten, fibro‑ossäre Läsionen, Bruch/Desorganisation der Epiphysenfuge/Wachstumslinie). Diese Befunde waren mit einer strahlenbedingten Beeinträchtigung der Hämatopoese und einer verminderten Osteogenese verbunden und traten ab der niedrigsten Aktivität von 22 kBq pro kg Körpergewicht auf (dem 0,4‑fachen der klinisch empfohlenen Dosis).
In Hunden wurden hämatologische Veränderungen ab der niedrigsten Aktivität von 55 kBq/kg, d. h. der klinisch empfohlenen Dosis, beobachtet. Bei Hunden wurde nach Einzelgabe von 497 kBq Radium‑223‑dichlorid pro kg Körpergewicht (dem 9‑fachen der klinisch empfohlenen Aktivität) eine dosislimitierende Myelotoxizität festgestellt.
Nach der wiederholten Applikation der klinisch empfohlenen Aktivität von 55 kBq/kg einmal alle 4 Wochen für 6 Monate entwickelten zwei Hunde nicht verschobene Beckenfrakturen. Aufgrund des Vorkommens der Osteolyse trabekulärer Knochen in anderen Knochenregionen behandelter Tiere in unterschiedlichem Ausmaß, kann eine Spontanfraktur im Rahmen der Osteolyse nicht ausgeschlossen werden. Die klinische Bedeutung dieser Befunde ist unbekannt.
Bei Hunden wurde nach einer Einzelgabe von Aktivitäten von 166 und 497 kBq pro kg Körpergewicht (dem 3‑ bzw. 9‑fachen der klinisch empfohlenen Dosis) eine Netzhautablösung beobachtet, nicht aber nach der wiederholten Applikation der klinisch empfohlenen Aktivität von 55 kBq pro kg Körpergewicht einmal alle 4 Wochen für 6 Monate. Der genaue Mechanismus, der zur Netzhautablösung führt, ist nicht bekannt, Daten aus der Literatur lassen jedoch vermuten, dass Radium spezifisch vom Tapetum lucidum des Hundeauges aufgenommen wird. Da Menschen kein Tapetum lucidum haben, ist die klinische Bedeutung dieser Befunde für den Menschen ungeklärt. In klinischen Studien wurden keine Fälle von Netzhautablösung gemeldet.
In Organen, die an der Ausscheidung von Radium‑223‑dichlorid beteiligt sind, wurden keine histologischen Veränderungen beobachtet.
Osteosarkome, eine bekannte Wirkung knochenaffiner Radionuklide, wurden bei Ratten bei klinisch relevanten Dosen 7 ‑ 12 Monate nach Beginn der Behandlung beobachtet. Osteosarkome wurden bei Studien an Hunden nicht beobachtet. In klinischen Studien mit Xofigo wurden keine Fälle von Osteosarkomen gemeldet. Das Risiko für Patienten, bei Exposition gegenüber Radium‑223 ein Osteosarkom auszubilden, ist derzeit nicht bekannt. Von den längerfristigen (12 ‑ 15 Monate) Toxizitätsstudien an Ratten wurde auch das Auftreten anderer neoplastischer Veränderungen als Osteosarkome berichtet (siehe Abschnitt 4.8).
Embryotoxizität/Reproduktionstoxizität
Studien zur Reproduktions‑ und Entwicklungstoxizität wurden nicht durchgeführt. Im Allgemeinen induzieren Radionuklide Reproduktions‑ und Entwicklungsschäden.
In einigen Samenkanälchen von Hoden männlicher Ratten wurde nach einmaliger Gabe von ≥ 2270 kBq/kg Körpergewicht Radium‑223‑dichlorid (dem ≥ 41‑fachen der klinisch empfohlenen Aktivität) eine geringfügige Anzahl abnormer Spermatozyten festgestellt. Ansonsten schienen die Hoden normal zu funktionieren und die Nebenhoden zeigten einen normalen Gehalt an Spermatozyten. In weiblichen Ratten wurden nach einzelner oder wiederholter Gabe von ≥ 359 kBq/kg Körpergewicht Radium‑223‑dichlorid (dem ≥ 6,5‑fachen der klinisch empfohlenen Aktivität) Uteruspolypen (Endometriumstroma) beobachtet.
Da Radium‑223 hauptsächlich im Knochen angereichert wird, ist das potenzielle Risiko für toxische Auswirkungen auf die männlichen Keimdrüsen von Krebspatienten mit kastrationsresistentem Prostatakarzinom sehr gering, kann jedoch nicht ausgeschlossen werden (siehe Abschnitt 4.6).
Genotoxizität/Karzinogenität
Studien zum mutagenen und karzinogenen Potential von Xofigo wurden nicht durchgeführt. Im Allgemeinen werden Radionuklide als genotoxisch und karzinogen eingestuft.
Sicherheitspharmakologie
Nach Einzelgabe von Aktivitäten von 497 bis 1100 kBq pro kg Körpergewicht (dem 9‑ [Hund] bis 20‑ [Ratte] fachen der klinisch empfohlenen Aktivität) wurden keine signifikanten Wirkungen auf lebenswichtige Organsysteme, d. h. das kardiovaskuläre (Hund), respiratorische oder zentrale Nervensystem (Ratte), beobachtet.
Wasser für Injektionszwecke
Natriumcitrat
Natriumchlorid
Salzsäure 10 %
Da keine Kompatibilitätsstudien durchgeführt wurden, darf dieses Arzneimittel nicht mit anderen Arzneimitteln gemischt werden.
28 Tage
Für dieses Arzneimittel sind bezüglich der Temperatur keine besonderen Lagerungsbedingungen erforderlich.
Die Lagerung von radioaktiven Arzneimitteln muss den nationalen Bestimmungen für radioaktive Substanzen entsprechen.
Farblose Durchstechflasche aus Typ‑I‑Glas, verschlossen mit einem grauen Brombutylgummistopfen, entweder mit oder ohne Folienbeschichtung aus Ethylen-Tetrafluorethylen (ETFE), jeweils mit einer Bördelkappe aus Aluminium versehen; sie enthält 6 ml Injektionslösung.
Die Durchstechflasche ist in einem Bleibehälter verpackt.
Allgemeine Warnhinweise
Radioaktive Arzneimittel dürfen nur von autorisierten Personen in dafür vorgesehenen klinischen Bereichen entgegengenommen, gehandhabt und angewendet werden. Der Empfang, die Lagerung, Anwendung, Transfer und Entsorgung unterliegen den strahlenschutzrechtlichen Bestimmungen und der Aufsicht der örtlich zuständigen Aufsichtsbehörde und/oder entsprechenden Genehmigungen durch die zuständige Aufsichtsbehörde.
Radioaktive Arzneimittel müssen unter Vorkehrungen zum Schutz vor ionisierenden Strahlen und unter Beachtung pharmazeutischer Qualitätsanforderungen gehandhabt werden. Es sind geeignete aseptische Vorsichtsmaßnahmen zu treffen.
Strahlenschutz
Die mit dem Zerfall von Radium‑223 und dessen Tochternukliden verbundene Gammastrahlung ermöglicht die Radioaktivitätsmessung von Xofigo und den Nachweis von Kontaminationen mit herkömmlichen Instrumenten.
Die Anwendung von radioaktiven Arzneimitteln stellt einen Risikofaktor für Andere aufgrund der vom Patienten ausgehenden Strahlung bzw. durch Kontamination durch Verschütten von Urin, durch Stuhl, Erbrochenes usw. dar. Daher sind die den nationalen Strahlenschutzverordnungen entsprechenden Vorsichtsmaßnahmen zu treffen. Beim Umgang mit Materialien wie z. B. Bettwäsche, die mit solchen Körperflüssigkeiten in Kontakt kommen können, ist Sorgfalt notwendig. Obwohl Radium‑223 in erster Linie ein Alphastrahler ist, tritt beim Zerfall von Radium‑223 und dessen radioaktiven Tochternukliden Gamma‑ und Betastrahlung auf. Die im Zusammenhang mit der Handhabung der Patientendosen verbundene externe Strahlenexposition ist im Vergleich zu anderen radioaktiven Arzneimitteln für therapeutische Zwecke deutlich geringer, da die angewendete Radioaktivität normalerweise weniger als 8 MBq beträgt. Gemäß dem ALARA‑Prinzip („As Low As Reasonably Achievable“, d. h. so wenig wie vernünftigerweise erreichbar) wird zur Minimierung der Strahlenexposition empfohlen, die in Bereichen mit radioaktiver Strahlung verbrachte Zeit zu minimieren, den Abstand zu Strahlungsquellen zu maximieren und eine angemessene Abschirmung zu verwenden.
Nicht verwendetes radioaktives Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu beseitigen. Alle in Verbindung mit der Zubereitung oder Anwendung von Xofigo verwendete Materialien müssen als radioaktiver Abfall behandelt werden.
Bayer AG
51368 Leverkusen
Deutschland
EU/1/13/873/001
Datum der Erteilung der Zulassung: 13. November 2013
Datum der letzten Verlängerung der Zulassung: 15. September 2023
September 2023
Die Berechnung der absorbierten Strahlendosis wurde auf der Basis der klinischen Biodistributionsdaten durchgeführt. Die Berechnungen der absorbierten Dosen erfolgten mit OLINDA/EXM (Organ Level INternal Dose Assessment/EXponential Modeling), einem Softwareprogramm auf Grundlage des Medical‑Internal‑Radiation‑Dose(MIRD)‑Algorithmus, der für herkömmliche Beta‑ und Gammastrahlen emittierende Radionuklide weit verbreitet ist. Da Radium‑223 in erster Linie ein Alphastrahler ist, wurden zusätzliche Annahmen für den Darm, das rote Knochenmark und Knochen-/osteogene Zellen gemacht, um die bestmöglichen Berechnungen der absorbierten Dosen von Xofigo unter Berücksichtigung der beobachteten Biodistributionsmerkmale und anderer spezifischer Eigenschaften zu erstellen (siehe Tabelle 4).
Tabelle 4: Berechnete in den Organen absorbierte Strahlendosis
Zielorgan |
Alpha‑ |
Beta‑ |
Gamma‑ |
Gesamtdosis (Gy/MBq) |
Variationskoeffizient |
Nebennieren |
0,00000 |
0,00002 |
0,00009 |
0,00012 |
56 |
Gehirn |
0,00000 |
0,00002 |
0,00008 |
0,00010 |
80 |
Brüste |
0,00000 |
0,00002 |
0,00003 |
0,00005 |
120 |
Gallenblasenwand |
0,00000 |
0,00002 |
0,00021 |
0,00023 |
14 |
Wand des UDD2 |
0,00000 |
0,04561 |
0,00085 |
0,04645 |
83 |
Dünndarmwand |
0,00319 |
0,00360 |
0,00047 |
0,00726 |
45 |
Magenwand |
0,00000 |
0,00002 |
0,00011 |
0,00014 |
22 |
Wand des ODD3 |
0,00000 |
0,03149 |
0,00082 |
0,03232 |
50 |
Herzwand |
0,00161 |
0,00007 |
0,00005 |
0,00173 |
42 |
Nieren |
0,00299 |
0,00011 |
0,00011 |
0,00321 |
36 |
Leber |
0,00279 |
0,00010 |
0,00008 |
0,00298 |
36 |
Lungen |
0,00109 |
0,00007 |
0,00005 |
0,00121 |
--4 |
Muskulatur |
0,00000 |
0,00002 |
0,00010 |
0,00012 |
41 |
Ovarien |
0,00000 |
0,00002 |
0,00046 |
0,00049 |
40 |
Pankreas |
0,00000 |
0,00002 |
0,00009 |
0,00011 |
43 |
Rotes Knochenmark |
0,13217 |
0,00642 |
0,00020 |
0,13879 |
41 |
Osteogene Zellen |
1,13689 |
0,01487 |
0,00030 |
1,15206 |
41 |
Haut |
0,00000 |
0,00002 |
0,00005 |
0,00007 |
79 |
Milz |
0,00000 |
0,00002 |
0,00007 |
0,00009 |
54 |
Hoden |
0,00000 |
0,00002 |
0,00006 |
0,00008 |
59 |
Thymus |
0,00000 |
0,00002 |
0,00003 |
0,00006 |
109 |
Schilddrüse |
0,00000 |
0,00002 |
0,00005 |
0,00007 |
96 |
Harnblasenwand |
0,00371 |
0,00016 |
0,00016 |
0,00403 |
63 |
Uterus |
0,00000 |
0,00002 |
0,00023 |
0,00026 |
28 |
Gesamtkörper |
0,02220 |
0,00081 |
0,00012 |
0,02312 |
16 |
1 Da in den meisten Weichgeweben keine Aufnahme von Radium‑223 zu beobachten war, wurde der Alphastrahlenanteil an der Gesamtorgandosis bei diesen Organen auf Null gesetzt.
2 UDD: unterer Dickdarm
3 ODD: oberer Dickdarm
4 Die Angaben zur absorbierten Dosis in der Lunge basieren auf einer Modell‑unterstützten Berechnung unter Verwendung der von allen Testpersonen erhobenen gepoolten Daten der im Blut über die Zeit gemessenen Aktivität.
Die in klinischen Studien mit Xofigo beobachteten hämatologischen Nebenwirkungen sind viel seltener und von deutlich geringerem Schweregrad als nach den berechneten im roten Knochenmark absorbierten Dosen zu erwarten wäre. Dies könnte mit der räumlichen Verteilung der Alphastrahlung zusammenhängen, die im roten Knochenmark zu einer ungleichmäßigen Strahlendosis führt.
Dieses Arzneimittel muss vor Gebrauch einer Sichtprüfung unterzogen werden. Xofigo ist eine klare, farblose Lösung und darf bei Verfärbung, Anwesenheit von Schwebstoffen oder einem defekten Behältnis nicht verwendet werden.
Xofigo ist eine gebrauchsfertige Lösung und darf nicht verdünnt oder mit anderen Lösungen gemischt werden.
Jede Durchstechflasche ist nur zur einmaligen Anwendung bestimmt.
Das einem bestimmten Patienten zu applizierende Volumen wird mit folgenden Werten berechnet:
Körpergewicht des Patienten (kg)
Dosierung (55 kBq/kg Körpergewicht)
Konzentration der Radioaktivität des radioaktiven Arzneimittels (1100 kBq/ml) am Referenzdatum. Das Referenzdatum ist auf der Durchstechflasche und dem Etikett des Bleibehälters angegeben.
Zerfallskorrekturfaktor (ZK‑Faktor), um den physischen Zerfall des Radium‑223 zu berücksichtigen. Eine Tabelle mit Zerfallskorrekturfaktoren ist jeder Durchstechflasche als Teil der Broschüre (vor der Packungsbeilage) beigefügt.
Die Radioaktivitätsmenge im dispensierten Volumen ist durch Messung in einem ordnungsgemäß kalibrierten Aktivimeter zu bestätigen.
Das gesamte einem Patienten zu applizierende Volumen wird wie folgt berechnet:
Zu verabreichendes Volumen (ml) |
= |
Körpergewicht (kg) × Aktivität (55 kBq/kg Körpergewicht) |
ZK‑Faktor × 1100 kBq/ml |
Nicht verwendetes radioaktives Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu beseitigen.
Ausführliche Informationen zu diesem radioaktiven Arzneimittel sind auf den Internetseiten der Europäischen Arzneimittel‑Agentur http://www.ema.europa.eu verfügbar.
Verschreibungspflichtig
Bayer Vital GmbH
51368 Leverkusen
Tel.: +49 (0)214-30 513 48
Fax: +49 (0)214-2605 516 03
E-Mail: medical-information@bayer.com
DE/11