Olumiant® 1 mg Filmtabletten
Olumiant® 2 mg Filmtabletten
Olumiant® 4 mg Filmtabletten
Olumiant® 1 mg Filmtabletten
Jede Filmtablette enthält 1 mg Baricitinib.
Olumiant® 2 mg Filmtabletten
Jede Filmtablette enthält 2 mg Baricitinib.
Olumiant® 4 mg Filmtabletten
Jede Filmtablette enthält 4 mg Baricitinib.
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
Filmtablette (Tablette)
Olumiant® 1 mg Filmtabletten
Blassrosa, runde Tabletten, Durchmesser 6,75 mm, mit der Prägung „Lilly” auf der einen und „1” auf der anderen Seite.
Olumiant® 2 mg Filmtabletten
Hellrosa, längliche Tabletten, 9 x 7,5 mm, mit der Prägung „Lilly” auf der einen und „2” auf der anderen Seite.
Olumiant® 4 mg Filmtabletten
Rosa, runde Tabletten, Durchmesser 8,5 mm, mit der Prägung „Lilly” auf der einen und „4” auf der anderen Seite.
Die Tabletten haben auf beiden Seiten eine Vertiefung.
Rheumatoide Arthritis
Baricitinib wird angewendet zur Behandlung von mittelschwerer bis schwerer aktiver rheumatoider Arthritis bei erwachsenen Patienten, die auf eine vorangegangene Behandlung mit einem oder mehreren krankheitsmodifizierenden Antirheumatika (DMARDs) unzureichend angesprochen oder diese nicht vertragen haben. Baricitinib kann als Monotherapie oder in Kombination mit Methotrexat angewendet werden (siehe Abschnitte 4.4, 4.5 und 5.1 zu verfügbaren Daten verschiedener Kombinationen).
Atopische Dermatitis
Baricitinib wird angewendet zur Behandlung von mittelschwerer bis schwerer atopischer Dermatitis bei erwachsenen und pädiatrischen Patienten ab 2 Jahren, die für eine systemische Therapie infrage kommen.
Alopecia areata
Baricitinib wird angewendet zur Behandlung von schwerer Alopecia areata bei erwachsenen und jugendlichen Patienten ab 12 Jahren (siehe Abschnitt 5.1).
Juvenile idiopathische Arthritis
Baricitinib wird angewendet zur Behandlung der aktiven juvenilen idiopathischen Arthritis bei Patienten ab 2 Jahren, die zuvor unzureichend auf eines oder mehrere herkömmlich synthetische oder biologische DMARDs angesprochen oder diese nicht vertragen haben:
̶ |
Polyartikuläre juvenile idiopathische Arthritis (polyartikulärer Rheumafaktor positiv [RF+] oder negativ [RF-], erweitert oligoartikulär), |
̶ |
Enthesitis-assoziierte Arthritis, und |
̶ |
Juvenile Psoriasis-Arthritis. |
Baricitinib kann als Monotherapie oder in Kombination mit Methotrexat angewendet werden.
Die Therapie sollte durch einen Arzt begonnen werden, der in der Diagnose und Behandlung von Erkrankungen, für die dieses Arzneimittel angezeigt ist, Erfahrung hat.
Dosierung
Rheumatoide Arthritis
Die empfohlene Dosis für Baricitinib beträgt 4 mg einmal täglich. Für Patienten mit erhöhtem Risiko für venöse Thromboembolien (VTE), schwerwiegende unerwünschte kardiovaskuläre Ereignisse (MACE) und maligne Erkrankungen, sowie für Patienten ab 65 Jahren und für Patienten mit chronischen bzw. wiederkehrenden Infekten in der Vorgeschichte beträgt die empfohlene Dosis 2 mg einmal täglich (siehe Abschnitt 4.4). Für Patienten, die mit 2 mg einmal täglich keine anhaltende Kontrolle über die Krankheitsaktivität erreichen, kann eine Dosis von 4 mg einmal täglich in Betracht gezogen werden. Für Patienten, die mit 4 mg täglich eine anhaltende Kontrolle über die Krankheitsaktivität erreicht haben und die für eine Dosisreduktion infrage kommen, sollte eine Dosierung von 2 mg täglich in Betracht gezogen werden (siehe Abschnitt 5.1).
Atopische Dermatitis
Erwachsene
Die empfohlene Dosis für Baricitinib beträgt 4 mg einmal täglich. Für Patienten mit erhöhtem Risiko für VTE, MACE und maligne Erkrankungen, sowie für Patienten ab 65 Jahren und für Patienten mit chronischen bzw. wiederkehrenden Infekten in der Vorgeschichte beträgt die empfohlene Dosis 2 mg einmal täglich (siehe Abschnitt 4.4). Für Patienten, die mit 2 mg einmal täglich keine anhaltende Kontrolle über die Krankheitsaktivität erreichen, kann eine Dosis von 4 mg einmal täglich in Betracht gezogen werden. Für Patienten, die mit 4 mg täglich eine anhaltende Kontrolle über die Krankheitsaktivität erreicht haben und die für eine Dosisreduktion infrage kommen, sollte eine Dosierung von 2 mg täglich in Betracht gezogen werden (siehe Abschnitt 5.1).
Baricitinib kann mit oder ohne topische Kortikosteroide angewendet werden. Die Wirksamkeit von Baricitinib kann bei gleichzeitiger Gabe von topischen Kortikosteroiden verbessert werden (siehe Abschnitt 5.1). Topische Calcineurin-Inhibitoren können angewendet werden, sollten aber auf empfindliche Bereiche wie Gesicht, Hals, intertriginöse Bereiche und den Genitalbereich beschränkt werden.
Bei Patienten, bei denen nach 8 Behandlungswochen kein therapeutischer Nutzen nachgewiesen werden kann, ist ein Beenden der Behandlung in Betracht zu ziehen.
Kinder und Jugendliche (ab 2 Jahren)
Die empfohlene Dosis für Baricitinib beträgt 4 mg einmal täglich für Patienten mit einem Körpergewicht ab 30 kg. Für Patienten mit einem Körpergewicht von 10 kg bis unter 30 kg beträgt die empfohlene Dosis 2 mg einmal täglich. Für Patienten, die mit der empfohlenen Dosis eine anhaltende Kontrolle über die Krankheitsaktivität erreicht haben und die für eine Dosisreduktion infrage kommen, sollte in Betracht gezogen werden, die Dosis auf die Hälfte zu reduzieren.
Baricitinib kann mit oder ohne topische Kortikosteroide angewendet werden. Topische Calcineurin-Inhibitoren können angewendet werden, sollten aber auf empfindliche Bereiche wie Gesicht, Hals, intertriginöse Bereiche und den Genitalbereich beschränkt werden.
Bei Patienten, bei denen nach 8 Behandlungswochen kein therapeutischer Nutzen nachgewiesen werden kann, ist ein Beenden der Behandlung in Betracht zu ziehen.
Alopecia areata
Erwachsene
Die empfohlene Dosis für Baricitinib beträgt 4 mg einmal täglich. Für Patienten mit erhöhtem Risiko für VTE, MACE und maligne Erkrankungen, sowie für Patienten ab 65 Jahren und für Patienten mit chronischen bzw. wiederkehrenden Infekten in der Vorgeschichte beträgt die empfohlene Dosis 2 mg einmal täglich (siehe Abschnitt 4.4). Für Patienten, die mit 2 mg einmal täglich keine anhaltende Kontrolle über die Krankheitsaktivität erreichen, kann eine Dosis von 4 mg einmal täglich in Betracht gezogen werden. Für Patienten, die mit 4 mg täglich eine anhaltende Kontrolle über die Krankheitsaktivität erreicht haben und die für eine Dosisreduktion infrage kommen, sollte eine Dosierung von 2 mg täglich in Betracht gezogen werden (siehe Abschnitt 5.1).
Sobald ein stabiles Ansprechen erreicht ist, wird eine Fortsetzung der Behandlung für mindestens mehrere Monate empfohlen, um einen Rückfall zu vermeiden. Das Nutzen-Risiko-Verhältnis der Behandlung ist in regelmäßigen Abständen auf individueller Basis neu zu bewerten.
Bei Patienten, bei denen nach 36 Behandlungswochen kein therapeutischer Nutzen nachgewiesen werden kann, ist ein Beenden der Behandlung in Betracht zu ziehen.
Jugendliche (ab 12 Jahren)
Die empfohlene Dosis für Baricitinib beträgt 4 mg einmal täglich für Patienten mit einem Körpergewicht ab 30 kg. Informationen zur Dosierung bei Patienten mit einem Körpergewicht unter 30 kg, siehe Abschnitt 4.2 Kinder und Jugendliche unten. Für Patienten, die mit 4 mg täglich eine anhaltende Kontrolle über die Krankheitsaktivität erreicht haben und die für eine Dosisreduktion infrage kommen, sollte eine Dosierung von 2 mg täglich in Betracht gezogen werden.
Sobald ein stabiles Ansprechen erreicht ist, wird eine Fortsetzung der Behandlung für mindestens mehrere Monate empfohlen, um einen Rückfall zu vermeiden. Das Nutzen-Risiko-Verhältnis der Behandlung ist in regelmäßigen Abständen auf individueller Basis neu zu bewerten.
Bei Patienten, bei denen nach 36 Behandlungswochen kein therapeutischer Nutzen nachgewiesen werden kann, ist ein Beenden der Behandlung in Betracht zu ziehen.
Juvenile idiopathische Arthritis (von 2 bis unter 18 Jahre)
Die empfohlene Dosis für Baricitinib beträgt 4 mg einmal täglich für Patienten mit einem Körpergewicht ab 30 kg. Für Patienten mit einem Körpergewicht von 10 kg bis unter 30 kg beträgt die empfohlene Dosis 2 mg einmal täglich.
Bei Patienten, bei denen nach 12 Behandlungswochen kein therapeutischer Nutzen nachgewiesen werden kann, ist ein Beenden der Behandlung in Betracht zu ziehen.
Behandlungsbeginn
Bei Patienten mit einer absoluten Lymphozytenzahl (ALC) von weniger als 0,5 x 109 Zellen/l, einer absoluten Neutrophilenzahl (ANC) von weniger als 1 x 109 Zellen/l oder einem Hämoglobinwert unter 8 g/dl sollte eine Therapie nicht begonnen werden. Die Behandlung kann eingeleitet werden, sobald sich die Werte über diese Grenzwerte hinaus verbessert haben (siehe Abschnitt 4.4).
Dosisreduktion
Bei Patienten, die starke OAT3-Inhibitoren (Inhibitoren von Organischen Anionen-Transportern vom Typ 3), wie etwa Probenecid, anwenden, oder bei Patienten mit einer Kreatinin-Clearance zwischen 30 und 60 ml/min, sollte die empfohlene Dosis bei pädiatrischen Patienten auf die Hälfte reduziert werden und bei erwachsenen Patienten beträgt die empfohlene Dosis 2 mg (siehe Abschnitt 4.5).
Besondere Patientengruppen
Eingeschränkte Nierenfunktion
Bei erwachsenen Patienten mit einer Kreatinin-Clearance zwischen 30 und 60 ml/min beträgt die empfohlene Dosis 2 mg einmal täglich. Bei pädiatrischen Patienten mit einer Kreatinin-Clearance zwischen 30 und 60 ml/min sollte die empfohlene Dosis auf die Hälfte reduziert werden. Bei Patienten mit einer Kreatinin-Clearance < 30 ml/min wird die Anwendung von Baricitinib nicht empfohlen (siehe Abschnitt 5.2).
Eingeschränkte Leberfunktion
Bei Patienten mit leichter oder mittelschwerer Leberfunktionsstörung ist keine Dosisanpassung erforderlich. Bei Patienten mit schwerer Leberfunktionsstörung wird die Anwendung von Baricitinib nicht empfohlen (siehe Abschnitt 5.2).
Ältere Patienten
Die klinische Erfahrung bei Patienten ≥ 75 Jahren ist sehr begrenzt.
Kinder und Jugendliche
Die Sicherheit und Wirksamkeit von Baricitinib bei Kindern unter 2 Jahren mit atopischer Dermatitis und juveniler idiopathischer Arthritis ist bisher noch nicht erwiesen. Es liegen keine Daten vor. Informationen zur Dosierung bei Kindern ab 2 Jahren, siehe Abschnitt 4.2 oben.
Die Sicherheit und Wirksamkeit von Baricitinib bei Alopecia areata bei Kindern unter 12 Jahren oder mit einem Körpergewicht unter 30 kg ist bisher noch nicht erwiesen. Es liegen keine Daten vor. Informationen zur Dosierung bei Jugendlichen ab 12 Jahren und mit einem Körpergewicht ab 30 kg, siehe Abschnitt 4.2 oben.
Art der Anwendung
Zum Einnehmen.
Baricitinib ist einmal täglich unabhängig von den Mahlzeiten und der Tageszeit einzunehmen.
Alternative Anwendung bei Kindern
Bei pädiatrischen Patienten, die keine ganzen Tabletten schlucken können, sollte in Betracht gezogen werden, die Tabletten in Wasser zu suspendieren. Zum Suspendieren der Tablette sollte ausschließlich Wasser verwendet werden. Es sollte nur die für die Dosis erforderliche Anzahl an Tabletten suspendiert werden.
Sollte aus irgendeinem Grund nicht die gesamte Suspension angewendet werden, soll keine weitere Tablette suspendiert und angewendet, sondern bis zur nächsten geplanten Dosis gewartet werden.
Hinweise zum Suspendieren des Arzneimittels vor der Anwendung, siehe Abschnitt 6.6.
Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
Schwangerschaft (siehe Abschnitt 4.6).
Bei folgenden Patienten sollte Baricitinib nur angewendet werden, wenn keine geeigneten Behandlungsalternativen zur Verfügung stehen: | |
̶ |
Alter von 65 Jahren und älter; |
̶ |
Patienten mit einer atherosklerotischen Herz-Kreislauf-Erkrankung in der Vorgeschichte oder anderen kardiovaskulären Risikofaktoren (wie Raucher oder ehemalige Langzeitraucher); |
̶ |
Patienten mit Risikofaktoren für maligne Erkrankungen (z. B. bestehendes Malignom oder Malignom in der Vorgeschichte). |
Anwendung von JAK-Inhibitoren bei Patienten ab 65 Jahren
Angesichts des erhöhten Risikos für MACE, maligne Erkrankungen, schwerwiegende Infektionen und Gesamtmortalität bei Patienten ab 65 Jahren, das in einer großen randomisierten Studie zu Tofacitinib (einem anderen JAK-Inhibitor) beobachtet wurde, sollte Baricitinib bei diesen Patienten nur angewendet werden, wenn keine geeigneten Behandlungsalternativen zur Verfügung stehen.
Infektionen
Bei Patienten, die andere JAK-Inhibitoren erhielten, wurden schwerwiegende Infektionen mit gelegentlich tödlichem Ausgang, einschließlich opportunistischer Infektionen, berichtet.
Baricitinib ist im Vergleich zu Placebo mit einer erhöhten Infektionsrate wie etwa Infektionen der oberen Atemwege verbunden (siehe Abschnitt 4.8). In klinischen Studien zu rheumatoider Arthritis führte eine Kombination mit Methotrexat im Vergleich zu einer Baricitinib-Monotherapie zu höheren Infektionsraten.
Bei Patienten mit aktiven, chronischen oder wiederkehrenden Infektionen sollten vor Therapiebeginn mit Baricitinib die Risiken und Vorteile einer Behandlung sorgfältig abgewogen werden (siehe Abschnitt 4.2). Falls sich eine Infektion entwickelt, ist der Patient sorgfältig zu überwachen und die Therapie vorübergehend zu unterbrechen, sollte der Patient auf eine Standardtherapie nicht ansprechen. Die Behandlung darf erst wieder begonnen werden, nachdem die Infektion ausgeheilt ist.
Da bei älteren Patienten und Diabetes-Patienten generell eine höhere Infektionsinzidenz vorliegt, ist bei der Behandlung dieser Patientengruppen Vorsicht geboten. Bei Patienten ab 65 Jahren sollte Baricitinib nur angewendet werden, wenn keine geeigneten Behandlungsalternativen zur Verfügung stehen.
Tuberkulose
Die Patienten sollten vor Beginn einer Therapie auf Tuberkulose (TB) getestet werden. Baricitinib sollte nicht bei Patienten mit aktiver TB angewendet werden. Bei Patienten mit zuvor unbehandelter latenter TB ist vor der Einleitung der Behandlung eine Anti-TB-Therapie in Betracht zu ziehen.
Hämatologische Anomalien
Eine absolute Neutrophilenzahl (ANC) < 1 x 109 Zellen/l, eine absolute Lymphozytenzahl (ALC) < 0,5 x 109 Zellen/l und ein Hämoglobinwert < 8 g/dl wurden in klinischen Studien berichtet.
Bei Patienten, bei denen im Rahmen einer Routineuntersuchung eine ANC < 1 x 109 Zellen/l, eine ALC < 0,5 x 109 Zellen/l oder ein Hämoglobinwert < 8 g/dl beobachtet wurde, sollte eine Therapie nicht begonnen bzw. diese vorübergehend unterbrochen werden (siehe Abschnitt 4.2).
Bei älteren Patienten mit rheumatoider Arthritis ist das Risiko einer Lymphozytose erhöht. Es wurden seltene Fälle von lymphoproliferativen Erkrankungen berichtet.
Virusreaktivierung
Virusreaktivierungen, einschließlich Fälle der Reaktivierung von Herpes-Viren (z. B. Herpes zoster, Herpes simplex), wurden in klinischen Studien berichtet (siehe Abschnitt 4.8). In klinischen Studien zu rheumatoider Arthritis wurde bei Patienten ab 65 Jahren, die vorher bereits sowohl mit biologischen als auch mit synthetischen konventionellen DMARDs behandelt wurden, Herpes zoster häufiger berichtet. Falls ein Patient Herpes zoster entwickelt, sollte die Behandlung vorübergehend unterbrochen werden, bis die Infektion abgeklungen ist.
Vor Beginn einer Therapie mit Baricitinib sollte ein Screening auf eine Virushepatitis entsprechend der klinischen Leitlinien durchgeführt werden. Patienten mit nachweislich aktiver Hepatitis-B- oder Hepatitis-C-Infektion waren von den klinischen Studien ausgeschlossen. Patienten, die für Hepatitis-C-Antikörper positiv, aber für Hepatitis-C-Virus-RNA negativ waren, konnten an den Studien teilnehmen. Patienten mit Hepatitis-B-Oberflächen-Antikörpern und Hepatitis-B-Kern-Antikörpern, aber ohne Hepatitis-B-Oberflächen-Antigen, konnten ebenfalls an den Studien teilnehmen. Solche Patienten sollten auf die Expression von Hepatitis-B-Virus (HBV)-DNA überwacht werden. Falls HBV-DNA festgestellt wird, ist ein Hepatologe zu konsultieren, um zu entscheiden, ob die Behandlung zu unterbrechen ist.
Impfungen
Es liegen keine Daten zum Ansprechen auf Impfungen mit Lebendimpfstoffen bei Patienten unter Behandlung mit Baricitinib vor. Die Anwendung von attenuierten Lebendimpfstoffen wird während oder unmittelbar vor einer Behandlung mit Baricitinib nicht empfohlen. Vor Beginn der Therapie wird empfohlen, bei allen Patienten, insbesondere pädiatrischen Patienten, alle Immunisierungen in Übereinstimmung mit den geltenden Impfempfehlungen auf den aktuellen Stand zu bringen.
Lipide
Dosisabhängige Erhöhungen der Blutlipidwerte wurden bei mit Baricitinib behandelten pädiatrischen und erwachsenen Patienten berichtet (siehe Abschnitt 4.8). Erhöhungen des Low Density Lipoprotein (LDL)-Cholesterins gingen bei Erwachsenen mit einer Statintherapie wieder auf die Werte vor Behandlungsbeginn zurück. Sowohl bei pädiatrischen als auch bei erwachsenen Patienten sollten die Lipidparameter etwa 12 Wochen nach Beginn der Therapie überprüft werden, und die Patienten danach entsprechend den internationalen klinischen Leitlinien für Hyperlipidämie behandelt werden.
Erhöhungen der Lebertransaminasen
Dosisabhängige Erhöhungen von Alanin-Aminotransferase (ALT) und Aspartat-Aminotransferase (AST) wurden bei mit Baricitinib behandelten Patienten berichtet (siehe Abschnitt 4.8).
Erhöhungen von ALT und AST auf mindestens das 5- bis 10‑fache der Obergrenze der Normalwerte (ULN) wurden in den klinischen Studien berichtet. In klinischen Studien zu rheumatoider Arthritis führte eine Kombination mit Methotrexat im Vergleich zu einer Baricitinib-Monotherapie häufiger zu einer Erhöhung der Lebertransaminasen (siehe Abschnitt 4.8).
Falls im Rahmen von Routineuntersuchungen Erhöhungen von ALT oder AST beobachtet werden und eine arzneimittelbedingte Leberschädigung vermutet wird, ist die Behandlung vorübergehend abzusetzen, bis eine solche Diagnose ausgeschlossen werden kann.
Maligne Erkrankungen
Immunmodulatorische Arzneimittel könnten das Risiko für maligne Erkrankungen, einschließlich Lymphomen, erhöhen. Lymphome und andere maligne Erkrankungen wurden bei Patienten unter einer Behandlung mit JAK-Inhibitoren, einschließlich Baricitinib, berichtet.
In einer großen randomisierten, aktiv kontrollierten Studie zu Tofacitinib (einem anderen JAK-Inhibitor) bei Patienten mit rheumatoider Arthritis, die 50 Jahre oder älter waren und mindestens einen zusätzlichen kardiovaskulären Risikofaktor aufwiesen, wurde unter Tofacitinib im Vergleich zu TNF-Inhibitoren eine erhöhte Rate von malignen Erkrankungen, insbesondere Lungenkarzinom, Lymphom und nicht-melanozytärem Hautkrebs (NMSC), beobachtet.
Bei Patienten ab 65 Jahren, Rauchern oder ehemaligen Langzeitrauchern und bei Patienten mit anderen Risikofaktoren für maligne Erkrankungen (z. B. bestehendes Malignom oder Malignom in der Vorgeschichte) sollte Baricitinib nur angewendet werden, wenn keine geeigneten Behandlungsalternativen zur Verfügung stehen.
Regelmäßige Hautuntersuchungen werden für alle Patienten empfohlen, insbesondere für jene mit Risikofaktoren für Hautkrebs.
Venöse Thromboembolien
In einer retrospektiven Beobachtungsstudie zu Baricitinib bei Patienten mit rheumatoider Arthritis wurde eine erhöhte Rate von venösen thromboembolischen Ereignissen (VTE) im Vergleich zu Patienten, die mit TNF-Inhibitoren behandelten wurden, beobachtet (siehe Abschnitt 4.8).
In einer großen randomisierten, aktiv kontrollierten Studie zu Tofacitinib (einem anderen JAK-Inhibitor) bei Patienten mit rheumatoider Arthritis, die 50 Jahre oder älter waren und mindestens einen zusätzlichen kardiovaskulären Risikofaktor aufwiesen, wurde unter Tofacitinib im Vergleich zu TNF-Inhibitoren dosisabhängig eine erhöhte Rate von VTE, einschließlich tiefer Venenthrombose (TVT) und Lungenembolie (LE), beobachtet.
Bei Patienten mit kardiovaskulären oder malignen Risikofaktoren (siehe auch Abschnitt 4.4 „Schwerwiegende unerwünschte kardiovaskuläre Ereignisse (MACE)“ und „Maligne Erkrankungen“) sollte Baricitinib nur angewendet werden, wenn keine geeigneten Behandlungsalternativen zur Verfügung stehen.
Bei Patienten mit anderen bekannten Risikofaktoren für VTE, die keine kardiovaskulären oder malignen Risikofaktoren sind, sollte Baricitinib mit Vorsicht angewendet werden. Diese Risikofaktoren umfassen: Frühere VTE, größerer chirurgischer Eingriff, Immobilisation, Anwendung von kombinierten hormonellen Kontrazeptiva oder Hormonersatztherapie und Vorliegen einer erblichen Gerinnungsstörung.
Während der Behandlung mit Baricitinib sollten Patienten in regelmäßigen Abständen auf Veränderungen des VTE-Risikos untersucht werden.
Patienten mit Anzeichen und Symptomen einer VTE sind unverzüglich zu untersuchen. Bei Patienten mit VTE-Verdacht ist Baricitinib unabhängig von Dosierung und Anwendungsgebiet abzusetzen.
Schwerwiegende unerwünschte kardiovaskuläre Ereignisse (MACE)
In einer retrospektiven Beobachtungsstudie zu Baricitinib bei Patienten mit rheumatoider Arthritis wurde eine erhöhte Rate von MACE im Vergleich zu Patienten, die mit TNF-Inhibitoren behandelt wurden, beobachtet.
In einer großen randomisierten, aktiv kontrollierten Studie zu Tofacitinib (einem anderen JAK-Inhibitor) bei Patienten mit rheumatoider Arthritis, die 50 Jahre oder älter waren und mindestens einen zusätzlichen kardiovaskulären Risikofaktor aufwiesen, wurde unter Tofacitinib im Vergleich zu TNF-Inhibitoren eine erhöhte Rate schwerwiegender kardiovaskulärer Ereignisse (MACE), definiert als kardiovaskulärer Tod, nicht tödlicher Myokardinfarkt (MI) und nicht tödlicher Schlaganfall, beobachtet.
Daher sollte bei Patienten ab 65 Jahren, Rauchern oder ehemaligen Langzeitrauchern und Patienten mit einer Vorgeschichte einer atherosklerotischen Herz-Kreislauf-Erkrankung oder anderen kardiovaskulären Risikofaktoren Baricitinib nur angewendet werden, wenn keine geeigneten Behandlungsalternativen zur Verfügung stehen.
Laborkontrollen
Tabelle 1. Laborkontrollen und Überwachungsempfehlungen
Laborkontrollen |
Maßnahme |
Überwachungsempfehlungen |
Lipidparameter |
Die Patienten sollten entsprechend den internationalen klinischen Leitlinien für Hyperlipidämie behandelt werden. |
12 Wochen nach Behandlungsbeginn und danach entsprechend den internationalen klinischen Leitlinien für Hyperlipidämie |
Absolute Neutrophilenzahl (ANC) |
Die Behandlung sollte unterbrochen werden, wenn ANC weniger als 1 x 109 Zellen/l beträgt, und kann erneut begonnen werden, sobald ANC wieder über diesem Wert liegt. |
Vor Behandlungsbeginn und danach im Rahmen der Patientenroutineuntersuchung |
Absolute Lymphozytenzahl (ALC) |
Die Behandlung sollte unterbrochen werden, wenn ALC weniger als 0,5 x 109 Zellen/l beträgt, und kann erneut begonnen werden, sobald ALC wieder über diesem Wert liegt. |
|
Hämoglobin (Hb) |
Die Behandlung sollte unterbrochen werden, wenn Hb weniger als 8 g/dl beträgt, und kann erneut begonnen werden, sobald Hb wieder über diesem Wert liegt. |
|
Lebertransaminasen |
Die Behandlung sollte vorübergehend unterbrochen werden, falls eine arzneimittelbedingte Leberschädigung vermutet wird. |
Immunsuppressiva
Die Kombination mit biologischen DMARDs, biologischen Immunmodulatoren oder anderen Januskinase (JAK)-Inhibitoren wird nicht empfohlen, da das Risiko eines additiven immunsuppressiven Effekts nicht ausgeschlossen werden kann.
Für rheumatoide Arthritis und juvenile idiopathische Arthritis liegen nur begrenzte Daten, die die gemeinsame Anwendung von Baricitinib mit potenten Immunsuppressiva außer Methotrexat (z. B. Azathioprin, Tacrolimus, Ciclosporin) betreffen, vor. Bei der Anwendung solcher Kombinationen ist Vorsicht geboten (siehe Abschnitt 4.5).
Für atopische Dermatitis und Alopecia areata wurde eine Kombination mit Ciclosporin oder anderen potenten Immunsuppressiva nicht untersucht und wird nicht empfohlen (siehe Abschnitt 4.5).
Überempfindlichkeit
Seit Markteinführung wurden Fälle von Überempfindlichkeit in Zusammenhang mit der Anwendung von Baricitinib berichtet. Bei schweren allergischen oder anaphylaktischen Reaktionen ist die Behandlung sofort abzusetzen.
Divertikulitis
In klinischen Studien und aus verschiedenen Datenquellen nach der Markteinführung wurden Fälle von Divertikulitis und gastrointestinaler Perforation berichtet (siehe Abschnitt 4.8). Baricitinib sollte vorsichtig angewendet werden bei Patienten mit Divertikelerkrankung und insbesondere bei Patienten, die gleichzeitig dauerhaft mit Arzneimitteln behandelt werden, die mit einem erhöhten Divertikulitisrisiko assoziiert sind: Nichtsteroidale Entzündungshemmer, Kortikosteroide und Opioide. Patienten mit neu aufgetretenen abdominalen Beschwerden und Symptomen sind unverzüglich zu untersuchen, um eine Divertikulitis oder gastrointestinale Perforation frühzeitig zu erkennen.
Hypoglykämie bei Patienten, die wegen Diabetes behandelt werden
Es liegen Berichte über Hypoglykämie nach Beginn der Anwendung von JAK-Inhibitoren, einschließlich Baricitinib, bei Patienten vor, die Arzneimittel gegen Diabetes erhalten. Bei Auftreten einer Hypoglykämie kann eine Anpassung der Dosis der Diabetesmedikation erforderlich sein.
Sonstige Bestandteile
Dieses Arzneimittel enthält weniger als 1 mmol Natrium (23 mg) pro Filmtablette, d. h., es ist nahezu „natriumfrei“.
Pharmakodynamische Wechselwirkungen
Immunsuppressiva
Die Kombination mit biologischen DMARDs, biologischen Immunmodulatoren oder anderen JAK-Inhibitoren wurde nicht untersucht. Für rheumatoide Arthritis und juvenile idiopathische Arthritis war die gemeinsame Anwendung von Baricitinib mit potenten Immunsuppressiva (z. B. Azathioprin, Tacrolimus, Ciclosporin) in klinischen Studien begrenzt und das Risiko eines additiven immunsuppressiven Effekts kann nicht ausgeschlossen werden. Für atopische Dermatitis und Alopecia areata wurde eine Kombination mit Ciclosporin oder anderen potenten Immunsuppressiva nicht untersucht und wird nicht empfohlen (siehe Abschnitt 4.4).
Potential anderer Arzneimittel, die Pharmakokinetik von Baricitinib zu beeinflussen
Transport-Proteine
In vitro ist Baricitinib ein Substrat für Organische Anionen-Transporter (OAT)3, für das P-Glykoprotein (Pgp), das Brustkrebsresistenzprotein (BCRP) und das Multidrug and Toxic Extrusion-Protein (MATE)2-K. In einer klinischen pharmakologischen Studie führte die Gabe von Probenecid (ein OAT3-Inhibitor mit starkem Hemmpotenzial) zu einer Erhöhung der AUC (0 - ∞) um etwa das 2‑fache ohne Veränderung der tmax oder der Cmax von Baricitinib. Daher ist die empfohlene Dosis von Baricitinib bei Patienten, die gleichzeitig OAT3-Inhibitoren mit starkem Hemmpotenzial wie etwa Probenecid erhalten, auf die Hälfte zu reduzieren (siehe Abschnitt 4.2). Es wurde keine klinische pharmakologische Studie mit OAT3-Inhibitoren mit geringerem Hemmpotenzial durchgeführt. Das Prodrug Leflunomid wird schnell in Teriflunomid umgewandelt, letzteres ist ein schwacher OAT3-Inhibitor und kann daher zu einer erhöhten Baricitinib-Exposition führen. Da keine entsprechenden Wechselwirkungsstudien durchgeführt wurden, ist bei der gleichzeitigen Anwendung von Leflunomid oder Teriflunomid und Baricitinib Vorsicht geboten. Die gleichzeitige Anwendung der OAT3-Inhibitoren Ibuprofen und Diclofenac kann zu einer erhöhten Baricitinib-Exposition führen, jedoch ist ihr Hemmpotential gegenüber OAT3 schwächer als das von Probenecid und daher ist eine klinisch relevante Wechselwirkung nicht zu erwarten. Eine gemeinsame Anwendung von Baricitinib mit Ciclosporin (Pgp/BCRP-Inhibitor) oder Methotrexat (Substrat mehrerer Transporter – unter anderem OATP1B1, OAT1, OAT3, BCRP, MRP2, MRP3 oder MRP4) hatte keine klinisch relevanten Effekte auf die Baricitinib-Exposition.
Cytochrom P450-Enzyme
In vitro ist Baricitinib ein Substrat des Cytochrom P450-Enzyms (CYP)3A4, obwohl weniger als 10 % der Dosis über Oxidation metabolisiert werden. In klinischen pharmakologischen Studien führte eine gemeinsame Anwendung von Baricitinib mit Ketoconazol (starker CYP3A-Inhibitor) zu keinem klinisch relevanten Effekt auf die PK von Baricitinib. Eine gemeinsame Anwendung von Baricitinib mit Fluconazol (moderater CYP3A/CYP2C19/CYP2C9-Inhibitor) oder Rifampicin (starker CYP3A-Induktor) führte zu keinen klinisch relevanten Veränderungen der Baricitinib-Exposition.
Wirkstoffe, die den Magen-pH-Wert modifizieren
Die Erhöhung des Magen-pH-Werts mittels Omeprazol hatte keinen signifikanten Effekt auf die Baricitinib-Exposition.
Potential von Baricitinib, die Pharmakokinetik anderer Arzneimittel zu beeinflussen
Transport-Proteine
In vitro ist Baricitinib in klinisch relevanten Konzentrationen kein Inhibitor von OAT1, OAT2, OAT3, dem Organischen Kationen-Transporter (OCT)2, OATP1B1, OATP1B3, BCRP, MATE1 und MATE2-K. Baricitinib könnte ein klinisch relevanter Inhibitor von OCT1 sein, jedoch sind bisher keine selektiven OCT1-Substrate bekannt, für die klinisch signifikante Wechselwirkungen vorhergesagt werden könnten. In klinischen pharmakologischen Studien zeigten sich keine klinisch relevanten Effekte auf die Exposition, wenn Baricitinib gemeinsam mit Digoxin (Pgp-Substrat) oder Methotrexat (Substrat mehrerer Transporter) angewendet wurde.
Cytochrom P450-Enzyme
In klinischen pharmakologischen Studien führte eine gemeinsame Anwendung von Baricitinib mit den CYP3A-Substraten Simvastatin, Ethinylestradiol oder Levonorgestrel zu keinen klinisch relevanten Änderungen der PK dieser Arzneimittel.
Schwangerschaft
Es zeigte sich, dass der JAK/STAT-Signalweg an Zelladhäsion und Zellpolarität beteiligt ist, welche die frühe embryonale Entwicklung beeinflussen können. Es liegen keine adäquaten Daten zur Anwendung von Baricitinib bei schwangeren Frauen vor. Tierexperimentelle Studien haben eine Reproduktionstoxizität gezeigt (siehe Abschnitt 5.3). Baricitinib war bei Ratten und Kaninchen teratogen. Tierstudien weisen darauf hin, dass Baricitinib in höheren Dosen die Knochenentwicklung in utero beeinträchtigen könnte.
Baricitinib ist während einer Schwangerschaft kontraindiziert (siehe Abschnitt 4.3). Frauen im gebärfähigen Alter müssen während der Anwendung und nach Beendigung der Behandlung mindestens eine weitere Woche eine zuverlässige Verhütungsmethode anwenden. Falls eine Patientin während der Anwendung von Baricitinib schwanger wird, sind die werdenden Eltern über das mögliche Risiko für den Fötus zu informieren.
Stillzeit
Es ist nicht bekannt, ob Baricitinib/seine Metaboliten in die Muttermilch übergehen. Die zur Verfügung stehenden pharmakodynamischen/toxikologischen Daten vom Tier zeigten, dass Baricitinib in die Milch übergeht (siehe Abschnitt 5.3).
Ein Risiko für Neugeborene/Kind kann nicht ausgeschlossen werden, und Baricitinib soll während der Stillzeit nicht angewendet werden. Es muss eine Entscheidung darüber getroffen werden, ob das Stillen zu unterbrechen ist oder ob auf die Behandlung mit Olumiant verzichtet werden soll. Dabei soll sowohl der Nutzen des Stillens für das Kind als auch der Nutzen der Therapie für die Frau berücksichtigt werden.
Fertilität
Tierstudien deuten darauf hin, dass während einer Behandlung mit Baricitinib die weibliche Fertilität vermindert sein kann. Es zeigte sich jedoch kein Effekt auf die männliche Spermatogenese (siehe Abschnitt 5.3).
Baricitinib hat keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Zusammenfassung des Sicherheitsprofils
Die am häufigsten berichteten Nebenwirkungen mit Baricitinib sind erhöhtes LDL-Cholesterin (26,0 %), Infektionen der oberen Atemwege (16,9 %), Kopfschmerzen (5,2 %), Herpes simplex (3,2 %) und Harnwegsinfektionen (2,9 %). Schwerwiegende Pneumonie und schwerwiegender Herpes zoster traten bei Patienten mit rheumatoider Arthritis gelegentlich auf.
Tabellarische Auflistung der Nebenwirkungen
Geschätzte Häufigkeit: Sehr häufig (≥ 1/10), häufig (≥ 1/100 bis < 1/10), gelegentlich (≥ 1/1 000 bis < 1/100), selten (≥ 1/10 000 bis < 1/1 000), sehr selten (< 1/10 000). Die Häufigkeiten in Tabelle 2 basieren, sofern nicht anders angegeben, auf integrierten Daten aus klinischen Studien bei Erwachsenen und/oder aus Daten nach der Markteinführung der Indikationen rheumatoide Arthritis, atopische Dermatitis und Alopecia areata; bemerkenswerte Unterschiede in der Häufigkeit zwischen den Indikationen sind in den Fußnoten unterhalb der Tabelle angegeben.
Tabelle 2. Nebenwirkungen
Systemorganklasse |
Sehr häufig |
Häufig |
Gelegentlich |
Infektionen und parasitäre Erkrankungen |
Infektionen der |
Herpes zoster b |
|
Erkrankungen des Blutes und des Lymphsystems |
Thrombozytose > 600 x 109 Zellen/l a, d |
Neutropenie < 1 x 109 Zellen/l a |
|
Erkrankungen des Immunsystems |
Schwellung des Gesichts, |
||
Stoffwechsel- und Ernährungsstörungen |
Hypercholesterinämie a |
Hypertriglyzeridämie a |
|
Erkrankungen des Nervensystems |
Kopfschmerzen |
||
Gefäßerkrankungen |
Tiefe Venenthrombose b |
||
Erkrankungen der Atemwege, des Brustraums und Mediastinums |
Lungenembolie f |
||
Erkrankungen des Gastrointestinal-trakts |
Übelkeit d |
Divertikulitis |
|
Leber- und Gallenerkrankungen |
Erhöhte Alanin-Aminotransferase (ALT) ≥ 3 x Obergrenze des Normalwertes (ULN) a, d |
Erhöhte Aspartat-Aminotransferase (AST) ≥ 3 x Obergrenze des Normalwertes (ULN) a, e |
|
Erkrankungen der Haut und des Unterhautzellgewebes |
Ausschlag |
||
Untersuchungen |
Erhöhte Kreatinphosphokinase > 5 x Obergrenze des Normalwertes (ULN) a, c |
Gewichtszunahme |
a |
Beinhaltet bei routinemäßigen Laborkontrollen gemessene Veränderungen (siehe Text unten). |
b |
Die Häufigkeit von Herpes zoster und tiefer Venenthrombose basiert auf klinischen Studien zu rheumatoider Arthritis. |
c |
In klinischen Studien zu rheumatoider Arthritis war die Häufigkeit von Akne und erhöhter Kreatinphosphokinase > 5 x Obergrenze des Normalwertes (ULN) gelegentlich. |
d |
In klinischen Studien zu atopischer Dermatitis war die Häufigkeit von Übelkeit und erhöhter Alanin-Aminotransferase (ALT) ≥ 3 x Obergrenze des Normalwertes (ULN) gelegentlich. In klinischen Studien zu Alopecia areata trat Abdominalschmerz gelegentlich auf. In klinischen Studien zu atopischer Dermatitis und Alopecia areata traten Pneumonie und Thrombozytose > 600 x 109 Zellen/l gelegentlich auf. |
e |
In klinischen Studien zu Alopecia areata war die Häufigkeit von AST ≥ 3 x ULN häufig. |
f |
Die Häufigkeit von Lungenembolien basiert auf klinischen Studien zu rheumatoider Arthritis und atopischer Dermatitis. |
g |
Follikulitis wurde in klinischen Studien zu Alopecia areata beobachtet. Sie war meist mit dem Nachwachsen der Haare assoziiert und in der Kopfhautregion lokalisiert. |
Beschreibung ausgewählter Nebenwirkungen
Erkrankungen des Gastrointestinaltrakts
In klinischen Studien zu rheumatoider Arthritis war bei den behandlungsnaiven Patienten während eines Zeitraums von 52 Wochen die Häufigkeit von Übelkeit unter der Kombination von Methotrexat und Baricitinib (9,3 %) größer als unter Methotrexat-Monotherapie (6,2 %) oder Baricitinib-Monotherapie (4,4 %). Basierend auf den integrierten Daten aus klinischen Studien zu rheumatoider Arthritis, atopischer Dermatitis und Alopecia areata trat die Übelkeit in den ersten zwei Behandlungswochen am häufigsten auf.
Fälle von Abdominalschmerz waren meist leicht, vorübergehend, wurden nicht mit infektiösen oder entzündlichen Erkrankungen des Gastrointestinaltraktes in Zusammenhang gebracht und führten nicht zu einer Unterbrechung der Behandlung.
Infektionen
Basierend auf den integrierten Daten aus klinischen Studien zu rheumatoider Arthritis, atopischer Dermatitis und Alopecia areata, waren die Infektionen meist von leichtem bis mäßigem Schweregrad. In Studien, die beide Dosierungen einschlossen, wurden Infektionen bei 31,0 %, 25,7 % und 26,7 % der Patienten in der 4 mg, 2 mg bzw. der Placebo-Gruppe berichtet. In klinischen Studien zu rheumatoider Arthritis traten Infektionen unter einer Kombination mit Methotrexat im Vergleich zur Baricitinib-Monotherapie häufiger auf. Herpes zoster trat bei rheumatoider Arthritis häufig, bei atopischer Dermatitis sehr selten, und bei Alopecia areata gelegentlich auf. In klinischen Studien zu atopischer Dermatitis traten unter einer Behandlung mit Baricitinib weniger Hautinfektionen auf, die eine antibiotische Behandlung benötigen, als mit Placebo.
Die Inzidenz schwerwiegender Infektionen unter Baricitinib war ähnlich zu Placebo. Die Inzidenz schwerwiegender Infektionen blieb unter Langzeitbehandlung stabil. Die Gesamtinzidenzrate schwerwiegender Infektionen betrug im Rahmen des klinischen Studienprogramms 3,2 pro 100 Patientenjahre bei rheumatoider Arthritis, 2,1 bei atopischer Dermatitis und 0,8 bei Alopecia areata. Schwerwiegende Pneumonie und schwerwiegender Herpes zoster traten bei Patienten mit rheumatoider Arthritis gelegentlich auf.
Erhöhung der Lebertransaminasen
In Studien mit einer Dauer über 16 Wochen hinaus wurden dosisabhängige Erhöhungen von ALT und AST berichtet. Erhöhungen der mittleren ALT/AST-Werte blieben im Zeitverlauf stabil. Die meisten Fälle einer Erhöhung der Lebertransaminasen ≥ 3 x ULN waren asymptomatisch und vorübergehend.
Die Kombination von Baricitinib mit potenziell hepatotoxischen Arzneimitteln wie Methotrexat führte bei Patienten mit rheumatoider Arthritis häufiger zu solchen Erhöhungen.
Erhöhungen der Lipidwerte
Basierend auf den integrierten Daten aus klinischen Studien zu rheumatoider Arthritis, atopischer Dermatitis und Alopecia areata war die Behandlung mit Baricitinib dosisabhängig mit Erhöhungen der Lipidparameter verbunden, einschließlich Gesamtcholesterin, LDL-Cholesterin und High Density Lipoprotein (HDL)-Cholesterin. Es gab keine Veränderung beim LDL/HDL-Quotienten. Erhöhungen wurden nach 12 Wochen beobachtet und blieben danach stabil auf einem höheren Wert als dem Ausgangwert, auch während der Verlängerungsstudie zu rheumatoider Arthritis. Bei Patienten mit atopischer Dermatitis und Alopecia areata stiegen das mittlere Gesamtcholesterin und das LDL-Cholesterin bis Woche 52 an. In klinischen Studien zu rheumatoider Arthritis war die Behandlung mit Baricitinib mit einem dosisabhängigen Anstieg der Triglyceride verbunden. In klinischen Studien zu atopischer Dermatitis und Alopecia areata wurde kein Anstieg der Triglyceridwerte beobachtet.
Erhöhungen des LDL-Cholesterins gingen unter einer Statintherapie wieder auf die Werte vor Beginn der Behandlung zurück.
Kreatinphosphokinase (CPK)
Die Behandlung mit Baricitinib war mit einem dosisabhängigen Anstieg der CPK-Werte verbunden. Der mittlere CPK-Wert war in Woche 4 erhöht und blieb danach auf einem höheren Wert als dem Ausgangswert. Indikationsübergreifend waren die CPK-Erhöhungen > 5 x ULN in den meisten Fällen vorübergehend und erforderten kein Absetzen der Behandlung.
In den klinischen Studien gab es keine bestätigten Fälle von Rhabdomyolyse.
Neutropenie
Die mittleren Neutrophilenzahlen nahmen in Woche 4 ab und blieben im Zeitverlauf stabil auf einem niedrigeren Wert als dem Ausgangswert. Es gab keinen eindeutigen Zusammenhang zwischen der Neutropenie und dem Auftreten von schwerwiegenden Infektionen. Allerdings wurde in klinischen Studien die Behandlung im Falle einer ANC < 1 x 109 Zellen/l unterbrochen.
Thrombozytose
Dosisabhängige Erhöhungen der mittleren Thrombozytenzahlen wurden beobachtet und blieben im Zeitverlauf stabil auf einem höheren Wert als dem Ausgangswert.
Kinder und Jugendliche
Juvenile idiopathische Arthritis
Insgesamt 220 Patienten im Alter von 2 bis unter 18 Jahren erhielten im Rahmen des klinischen Studienprogramms für juvenile idiopathische Arthritis eine unterschiedliche Studiendosis Baricitinib, was einer Exposition von 326 Patientenjahren entspricht.
Bei pädiatrischen Patienten, die in der placebokontrollierten, doppelblinden, randomisierten Absetzphase der klinischen Studie zur juvenilen idiopathischen Arthritis (n = 82) mit Baricitinib behandelt wurden, traten Kopfschmerzen sehr häufig auf (11 %), Neutropenie < 1 000 Zellen/mm3 häufig (2,4 %, ein Patient) und Lungenembolie ebenfalls häufig (1,2 %, ein Patient).
Atopische Dermatitis bei Kindern und Jugendlichen
Die Sicherheitsbeurteilung bei Kindern und Jugendlichen basiert auf den Sicherheitsdaten der Phase-III-Studie BREEZE-AD-PEDS, bei der 466 Patienten zwischen 2 und 18 Jahren eine unterschiedliche Studiendosis Baricitinib erhielten. Insgesamt war das Sicherheitsprofil bei diesen Patienten vergleichbar mit dem der Erwachsenenpopulation. Neutropenie (< 1 x 109 Zellen/l) war häufiger (1,7 %) im Vergleich zu Erwachsenen.
Alopecia areata bei Jugendlichen
Insgesamt 245 Patienten im Alter von 12 bis unter 18 Jahren erhielten im Rahmen der Phase-III-Studie BRAVE-AA-PEDS eine unterschiedliche Studiendosis Baricitinib. Von diesen wurden 85 Patienten während der placebokontrollierten Phase mit 4 mg behandelt. Insgesamt war das Sicherheitsprofil bei jugendlichen Patienten vergleichbar mit dem der Erwachsenenpopulation. Akne (10,6 %) und Neutropenie (3,6 %) (< 1 x 109 Zellen/l) waren häufiger im Vergleich zu Erwachsenen.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung über das nationale Meldesystem anzuzeigen:
Bundesinstitut für Arzneimittel und
Medizinprodukte
Abt. Pharmakovigilanz
Kurt-Georg-Kiesinger-Allee 3
D-53175 Bonn
Website: https://www.bfarm.de
Einzeldosen von bis zu 40 mg und Mehrfachdosen von bis zu 20 mg täglich für 10 Tage wurden bei erwachsenen Patienten in klinischen Studien ohne dosislimitierende Toxizität angewendet. Es wurden keine spezifischen Toxizitäten erkannt. Die pharmakokinetischen Daten für eine Einzeldosis von 40 mg bei gesunden Probanden zeigen, dass zu erwarten ist, dass mehr als 90 % der angewendeten Dosis innerhalb von 24 Stunden eliminiert werden. Im Falle einer Überdosierung wird empfohlen, den Patienten auf Anzeichen und Symptome von Nebenwirkungen zu überwachen. Bei Patienten, die Nebenwirkungen entwickeln, ist eine adäquate Behandlung einzuleiten.
Pharmakotherapeutische Gruppe: Immunsuppressiva, Janus-assoziierte Kinase (JAK)-Inhibitoren, ATC-Code: L04AF02
Wirkmechanismus
Baricitinib ist ein selektiver und reversibler Inhibitor von Januskinase (JAK)1 und JAK2. In isolierten Enzym-Assays hemmte Baricitinib die Aktivität von JAK1, JAK2, Tyrosinkinase 2 und JAK3 mit IC50-Werten von jeweils 5,9; 5,7; 53 bzw. > 400 nM.
Januskinasen (JAKs) sind Enzyme, die intrazelluläre Signale von Zelloberflächenrezeptoren für eine Reihe von Zytokinen und Wachstumsfaktoren weiterleiten, die an Hämatopoese, Entzündung und Immunabwehr beteiligt sind. Innerhalb des intrazellulären Signalweges phosphorylieren und aktivieren JAKs Signaltransduktoren und Aktivatoren der Transkription (STATs), die wiederum die Genexpression innerhalb der Zelle aktivieren. Baricitinib moduliert diese Signalwege, indem es die enzymatische Aktivität von JAK1 und JAK2 teilweise hemmt und damit die Phosphorylierung und Aktivierung von STATs reduziert.
Pharmakodynamische Wirkungen
Hemmung der durch IL-6 induzierten STAT3-Phosphorylierung
Die Anwendung von Baricitinib führte zu einer dosisabhängigen Hemmung der durch IL-6 induzierten STAT3-Phosphorylierung im Vollblut gesunder Probanden, wobei die maximale Hemmung 2 Stunden nach der Verabreichung beobachtet wurde und sich die Werte nach 24 Stunden wieder auf Werte im Baseline-Bereich normalisiert hatten.
Immunglobuline
Die mittleren Serumwerte für IgG, IgM und IgA hatten sich innerhalb von 12 Wochen nach Behandlungsbeginn vermindert und blieben für mindestens 104 Wochen stabil auf einem niedrigeren Wert als dem Ausgangswert. Bei den meisten Patienten blieben die Veränderungen bei den Immunglobulinen innerhalb des üblichen Referenzbereichs.
Lymphozyten
Die mittlere absolute Lymphozytenzahl erhöhte sich innerhalb einer Woche nach Behandlungsbeginn, ging bis Woche 24 wieder auf die Ausgangswerte zurück und blieb danach für mindestens 104 Wochen stabil. Bei den meisten Patienten blieben die Veränderungen der Lymphozytenzahl innerhalb des üblichen Referenzbereichs.
C-reaktives Protein
Bei Patienten mit rheumatoider Arthritis wurde eine Reduktion von C-reaktivem Protein (CRP) bereits eine Woche nach Behandlungsbeginn beobachtet. Diese hielt über die gesamte Behandlungsdauer an.
Kreatinin
In klinischen Studien induzierte Baricitinib nach zwei Behandlungswochen einen mittleren Anstieg des Serumkreatininlevels von 3,8 µmol/l, der dann stabil blieb. Dies wird möglicherweise durch eine Inhibierung der Kreatininsekretion in den Nierentubuli verursacht. Infolgedessen könnte die geschätzte glomeruläre Filtrationsrate (eGFR) basierend auf dem Serumkreatinin etwas niedriger sein, ohne dass tatsächlich eine Minderung der Nierenfunktion besteht oder renale Nebenwirkungen eintreten. Bei Alopecia areata stieg der mittlere Serumkreatinin-Wert bis Woche 52 weiter an. Bei atopischer Dermatitis und Alopecia areata wurde Baricitinib in Zusammenhang mit einer Reduktion von Cystatin C (auch zur Abschätzung der glomerulären Filtrationsrate verwendet) in Woche 4 gebracht, wobei danach keine weitere Reduktion zu verzeichnen war.
In-vitro-Hautmodelle
In einem mit pro-inflammatorischen Cytokinen (d. h. IL-4, IL-13, IL-31) behandelten in vitro humanen Hautmodell reduzierte Baricitinib die Expression von pSTAT3 in epidermalen Keratinozyten und erhöhte die Expression von Filaggrin, einem Protein, das in der Hautbarrierefunktion und der Pathogenese von atopischer Dermatitis eine Rolle spielt.
Impfstudien
Die Wirkung von Baricitinib auf die humorale Immunantwort auf Totimpfstoffe wurde bei 106 Patienten mit rheumatoider Arthritis unter stabiler Therapie mit Baricitinib 2 bzw. 4 mg, die eine inaktivierte Pneumokokken- oder Tetanus-Impfung verabreicht bekamen, untersucht. Die Mehrheit dieser Patienten (n = 94) erhielt gleichzeitig Methotrexat. Die Pneumokokken-Impfung führte für die Gesamtpopulation zu einer zufriedenstellenden IgG-Immunantwort bei 68 % der Patienten (95 % KI: 58,4 %, 76,2 %). Bei 43,1 % (95 % KI: 34 %, 52,8 %) der Patienten wurde eine zufriedenstellende IgG-Immunantwort auf die Tetanus-Impfung erreicht.
Klinische Wirksamkeit
Rheumatoide Arthritis
Die Wirksamkeit und Sicherheit von Baricitinib einmal täglich wurden in 4 randomisierten, doppelblinden, multizentrischen Phase-III-Studien bei erwachsenen Patienten mit mittelschwerer bis schwerer aktiver rheumatoider Arthritis mit Diagnose gemäß der ACR/EULAR-Kriterien von 2010 untersucht (Tabelle 3). Das Vorliegen von mindestens 6 druckschmerzhaften und 6 geschwollenen Gelenken bei Studienbeginn war für eine Teilnahme erforderlich. Alle Patienten, die diese Studien abgeschlossen hatten, konnten an einer Verlängerungsstudie mit bis zu 7 Jahren zusätzlicher Behandlung teilnehmen.
Tabelle 3. Zusammenfassung der klinischen Studien
Studientitel (Dauer) |
Population |
Therapiearme |
Zusammenfassung der wichtigsten Ergebnisparameter |
||
RA-BEGIN |
MTX-naiv 1 |
• |
Baricitinib 4 mg QD |
• |
Primärer Endpunkt: ACR20 in Woche 24 |
• |
Baricitinib 4 mg QD + MTX |
• |
Körperliche Funktion (HAQ-DI) |
||
• |
MTX |
• |
Radiologische Progression (mTSS) |
||
• |
Geringe Krankheitsaktivität und Remission (SDAI) |
||||
RA-BEAM |
MTX-IR 2 |
• |
Baricitinib 4 mg QD |
• |
Primärer Endpunkt: ACR20 in Woche 12 |
• |
Adalimumab 40 mg s.c. Q2W |
• |
Körperliche Funktion (HAQ-DI) |
||
• |
Placebo |
• |
Radiologische Progression (mTSS) |
||
Alle Patienten mit MTX-Begleittherapie |
• |
Geringe Krankheitsaktivität und Remission (SDAI) |
|||
• |
Morgendliche Gelenksteifigkeit |
||||
RA-BUILD |
cDMARD-IR 3 |
• |
Baricitinib 4 mg QD |
• |
Primärer Endpunkt: ACR20 in Woche 12 |
• |
Baricitinib 2 mg QD |
• |
Körperliche Funktion (HAQ-DI) |
||
• |
Placebo |
• |
Geringe Krankheitsaktivität und Remission (SDAI) |
||
Mit cDMARD-Begleittherapie 5, falls auf stabiler cDMARD-Therapie bei Studieneintritt |
• |
Radiologische Progression (mTSS) |
|||
• |
Morgendliche Gelenksteifigkeit |
||||
RA-BEACON |
TNF-IR 4 |
• |
Baricitinib 4 mg QD |
• |
Primärer Endpunkt: ACR20 in Woche 12 |
• |
Baricitinib 2 mg QD |
• |
Körperliche Funktion (HAQ-DI) |
||
• |
Placebo |
• |
Geringe Krankheitsaktivität und Remission (SDAI) |
||
Mit cDMARD-Begleittherapie 5 |
|||||
Abkürzungen: IR = Inadequate Responder; QD = einmal täglich; Q2W = einmal alle 2 Wochen; s.c. = subkutan; ACR = American College of Rheumatology; SDAI = Simplified Disease Activity Index; HAQ-DI = Health Assessment Questionnaire-Disability Index; mTSS = modified Total Sharp Score | |||||
1 |
Patienten, die weniger als 3 Dosen Methotrexat (MTX) erhalten hatten; ohne Vorbehandlung mit anderen konventionellen oder biologischen DMARDs |
2 |
Patienten mit unzureichendem Ansprechen (IR) auf MTX (+/- andere cDMARDs); ohne Vorbehandlung mit Biologika |
3 |
Patienten mit unzureichendem Ansprechen auf oder Unverträglichkeit gegen mindestens einen cDMARD; ohne Vorbehandlung mit Biologika |
4 |
Patienten mit unzureichendem Ansprechen auf oder Unverträglichkeit gegen mindestens einen bDMARD; einschließlich mindestens eines TNF-Inhibitors |
5 |
Die am häufigsten gleichzeitig eingesetzten cDMARDs schlossen MTX, Hydroxychloroquin, Leflunomid und Sulfasalazin ein. |
Klinisches Ansprechen
In allen Studien hatten die Patienten, die 4 mg Baricitinib einmal täglich erhielten, in Woche 12 statistisch signifikant höhere ACR20, ACR50 und ACR70-Ansprechraten als mit Placebo, Methotrexat (MTX) oder Adalimumab (Tabelle 4). Die Wirksamkeit trat für alle Parameter rasch ein, wobei ein signifikant stärkeres Ansprechen bereits nach Woche 1 beobachtet wurde. Es wurde ein anhaltendes und dauerhaftes Ansprechen beobachtet, wobei die ACR20/50/70-Ansprechenraten für mindestens 2 Jahre einschließlich der Verlängerungsstudie aufrechterhalten wurden.
Die Behandlung mit Baricitinib 4 mg allein oder in Kombination mit cDMARDs führte zu signifikanten Verbesserungen in allen einzelnen ACR-Komponenten, einschließlich der Anzahl der druckschmerzhaften und geschwollenen Gelenke, der Krankheitsaktivitätseinschätzung des Arztes und des Patienten, des HAQ-DI, der Schmerzbewertung und des CRP im Vergleich zu Placebo, MTX oder Adalimumab.
In den Untergruppen, definiert nach der Art der DMARD-Begleitmedikation, die gemeinsam mit Baricitinib angewendet wurde, konnten keine relevanten Unterschiede bezüglich Wirksamkeit und Sicherheit beobachtet werden.
Remission und geringe Krankheitsaktivität
Ein statistisch signifikant größerer Anteil der mit Baricitinib 4 mg behandelten Patienten erreichte im Vergleich zu jenen mit Placebo oder MTX eine Remission (SDAI ≤ 3,3 und CDAI ≤ 2,8) oder eine geringe Krankheitsaktivität oder eine Remission (DAS28-ESR oder DAS28-hsCRP ≤ 3,2 und DAS28-ESR oder DAS28-hsCRP < 2,6) in den Wochen 12 und 24 (Tabelle 4).
Höhere Remissionsraten im Vergleich zu Placebo wurden bereits ab Woche 4 beobachtet. Die Raten von Remission und geringer Krankheitsaktivität wurden für mindestens 2 Jahre aufrechterhalten. Daten aus der Langzeit-Verlängerungsstudie mit einem Follow-up von bis zu 6 Jahren deuten auf dauerhaft niedrige Krankheitsaktivitäts-/Remissionsraten hin.
Tabelle 4. Therapieansprechen, Remission und körperliche Funktionsfähigkeit
Studie |
RA-BEGIN |
RA-BEAM |
RA-BUILD |
RA-BEACON |
||||||||
Behandlungsgruppe |
MTX |
BARI |
BARI |
PBO |
BARI |
ADA |
PBO |
BARI |
BARI 4 mg |
PBO |
BARI 2 mg |
BARI |
N |
210 |
159 |
215 |
488 |
487 |
330 |
228 |
229 |
227 |
176 |
174 |
177 |
ACR20: | ||||||||||||
Woche 12 |
59 % |
79 %*** |
77 %*** |
40 % |
70 %***† |
61 %*** |
39 % |
66 %*** |
62 %*** |
27 % |
49 %*** |
55 %*** |
Woche 24 |
62 % |
77 %** |
78 %*** |
37 % |
74 %***† |
66 %*** |
42 % |
61 %*** |
65 %*** |
27 % |
45 %*** |
46 %*** |
Woche 52 |
56 % |
73 %*** |
73 %*** |
71 %†† |
62 % |
|||||||
ACR50: | ||||||||||||
Woche 12 |
33 % |
55 %*** |
60 %*** |
17 % |
45 %***†† |
35 %*** |
13 % |
33 %*** |
34 %*** |
8 % |
20 %** |
28 %*** |
Woche 24 |
43 % |
60 %** |
63 %*** |
19 % |
51 %*** |
45 %*** |
21 % |
41 %*** |
44 %*** |
13 % |
23 %* |
29 %*** |
Woche 52 |
38 % |
57 %*** |
62 %*** |
56 %† |
47 % |
|||||||
ACR70: | ||||||||||||
Woche 12 |
16 % |
31 %*** |
34 %*** |
5 % |
19 %***† |
13 %*** |
3 % |
18 %*** |
18 %*** |
2 % |
13 %*** |
11 %** |
Woche 24 |
21 % |
42 %*** |
40 %*** |
8 % |
30 %***† |
22 %*** |
8 % |
25 %*** |
24 %*** |
3 % |
13 %*** |
17 %*** |
Woche 52 |
25 % |
42 %*** |
46 %*** |
37 % |
31 % |
|||||||
DAS28-hsCRP ≤ 3,2: | ||||||||||||
Woche 12 |
30 % |
47 %*** |
56 %*** |
14 % |
44 %***†† |
35 %*** |
17 % |
36 %*** |
39 %*** |
9 % |
24 %*** |
32 %*** |
Woche 24 |
38 % |
57 %*** |
60 %*** |
19 % |
52 %*** |
48 %*** |
24 % |
46 %*** |
52 %*** |
11 % |
20 %* |
33 %*** |
Woche 52 |
38 % |
57 %*** |
63 %*** |
56 %† |
48 % |
|||||||
SDAI ≤ 3,3: | ||||||||||||
Woche 12 |
6 % |
14 %* |
20 %*** |
2 % |
8 %*** |
7 %*** |
1 % |
9 %*** |
9 %*** |
2 % |
2 % |
5 % |
Woche 24 |
11 % |
22 %** |
23 %*** |
3 % |
16 %*** |
14 %*** |
4 % |
17 %*** |
15 %*** |
2 % |
5 % |
9 %** |
Woche 52 |
13 % |
25 %** |
30 %*** |
23 % |
18 % |
|||||||
CDAI ≤ 2,8: | ||||||||||||
Woche 12 |
7 % |
14 %* |
19 %*** |
2 % |
8 %*** |
7 %** |
2 % |
10 %*** |
9 %*** |
2 % |
3 % |
6 % |
Woche 24 |
11 % |
21 %** |
22 %** |
4 % |
16 %*** |
12 %*** |
4 % |
15 %*** |
15 %*** |
3 % |
5 % |
9 %* |
Woche 52 |
16 % |
25 %* |
28 %** |
22 % |
18 % |
|||||||
HAQ-DI Minimale klinisch relevante Differenz (Reduktion des HAQ-DI Scores um ≥ 0,30): | ||||||||||||
Woche 12 |
60 % |
81 %*** |
77 %*** |
46 % |
68 %*** |
64 %*** |
44 % |
60 %*** |
56 %** |
35 % |
48 %* |
54 %*** |
Woche 24 |
66 % |
77 %* |
74 % |
37 % |
67 %***† |
60 %*** |
37 % |
58 %*** |
55 %*** |
24 % |
41 %*** |
44 %*** |
Woche 52 |
53 % |
65 %* |
67 %** |
61 % |
55 % |
|||||||
Anmerkung: Der Anteil der Responder bezieht sich zu jedem Zeitpunkt auf die Anzahl der ursprünglich behandlungsrandomisierten Patienten (N). Patienten, die abbrachen oder eine Rescue-Therapie erhielten, wurden ab dann den Non-Respondern zugeordnet. | ||||||||||||
* |
p ≤ 0,05; |
** |
p ≤ 0,01; |
*** |
p ≤ 0,001 vs. Placebo (vs. MTX für Studie RA-BEGIN) |
† |
p ≤ 0,05; |
†† |
p ≤ 0,01; |
††† |
p ≤ 0,001 vs. Adalimumab |
Radiologisches Ansprechen
Die Wirkung von Baricitinib auf die Progression von strukturellen Gelenkschäden wurde in den Studien RA-BEGIN, RA-BEAM und RA-BUILD radiologisch untersucht und anhand des modifizierten Total Sharp Score (mTSS) und seiner Komponenten, dem Erosions-Score und dem Score für Gelenksspaltverengung, bewertet.
Die Behandlung mit Baricitinib 4 mg führte zu einer statistisch signifikanten Hemmung der Progression von strukturellen Gelenkschäden (Tabelle 5). Analysen des Erosion-Scores und des Scores für eine Gelenksspaltverengung waren konsistent mit den Gesamtscores. Der Prozentsatz der Patienten ohne radiologische Progression (Veränderung im mTSS ≤ 0) war in den Wochen 24 und 52 mit Baricitinib 4 mg signifikant höher als mit Placebo.
Tabelle 5. Radiologische Veränderungen
Studie |
RA-BEGIN |
RA-BEAM |
RA-BUILD |
||||||
Behandlungsgruppe |
MTX |
BARI 4 mg |
BARI 4 mg |
PBO a |
BARI 4 mg |
ADA 40 mg Q2W |
PBO |
BARI 2 mg |
BARI 4 mg |
Modifizierter Total Sharp Score, mittlere Veränderung gegenüber Ausgangswert: | |||||||||
Woche 24 |
0,61 |
0,39 |
0,29 * |
0,90 |
0,41 *** |
0,33 *** |
0,70 |
0,33 * |
0,15 ** |
Woche 52 |
1,02 |
0,80 |
0,40 ** |
1,80 |
0,71 *** |
0,60 *** |
|||
Prozentsatz der Patienten ohne radiologische Progression b: | |||||||||
Woche 24 |
68 % |
76 % |
81 % ** |
70 % |
81 % *** |
83 % *** |
74 % |
72 % |
80 % |
Woche 52 |
66 % |
69 % |
80 % ** |
70 % |
79 % ** |
81 % ** |
|||
Abkürzungen: ADA = Adalimumab; BARI = Baricitinib; IR = Inadequate Responder; | |||||||||
a |
Placeboraten in Woche 52 wurden mittels linearer Extrapolation abgeleitet |
||||
b |
Keine Progression, definiert als mTSS-Veränderung ≤ 0. |
||||
* |
p ≤ 0,05; |
** |
p ≤ 0,01; |
*** |
p ≤ 0,001 vs. Placebo (vs. MTX für Studie RA-BEGIN) |
Ansprechen der körperlichen Funktionsfähigkeit und der gesundheitsbezogenen Outcome-Parameter
Die Behandlung mit Baricitinib 4 mg als Mono- oder Kombinationstherapie mit cDMARDs führte zu einer signifikanten Verbesserung der körperlichen Funktionsfähigkeit (HAQ-DI) und Schmerzen (visuelle Analogskala 0-100) im Vergleich zu allen Vergleichspräparaten (Placebo, MTX, Adalimumab). Verbesserungen wurden bereits nach Woche 1 beobachtet und konnten in den Studien RA-BEGIN und RA-BEAM bis zu 52 Wochen aufrechterhalten werden.
In den Studien RA-BEAM und RA-BUILD resultierte die Behandlung mit Baricitinib 4 mg verglichen mit Placebo oder Adalimumab in einer signifikanten Verbesserung der mittleren Dauer und des Schweregrades der morgendlichen Gelenksteifigkeit, bewertet mittels elektronischer Patiententagebücher.
In allen Studien berichteten mit Baricitinib behandelte Patienten von Verbesserungen bei der Lebensqualität, gemessen anhand des Short Form (36) Health Survey (SF‑36) Physical Component Score und bei Fatigue, gemessen anhand des Functional Assessment of Chronic Illness Therapy-Fatigue-Scores (FACIT-F).
Baricitinib 4 mg vs. 2 mg
Unterschiede in der Wirksamkeit zwischen der 4 mg- und der 2 mg-Dosierung waren in der Population bDMARD-Inadequate Responder (IR) (RA-BEACON) am auffälligsten, in welcher statistisch signifikante Verbesserungen bei den ACR-Komponenten der Anzahl der geschwollenen Gelenke, der Anzahl der druckschmerzhaften Gelenke und bei ESR für Baricitinib 4 mg im Vergleich zu Placebo in Woche 24 gezeigt werden konnten, nicht jedoch für Baricitinib 2 mg im Vergleich zu Placebo. Zudem erfolgte in den beiden Studien RA-BEACON und RA-BUILD bei den Gruppen mit einer Dosis von 4 mg der Eintritt der Wirksamkeit am raschesten, und die Effektstärke war für die Dosis von 4 mg im Vergleich zu 2 mg generell größer.
In einer Verlängerungsstudie wurden Patienten aus den Studien RA-BEAM, RA-BUILD und RA-BEACON, die nach mindestens 15 Monaten Behandlung mit Baricitinib 4 mg einmal täglich eine anhaltend niedrige Krankheitsaktivität oder Remission (CDAI ≤ 10) erreichten, im Verhältnis 1:1 und in doppelblinder Form für eine Fortsetzung der Behandlung mit 4 mg einmal täglich oder für eine reduzierte Dosis von 2 mg einmal täglich randomisiert. Bei einem Großteil der Patienten blieb eine geringe Krankheitsaktivität oder Remission basierend auf dem CDAI-Score erhalten:
• |
In Woche 12: 451/498 (91 %) mit fortgesetzter 4 mg-Dosierung vs. 405/498 (81 %) mit auf 2 mg reduzierte Dosis (p ≤ 0,001) |
• |
In Woche 24: 434/498 (87 %) mit fortgesetzter 4 mg-Dosierung vs. 372/498 (75 %) mit auf 2 mg reduzierte Dosis (p ≤ 0,001) |
• |
In Woche 48: 400/498 (80 %) mit fortgesetzter 4 mg-Dosierung vs. 343/498 (69 %) mit auf 2 mg reduzierte Dosis (p ≤ 0,001) |
• |
In Woche 96: 347/494 (70 %) mit fortgesetzter 4 mg-Dosierung vs. 297/496 (60 %) mit auf 2 mg reduzierte Dosis (p ≤ 0,001) |
Ein Großteil der Patienten, die die geringe Krankheitsaktivität oder den Remissionsstatus nach der Dosisreduktion eingebüßt hatten, konnte die Kontrolle über den Krankheitsverlauf wiedererlangen, nachdem die Dosis wieder auf 4 mg angehoben wurde.
Atopische Dermatitis bei Erwachsenen
Die Wirksamkeit und Sicherheit von Baricitinib als Monotherapie oder in Kombination mit topischen Kortikosteroiden (TCS) wurde in drei randomisierten, doppelblinden, placebokontrollierten Phase-III-Studien (BREEZE-AD1, -AD2 und -AD7) über 16 Wochen untersucht. Die Studien schlossen 1 568 Patienten mit mittelschwerer bis schwerer atopischer Dermatitis ein. Diese wurde definiert als ein Wert ≥ 3 gemäß IGA (Investigator’s Global Assessment), ein Wert ≥ 16 gemäß EASI (Eczema Area and Severity Index) und eine betroffene Körperoberfläche (Body Surface Area, BSA) ≥ 10 %. Geeignete Patienten waren über 18 Jahre alt und wiesen zuvor ein unzureichendes Ansprechen oder eine Unverträglichkeit gegenüber topischen Arzneimitteln auf. Patienten konnten eine Rescue-Therapie erhalten (die eine topische oder systemische Therapie beinhaltete), woraufhin diese Patienten im Rahmen der jeweiligen Studien den Non-Respondern zugeordnet wurden. Zum Beginn der Studie BREEZE-AD7 erhielten alle Patienten eine Begleittherapie mit topischen Kortikosteroiden und durften topische Calcineurin-Inhibitoren anwenden. Alle Patienten, die diese Studien abgeschlossen hatten, konnten an einer Verlängerungsstudie (BREEZE AD-3) mit bis zu 4 Jahren fortlaufender Behandlung teilnehmen.
In der randomisierten, doppelblinden, placebokontrollierten Phase-III-Studie BREEZE-AD4 wurde die Wirksamkeit von Baricitinib in Kombination mit topischen Kortikosteroiden über 52 Wochen bei 463 Patienten mit mittelschwerer bis schwerer atopischer Dermatitis, die ein Versagen, eine Unverträglichkeit oder eine Kontraindikation gegen eine orale Ciclosporin-Behandlung aufwiesen, untersucht.
Patientencharakteristika bei Baseline
In den placebokontrollierten Phase-III-Studien (BREEZE-AD1, -AD2, -AD7 und -AD4) waren behandlungsgruppenübergreifend 37 % der Studienteilnehmer weiblich, 64 % Kaukasier, 31 % Asiaten, 0,6 % Schwarze und das mittlere Alter lag bei 35,6 Jahren. In diesen Studien hatten 42 % bis 51 % der Patienten einen IGA-Ausgangswert von 4 (schwere atopische Dermatitis) und 54 % bis 79 % der Patienten hatten bereits eine systemische Behandlung ihrer atopischen Dermatitis erhalten. Zum Studienbeginn betrug der mittlere EASI-Wert zwischen 29,6 und 33,5, der wöchentliche Durchschnittswert gemäß Pruritus Numerical Rating Scale (NRS) zwischen 6,5 und 7,1, der mittlere Dermatology Life Quality Index (DLQI) zwischen 13,6 und 14,9 und der mittlere Hospital Anxiety and Depression Scale (HADS)-Gesamtwert zwischen 10,9 und 12,1.
Klinisches Ansprechen
16-wöchige Monotherapie (BREEZE-AD1, -AD2) und TCS Kombination (BREEZE-AD7) Studien:
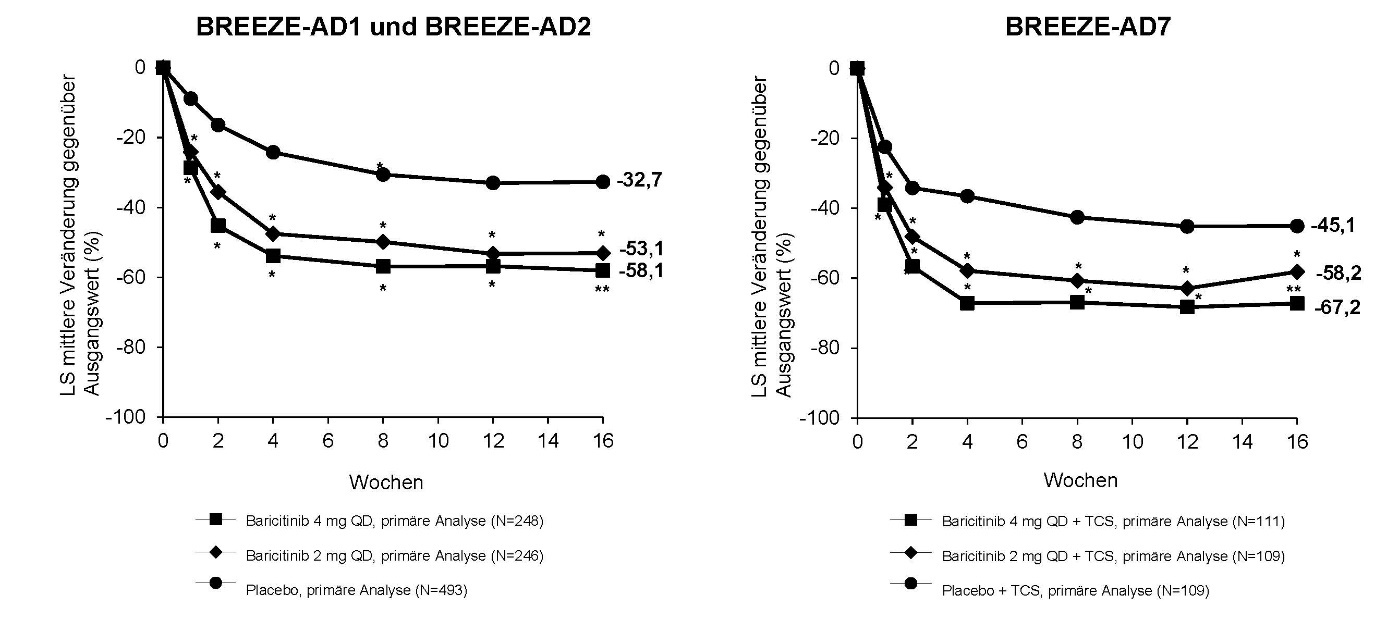
Ein signifikant höherer Anteil an Patienten, die auf Baricitinib 4 mg randomisiert wurden, erreichte ein IGA-Ansprechen von 0 oder 1 (primärer Endpunkt), ein EASI-75-Ansprechen, oder eine Verbesserung um ≥ 4 Punkte auf der Pruritus NRS im Vergleich zu Placebo in Woche 16 (Tabelle 6). Abbildung 1 zeigt die mittlere prozentuale Veränderung der EASI-Werte vom Ausgangswert bis Woche 16.
Im Vergleich zu Placebo erreichte ein signifikant höherer Anteil an Patienten, die auf Baricitinib 4 mg randomisiert wurden, eine ≥ 4 Punkte Verbesserung auf der Pruritus NRS (innerhalb der ersten Behandlungswoche für BREEZE-AD1 und -AD2, und bereits in Woche 2 für BREEZE-AD7; p < 0,002).
Die Behandlungseffekte in den Untergruppen (Gewicht, Alter, Geschlecht, ethnische Herkunft, Schweregrad der Erkrankung und Vortherapie, einschließlich Immunsuppressiva) waren mit den Ergebnissen der gesamten Studienpopulation konsistent.
Tabelle 6. Wirksamkeit von Baricitinib in Woche 16 (FAS a)
Monotherapie |
TCS-Kombination |
||||||||
Studie |
BREEZE-AD1 |
BREEZE-AD2 |
BREEZE-AD7 |
||||||
Behandlungsgruppe |
PBO |
BARI |
BARI |
PBO |
BARI |
BARI |
PBO + TCS |
BARI 2 mg + TCS |
BARI |
N |
249 |
123 |
125 |
244 |
123 |
123 |
109 |
109 |
111 |
IGA 0 oder 1, |
4,8 |
11,4 ** |
16,8 ** |
4,5 |
10,6 ** |
13,8 ** |
14,7 |
23,9 |
30,6 ** |
EASI-75, |
8,8 |
18,7 ** |
24,8 ** |
6,1 |
17,9 ** |
21,1 ** |
22,9 |
43,1 * |
47,7 ** |
Pruritus NRS |
7,2 |
12,0 |
21,5 ** |
4,7 |
15,1 ** |
18,7 ** |
20,2 |
38,1 * |
44,0 ** |
BARI = Baricitinib; PBO = Placebo | |||||||||
* |
Statistisch signifikant vs. Placebo ohne Adjustierung für Mehrfachtestung; ** Statistisch signifikant vs. Placebo mit Adjustierung für Mehrfachtestung. |
|
a |
Der Gesamtanalyse-Datensatz FAS (Full Analysis Set) umfasst alle randomisierten Patienten. |
|
b |
Responder wurde definiert als ein Patient mit IGA 0 oder 1 („erscheinungsfrei“ oder „fast erscheinungsfrei“) und einer Verbesserung um ≥ 2 Punkte auf der von 0 bis 4 reichenden IGA-Skala. |
|
c |
Non-Responder Imputation: Patienten, die eine Rescue-Therapie erhielten oder bei denen Daten fehlten, wurden den Non-Respondern zugeordnet. |
|
d |
Ergebnisse zeigen die Untergruppe von Patienten, die sich zur Beurteilung eigneten (Patienten mit Pruritus NRS Ausgangswert ≥ 4). |
|
Abbildung 1. Mittlere prozentuale EASI-Verbesserung gegenüber Ausgangswert (FAS) a
LS = Methode der kleinsten Quadrate, * Statistisch signifikant vs. Placebo ohne Adjustierung | |
für Mehrfachtestung; ** Statistisch signifikant vs. Placebo mit Adjustierung für Mehrfachtestung. | |
a |
Der Gesamtanalyse-Datensatz (FAS) umfasst alle randomisierten Patienten. Daten, die nach Rescue-Therapie oder nach dauerhaftem Absetzen des Arzneimittels gesammelt wurden, wurden als fehlend eingestuft. LS-Mittelwerte stammen von gemischtem Modell mit Messwiederholungen (Mixed Model with Repeated Measures (MMRM))-Analysen. |
Aufrechterhalten des Ansprechens
Um das Aufrechterhalten des Ansprechens zu bewerten, konnten 1 398 Studienteilnehmer, die in den BREEZE-AD1 (N = 566), BREEZE-AD2 (N = 540) und BREEZE-AD7 (N = 292) Studien 16 Wochen mit Baricitinib behandelt wurden, an der Verlängerungsstudie BREEZE-AD3 teilnehmen. Es liegen Daten von bis zu 4 Jahren (216 Wochen) kumulativer Behandlung vor. Ein anhaltendes Ansprechen wurde bei Patienten mit einem Ansprechen (IGA 0, 1 oder 2) nach Behandlungsbeginn mit Baricitinib beobachtet.
Dosisreduktion
In der Langzeit-Verlängerungsstudie BREEZE-AD3 wurden Patienten, die mit Baricitinib 4 mg einmal täglich eine erscheinungsfreie Haut, eine nahezu erscheinungsfreie Haut oder eine milde Erkrankung (d. h. IGA 0, 1 oder 2) aufwiesen, in Woche 52 erneut randomisiert, um entweder die Therapie mit 4 mg einmal täglich fortzusetzen oder die Dosis auf 2 mg einmal täglich zu reduzieren. Von den Patienten, die die Dosis auf 2 mg reduzierten, hatten 37 % ein IGA-Ansprechen von 0, 1 oder 2 und 52 % ein EASI75-Ansprechen in Woche 200. In dieser Gruppe zeigten 47 % der Patienten in Woche 52 eine Verbesserung des Pruritus NRS ≥ 4 Punkte, und 40 % zeigten diese Verbesserung in Woche 68. Der Anteil an Patienten mit einem Rückfall (IGA ≥ 3) war in der Untergruppe der Patienten, die zu Beginn der Dosisreduktion eine erscheinungsfreie Haut oder eine nahezu erscheinungsfreie Haut (IGA 0 oder 1) aufwiesen, geringer. Bei Patienten, bei denen ein Rückfall (IGA ≥ 3) nach Dosisreduktion auftrat, erlangte die Mehrheit nach erneuter Behandlung mit Baricitinib 4 mg die Krankheitskontrolle wieder.
Lebensqualität / Patienten-berichtete Endpunkte bei atopischer Dermatitis
Im Vergleich zu Placebo verbesserte Baricitinib 4 mg sowohl in beiden Monotherapie-Studien (BREEZE-AD1 und BREEZE-AD2) als auch in der Kombinationsstudie mit TCS (BREEZE-AD 7) in Woche 16 die von Patienten-berichteten Endpunkte einschließlich Pruritus NRS, Schlaf (ADSS), Hautschmerzen (Hautschmerz NRS), Lebensqualität (DLQI) und Symptomen von Angst und Depression (HADS), welche für Mehrfachtestung nicht adjustiert wurden, in Woche 16 signifikant (siehe Tabelle 7).
Tabelle 7. Lebensqualität/Patienten-berichtete Endpunkte von Baricitinib Monotherapie und
Baricitinib in Kombination mit TCS in Woche 16 (FAS) a
Monotherapie |
TCS-Kombination |
|||||||||||
Studie |
BREEZE-AD1 |
BREEZE-AD2 |
BREEZE-AD7 |
|||||||||
Behandlungsgruppe |
PBO |
BARI |
BARI |
PBO |
BARI |
BARI |
PBO + TCS |
BARI |
BARI |
|||
N |
249 |
123 |
125 |
244 |
123 |
123 |
109 |
109 |
111 |
|||
ADSS Item 2 |
12,8 |
11,4 |
32,7 * |
8,0 |
19,6 |
24,4 * |
30,6 |
61,5 * |
66,7 * |
|||
Veränderung des Hautschmerz NRS, Mittelwert (SE) b |
-0,84 |
-1,58 |
-1,93 ** |
-0,86 |
-2,61 ** |
-2,49 ** |
-2,06 |
-3,22 * (0,22) |
-3,73 * |
|||
Veränderung des DLQI, |
-2,46 |
-4,30 * |
-6,76 * |
-3,35 |
-7,44 * |
-7,56 * |
-5,58 |
-7,50 * |
-8,89 * |
|||
Veränderung des HADS, |
-1,22 |
-3,22 * |
-3,56 * |
-1,25 |
-2,82 |
-3,71 * |
-3,18 |
-4,75 * |
-5,12 * |
|||
BARI = Baricitinib; PBO = Placebo | ||||||||||||
* |
Statistisch signifikant vs. Placebo ohne Adjustierung für Mehrfachtestung; ** Statistisch signifikant vs. Placebo mit Adjustierung für Mehrfachtestung. |
a |
Der Gesamtanalyse-Datensatz (FAS) umfasst alle randomisierten Patienten. |
b |
Dargestellte Ergebnisse sind mittlere LS-Veränderungen gegenüber Ausgangswert (SE). Daten, die nach Rescue-Therapie oder nach dauerhaftem Absetzen des Arzneimittels gesammelt wurden, wurden als fehlend eingestuft. LS-Mittelwerte stammen von MMRM-Analysen. |
c |
ADSS Item 2: Anzahl an nächtlichem Aufwachen wegen Pruritus. |
d |
Non-Responder-Imputation: Patienten, die eine Rescue-Therapie erhielten oder bei denen Daten fehlten, wurden den Non-Respondern zugeordnet. Ergebnisse zeigen die Untergruppe von Patienten, die sich zur Beurteilung eigneten (Patienten mit ADSS Item 2 ≥ 2 zum Ausgangswert). |
Klinisches Ansprechen bei Patienten, die Erfahrung mit oder eine Kontraindikation gegen eine Ciclosporin-Behandlung hatten (BREEZE-AD4 Studie)
Insgesamt waren 463 Patienten eingeschlossen, die ein Versagen (N = 173), eine Unverträglichkeit (N = 75) oder eine Kontraindikation (N = 126) gegen eine orale Ciclosporin-Behandlung aufwiesen. Der primäre Endpunkt war der Anteil an Patienten, die ein EASI-75-Ansprechen in Woche 16 erreichten. Der primäre Endpunkt und einige der wichtigsten sekundären Endpunkte in Woche 16 sind in Tabelle 8 zusammengefasst.
Tabelle 8. Wirksamkeit von Baricitinib in Kombination mit TCS a in Woche 16 in der BREEZE-AD4 Studie (FAS) b
Studie |
BREEZE-AD4 |
||
Behandlungsgruppe |
PBO a |
BARI 2 mg a |
BARI 4 mg a |
N |
93 |
185 |
92 |
EASI-75, |
17,2 |
27,6 |
31,5 ** |
IGA 0 oder 1, |
9,7 |
15,1 |
21,7 * |
Pruritus NRS (≥ 4-Punkt Verbesserung), |
8,2 |
22,9 * |
38,2 ** |
DLQI, mittlere Veränderung (SE) d |
-4,95 (0,752) |
-6,57 (0,494) |
-7,95 * (0,705) |
BARI = Baricitinib; PBO = Placebo | |||
* |
Statistisch signifikant vs. Placebo ohne Adjustierung für Mehrfachtestung; ** Statistisch signifikant vs. Placebo mit Adjustierung für Mehrfachtestung. |
|
a |
Alle Patienten erhielten eine Begleittherapie mit topischen Kortikosteroiden, auch topische Calcineurin-Inhibitoren waren erlaubt. |
|
b |
Der Gesamtanalyse-Datensatz (FAS) umfasst alle randomisierten Patienten. |
|
c |
Non-Responder Imputation: Patienten, die Rescue-Therapie erhielten oder bei denen Daten fehlten, wurden den Non-Respondern zugeordnet. |
|
d |
Daten, die nach Rescue-Therapie oder nach dauerhaftem Absetzen des Arzneimittels gesammelt wurden, wurden als fehlend eingestuft. LS-Mittelwerte stammen von MMRM-Analysen. |
|
e |
Responder wurde definiert als ein Patient mit IGA 0 oder 1 („erscheinungsfrei“ oder „fast erscheinungsfrei“) und mit einer Reduktion ≥ 2 Punkte auf einer von 0 bis 4 reichenden IGA-Skala. |
|
f |
Ergebnisse zeigen die Untergruppe von Patienten, die sich zur Beurteilung eigneten (Patienten mit Pruritus NRS Ausgangswert ≥ 4). |
|
Alopecia areata bei Erwachsenen
Die Wirksamkeit und Sicherheit von Baricitinib einmal täglich wurden in einer adaptiven Phase-II/III-Studie (BRAVE-AA1) und einer Phase-III-Studie (BRAVE-AA2) untersucht. Der Phase-III-Teil der BRAVE-AA1-Studie und die Phase-III-BRAVE-AA2-Studie waren randomisierte, doppelblinde, placebokontrollierte, 36-wöchige Studien mit Verlängerungsphasen von bis zu 200 Wochen. In beiden Phase-III-Studien wurden die Patienten auf Placebo, 2 mg oder 4 mg Baricitinib im Verhältnis 2:2:3 randomisiert. In die Studien eingeschlossene Patienten waren Männer zwischen 18 und 60 Jahren und Frauen zwischen 18 und 70 Jahren mit einer aktuellen Episode von mehr als 6 Monaten schwerer Alopecia areata (Haarausfall ≥ 50 % der Kopfhaut). Patienten mit einer aktuellen Episode von mehr als 8 Jahren Dauer wurden nicht eingeschlossen, es sei denn es wurden in den letzten 8 Jahren Episoden erneuten Haarwachstums auf den betroffenen Bereichen der Kopfhaut beobachtet. Die einzigen zulässigen Begleittherapien zur Behandlung der Alopecia areata waren Finasterid (oder andere 5-Alpha-Reduktase-Hemmer), Minoxidil zur oralen bzw. topischen Anwendung und Bimatoprost-Augenlösung für Wimpern, unter der Bedingung einer stabilen Dosis bei Studienbeginn.
Beide Studien bewerteten als primären Endpunkt den Anteil der Patienten, die in Woche 36 einen SALT (Severity of Alopecia Tool)-Score von ≤ 20 (mindestens 80 % der Kopfhaut mit Haaren bedeckt) erreichten. Zusätzlich wurde in beiden Studien eine klinische Beurteilung des Augenbrauen- und Wimpernverlusts anhand einer 4-Punkte Skala vorgenommen (ClinRO Measure for Eyebrow Hair Loss™, ClinRO Measure for Eyelash Hair Loss™).
Patientencharakteristika bei Baseline
Der Phase-III-Teil der BRAVE-AA1-Studie und die Phase-III-BRAVE-AA2-Studie umfassten 1 200 erwachsene Patienten. Über alle Behandlungsgruppen hinweg betrug das Durchschnittsalter 37,5 Jahre und 61 % der Patienten waren weiblich. Die durchschnittliche Erkrankungsdauer seit Beginn der Alopecia areata und die durchschnittliche Dauer der aktuellen Haarausfallepisode betrugen 12,2 bzw. 3,9 Jahre. Der studienübergreifende Median des SALT-Scores betrug 96 (entspricht 96 % Haarausfall der Kopfhaut) und bei ungefähr 44 % der Patienten wurde Alopecia universalis berichtet. Studienübergreifend hatten bei Baseline 69 % der Patienten signifikanten oder vollständigen Verlust der Augenbrauen und 58 % hatten signifikanten oder vollständigen Verlust der Wimpern, gemessen anhand der ClinRO-Skalen für Augenbrauen und Wimpern, mit Scores von 2 bzw. 3. Vor Studieneintritt hatten ungefähr 90 % der Patienten zumindest eine Behandlung für Alopecia areata erhalten und bei 50 % wurde zumindest ein systemisches Immunsuppressivum angewendet. Die Anwendung zugelassener Begleittherapien zur Behandlung der Alopecia areata wurde während der Studien nur von 4,3 % der Patienten angegeben.
Klinisches Ansprechen
In beiden Studien erreichte im Vergleich zu Placebo ein signifikant größerer Anteil der Patienten, die auf Baricitinib 4 mg einmal täglich randomisiert wurden, einen SALT-Score von ≤ 20 in Woche 36, beginnend bereits in Woche 8 in Studie BRAVE-AA1 und Woche 12 in Studie BRAVE-AA2. Bei den meisten sekundären Endpunkten wurde eine konsistente Wirksamkeit beobachtet (Tabelle 9). Abbildung 2 zeigt den Anteil der Patienten, die bis Woche 36 einen SALT-Score von ≤ 20 erreichten.
Die Behandlungseffekte in den Untergruppen (Geschlecht, Alter, Gewicht, eGFR, ethnische Zugehörigkeit, geografische Region, Schweregrad der Erkrankung, Dauer der aktuellen Alopecia areata-Episode) waren mit den Ergebnissen in der gesamten Studienpopulation in Woche 36 konsistent.
Tabelle 9. Wirksamkeit von Baricitinib bis Woche 36 für gepoolte Studien (gepoolte Wirksamkeitspopulationa in Woche 36)
BRAVE-AA1 (Phase-III-Teil einer Phase-II/III-Studie) und BRAVE-AA2 (Phase-III-Studie) gepoolte Daten * |
|||
Placebo |
Baricitinib 2 mg |
Baricitinib 4 mg |
|
SALT ≤ 20 in Woche 36 |
4,1 % |
19,7 % ** |
34,0 % ** |
SALT ≤ 20 in Woche 24 |
3,2 % |
11,2 % |
27,4 % ** |
ClinRO-Score für Augenbrauenverlust von 0 oder 1 in Woche 36 mit einer ≥ 2 Punkte Verbesserung gegenüber dem Ausgangswert b |
3,8 % |
15,8 % |
33,0 % ** |
ClinRO-Score für Wimpernverlust von 0 oder 1 in Woche 36 mit einer ≥ 2 Punkte Verbesserung gegenüber dem Ausgangswert b |
4,3 % |
12,0 % |
33,9 % ** |
Änderung im Skindex-16, angepasst für Alopecia areata-Emotionsdomäne, Mittelwert (SE) c |
-11,33 (1,768) |
-19,89 (1,788) |
-23,81 (1,488) |
Änderung im Skindex-16, angepasst für Alopecia areata-Funktionsdomäne, Mittelwert (SE) c |
-9,26 (1,605) |
-13,68 (1,623) |
-16,93 (1,349) |
ClinRO = clinician-reported outcome; SE = Standardfehler | |||
a |
Gepoolte Wirksamkeitspopulation in Woche 36: Alle Patienten, die in den Phase-III-Teil der Studie BRAVE-AA1 und in die Studie BRAVE-AA2 eingeschlossen waren. |
* |
Die Ergebnisse der gepoolten Analyse waren mit denen der Einzelstudien konsistent. |
** |
Statistisch signifikant mit Adjustierung für Mehrfachtestung im grafischen Testschema innerhalb der jeweiligen Studie. |
b |
Patienten mit ClinRO-Score für Augenbrauenverlust von ≥ 2 zu Studienbeginn: 236 (Placebo), 240 (Baricitinib 2 mg), 349 (Baricitinib 4 mg). Patienten mit einem ClinRO-Score für Wimpernverlust von ≥ 2 zu Studienbeginn: 186 (Placebo), 200 (Baricitinib 2 mg), 307 (Baricitinib 4 mg). Beide ClinRO-Messungen verwenden eine 4-Punkte-Skala, die von 0 bis 3 reicht, wobei 0 kein Haarverlust und 3 keine erkennbaren Augenbrauen bzw. Wimpern bedeutet. |
c |
Die Größe der Analysepopulation in Bezug auf den Skindex-16, angepasst für Alopecia areata, in Woche 36 ist n = 256 (Placebo), 249 (Baricitinib 2 mg), 392 (Baricitinib 4 mg). |
Abbildung 2: Anteil der Patienten mit SALT ≤ 20 bis Woche 36
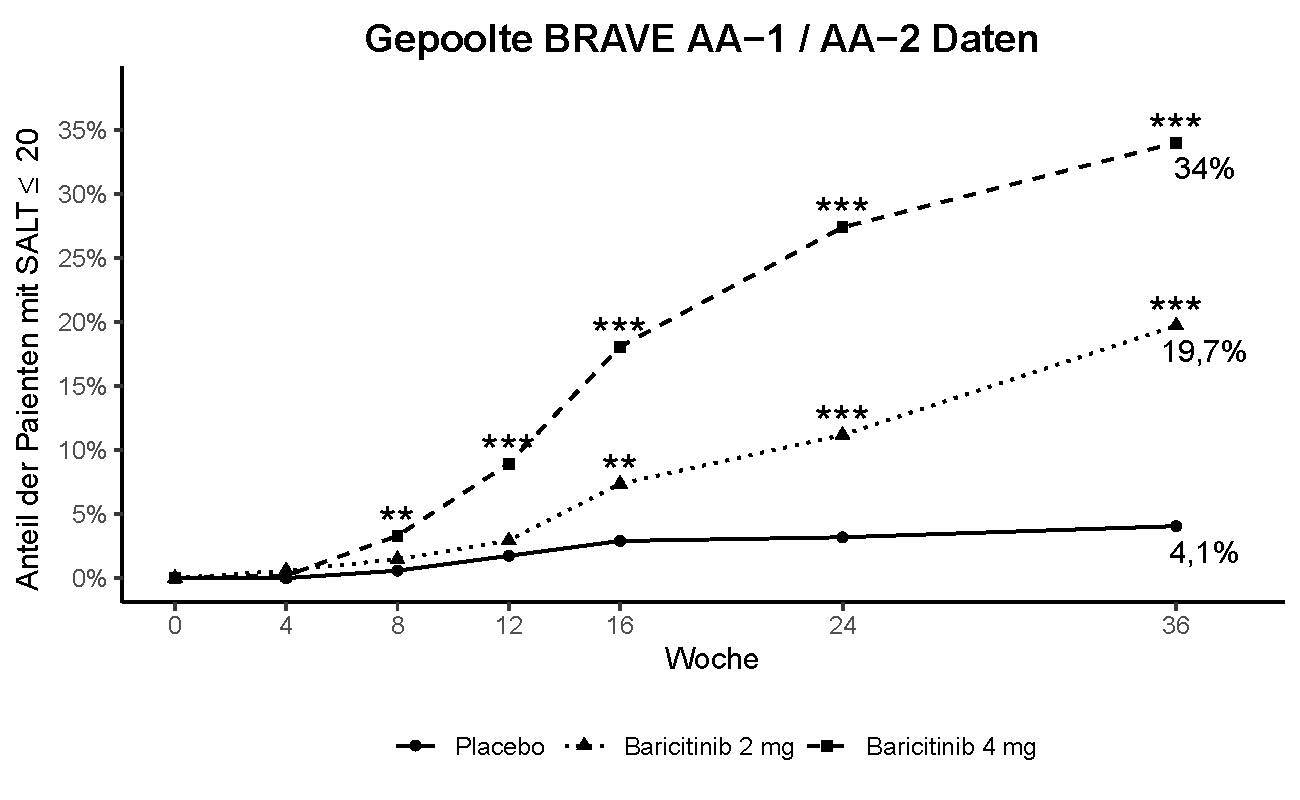
** p-Wert für Baricitinib versus Placebo ≤ 0,01; *** p-Wert für Baricitinib versus Placebo ≤ 0,001. |
Wirksamkeit bis Woche 52
Der Anteil der mit Baricitinib behandelten Patienten mit einem SALT-Score von ≤ 20 stieg nach Woche 36 weiter an und wurde in Woche 52 von 39,0 % der Patienten unter Baricitinib 4 mg erreicht. Die Ergebnisse für die Subpopulationen bezüglich Schweregrad der Erkrankung zu Studienbeginn und Episodendauer waren in Woche 52 mit den in Woche 36 beobachteten Ergebnissen und mit den Ergebnissen in der gesamten Studienpopulation konsistent.
Teilstudie zur Dosisreduktion
In der Studie BRAVE-AA2 wurden Patienten, die seit der ersten Randomisierung Baricitinib 4 mg einmal täglich erhalten hatten und in Woche 52 einen SALT-Score von ≤ 20 erreichten, erneut in doppelblinder Form randomisiert, um die Behandlung mit 4 mg einmal täglich fortzusetzen oder die Dosis auf 2 mg einmal täglich zu reduzieren. Die Ergebnisse zeigen, dass 96 % der Patienten, die weiterhin Baricitinib 4 mg erhielten, und 74 % der Patienten, die auf Baricitinib 2 mg randomisiert wurden, ihr Ansprechen in Woche 76 aufrechterhalten konnten.
Juvenile idiopathische Arthritis
Das klinische Entwicklungsprogramm von Baricitinib für juvenile idiopathische Arthritis bestand aus einer abgeschlossenen pivotalen Phase-III-Studie (JUVE-BASIS) und einer unverblindeten Langzeit-Sicherheits-Follow-up Studie (JUVE-X).
Bei JUVE-BASIS handelte es sich um eine bis zu 44 Wochen andauernde, doppelblinde, randomisierte, Placebo-kontrollierte Absetzstudie (DBW - double-blind withdrawal), um die Wirksamkeit und Sicherheit von Baricitinib bei einmal täglicher Anwendung bei Patienten im Alter von 2 bis unter 18 Jahren mit juveniler idiopathischer Arthritis zu evaluieren, die unzureichend auf die Behandlung mit mindestens einem herkömmlichen synthetischen oder biologischen DMARD angesprochen oder diese nicht vertragen haben. Eingeschlossen waren Patienten mit polyartikulärer juveniler idiopathischer Arthritis (Rheumafaktor positiv oder Rheumafaktor negativ), juveniler idiopathischer Arthritis mit erweitertem oligoartikulärem Verlauf, Enthesitis-assoziierter juveniler idiopathischer Arthritis und juveniler Psoriasis-Arthritis gemäß den Kriterien der International League of Associations for Rheumatology (ILAR). Patienten, die an JUVE-BASIS teilnahmen, konnten in die Studie JUVE-X eingeschlossen werden.
Bei JUVE-BASIS erhielten die Patienten ab Studienbeginn etwa 12 Wochen lang einmal täglich unverblindet Baricitinib. Patienten im Alter von 2 bis unter 9 Jahren erhielten 2 mg täglich und Patienten im Alter von 9 bis unter 18 Jahren erhielten 4 mg täglich, um die äquivalente Dosis zu 4 mg bei Erwachsenen zu erreichen. In Woche 12 wurde das Ansprechen auf die Behandlung (basierend auf den PedACR30-Kriterien) für jeden Patienten überprüft. Patienten, die mindestens ein PedACR30-Ansprechen erreichten, wurden randomisiert (Verhältnis 1:1) und erhielten entweder Placebo oder blieben in der 32-wöchigen doppelblinden, placebokontrollierten Phase mit der gleichen Baricitinib-Dosis. Patienten, die PedACR30 nicht erreichten, hatten die Möglichkeit, in die Studie JUVE-X eingeschlossen zu werden.
In der Studie JUVE-BASIS war der primäre Endpunkt zur Wirksamkeit die Zeit bis zum nächsten Krankheitsschub innerhalb der doppelblinden Studienphase.
Patientencharakteristika bei Baseline
Insgesamt wurden 220 Patienten in JUVE-BASIS eingeschlossen. Davon kamen 163 (74,4 %) Patienten in die doppelblinden Studienphase und wurden auf Baricitinib (n = 82) oder Placebo (n = 81) randomisiert. Es gab 144 Patienten mit polyartikulärer juveniler idiopathischer Arthritis, 16 mit erweiterter oligoartikulärer juveniler idiopathischer Arthritis, 50 mit Enthesitis-assoziierter juveniler idiopathischer Arthritis und 10 mit juveniler Psoriasis-Arthritis.
Bei JUVE-BASIS lag das Durchschnittsalter bei 13 Jahren (Standardabweichung 3,0) und 69,1 % waren weiblich. Die Patientenzahlen pro Altersgruppe waren wie folgt: 2 bis < 6 Jahre: n = 6; 6 bis < 9 Jahre: n = 9; 9 bis < 12 Jahre: n = 30; und 12 bis < 18 Jahre: n = 175.
Die durchschnittliche Zeit seit der Diagnose der juvenilen idiopathischen Arthritis, die von allen Patienten in der Studie angegeben wurde, betrug 4 Jahre. Der Einsatz von Begleittherapien war in der doppelblinden Studienphase in allen Behandlungsgruppen ähnlich (die häufigste Begleittherapie waren csDMARDs einschließlich MTX, Sulfasalazin und Leflunomid). Insgesamt 127 (57,7 %) Patienten erhielten zu Studienbeginn MTX.
Klinisches Ansprechen
Bei JUVE-BASIS war in der Gruppe der mit Baricitinib behandelten Patienten die Zeit bis zum Krankheitsschub deutlich länger im Vergleich zu den mit Placebo behandelten Patienten (Abbildung 3). Darüber hinaus erreichten mehr Patienten, die mit Baricitinib behandelt wurden, in der gesamten doppelblinden Studienphase ein PedACR-Ansprechen von 30/50/70/90/100 im Vergleich zu Placebo.
Abbildung 3. Zeit bis zum Krankheitsschub während der doppelblinden Studienphase
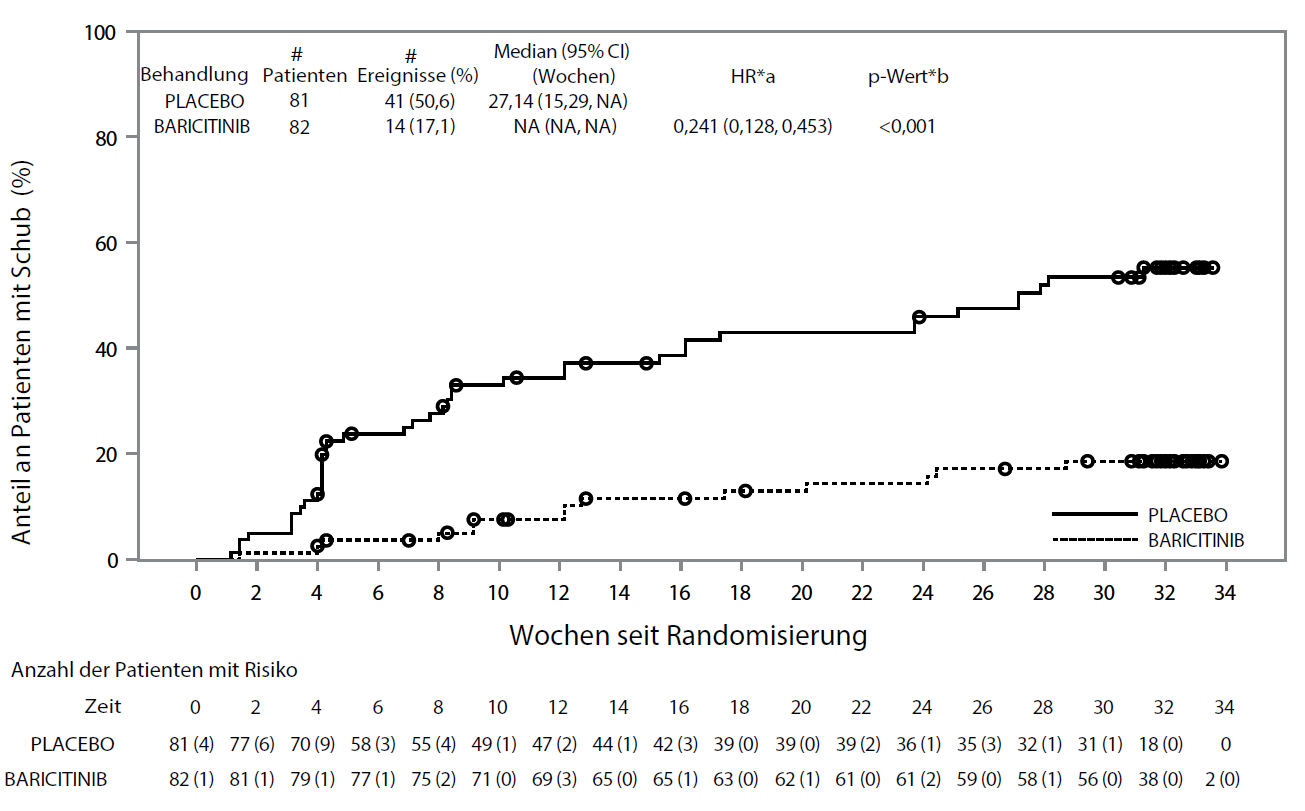
CI = Konfidenzintervall; HR = Hazard Ratio; NA = nicht anwendbar |
Die Zeit bis zum Krankheitsschub und die Ergebnisse des PedACR-Ansprechens waren übergreifend konsistent bei den Subtypen der juvenilen idiopathischen Arthritis und den Hintergrundmerkmalen (einschließlich Alter, Geographie, Gewicht, vorherige Einnahme von Biologika, gleichzeitige Anwendung von MTX oder Kortikosteroiden) und stimmten mit denen der gesamten Studienpopulation überein.
Atopische Dermatitis bei Kindern und Jugendlichen
Die Wirksamkeit und Sicherheit von Baricitinib in Kombination mit TCS wurden in einer einzigen randomisierten, doppelblinden, placebokontrollierten Phase-III-Studie über 16 Wochen (BREEZE-AD-PEDS) bewertet. Die Studie schloss 483 Patienten mit mittelschwerer bis schwerer atopischer Dermatitis ein, definiert durch einen IGA-Score ≥ 3, einen EASI-Score ≥ 16 und eine BSA-Beteiligung von ≥ 10 %. Geeignete Patienten waren 2 bis unter 18 Jahre alt und hatten zuvor nur unzureichend auf topische Arzneimittel angesprochen oder diese nicht vertragen und kamen für eine systemische Therapie infrage. Allen Patienten wurden gleichzeitig topische Kortikosteroide niedriger oder mittlerer Wirkstärke verschrieben und die Patienten durften während der Studie topische Calcineurin-Inhibitoren anwenden. Die Patienten wurden im Verhältnis 1:1:1:1 randomisiert einer Behandlung mit Placebo, niedriger, mittlerer oder hoher Baricitinib-Dosis zugeteilt (was einer äquivalenten Exposition von 1 mg, 2 mg bzw. 4 mg bei erwachsenen AD-Patienten entspricht). Die Studie beinhaltet eine noch andauernde Langzeitverlängerung von bis zu 4 Jahren.
Patientencharakteristika zu Studienbeginn
Über alle Behandlungsgruppen hinweg waren 76 % Kaukasier, 15 % Asiaten und 3 % Schwarze, 50 % waren weiblich. Das Durchschnittsalter betrug 12 Jahre, wobei 72 % mindestens 10 Jahre alt und 28 % jünger als 10 Jahre alt waren. Patienten im Alter von 6 Jahren und jünger machten 14 % der Population aus (6 Jahre [N = 28], 5 Jahre [N = 11], 4 Jahre [N = 16], 3 Jahre [N = 8], 2 Jahre [N = 5]). In dieser Studie hatten 38 % der Patienten einen IGA-Ausgangswert von 4 (schwere atopische Dermatitis) und 42 % der Patienten hatten zuvor eine systemische Behandlung für atopische Dermatitis erhalten. Der EASI-Ausgangswert lag zwischen 12,2 und 70,8, der wöchentliche Ausgangs-Durchschnittswert der Pruritus Numeric Rating Scale (NRS) bei Patienten im Alter von mindestens 10 Jahren betrug 5,5 (SD = 2,6).
Klinisches Ansprechen
Ein statistisch signifikant größerer Anteil der Patienten, die randomisiert der Baricitinib-Äquivalentdosis von 4 mg zugeteilt wurden, erreichte in Woche 16 ein Ansprechen von IGA 0 oder 1 (primärer Endpunkt), EASI75 oder eine Verbesserung von ≥ 4 Punkten auf der Pruritus NRS im Vergleich zu Placebo (Tabelle 10). Abbildung 4 zeigt den zeitlichen Verlauf bis zum Erreichen von IGA 0 oder 1.
Die Behandlungseffekte in den Untergruppen (Gewicht, Alter, Geschlecht, ethnische Herkunft, Schwere der Erkrankung und vorherige Behandlung, einschließlich Immunsuppressiva) stimmten mit den Ergebnissen in der gesamten Studienpopulation überein.
Tabelle 10. Wirksamkeit von Baricitinib bei pädiatrischen Patienten in Woche 16 a
Studie |
BREEZE-AD-PEDS |
|
Behandlungsgruppe |
PBO |
BARI 4 mg Äquivalent |
N |
122 |
120 |
IGA 0 oder 1, |
16,4 |
41,7 ** |
EASI75, |
32,0 |
52,5 ** |
Pruritus NRS |
16,4 |
35,5 ** |
BARI = Baricitinib; PBO = Placebo | ||
** |
Statistisch signifikant vs. Placebo mit Adjustierung für Mehrfachtestung |
a |
Intent to Treat (ITT) Population (alle randomisierten Patienten) |
b |
Responder wurde definiert als Patient mit IGA 0 oder 1 (“erscheinungsfrei” oder “fast erscheinungsfrei”) mit einer Reduktion von ≥ 2 Punkten auf der IGA-Skala von 0‑4. |
c |
Non-Responder Imputation: Patienten, die eine Rescue-Therapie erhielten oder bei denen Daten fehlten, wurden als Non-Responder betrachtet. |
d |
Ergebnisse werden in einer Untergruppe von Patienten angezeigt, die für eine Beurteilung infrage kommen (Patienten im Alter von ≥ 10 Jahren mit Pruritus NRS ≥ 4 zu Studienbeginn, BARI 4 mg Äquivalent N = 62; Placebo, N = 55). |
Abbildung 4. Zeitverlauf bis zum Erreichen von IGA 0 oder 1 mit einer Verbesserung um ≥ 2 Punkte bei pädiatrischen Patienten bis Woche 16
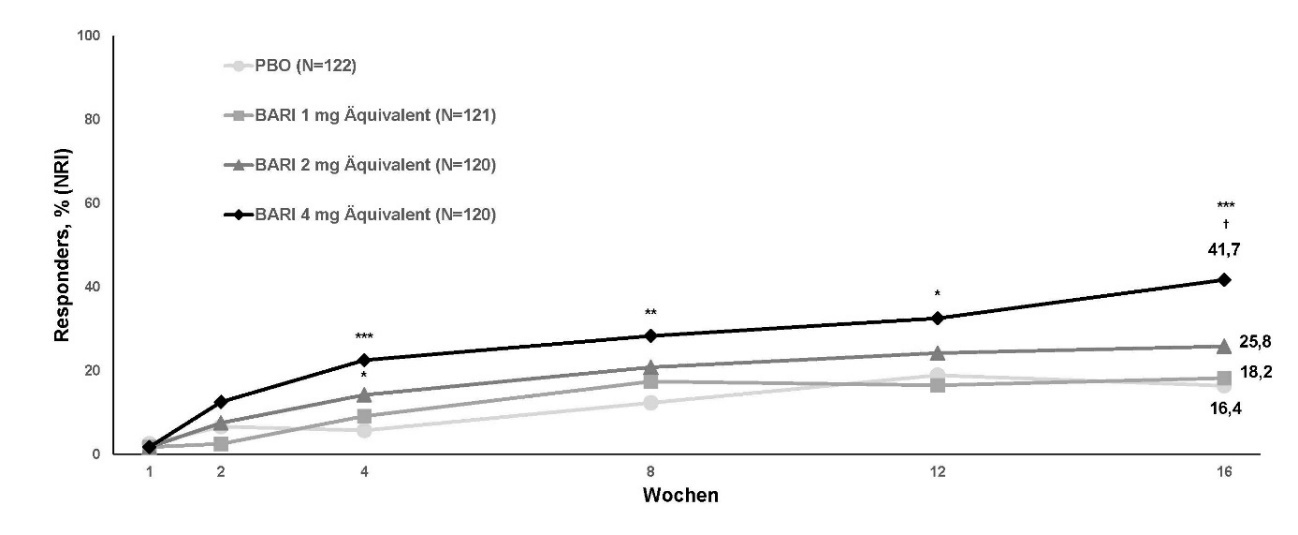
BARI = Baricitinib; NRI = Non-Responder Imputation; PBO = Placebo * p< 0,05; ** p< 0,01; *** p< 0,001 vs. PBO (nomineller p-Wert; logistische Regressionsanalyse); † Statistisch signifikant mit Adjustierung für Mehrfachtestung |
Ein signifikant größerer Anteil der Patienten, die randomisiert der Baricitinib-Äquivalentdosis von 4 mg zugeteilt wurden, erreichte bereits in Woche 4 eine Verbesserung des Pruritus NRS um ≥ 4 Punkte im Vergleich zu Placebo (adjustiert um Multiplizität).
Der Bedarf an gleichzeitiger TCS-Anwendung wurde verringert, was durch eine mittlere Reduktion der Menge in Gramm der TCS-Anwendung bei der Baricitinib-Äquivalentdosis von 4 mg im Vergleich zu Placebo über 16 Wochen und eine höhere mittlere Anzahl an TCS-freier Tage bei der Baricitinib-Äquivalentdosis von 4 mg (25 Tage) im Vergleich zu Placebo (11 Tage) über 16 Wochen gezeigt wurde.
Alopecia areata bei Jugendlichen
Die Wirksamkeit und Sicherheit von Baricitinib einmal täglich wurde in einer einzigen, doppelblinden, randomisierten, placebokontrollierten Phase-III-Studie (BRAVE-AA-PEDS) über 36 Wochen untersucht. Die Patienten wurden auf Placebo, 2 mg oder 4 mg Baricitinib im Verhältnis 1:1:1 randomisiert. In die Studie eingeschlossene Patienten waren Jugendliche im Alter von 12 bis unter 18 Jahren, mit einem Körpergewicht ab 30 kg, mit einer aktuellen Episode von mehr als 6 Monaten schwerer Alopecia areata (Haarausfall ≥ 50 % der Kopfhaut). Patienten mit einer aktuellen Episode von mehr als 8 Jahren Dauer wurden nicht eingeschlossen, es sei denn es wurden in den letzten 8 Jahren Episoden erneuten Haarwachstums auf den betroffenen Bereichen der Kopfhaut beobachtet. Die einzigen zulässigen Begleittherapien zur Behandlung der Alopecia areata waren Minoxidil zur oralen bzw. topischen Anwendung und Bimatoprost-Augenlösung für Wimpern, unter der Bedingung einer stabilen Dosis bei Studienbeginn. Die Studie beinhaltet eine noch andauernde Langzeitverlängerung von bis zu 2 Jahren.
Der primäre Endpunkt der Studie war der Anteil der Patienten, die in Woche 36 einen SALT (Severity of Alopecia Tool)-Score von ≤ 20 (mindestens 80 % der Kopfhaut mit Haaren bedeckt) erreichten. Zusätzlich wurde in der Studie eine klinische Beurteilung des Augenbrauen- und Wimpernverlusts anhand einer 4-Punkte-Skala vorgenommen (ClinRO Measure for Eyebrow Hair Loss™, ClinRO Measure for Eyelash Hair Loss™).
Patientencharakteristika zu Studienbeginn
In die placebokontrollierte Studie BRAVE-AA-PEDS wurden 257 jugendliche Patienten eingeschlossen. Über alle Behandlungsgruppen hinweg betrug das Durchschnittsalter 14,7 Jahre und 49 % der Patienten waren weiblich. Die durchschnittliche Erkrankungsdauer seit Beginn der Alopecia areata und die durchschnittliche Dauer der aktuellen Haarausfallepisode betrugen 6,4 bzw. 3,2 Jahre. Der Median des SALT-Scores betrug 100 (entspricht 100 % Haarausfall der Kopfhaut) und bei ungefähr 54 % der Patienten wurde Alopecia universalis berichtet. Bei Baseline hatten 65 % der Patienten signifikanten oder vollständigen Verlust der Augenbrauen und 57 % hatten signifikanten oder vollständigen Verlust der Wimpern, gemessen anhand der ClinRO-Skalen für Augenbrauen und Wimpern, mit Scores von 2 bzw. 3. Vor Studieneintritt hatten alle Patienten zumindest eine Behandlung für Alopecia areata erhalten und bei 52 % wurde zumindest eine systemische Behandlung angewendet. Die Anwendung zugelassener Begleittherapien zur Behandlung der Alopecia areata wurde während der Studie nur von 3,1 % der Patienten angegeben.
Klinisches Ansprechen
Ein statistisch signifikant größerer Anteil der Patienten, die auf Baricitinib 4 mg einmal täglich randomisiert wurden, erreichte in Woche 36 einen SALT-Score ≤ 20 verglichen mit Placebo, beginnend bereits in Woche 12. Bei allen wesentlichen sekundären Endpunkten wurde eine konsistente Wirksamkeit von Baricitinib 4 mg beobachtet (Tabelle 11), numerisch gestützt durch die Mehrzahl der sekundären Endpunkte, einschließlich arzt‑ und patientenberichteter Ergebnisse. Abbildung 5 zeigt den Anteil der Patienten, die bis Woche 36 einen SALT-Score von ≤ 20 erreichten.
Die Behandlungseffekte in den Untergruppen (Geschlecht, ethnische Zugehörigkeit, geografische Region, Schweregrad der Erkrankung, Dauer der aktuellen Alopecia areata-Episode) waren mit den Ergebnissen in der gesamten Studienpopulation in Woche 36 konsistent.
Tabelle 11. Wirksamkeit von Baricitinib bei jugendlichen Patienten bis Woche 36
BRAVE-AA-PEDS |
|||
Placebo |
Baricitinib 2 mg |
Baricitinib 4 mg |
|
SALT ≤ 20 in Woche 36 |
4,5 % |
27,4 % ** |
42,4 % ** |
SALT ≤ 20 in Woche 24 |
3,4 % |
16,7 % ** |
31,8 % ** |
SALT ≤ 10 in Woche 36 |
2,3 % |
21,4 % ** |
36,5 % ** |
ClinRO-Score für Augenbrauenverlust von 0 oder 1 in Woche 36 mit einer ≥ 2 Punkte Verbesserung gegenüber dem Ausgangswert a |
0 % |
24,1 % * |
50,0 % * |
ClinRO-Score für Wimpernverlust von 0 oder 1 in Woche 36 mit einer ≥ 2 Punkte Verbesserung gegenüber dem Ausgangswert a |
14,0 % |
25,5 % |
42,9 % * |
Änderung im Skindex-16, angepasst für Alopecia areata-Emotionsdomäne, Mittelwert LSM (SE) b |
-3,98 (2,63) |
-12,87 (2,55) * |
-18,22 (2,60) * |
ClinRO = clinician-reported outcome; LSM = kleinster Mittelwert, quadratisch; SE = Standardfehler | |||
* |
Statistisch signifikant versus Placebo ohne Adjustierung für Mehrfachtestung. |
** |
Statistisch signifikant versus Placebo mit Adjustierung für Mehrfachtestung. |
a |
Patienten mit ClinRO-Score für Augenbrauenverlust von ≥ 2 zu Studienbeginn: 60 (Placebo), 54 (Baricitinib 2 mg), 54 (Baricitinib 4 mg). Patienten mit einem ClinRO-Score für Wimpernverlust von ≥ 2 zu Studienbeginn: 50 (Placebo), 47 (Baricitinib 2 mg), 49 (Baricitinib 4 mg). Beide ClinRO-Messungen verwenden eine 4-Punkte-Skala, die von 0 bis 3 reicht, wobei 0 kein Haarverlust und 3 keine erkennbaren Augenbrauen bzw. Wimpern bedeutet. |
b |
Die Größe der Analysepopulation in Bezug auf den Skindex-16, angepasst für Alopecia areata, in Woche 36 ist n = 87 (Placebo), 84 (Baricitinib 2 mg), 85 (Baricitinib 4 mg). |
Abbildung 5: Anteil jugendlicher Patienten mit einem SALT ≤ 20 bis Woche 36
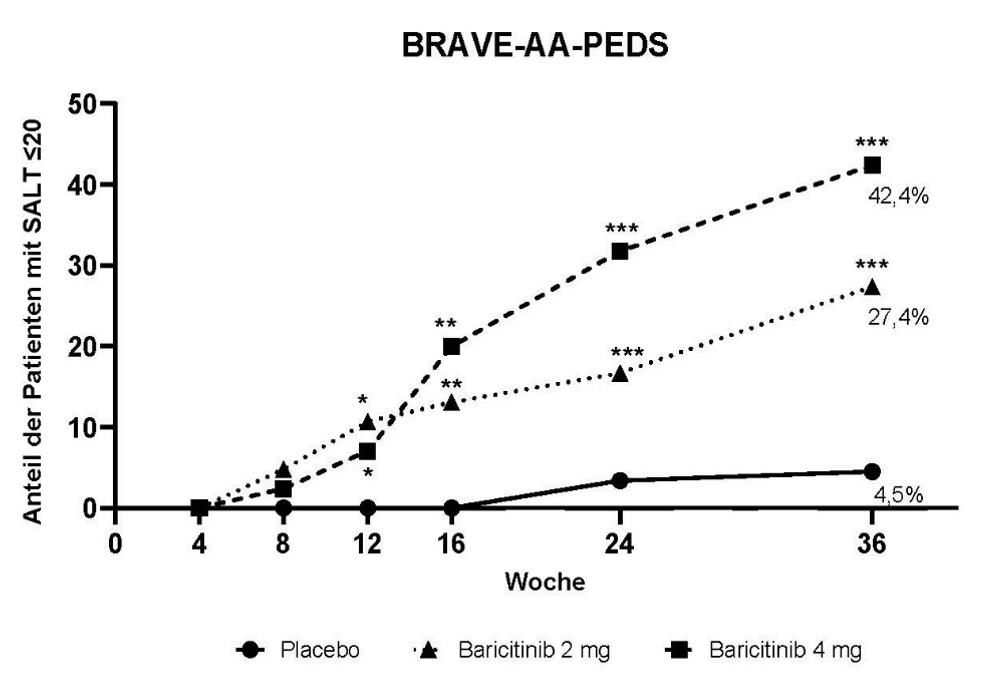 * p‑Wert für Baricitinib versus Placebo ≤ 0,05; ** p‑Wert für Baricitinib versus Placebo ≤ 0,01; |
*** p‑Wert für Baricitinib versus Placebo ≤ 0,001. |
Kinder und Jugendliche
Die Europäische Arzneimittel-Agentur hat für Baricitinib eine Zurückstellung von der Verpflichtung zur Vorlage von Ergebnissen zu Studien in einer oder mehreren pädiatrischen Altersklassen bei chronischer idiopathischer Arthritis und Alopecia areata gewährt (siehe Abschnitt 4.2 bzgl. Informationen zur Anwendung bei Kindern und Jugendlichen).
Die Wirksamkeit von Baricitinib von bis zu 12 mg täglich wurde untersucht bei 71 Patienten mit CANDLE (chronisch atypische neutrophile Dermatose mit Lipodystrophie und erhöhter Temperatur, n = 10), CANDLE-bezogenen Erkrankungen (CANDLE-RC, n = 9), SAVI (Stimulator von Interferongenen assoziierte Vaskulopathie mit Beginn in der Kindheit, n = 8), juveniler Dermatomyositis (JDM, n = 5) und Aicardi-Goutières-Syndrom (AGS, n = 39). Die Gesamtexposition (PYE) betrug 251 Patientenjahre. Aufgrund methodischer Mängel konnten keine eindeutigen Schlussfolgerungen zur Wirksamkeit von Baricitinib bei diesen Patienten gezogen werden. Obwohl die Sicherheitsmuster Ähnlichkeiten mit den Indikationen bei Erwachsenen aufwiesen, waren die Häufigkeiten unerwünschter Ereignisse im Allgemeinen höher. In der AGS-Population wurden drei Todesfälle beobachtet; es ist unklar, ob diese Todesfälle im Zusammenhang mit der Baricitinib-Behandlung standen.
Die Wirksamkeit und Sicherheit von Baricitinib wurde bei 29 Patienten im Alter von 2 bis < 18 Jahren mit aktiver JIA-assoziierter Uveitis oder chronischer anteriorer Antikörper-positiver Uveitis untersucht. MTX-IR (n = 10) wurden Baricitinib (n = 5) oder Adalimumab (n = 5) zugeordnet; bDMARD-IR (n = 19) wurden alle Baricitinib zugeordnet. Baricitinib wurde 2 mg einmal täglich für Patienten im Alter von 2 bis < 9 Jahren und 4 mg einmal täglich für Patienten im Alter von 9 bis < 18 Jahren verabreicht, die Dosierung von Adalimumab betrug 20 mg (bei < 30 kg) oder 40 mg (bei ≥ 30 kg) einmal alle zwei Wochen.
Der primäre Endpunkt war der Anteil an Patienten mit einer 2-stufigen Reduktion des Entzündungswertes (Vorderkammerzellen) gemäß den SUN-Kriterien (Standardisierung der Uveitis-Nomenklatur) oder einer Reduktion auf Null bis Woche 24 in dem Auge, das zu Studienbeginn am stärksten betroffen war. Acht (33,3 %) Patienten waren Baricitinib-Responder (7 bDMARD-IR und 1 MTX-IR), die Ansprechrate zwischen den beiden Kohorten zeigte jedoch keine statistische Signifikanz.
Nach vorangegangener Einnahme von Baricitinib wurde ein dosisabhängiger Anstieg der systemischen Exposition im Rahmen der therapeutischen Dosierung beobachtet. Die Pharmakokinetik ist linear abhängig von der Zeit.
Resorption
Nach oraler Gabe wird Baricitinib rasch resorbiert, wobei die mediane Zeit bis zum mittleren höchsten Plasmaspiegel (tmax) etwa eine Stunde (Bereich von 0,5 – 3,0 h) und die absolute Bioverfügbarkeit etwa 79 % (CV [Variationskoeffizient] = 3,94 %) beträgt. Eine Nahrungsaufnahme führte zu einer um bis zu 14 % verringerten Exposition, einer Reduktion von Cmax um bis zu 18 % und verzögerte tmax um 0,5 Stunden. Eine Einnahme zusammen mit den Mahlzeiten war mit keiner klinisch relevanten Wirkung auf die Exposition verbunden.
Verteilung
Das mittlere Verteilungsvolumen nach einer intravenösen Infusion betrug 76 Liter, was auf eine Verteilung von Baricitinib in das Gewebe hinweist. Baricitinib wird zu etwa 50 % an Plasmaproteine gebunden.
Biotransformation
Die Metabolisierung von Baricitinib wird durch CYP3A4 vermittelt, wobei weniger als 10 % der verabreichten Dosis eine Biotransformation durchlaufen. Im Plasma konnten keine Metaboliten quantifiziert werden. In einer klinischen pharmakologischen Studie wurde Baricitinib vorwiegend als unveränderter Wirkstoff über den Urin (69 %) und die Faeces (15 %) ausgeschieden. Nur vier unwesentliche oxidative Metaboliten wurden identifiziert (3 im Urin, 1 in den Faeces), was ungefähr 5 % bzw. 1 % der Dosis ausmacht. In vitro ist Baricitinib ein Substrat für CYP3A4, OAT3, Pgp, BCRP und MATE2-K und könnte ein klinisch relevanter Inhibitor des Transporters OCT1 sein (siehe Abschnitt 4.5). Baricitinib ist in klinisch relevanten Konzentrationen kein Inhibitor der Transporter OAT1, OAT2, OAT3, OCT2, OATP1B1, OATP1B3, BCRP, MATE1 und MATE2-K.
Elimination
Die renale Elimination ist der wesentliche Clearance-Mechanismus für Baricitinib, mittels glomerulärer Filtration und aktiver Ausscheidung über OAT3, Pgp, BCRP und MATE2-K. In einer klinischen pharmakologischen Studie wurden etwa 75 % der verabreichten Dosis über den Urin eliminiert, während etwa 20 % der Dosis über die Faeces ausgeschieden wurden.
Die mittlere scheinbare Clearance (CL/F) und die Halbwertszeit bei Patienten mit rheumatoider Arthritis betrugen 9,42 l/Std (CV = 34,3 %) und 12,5 Stunden (CV = 27,4 %). Bei Patienten mit rheumatoider Arthritis sind Cmax und AUC im Steady State um jeweils das 1,4- bzw. 2,0‑fache höher als bei Gesunden.
Die mittlere scheinbare Clearance (CL/F) und die Halbwertszeit bei Patienten mit atopischer Dermatitis betrug 11,2 l/Std (CV = 33,0 %) bzw. 12,9 Std (CV = 36,0 %). Bei Patienten mit atopischer Dermatitis sind Cmax und AUC im Steady State jeweils das 0,8‑fache von jenen Werten bei Patienten mit rheumatoider Arthritis.
Die mittlere scheinbare Clearance (CL/F) und die Halbwertszeit bei Patienten mit Alopecia areata betrug 11,0 l/Std (CV = 36,0 %) bzw. 15,8 Std (CV = 35,0 %). Bei Patienten mit Alopecia areata betragen Cmax und AUC im Steady State jeweils das 0,9‑fache von jenen Werten bei Patienten mit rheumatoider Arthritis.
Eingeschränkte Nierenfunktion
Es zeigte sich, dass die Nierenfunktion die Baricitinib-Exposition signifikant beeinflusst. Die mittleren Verhältnisse von AUC bei Patienten mit leichter bis moderater Nierenfunktionseinschränkung zu Patienten mit normaler Nierenfunktion betragen 1,41 (90 % CI: 1,15 - 1,74) und 2,22 (90 % CI: 1,81 - 2,73). Die mittleren Verhältnisse von Cmax bei Patienten mit leichter bis moderater Nierenfunktionseinschränkung zu Patienten mit normaler Nierenfunktion betragen 1,16 (90 % CI: 0,92 - 1,45) und 1,46 (90 % CI: 1,17 - 1,83). Siehe Abschnitt 4.2 für Dosierungsempfehlungen.
Eingeschränkte Leberfunktion
Bei Patienten mit leichter bis mäßiger Leberfunktionseinschränkung gab es keinen klinisch relevanten Einfluss auf die Pharmakokinetik von Baricitinib. Die Anwendung von Baricitinib bei Patienten mit schwerer Leberfunktionseinschränkung wurde nicht untersucht.
Ältere Patienten
Ein Alter von ≥ 65 Jahren oder ≥ 75 Jahren hat keinen Einfluss auf die Baricitinib-Exposition (Cmax und AUC).
Kinder und Jugendliche
Pharmakokinetik bei pädiatrischen Patienten mit juveniler idiopathischer Arthritis
Die Halbwertszeit bei pädiatrischen Patienten im Alter von 2 bis unter 18 Jahren betrug 8 bis 9 Stunden.
Exposition bei pädiatrischen Patienten mit einem Körpergewicht von < 30 kg und ≥ 30 kg: Bei Patienten < 30 kg mit einem Durchschnittsalter von 8,1 Jahren (Spanne 2,0 - 16,0 Jahre) betrug der Mittelwert für AUC 381 h*ng/ml (CV = 76 %) und für Cmax . 62,1 ng/ml (CV = 39 %). Bei Patienten ≥ 30 kg mit einem Durchschnittsalter von 14,1 (Spanne 9,0 - 17,0 Jahre) betrug der Mittelwert für AUC 438 h*ng/ml (CV = 68 %) und für Cmax 60,7 ng/ml (CV = 30 %).
Exposition bei pädiatrischen Patienten mit einem Körpergewicht von 10 bis < 20 kg und 20 bis < 30 kg: Bei Patienten 10 bis < 20 kg mit einem Durchschnittsalter von 5,1 Jahren (Spanne 2,0 - 8,0 Jahre) betrug der Mittelwert für AUC 458 h*ng/ml (CV = 81 %) und für Cmax 77,6 ng/ml (CV = 38 %). Bei Patienten mit einem Gewicht von 20 bis < 30 kg mit einem Durchschnittsalter von 10,3 Jahren (Spanne 6,0 - 16,0 Jahre) betrug der Mittelwert für AUC 327 h*ng/ml (CV = 66 %) und für Cmax 51,2 ng/ml (CV = 22 %).
Pharmakokinetik bei pädiatrischen Patienten mit atopischer Dermatitis
Die mittlere Halbwertszeit bei pädiatrischen Patienten im Alter von 2 bis unter 18 Jahren betrug 13 bis 18 Stunden.
Exposition bei pädiatrischen Patienten mit einem Gewicht von < 30 kg und ≥ 30 kg: Bei Patienten < 30 kg mit einem Durchschnittsalter von 6,4 (Spanne 2,0 - 11,1 Jahre) betrug der Mittelwert für AUC 404 h*ng/ml (CV = 78%) und für Cmax 60,4 ng/ml (CV = 28%). Bei Patienten ≥ 30 kg mit einem Durchschnittsalter von 13,5 (Spanne 6,2 - 17,9 Jahre) betrug der Mittelwert für AUC 529 h*ng/ml (CV = 102 %) und für Cmax 57,0 ng/ml (CV = 42 %).
Exposition bei pädiatrischen Patienten mit einem Gewicht von 10 bis < 20 kg und 20 bis < 30 kg: Bei Patienten mit einem Gewicht von 10 bis < 20 kg mit einem Durchschnittsalter von 4,8 Jahren (Spanne 2,0 - 6,9 Jahre) betrug der Mittelwert für AUC 467 h*ng/ml (CV = 80 %) und für Cmax 73,4 ng/ml (CV = 21 %). Bei Patienten mit einem Gewicht von 20 bis < 30 kg mit einem Durchschnittsalter von 7,5 Jahren (Spanne 4,8 - 11,1 Jahre) betrug der Mittelwert für AUC 363 h*ng/ml (CV = 72 %) und für Cmax 52,0 ng/ml (CV = 21 %).
Pharmakokinetik bei jugendlichen Patienten mit Alopecia areata
Die mittlere Halbwertszeit bei jugendlichen Patienten im Alter von 12 bis unter 18 Jahren betrug etwa 10 Stunden.
Exposition bei jugendlichen Patienten im Alter von 12 bis unter 18 Jahren mit einem Körpergewicht von ≥ 30 kg: Bei Patienten mit einem Körpergewicht von ≥ 30 kg mit einem Durchschnittsalter von 14,7 Jahren (Spanne 12 - 18 Jahre) betrug der Mittelwert für AUC 334 h*ng/ml (CV = 45 %) und für Cmax 52,9 ng/ml (CV = 23 %).
Andere intrinsische Faktoren
Körpergewicht, Alter, Geschlecht und ethnische Herkunft hatten keinen klinisch relevanten Effekt auf die Pharmakokinetik von Baricitinib bei erwachsenen Patienten. Die mittleren Effekte von intrinsischen Faktoren auf pharmakokinetische Parameter (AUC und Cmax) lagen generell im inter-individuellen pharmakokinetischen Schwankungsbereich. Es ist daher aufgrund dieser Patientencharakteristika keine Dosisanpassung erforderlich.
Basierend auf den konventionellen Studien zur Sicherheitspharmakologie, zur Genotoxizität und zum kanzerogenen Potential lassen die präklinischen Daten keine besonderen Gefahren für den Menschen erkennen.
Eine Reduktion der Lymphozyten, eosinophilen und basophilen Granulozyten sowie eine lymphoide Depletion von Organen/Geweben des Immunsystems wurden in Mäusen, Ratten und Hunden beobachtet. Opportunistische Infektionen in Form von Demodikosen (Räude) wurden bei Hunden bei ungefähr der 7‑fachen humantherapeutischen Exposition beobachtet. Abnahmen der roten Blutzellparameter wurden bei Mäusen, Ratten und Hunden bei etwa der 6- bis 36‑fachen humantherapeutischen Exposition beobachtet. Bei einigen Hunden wurde eine Degeneration der sternalen Wachstumsfuge beobachtet, in geringer Häufigkeit und auch bei den Kontrolltieren, aber mit einer dosisabhängigen Wirkung hinsichtlich des Schweregrades. Zurzeit ist nicht bekannt, ob dies klinisch relevant ist.
In reproduktionstoxikologischen Studien bei Ratten und Kaninchen zeigte sich, dass Baricitinib (bei Exposition von ungefähr der 10- bzw. der 39‑fachen humantherapeutischen Exposition) das Wachstum/Gewicht der Föten reduziert und zu Skelettmissbildungen führt. Bei der 2‑fachen humantherapeutischen Exposition basierend auf der AUC wurden an den Föten keine Nebenwirkungen beobachtet.
In einer kombinierten Fertilitätsstudie an männlichen/weiblichen Ratten verminderte Baricitinib die Gesamtpaarungsleistung (verminderte Fertilitäts- und Konzeptionsindizes). Bei weiblichen Ratten zeigte sich eine verminderte Anzahl von Corpora lutea und Implantationsstellen, vermehrte Präimplantationsverluste und/oder schädliche Wirkungen auf das intrauterine Überleben der Embryos. Da weder auf die Spermatogenese (Bewertung mittels Histopathologie) noch auf die Samen/Spermien-Endpunkte bei männlichen Ratten Effekte festgestellt wurden, war die verminderte Gesamtpaarungsleistung wahrscheinlich die Folge der Effekte bei weiblichen Tieren.
Baricitinib wurde in der Milch von laktierenden Ratten festgestellt. In einer prä- und postnatalen Entwicklungsstudie wurden bei der 4- bzw. 21‑fachen humantherapeutischen Exposition sowohl ein vermindertes Gewicht der Jungtiere als auch eine verringerte postnatale Überlebensrate beobachtet.
Tablettenkern
Mikrokristalline Cellulose
Croscarmellose-Natrium
Magnesiumstearat (Ph.Eur.)
Mannitol (Ph.Eur.)
Filmüberzug
Eisen (III)-oxid (E 172)
Phospholipide aus Sojabohnen (E 322)
Macrogol
Poly(vinylalkohol)
Talkum
Titandioxid (E 171)
Nicht zutreffend.
3 Jahre
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
Olumiant® 1 mg Filmtabletten
Polyvinylchlorid/Polyethylen/Polychlortrifluorethylen//Aluminium Blisterpackungen in Umkartons mit 14 oder 28 Filmtabletten.
Polyvinylchlorid/Aluminium/orientiertes Polyamid//Aluminium perforierte Einzeldosis-Blisterpackungen in Umkartons mit 28 x 1 Filmtablette.
Olumiant® 2 mg und 4 mg Filmtabletten
Polyvinylchlorid/Polyethylen/Polychlortrifluorethylen//Aluminium Blisterpackungen in Umkartons mit 14, 28, 35, 56, 84 oder 98 Filmtabletten.
Polyvinylchlorid/Aluminium/orientiertes Polyamid//Aluminium perforierte Einzeldosis-Blisterpackungen in Umkartons mit 28 x 1 oder 84 x 1 Filmtablette.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
Bei pädiatrischen Patienten, die nicht in der Lage sind, ganze Tabletten zu schlucken, sollte in Betracht gezogen werden, die Tabletten in Wasser zu suspendieren. Zum Suspendieren der Tablette sollte ausschließlich Wasser verwendet werden. Es sollte nur die für die Dosis erforderliche Anzahl an Tabletten suspendiert werden.
̶ |
Geben Sie die ganze Tablette in ein Behältnis mit 5-10 ml Wasser (Raumtemperatur) und schwenken Sie das Behältnis vorsichtig, um die Tablette zu suspendieren. Es kann bis zu 10 Minuten dauern, bis die Tablette zu einer trüben, blassrosa Suspension zerfällt. Es kann zu einem Bodensatz kommen. |
̶ |
Nachdem die Tablette suspendiert wurde, schwenken Sie das Behältnis erneut vorsichtig und wenden Sie die Suspension dann sofort an. |
̶ |
Spülen Sie das Behältnis mit 5 bis 10 ml Wasser (Raumtemperatur) und wenden Sie den gesamten Inhalt sofort an. |
Die in Wasser suspendierte Tablette ist bei Raumtemperatur bis zu 4 Stunden stabil.
Sollte aus irgendeinem Grund nicht die gesamte Suspension angewendet werden, soll keine weitere Tablette suspendiert und angewendet, sondern bis zur nächsten geplanten Dosis gewartet werden.
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu beseitigen.
Eli Lilly Nederland B.V.
Orteliuslaan 1000
3528 BD Utrecht
Niederlande
Olumiant® 1 mg Filmtabletten
EU/1/16/1170/017
EU/1/16/1170/018
EU/1/16/1170/019
Olumiant® 2 mg Filmtabletten
EU/1/16/1170/001
EU/1/16/1170/002
EU/1/16/1170/003
EU/1/16/1170/004
EU/1/16/1170/005
EU/1/16/1170/006
EU/1/16/1170/007
EU/1/16/1170/008
Olumiant® 4 mg Filmtabletten
EU/1/16/1170/009
EU/1/16/1170/010
EU/1/16/1170/011
EU/1/16/1170/012
EU/1/16/1170/013
EU/1/16/1170/014
EU/1/16/1170/015
EU/1/16/1170/016
Datum der Erteilung der Zulassung: 13. Februar 2017
Datum der letzten Verlängerung der Zulassung: 12. November 2021
März 2026
Ausführliche Informationen zu diesem Arzneimittel sind auf den Internetseiten der Europäischen Arzneimittel-Agentur https://www.ema.europa.eu verfügbar.
Verschreibungspflichtig
Olumiant® 1 mg Filmtabletten
Inhalt |
PZN |
28 Filmtabletten |
18840456 |
Olumiant® 2 mg Filmtabletten
Inhalt |
PZN |
28 Filmtabletten |
12652854 |
98 Filmtabletten |
12652908 |
Olumiant® 4 mg Filmtabletten
Inhalt |
PZN |
28 Filmtabletten |
12652920 |
98 Filmtabletten |
12652943 |
Für Olumiant Filmtabletten sind die im folgenden aufgeführten Schulungsmaterialien behördlich beauflagt. Die Schulungsmaterialien können mittels dem angegebenen QR-Code elektronisch aufgerufen werden. Printversionen der Materialien sind über die medizinische Information der Lilly Deutschland GmbH verfügbar.
Olumiant Patientenpass

Leitfaden zur Verringerung von Arzneimittel- und Anwendungsrisiken – Ärztinnen und Ärzte – Rheumatologie

Leitfaden zur Verringerung von Arzneimittel-und Anwendungsrisiken – Ärztinnen und Ärzte – Dermatologie

Lilly Deutschland GmbH
Werner-Reimers-Straße 2 - 4
D-61352 Bad Homburg
Tel. +49-(0) 6172 273 2222