Alecensa® 150 mg Hartkapseln
Jede Hartkapsel enthält Alectinibhydrochlorid, entsprechend 150 mg Alectinib.
Sonstige Bestandteile mit bekannter Wirkung
Jede Hartkapsel enthält 33,7 mg Lactose (als Monohydrat) und 6 mg Natrium (als Natriumdodecylsulfat).
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
Hartkapsel
Weiße Hartkapsel mit einer Länge von 19,2 mm und dem Aufdruck „ALE“ in schwarzer Tinte auf dem Kapseloberteil und dem Aufdruck „150 mg“ in schwarzer Tinte auf dem Kapselunterteil.
Adjuvante Behandlung des resezierten nicht-kleinzelligen Lungenkarzinoms (non-small cell lung cancer, NSCLC)
Alecensa wird als Monotherapie angewendet zur adjuvanten Behandlung nach vollständiger Tumorresektion bei erwachsenen Patienten mit ALK-positivem NSCLC mit hohem Risiko für ein Rezidiv (siehe Abschnitt 5.1 zu den Auswahlkriterien).
Behandlung des fortgeschrittenen NSCLC
Alecensa wird als Monotherapie angewendet zur Erstlinienbehandlung von erwachsenen Patienten mit ALK-positivem fortgeschrittenem NSCLC.
Alecensa wird als Monotherapie angewendet zur Behandlung des ALK-positiven fortgeschrittenen NSCLC bei erwachsenen Patienten, die zuvor mit Crizotinib behandelt wurden.
Die Behandlung mit Alecensa muss von einem Arzt, der Erfahrung in der Anwendung von Arzneimitteln gegen Krebs hat, eingeleitet und überwacht werden.
Ein validierter ALK-Test ist notwendig, um Patienten mit ALK-positivem NSCLC zu identifizieren. Ein ALK-positiver NSCLC-Status muss vor Beginn der Therapie mit Alecensa festgestellt worden sein.
Dosierung
Die empfohlene Dosierung von Alecensa beträgt 600 mg (vier Kapseln à 150 mg) zweimal täglich, die zusammen mit Nahrungsmitteln eingenommen wird (entsprechend einer Tagesgesamtdosis von 1 200 mg).
Patienten mit zugrunde liegender schwerer Leberfunktionsstörung (Child-Pugh C) sollen eine Anfangsdosis von 450 mg zweimal täglich erhalten, die zusammen mit Nahrungsmitteln eingenommen wird (entsprechend einer Tagesgesamtdosis von 900 mg).
Dauer der Behandlung
Adjuvante Behandlung des resezierten NSCLC
Eine Behandlung mit Alecensa soll bis zum Wiederauftreten der Erkrankung, Auftreten inakzeptabler Toxizitäten oder 2 Jahre lang fortgeführt werden.
Behandlung des fortgeschrittenen NSCLC
Eine Behandlung mit Alecensa soll bis zur Krankheitsprogression oder bis zum Auftreten inakzeptabler Toxizitäten fortgeführt werden.
Verspätete oder versäumte Dosen
Wenn eine geplante Dosis von Alecensa versäumt wurde, können die Patienten diese Dosis nachholen, es sei denn, die folgende Dosis muss innerhalb der nächsten 6 Stunden eingenommen werden. Patienten sollten nicht zwei Dosen gleichzeitig einnehmen, wenn die vorherige Dosis vergessen wurde. Wenn es nach der Einnahme einer Dosis von Alecensa zu Erbrechen kommt, sollen die Patienten ihre nächste Dosis zur gewohnten Zeit einnehmen.
Dosisanpassungen
Die Behandlung von Nebenwirkungen kann eine Dosisreduktion, eine vorübergehende Unterbrechung oder einen Abbruch der Behandlung mit Alecensa erforderlich machen. Die Dosis von Alecensa sollte abhängig von der Verträglichkeit in Schritten von 150 mg zweimal täglich reduziert werden. Die Behandlung mit Alecensa sollte dauerhaft abgebrochen werden, wenn die Patienten die Dosis von 300 mg zweimal täglich nicht vertragen.
Hinweise zur Dosisanpassung werden in den nachfolgenden Tabellen 1 und 2 gegeben.
Tabelle 1: Dosisreduktionsschema
Dosisreduktionsschema |
Dosierung |
Dosis |
600 mg zweimal täglich |
Erste Dosisreduktion |
450 mg zweimal täglich |
Zweite Dosisreduktion |
300 mg zweimal täglich |
Tabelle 2: Hinweise zur Dosisanpassung bei spezifischen Nebenwirkungen (siehe Abschnitte 4.4 und 4.8)
CTCAE Grad |
Behandlung mit Alecensa |
ILD/Pneumonitis jeglicher Schweregrade |
Die Behandlung mit Alecensa umgehend unterbrechen und dauerhaft abbrechen, wenn keine anderen potenziellen Ursachen für die ILD/Pneumonitis identifiziert werden konnten. |
ALT- oder AST-Erhöhung > 5 x ULN mit Gesamtbilirubin ≤ 2 x ULN |
Die Behandlung bis zur Erholung auf den Ausgangswert oder ≤ 3 x ULN unterbrechen, dann mit reduzierter Dosis (siehe Tabelle 1) fortsetzen. |
ALT- oder AST-Erhöhung > 3 x ULN mit Gesamtbilirubin-Erhöhung > 2 x ULN ohne Vorliegen einer Cholestase oder Hämolyse |
Behandlung mit Alecensa dauerhaft abbrechen. |
Bradykardiea Grad 2 oder Grad 3 (symptomatisch, kann schwer und medizinisch signifikant sein, medizinische Intervention indiziert) |
Die Behandlung bis zur Besserung der Bradykardie auf Grad ≤ 1 (asymptomatisch) oder bis zum Anstieg der Herzfrequenz auf ≥ 60 bpm unterbrechen. Gleichzeitig angewendete Arzneimittel, die bekanntermaßen Bradykardie verursachen können sowie begleitende blutdrucksenkende Arzneimittel überprüfen. |
Bradykardiea Grad 4 (lebensbedrohliche Konsequenzen, dringende Intervention indiziert) |
Behandlung mit Alecensa dauerhaft abbrechen, wenn kein gleichzeitig angewendetes mitverursachendes Arzneimittel identifiziert wurde. |
Erhöhung der CPK > 5 x ULN |
Die Behandlung bis zur Erholung auf den Ausgangswert oder ≤ 2,5 x ULN unterbrechen, danach mit der gleichen Dosis fortsetzen. |
Erhöhung der CPK > 10 x ULN oder eine erneute Erhöhung der CPK > 5 x ULN |
Die Behandlung bis zur Erholung auf den Ausgangswert oder ≤ 2,5 x ULN unterbrechen, danach mit der reduzierten Dosis gemäß Tabelle 1 fortsetzen. |
Hämolytische Anämie mit Hämoglobin von < 10 g/dl (Grad ≥ 2) |
Die Behandlung bis zum Abklingen unterbrechen, dann mit reduzierter Dosis (siehe Tabelle 1) fortsetzen. |
ALT = Alanin-Aminotransferase; AST = Aspartat-Aminotransferase; CPK = Kreatinphosphokinase; CTCAE = NCI Common Terminology Criteria for Adverse Events; ILD = interstitielle Lungenerkrankung; ULN = oberer Normalwert
a Herzfrequenz unter 60 Schläge pro Minute (bpm).
Spezielle Patientengruppen
Leberfunktionsstörung
Bei Patienten mit zugrunde liegender leichter (Child-Pugh A) oder mäßiger (Child-Pugh B) Leberfunktionsstörung ist keine Anpassung der Anfangsdosis erforderlich. Patienten mit zugrunde liegender schwerer (Child-Pugh C) Leberfunktionsstörung sollen eine Anfangsdosis von 450 mg zweimal täglich (entsprechend einer Tagesgesamtdosis von 900 mg) erhalten (siehe Abschnitt 5.2). Bei allen Patienten mit Leberfunktionsstörung wird eine angemessene Überwachung (z. B. Leberfunktionsparameter) empfohlen, siehe Abschnitt 4.4.
Nierenfunktionsstörung
Bei Patienten mit leichter bis mittlerer Nierenfunktionsstörung ist keine Dosisanpassung erforderlich. Alecensa wurde bei Patienten mit schwerer Nierenfunktionsstörung nicht untersucht. Da jedoch die Elimination von Alectinib über die Nieren vernachlässigbar ist, ist bei Patienten mit schwerer Nierenfunktionsstörung keine Dosisanpassung erforderlich (siehe Abschnitt 5.2).
Ältere Patienten (≥ 65 Jahre)
Begrenzte Daten zur Sicherheit und Wirksamkeit von Alecensa bei Patienten im Alter von 65 Jahren und älter deuten nicht darauf hin, dass eine Dosisanpassung bei älteren Patienten erforderlich ist (siehe Abschnitt 5.2). Es liegen keine Daten zu Patienten im Alter von über 80 Jahren vor.
Kinder und Jugendliche
Die Sicherheit und Wirksamkeit von Alecensa bei Kindern und Jugendlichen unter 18 Jahren ist nicht erwiesen. Es liegen keine Daten vor.
Extrem hohes Körpergewicht (> 130 kg)
Obwohl Pharmakokinetik(PK)-Simulationen für Alecensa nicht auf eine niedrige Exposition bei Patienten mit extrem hohem Körpergewicht (d. h. > 130 kg) hindeuten, wird Alectinib im Körper weitgehend verteilt. An den klinischen Studien mit Alectinib nahmen Patienten mit einem Körpergewicht von 36,9 kg bis 123 kg teil. Es liegen keine Daten zu Patienten mit einem Körpergewicht von über 130 kg vor.
Art der Anwendung
Alecensa ist zum Einnehmen bestimmt. Die Hartkapseln sind im Ganzen zu schlucken und dürfen nicht geöffnet oder aufgelöst werden. Sie müssen zusammen mit Nahrungsmitteln eingenommen werden (siehe Abschnitt 5.2).
Überempfindlichkeit gegen Alectinib oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
Interstitielle Lungenerkrankung (ILD)/Pneumonitis
Fälle von ILD/Pneumonitis wurden in klinischen Studien mit Alecensa berichtet (siehe Abschnitt 4.8). Patienten sind auf pulmonale Symptome, die auf eine Pneumonitis hinweisen, zu überwachen. Die Behandlung mit Alecensa ist bei Patienten, bei denen eine ILD/Pneumonitis diagnostiziert wurde, umgehend zu unterbrechen und dauerhaft abzubrechen, wenn keine anderen, möglichen Ursachen für die ILD/Pneumonitis identifiziert werden konnten (siehe Abschnitt 4.2).
Hepatotoxizität
In den zulassungsrelevanten klinischen Studien zu Alecensa traten bei Patienten sowohl Erhöhungen der Alanin-Aminotransferase (ALT) und der Aspartat-Aminotransferase (AST) um mehr als das 5‑Fache des oberen Normalwerts (ULN) als auch Erhöhungen des Bilirubins um mehr als 3 x ULN auf (siehe Abschnitt 4.8). Die Mehrzahl dieser Ereignisse trat während der ersten 3 Behandlungsmonate auf. In den zulassungsrelevanten klinischen Studien zu Alecensa wurde berichtet, dass bei drei Patienten mit AST/ALT-Erhöhungen von Grad 3 – 4 ein arzneimittelbedingter Leberschaden festgestellt wurde. Gleichzeitige Erhöhungen der ALT oder AST höher oder gleich 3 x ULN und Gesamtbilirubin höher oder gleich 2 x ULN mit einem normalen Wert der alkalischen Phosphatase traten bei einem Patienten in den klinischen Studien zu Alecensa auf.
Die Leberfunktion, einschließlich ALT, AST und Gesamtbilirubin, sollte vor Behandlungsbeginn und dann alle 2 Wochen während der ersten 3 Behandlungsmonate überwacht werden. Danach sollten in regelmäßigen Abständen Kontrollen erfolgen, da die Ereignisse auch nach 3 Monaten auftreten können. Bei Patienten, die Erhöhungen der Aminotransferasen oder des Bilirubins entwickeln, sind häufigere Kontrollen durchzuführen. Basierend auf dem Schweregrad der Nebenwirkung ist die Behandlung mit Alecensa zu unterbrechen und mit reduzierter Dosis wieder aufzunehmen oder dauerhaft abzubrechen, wie in Tabelle 2 beschrieben (siehe Abschnitt 4.2).
Schwere Myalgie und Erhöhung der Kreatinphosphokinase (CPK)
In den zulassungsrelevanten klinischen Studien zu Alecensa wurden Myalgien oder Schmerzen des Muskel- und Skelettsystems einschließlich Ereignissen von Grad 3 bei Patienten berichtet (siehe Abschnitt 4.8).
In den zulassungsrelevanten klinischen Studien zu Alecensa traten CPK-Erhöhungen, einschließlich Ereignisse von Grad 3, auf (siehe Abschnitt 4.8). Die mediane Zeit bis zum Auftreten einer CPK-Erhöhung von Grad ≥ 3 betrug in den klinischen Studien (BO40336, BO28984, NP28761, NP28673) 15 Tage.
Patienten sollten angewiesen werden, über unerklärliche Muskelschmerzen, Druckempfindlichkeit oder Schwächegefühl zu berichten. Im ersten Behandlungsmonat sind CPK-Spiegel alle 2 Wochen zu bestimmen bzw. bei Patienten mit Symptomen wie jeweils klinisch indiziert. Basierend auf dem Schweregrad der CPK-Erhöhung ist die Behandlung mit Alecensa zu unterbrechen und danach wieder mit der ursprünglichen oder mit reduzierter Dosis aufzunehmen (siehe Abschnitt 4.2).
Bradykardie
Unter Behandlung mit Alecensa kann eine symptomatische Bradykardie auftreten (siehe Abschnitt 4.8). Die Herzfrequenz und der Blutdruck sind, wie klinisch indiziert, zu überwachen. Bei Auftreten einer asymptomatischen Bradykardie ist keine Dosisanpassung erforderlich (siehe Abschnitt 4.2). Wenn bei Patienten eine symptomatische Bradykardie oder lebensbedrohliche Ereignisse auftreten, müssen gleichzeitig angewendete Arzneimittel, die bekanntermaßen eine Bradykardie verursachen, sowie antihypertensive Arzneimittel überprüft werden und die Behandlung mit Alecensa muss, wie in Tabelle 2 beschrieben, angepasst werden (siehe Abschnitte 4.2 und 4.5, „P‑gp-Substrate“ und „BCRP-Substrate“).
Hämolytische Anämie
Hämolytische Anämie wurde unter Behandlung mit Alecensa berichtet (siehe Abschnitt 4.8). Wenn die Hämoglobinkonzentration unter 10 g/dl liegt und der Verdacht auf eine hämolytische Anämie besteht, ist die Behandlung mit Alecensa zu unterbrechen und es sind entsprechende Laboruntersuchungen einzuleiten. Wenn eine hämolytische Anämie bestätigt wird, ist nach Abklingen der Anämie die Behandlung mit Alecensa mit reduzierter Dosis wie in Tabelle 2 beschrieben wiederaufzunehmen (siehe Abschnitt 4.2).
Gastrointestinale Perforation
Es wurden Fälle gastrointestinaler Perforation bei Patienten mit erhöhtem Risiko (z. B. Divertikulitis in der Anamnese, Metastasen im Gastrointestinaltrakt, gleichzeitige Anwendung von Arzneimitteln mit bekanntem Risiko für gastrointestinale Perforation) unter Anwendung von Alectinib berichtet. Das Absetzen von Alecensa sollte bei Patienten, die eine gastrointestinale Perforation entwickeln, in Betracht gezogen werden. Die Patienten sind über die Anzeichen und Symptome einer gastrointestinalen Perforation zu informieren und anzuhalten bei Auftreten dieser Anzeichen und Symptome umgehend einen Arzt aufzusuchen.
Lichtempfindlichkeit
Lichtempfindlichkeit gegenüber Sonnenlicht wurde unter Anwendung von Alecensa berichtet (siehe Abschnitt 4.8). Die Patienten sind anzuweisen, während der Anwendung und noch mindestens 7 Tage nach Beendigung der Behandlung längere Sonnenexpositionen zu vermeiden. Die Patienten sind ebenfalls dazu anzuhalten, eine Sonnencreme mit UVA/UVB-Breitspektrum-Lichtschutzfaktor sowie einen Lippenschutz (Lichtschutzfaktor [LSF] ≥ 50) zu verwenden, um sich gegen einen möglichen Sonnenbrand zu schützen.
Embryo-fetale Toxizität
Alecensa kann bei Gabe an Schwangere den Fetus schädigen. Patientinnen im gebärfähigen Alter müssen während der Behandlung mit Alecensa und für mindestens 5 Wochen nach der letzten Dosis von Alecensa hochwirksame Verhütungsmethoden anwenden (siehe Abschnitte 4.5, 4.6 und 5.3). Männliche Patienten mit Partnerinnen im gebärfähigen Alter müssen während der Behandlung und für mindestens 3 Monate nach der letzten Dosis von Alecensa hochwirksame Verhütungsmethoden anwenden (siehe Abschnitte 4.6 und 5.3).
Lactoseintoleranz
Dieses Arzneimittel enthält Lactose. Patienten mit der seltenen hereditären Galactose-Intoleranz, einem kongenitalen Lactase-Mangel oder einer Glucose-Galactose-Malabsorption sollten dieses Arzneimittel nicht einnehmen.
Natriumgehalt
Dieses Arzneimittel enthält 48 mg Natrium pro Tagesdosis (1 200 mg), entsprechend 2,4 % der von der WHO für einen Erwachsenen empfohlenen maximalen täglichen Natriumaufnahme mit der Nahrung von 2 g.
Wirkungen von anderen Arzneimitteln auf Alectinib
Basierend auf In-vitro-Daten ist CYP3A4 das primäre Enzym, das den Metabolismus sowohl von Alectinib als auch von dessen aktivem Hauptmetaboliten M4 vermittelt. CYP3A trägt mit 40 % – 50 % zum Gesamtlebermetabolismus bei. M4 zeigte eine vergleichbare In-vitro-Potenz und Aktivität gegen ALK.
CYP3A-Induktoren
Die gleichzeitige Anwendung wiederholter oraler Dosen von einmal täglich 600 mg Rifampicin, einem starken CYP3A-Induktor, zusammen mit einer oralen Einzeldosis von 600 mg Alectinib, verminderte Cmax und AUCinf von Alectinib um 51 % bzw. 73 % und erhöhte Cmax und AUCinf von M4 2,20- bzw. 1,79‑fach. Die Auswirkung auf die kombinierte Exposition mit Alectinib und M4 war geringfügig, mit einer Reduktion von Cmax und AUCinf um 4 % bzw. 18 %. Basierend auf den Auswirkungen der kombinierten Exposition mit Alectinib und M4 sind bei einer gleichzeitigen Anwendung von Alecensa und CYP3A-Induktoren keine Dosisanpassungen erforderlich. Für Patienten, die gleichzeitig starke CYP3A-Induktoren (einschließlich, aber nicht beschränkt auf Carbamazepin, Phenobarbital, Phenytoin, Rifabutin, Rifampicin und Johanniskraut [Hypericum perforatum]) einnehmen, wird eine angemessene Überwachung empfohlen.
CYP3A-Inhibitoren
Die gleichzeitige Anwendung wiederholter oraler Dosen von zweimal täglich 400 mg Posaconazol, einem starken CYP3A-Inhibitor, zusammen mit einer oralen Einzeldosis von 300 mg Alectinib, erhöhte Cmax und AUCinf von Alectinib auf das 1,18- bzw. 1,75-Fache und verminderte Cmax und AUCinf von M4 um 71 % bzw. 25 %. Die Auswirkung auf die kombinierte Exposition mit Alectinib und M4 war geringfügig, mit einer Reduktion von Cmax um 7 % und einer Erhöhung von AUCinf auf das 1,36-Fache. Basierend auf den Auswirkungen auf die kombinierte Exposition mit Alectinib und M4 sind bei einer gleichzeitigen Anwendung von Alecensa und CYP3A-Inhibitoren keine Dosisanpassungen erforderlich. Für Patienten, die gleichzeitig starke CYP3A-Inhibitoren (einschließlich, aber nicht beschränkt auf Ritonavir, Saquinavir, Telithromycin, Ketoconazol, Itraconazol, Voriconazol, Posaconazol, Nefazodon, Grapefruit oder Bitterorangen) einnehmen, wird eine angemessene Überwachung empfohlen.
Arzneimittel, die den gastrischen pH-Wert erhöhen
Esomeprazol, ein Protonenpumpeninhibitor, zeigte bei wiederholter Gabe von 40 mg einmal täglich keine klinisch relevante Wirkung auf die kombinierte Exposition mit Alectinib und M4. Daher sind bei gleichzeitiger Anwendung von Alecensa und Protonenpumpeninhibitoren oder anderen Arzneimitteln, die den gastrischen pH-Wert erhöhen (z. B. H2-Rezeptorantagonisten oder Antazida), keine Dosisanpassungen erforderlich.
Wirkung von Transportern auf die Verfügbarkeit von Alectinib
M4 ist ein P-Glykoprotein(P-gp)-Substrat. Obwohl Alectinib P-gp inhibiert, ist nicht zu erwarten, dass eine gleichzeitige Anwendung von Alectinib und P-gp-Inhibitoren eine wesentliche Wirkung auf die M4-Exposition zeigt.
Wirkungen von Alectinib auf andere Arzneimittel
CYP-Substrate
In vitro zeigen Alectinib und M4 eine schwache, zeitabhängige Inhibierung von CYP3A4; in klinischen Konzentrationen zeigt Alectinib in vitro ein schwaches Induktionspotenzial für CYP3A4 und CYP2B6.
Wiederholte Gaben von 600 mg Alectinib hatten keine Auswirkung auf die Exposition mit Midazolam (2 mg), ein sensitives CYP3A-Substrat. Daher ist für gleichzeitig angewendete CYP3A-Substrate keine Dosisanpassung erforderlich.
Das Risiko einer Induktion von CYP2B6 und Pregnan-X-Rezeptor(PXR)-regulierten Enzymen, abgesehen von CYP3A4, kann nicht vollkommen ausgeschlossen werden. Die Wirksamkeit gleichzeitig angewendeter oraler Kontrazeptiva kann verringert sein.
P‑gp-Substrate
In vitro sind Alectinib und sein aktiver Hauptmetabolit M4 Inhibitoren des Effluxtransporters P-gp. Deswegen können Alectinib und M4 das Potenzial besitzen, die Plasmakonzentrationen gleichzeitig angewendeter Substrate des P-gp-Transporters zu erhöhen. Bei gleichzeitiger Anwendung von Alecensa und P-gp-Substraten (z. B. Digoxin, Dabigatranetexilat, Topotecan, Sirolimus, Everolimus, Nilotinib und Lapatinib) wird eine angemessene Überwachung empfohlen.
Breast Cancer Resistance Protein(BCRP)-Substrate
In vitro sind Alectinib und M4 Inhibitoren des Effluxtransporters BCRP. Deswegen können Alectinib und M4 das Potenzial besitzen, die Plasmakonzentrationen gleichzeitig angewendeter Substrate von BCRP zu erhöhen. Bei gleichzeitiger Anwendung von Alecensa und BCRP-Substraten (z. B. Methotrexat, Mitoxantron, Topotecan und Lapatinib) wird eine angemessene Überwachung empfohlen.
Frauen im gebärfähigen Alter
Frauen im gebärfähigen Alter müssen angewiesen werden, während der Behandlung mit Alecensa eine Schwangerschaft zu vermeiden (siehe Abschnitt 4.4).
Verhütung bei Patientinnen
Patientinnen im gebärfähigen Alter, die Alecensa erhalten, müssen während der Behandlung und für mindestens 5 Wochen nach der letzten Dosis von Alecensa hochwirksame Verhütungsmethoden anwenden (siehe Abschnitte 4.4 und 4.5).
Verhütung bei männlichen Patienten
Männliche Patienten mit Partnerinnen im gebärfähigen Alter müssen während der Behandlung und für mindestens 3 Monate nach der letzten Dosis von Alecensa hochwirksame Verhütungsmethoden anwenden (siehe Abschnitt 4.4).
Schwangerschaft
Es gibt keine oder nur begrenzte Daten zur Anwendung von Alectinib bei Schwangeren. Aufgrund seines Wirkmechanismus kann Alectinib bei Verabreichung an Schwangere den Fetus schädigen. Tierexperimentelle Studien haben eine Reproduktionstoxizität gezeigt (siehe Abschnitt 5.3).
Patientinnen, die während der Anwendung oder bis zu 5 Wochen nach der letzten Dosis von Alecensa schwanger werden, müssen ihren Arzt kontaktieren und auf die potenzielle Schädigung des Fetus hingewiesen werden.
Männliche Patienten mit Partnerinnen, die schwanger werden, während der männliche Patient Alecensa einnimmt oder während der 3 Monate nach Einnahme der letzten Alecensa Dosis, müssen ihren Arzt kontaktieren; und ihre Partnerin soll ärztlichen Rat einholen, da aufgrund des aneugenen Potenzials eine Schädigung des Fetus möglich ist (siehe Abschnitt 5.3).
Stillzeit
Es ist nicht bekannt, ob Alectinib und/oder seine Metabolite in die Muttermilch übertreten. Ein Risiko für das Neugeborene/den Säugling kann nicht ausgeschlossen werden. Während der Behandlung mit Alecensa sollte nicht gestillt werden.
Fertilität
Es wurden keine tierexperimentellen Studien zur Fertilität durchgeführt, um die Auswirkung von Alectinib zu untersuchen. In allgemeinen Toxizitätsstudien wurden keine Nebenwirkungen auf die männlichen und weiblichen Fortpflanzungsorgane beobachtet (siehe Abschnitt 5.3).
Alecensa hat geringen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen. Vorsicht ist beim Führen eines Fahrzeugs oder beim Bedienen von Maschinen geboten, da bei Patienten während der Anwendung von Alecensa symptomatische Bradykardie (z. B. Synkope, Schwindel, Hypotonie) oder Sehstörungen auftreten können (siehe Abschnitt 4.8).
Zusammenfassung des Sicherheitsprofils
Die im Folgenden beschriebenen Daten beziehen sich auf die Alecensa Exposition bei 533 Patienten mit reseziertem oder fortgeschrittenem ALK-positivem NSCLC. Diese Patienten erhielten Alecensa in der empfohlenen Dosis von 600 mg zweimal täglich in den klinischen Zulassungsstudien zur adjuvanten Therapie des resezierten NSCLC (BO40336, ALINA) oder zur Therapie des fortgeschrittenen NSCLC (BO28984, ALEX; NP28761; NP28673). Siehe Abschnitt 5.1 für weitere Informationen zu Teilnehmern an klinischen Studien.
In der Studie BO40336 (ALINA; n = 128) lag die mediane Dauer der Exposition gegenüber Alecensa bei 23,9 Monaten. In der Studie BO28984 (ALEX, n = 152) betrug die mediane Dauer der Exposition gegenüber Alecensa 28,1 Monate. In den klinischen Phase-II-Studien (NP28761, NP28673, n = 253) betrug die mediane Dauer der Exposition gegenüber Alecensa 11,2 Monate.
Die häufigsten Nebenwirkungen (≥ 20 %) waren Obstipation, Myalgie, Ödem, erhöhtes Bilirubin, erhöhte AST, Anämie, Ausschlag und erhöhte ALT.
Tabellarische Auflistung der Nebenwirkungen
In Tabelle 3 sind die Nebenwirkungen, die bei Patienten während der Behandlung mit Alecensa in allen klinischen Studien (BO40336, BO28984, NP28761, NP28673) aufgetreten sind, aufgeführt.
Die in Tabelle 3 aufgelisteten Nebenwirkungen sind nach Systemorganklasse und Häufigkeitskategorien aufgeführt, wobei folgende Konvention verwendet wurde: sehr häufig (≥ 1/10), häufig (≥ 1/100, < 1/10), gelegentlich (≥ 1/1 000, < 1/100), selten (≥ 1/10 000, < 1/1 000), sehr selten (< 1/10 000). Innerhalb jeder Systemorganklasse sind die Nebenwirkungen nach abnehmender Häufigkeit und Schweregrad angegeben. Die Nebenwirkungen werden innerhalb jeder Häufigkeits- und Schweregradgruppe in absteigender Reihenfolge der Schwere dargestellt.
Tabelle 3: Nebenwirkungen, die in den klinischen Studien (BO40336, BO28984, NP28761, NP28673, n = 533) mit Alecensa berichtet wurden
Systemorganklasse |
Alecensa |
|
Häufigkeitskategorie (alle Grade) |
Häufigkeitskategorie (Grad 3 – 4) |
|
Erkrankungen des Blutes und des Lymphsystems |
||
Anämie1) |
Sehr häufig |
Häufig |
Hämolytische Anämie2) |
Häufig |
-* |
Erkrankungen des Nervensystems |
||
Dysgeusie3) |
Häufig |
Gelegentlich |
Augenerkrankungen |
||
Sehstörungen4) |
Häufig |
-* |
Herzerkrankungen |
||
Bradykardie5) |
Sehr häufig |
-* |
Erkrankungen der Atemwege, des Brustraums und Mediastinums |
||
Interstitielle Lungenerkrankung/Pneumonitis |
Häufig |
Gelegentlich |
Erkrankungen des Gastrointestinaltrakts |
||
Diarrhö |
Sehr häufig |
Häufig |
Erbrechen |
Sehr häufig |
Gelegentlich |
Obstipation |
Sehr häufig |
Gelegentlich |
Übelkeit |
Sehr häufig |
Gelegentlich |
Stomatitis6) |
Häufig |
Gelegentlich |
Leber- und Gallenerkrankungen |
||
AST erhöht |
Sehr häufig |
Häufig |
ALT erhöht |
Sehr häufig |
Häufig |
Bilirubin erhöht7) |
Sehr häufig |
Häufig |
Alkalische Phosphatase erhöht |
Sehr häufig |
Gelegentlich |
Arzneimittelbedingter Leberschaden8) |
Gelegentlich |
Gelegentlich |
Erkrankungen der Haut und des Unterhautgewebes |
||
Ausschlag9) |
Sehr häufig |
Häufig |
Photosensitivität |
Häufig |
Gelegentlich |
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen |
||
Myalgie10) |
Sehr häufig |
Gelegentlich |
Kreatinphosphokinase im Blut erhöht |
Sehr häufig |
Häufig |
Erkrankungen der Nieren und Harnwege |
||
Kreatinin im Blut erhöht |
Sehr häufig |
Gelegentlich** |
Akute Nierenschädigung |
Häufig |
Gelegentlich** |
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort |
||
Ödem11) |
Sehr häufig |
Gelegentlich |
Untersuchungen |
||
Gewichtszunahme |
Sehr häufig |
Gelegentlich |
Stoffwechsel- und Ernährungsstörungen | ||
Hyperurikämie12) |
Häufig |
-* |
* Es wurden keine Nebenwirkungen von Grad 3 - 4 beobachtet.
** Schließt ein Ereignis von Grad 5 ein (beobachtet im Rahmen des fortgeschrittenen NSCLC).
1) Schließt Fälle von Anämie, erniedrigtem Hämoglobin, und normochromer normozytärer Anämie ein.
2) Fälle berichtet in der Studie BO40336 (n = 128)
3) Schließt Fälle von Dysgeusie, Hypogeusie und Geschmacksstörung ein.
4) Schließt Fälle von verschwommenem Sehen, Sehverschlechterung, Mouches volantes, verringerter Sehschärfe, Asthenopie, Doppeltsehen, Photophobie und Photopsie ein.
5) Schließt Fälle von Bradykardie und Sinusbradykardie ein.
6) Schließt Fälle von Stomatitis und Mundulzerationen ein.
7) Schließt Fälle von erhöhtem Bilirubin im Blut, Hyperbilirubinämie, erhöhtem konjugierten Bilirubin und erhöhtem unkonjugierten Bilirubin im Blut ein.
8) Schließt zwei Patienten mit gemeldetem arzneimittelbedingtem Leberschaden (gemäß MedDRA-Terminologie) ein sowie einen Patienten mit gemeldeten erhöhten AST- und ALT-Spiegeln von Grad 4, bei dem ein arzneimittelbedingter Leberschaden mittels Leberbiopsie festgestellt wurde.
9) Schließt Fälle von Ausschlag, makulo-papulösem Ausschlag, Dermatitis, akneiformer Dermatitis, Erythem, papulösem Ausschlag, Ausschlag mit Juckreiz, makulärem Ausschlag, exfoliativem Ausschlag und erythematösem Ausschlag ein.
10) Schließt Fälle von Myalgie, Schmerzen des Muskel- und Skelettsystems und Arthralgie ein.
11) Schließt Fälle von peripherem Ödem, Ödem, generalisiertem Ödem, Augenlidödem, Periorbitalödem, Gesichtsödem, lokalisiertem Ödem, peripherer Schwellung, Schwellung des Gesichts, Schwellung der Lippe, Schwellung, Gelenkschwellung und Schwellung des Augenlids ein.
12) Schließt Fälle von Hyperurikämie und erhöhten Harnsäurewerten im Blut ein.
Beschreibung ausgewählter Arzneimittelnebenwirkungen
Interstitielle Lungenerkrankung (ILD)/Pneumonitis
In allen klinischen Studien trat eine ILD/Pneumonitis bei 1,7 % der Patienten auf, die mit Alecensa behandelt wurden. Von diesen Fällen waren 0,4 % von Grad 3, und bei 1,1 % der Patienten führte die ILD/Pneumonitis zum Absetzen der Behandlung. Bei 0,4 % der Patienten führte das Ereignis zu Dosisanpassungen. In der klinischen Phase-III-Studie BO28984 wurde keine ILD/Pneumonitis von Grad 3 oder 4 bei den mit Alecensa behandelten Patienten beobachtet, gegenüber 2,0 % der Patienten, die Crizotinib erhielten. In keiner der klinischen Studien traten tödliche Fälle von ILD auf. Die Patienten sind auf pulmonale Symptome, die auf eine Pneumonitis hinweisen, zu überwachen (siehe Abschnitte 4.2 und 4.4).
Hepatotoxizität
In allen klinischen Studien hatten drei Patienten einen dokumentierten arzneimittelbedingten Leberschaden (darunter zwei Patienten mit dem gemeldeten Begriff arzneimittelbedingter Leberschaden und ein Patient mit berichteten Erhöhungen von AST und ALT von Grad 4, bei dem ein arzneimittelbedingter Leberschaden durch Leberbiopsie dokumentiert wurde). Die Nebenwirkungen erhöhte AST- und ALT-Spiegel (23,6 % bzw. 20,5 %) wurden bei Patienten, die im Rahmen der klinischen Studien mit Alecensa behandelt wurden, berichtet. Die Mehrzahl dieser Ereignisse war von Grad 1 oder 2. Ereignisse von Grad ≥ 3 für erhöhte AST- und ALT-Spiegel wurden bei 3,0 % bzw. 3,2 % der Patienten berichtet. Die Ereignisse traten generell während der ersten 3 Behandlungsmonate auf, waren in der Regel vorübergehend und bildeten sich nach zeitweiliger Unterbrechung der Behandlung mit Alecensa (berichtet bei 2,3 % bzw. 3,6 % der Patienten) oder einer Dosisreduktion (1,7 % bzw. 1,5 %) zurück. Bei 1,3 % bzw. 1,5 % der Patienten führten AST- oder ALT-Erhöhungen zu einem Absetzen der Behandlung mit Alecensa. In der klinischen Phase-III-Studie BO28984 wurden ALT- oder AST-Erhöhungen von Grad 3 oder 4 bei 4,6 % bzw. 5,3 % der Patienten, die Alecensa erhielten, gegenüber 16,6 % und 10,6 % der Patienten, die Crizotinib erhielten, berichtet.
In den klinischen Studien wurden bei 25,9 % der mit Alecensa behandelten Patienten erhöhte Bilirubinwerte als Nebenwirkung berichtet. Die Mehrzahl der Ereignisse war von Grad 1 und 2. Ereignisse von Grad ≥ 3 wurden bei 3,9 % der Patienten berichtet. Die Ereignisse traten generell während der ersten 3 Behandlungsmonate auf, waren in der Regel vorübergehend und die Mehrzahl bildete sich nach Dosisanpassung zurück. Bei 8,3 % der Patienten führten Erhöhungen der Bilirubinwerte zu Dosisanpassungen und bei 2,1 % der Patienten führten die Erhöhungen der Bilirubinwerte zu einem Absetzen der Behandlung mit Alecensa. In der klinischen Phase‑III‑Studie BO28984 traten Bilirubin-Erhöhungen von Grad 3 oder 4 bei 5,9 % der Patienten, die Alecensa erhielten, auf, aber bei keinem Patienten unter Crizotinib.
Gleichzeitige Erhöhungen der ALT oder AST höher oder gleich 3 x ULN und des Gesamtbilirubins höher oder gleich 2 x ULN bei normaler alkalischer Phosphatase traten bei einem Patienten (0,2 %), der im Rahmen einer klinischen Studie mit Alecensa behandelt wurde, auf.
Die Leberfunktion der Patienten, einschließlich ALT, AST und Gesamtbilirubin, sollte wie in Abschnitt 4.4 beschrieben überwacht und das Vorgehen wie in Abschnitt 4.2 empfohlen befolgt werden.
Bradykardie
Fälle von Bradykardie (11,3 %) von Grad 1 oder 2 wurden bei Patienten berichtet, die in den klinischen Studien mit Alecensa behandelt wurden. Bei keinem Patienten traten Ereignisse eines Schweregrades ≥ 3 auf. 102 von 521 behandelten Patienten (19,6 %), von denen serielle EKGs vorlagen, hatten nach Einnahme von Alecensa eine Herzfrequenz von unter 50 Schlägen pro Minute (bpm). In der klinischen Phase-III-Studie BO28984 hatten 12,4 % der mit Alecensa behandelten Patienten nach der Gabe (post-Dosis) eine Herzfrequenz unter 50 bpm gegenüber 17,6 %, der mit Crizotinib behandelten Patienten. Patienten, die eine symptomatische Bradykardie entwickeln, sollten wie in den Abschnitten 4.2 und 4.4 empfohlen behandelt werden. Kein Fall von Bradykardie führte zum Absetzen der Behandlung mit Alecensa.
Schwere Myalgie und Erhöhungen der CPK
Fälle von Myalgie (35,3 %), einschließlich Myalgie-Ereignisse (24,2 %), Arthralgie (16,3 %) sowie Schmerzen des Muskel- und Skelettsystems (0,8 %) wurden bei Patienten berichtet, die in allen klinischen Studien mit Alecensa behandelt wurden. Die Mehrzahl der Ereignisse war von Grad 1 oder 2. Bei 5 Patienten (0,9 %) traten Ereignisse von Grad 3 auf. Eine Dosisanpassung der Behandlung mit Alecensa aufgrund dieser unerwünschten Ereignisse war bei 9 Patienten (1,7 %) erforderlich. Die Behandlung mit Alecensa wurde bei keinem dieser Ereignisse von Myalgie abgesetzt. Erhöhungen der CPK traten in allen klinischen Studien bei 56,2 % der 491 Patienten auf, von denen CPK-Laborwerte vorlagen. Die Inzidenz der CPK-Erhöhungen von Grad ≥ 3 betrug 5,5 %. Die mediane Zeit bis zum Auftreten einer CPK-Erhöhung von Grad ≥ 3 betrug in allen Studien 15 Tage. Dosisanpassungen aufgrund von CPK-Erhöhungen waren bei 5,4 % der Patienten erforderlich; ein Absetzen der Behandlung mit Alecensa wegen einer CPK-Erhöhung trat nicht auf. In der klinischen Studie BO28984 traten schwere Arthralgien bei einem Patienten (0,7 %) im Alectinib Arm sowie bei 2 Patienten (1,3 %) im Crizotinib Arm auf. Erhöhungen der CPK von Grad ≥ 3 wurden bei 3,3 % der Patienten, die Alecensa erhielten, und bei 4,6 % der Patienten, die Crizotinib erhielten, berichtet.
Hämolytische Anämie
Hämolytische Anämie wurde bei 3,1 % der Patienten beobachtet, die in klinischen Studien mit Alecensa behandelt wurden. Diese Fälle waren von Grad 1 oder 2 (nicht schwerwiegend) und führten nicht zum Absetzen der Behandlung (siehe Abschnitte 4.2 und 4.4).
Gastrointestinale Nebenwirkungen
Obstipation (39,6 %), Diarrhö (18,8 %), Übelkeit (17,6 %) und Erbrechen (12,4 %) waren die am häufigsten berichteten gastrointestinalen Reaktionen. Die meisten dieser Ereignisse waren von leichtem oder mäßigem Schweregrad; Ereignisse von Grad 3 wurden bei Diarrhö (1,1 %), Übelkeit (0,4 %), Obstipation (0,4 %) und Erbrechen (0,2 %) berichtet. Diese Ereignisse führten nicht zu einem Absetzen der Behandlung mit Alecensa. Die mediane Zeit bis zum Auftreten von Obstipation, Übelkeit, Diarrhö und/oder Erbrechen betrug in den klinischen Studien 21 Tage. Die Ereignisse nahmen nach dem ersten Behandlungsmonat an Häufigkeit ab. In der klinischen Phase-III-Studie BO28984 traten bei jeweils einem Patienten (0,7 %) im Alectinib Arm Ereignisse von Grad 3 und 4 bei Übelkeit und Obstipation auf, während Diarrhö bei 2 Patienten (1,3 %) im Alectinib Arm auftrat; die Inzidenz von Grad 3 und 4 Ereignissen bei Übelkeit, Erbrechen und Diarrhö lag bei 3,3 %, 3,3 % bzw. 2,0 % im Crizotinib Arm.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem
Bundesinstitut für Arzneimittel und Medizinprodukte
Abt. Pharmakovigilanz
Kurt-Georg-Kiesinger-Allee 3
53175 Bonn
Website: http://www.bfarm.de
anzuzeigen.
Patienten, bei denen es zu einer Überdosierung gekommen ist, sollten engmaschig überwacht und allgemeine unterstützende Maßnahmen eingeleitet werden. Es gibt kein spezifisches Antidot bei Überdosierung mit Alecensa.
Pharmakotherapeutische Gruppe: Antineoplastische Mittel, Proteinkinase-Inhibitor, ATC-Code: L01ED03.
Wirkmechanismus
Alectinib ist ein hoch selektiver und potenter ALK- und RET(rearranged during transfection)-Tyrosinkinase-Inhibitor. In präklinischen Studien führte eine Inhibierung der ALK-Tyrosinkinase-Aktivität zu einer Blockade der nachgeschalteten Signalwege einschließlich signal transducer and activator of transcription 3 (STAT3) und Phosphoinositid-3-Kinase (PI3K)/Proteinkinase B (AKT) und zu einer Induktion des Tumor-Zelltods (Apoptose).
Alectinib zeigte eine In-vitro- und In-vivo-Aktivität gegen mutierte Formen des ALK-Enzyms, einschließlich Mutationen, die für eine Resistenz gegenüber Crizotinib verantwortlich sind. Der Hauptmetabolit von Alectinib (M4) hat in vitro eine vergleichbare Wirksamkeit und Aktivität gezeigt.
Basierend auf präklinischen Daten ist Alectinib kein Substrat von P-gp oder BCRP, die beide Effluxtransporter in der Blut-Hirn-Schranke sind. Alectinib kann daher in das Zentralnervensystem übertreten und darin verbleiben.
Klinische Wirksamkeit und Sicherheit
Adjuvante Behandlung des resezierten ALK‑positiven NSCLC
Die Wirksamkeit von Alecensa bei der adjuvanten Behandlung von Patienten mit ALK‑positivem NSCLC nach vollständiger Tumorresektion wurde in einer globalen, randomisierten, offenen klinischen Phase‑III‑Studie (BO40336, ALINA) nachgewiesen. Geeignete Patienten mussten ein NSCLC Stadium IB (Tumoren ≥ 4 cm) bis Stadium IIIA gemäß der Stadieneinteilung der Union for International Cancer Control/American Joint Committee on Cancer (UICC/AJCC), 7. Auflage, aufweisen, deren ALK‑positive Erkrankung durch einen örtlich durchgeführten CE‑gekennzeichneten ALK‑Test oder mittels zentraler Testung mit dem Ventana ALK (D5F3) Immunhistochemie(IHC) Assay nachgewiesen wurde.
Die folgenden Auswahlkriterien definieren Patienten mit hohem Rezidivrisiko, die in das Anwendungsgebiet fallen, und spiegeln die Patientenpopulation mit NSCLC im Stadium IB (Tumoren ≥ 4 cm) – IIIA gemäß den UICC/AJCC-Staging-Kriterien, 7. Auflage, wider:
Tumorgröße ≥ 4 cm; oder Tumoren jeglicher Größe, die entweder mit einem N1- oder N2-Status einhergehen; oder Tumoren, die in thorakale Strukturen eindringen (direktes Eindringen in die parietale Pleura, die Brustwand, das Zwerchfell, den Nervus phrenicus, die mediastinale Pleura, den parietalen Herzbeutel, das Mediastinum, das Herz, die großen Gefäße, die Luftröhre, den Nervus laryngeus recurrens, die Speiseröhre, den Wirbelkörper oder die Carina); oder Tumoren, die den Hauptbronchus < 2 cm distal der Carina, aber nicht die Carina betreffen; oder Tumoren, die mit einer Atelektase oder obstruktiven Pneumonitis der gesamten Lunge einhergehen; oder Tumoren mit separaten Knoten im gleichen oder einem anderen ipsilateralen Lappen als dem primären.
Die Studie schloss keine Patienten mit N2-Status ein, deren Tumoren auch in das Mediastinum, das Herz, die großen Gefäße, die Luftröhre, den Nervus laryngeus recurrentis, die Speiseröhre, den Wirbelkörper oder die Carina eingedrungen waren, oder die separate(n) Tumorknoten in einem anderen ipsilateralen Lappen hatten.
Die Patienten wurden im Verhältnis 1:1 randomisiert und erhielten nach der Tumorresektion entweder Alecensa oder eine platinbasierte Chemotherapie. Die Randomisierung wurde nach ethnischer Herkunft (asiatisch und nicht-asiatisch) und Krankheitsstadium (IB, II und IIIA) stratifiziert. Alecensa wurde in der empfohlenen oralen Dosis von 600 mg zweimal täglich über einen Zeitraum von insgesamt 2 Jahren oder bis zum Wiederauftreten der Erkrankung oder dem Auftreten inakzeptabler Toxizität angewendet. Die platinbasierte Chemotherapie wurde entsprechend einem der folgenden Schemata über 4 Zyklen intravenös verabreicht, wobei jeder Zyklus 21 Tage dauerte:
Cisplatin 75 mg/m2 an Tag 1 plus Vinorelbin 25 mg/m2 an den Tagen 1 und 8
Cisplatin 75 mg/m2 an Tag 1 plus Gemcitabin 1 250 mg/m2 an den Tagen 1 und 8
Cisplatin 75 mg/m2 an Tag 1 plus Pemetrexed 500 mg/m2 an Tag 1
Im Falle einer Unverträglichkeit gegenüber einem cisplatinbasierten Behandlungsschema wurde Carboplatin anstelle von Cisplatin in den oben genannten Kombinationen in einer Dosis von Fläche unter der Plasma-Zeit-Kurve (AUC) von freiem Carboplatin von 5 mg/ml/min oder AUC von 6 mg/ml/min verabreicht.
Der primäre Wirksamkeitsendpunkt war das vom Prüfarzt bewertete krankheitsfreie Überleben (disease-free survival, DFS). Das DFS war definiert als die Zeit vom Datum der Randomisierung bis zum Datum des Auftretens eines der folgenden Ereignisse: Erstes dokumentiertes Wiederauftreten der Erkrankung, neues primäres NSCLC oder Tod jeglicher Ursache, je nachdem, was zuerst eintrat. Die sekundären und explorativen Wirksamkeitsendpunkte waren Gesamtüberleben (OS) und Zeit bis zum ZNS‑Rezidiv oder Tod (ZNS-DFS).
Insgesamt wurden 257 Patienten in die Studie aufgenommen: 130 Patienten wurden in den Arm mit Alecensa und 127 Patienten in den Chemotherapie-Arm randomisiert. Insgesamt betrug das mediane Alter 56 Jahre (Bereich: 26 bis 87 Jahre) und 24 % waren ≥ 65 Jahre alt, 52 % waren weiblich, 56 % waren Asiaten, 60 % waren lebenslange Nichtraucher, 53 % hatten einen ECOG PS von 0, 10 % der Patienten hatten Krankheitsstadium IB, 36 % Stadium II und 54 % Stadium IIIA.
Die Studie ALINA zeigte in den Patientenpopulationen mit Stadium II‑IIIA und Stadium IB (≥ 4 cm) ‑ IIIA (ITT) eine statistisch signifikante Verbesserung des DFS bei den mit Alecensa behandelten Patienten im Vergleich zu den mit Chemotherapie behandelten Patienten. Die OS‑Daten waren zum Zeitpunkt der DFS‑Analyse nicht ausgereift, wobei insgesamt 2,3 % Todesfälle berichtet wurden. Die mediane Nachbeobachtungszeit des Überlebens betrug 27,8 Monate im Arm mit Alecensa und 28,4 Monate im Chemotherapie-Arm.
Die Ergebnisse zur Wirksamkeit beim DFS sind in Tabelle 4 und Abbildung 1 zusammengefasst.
Tabelle 4: Vom Prüfarzt bewertete DFS‑Ergebnisse in der Studie ALINA
Wirksamkeitsparameter |
Stadium II‑IIIA |
ITT‑Population |
||
Alecensa |
Chemotherapie |
Alecensa |
Chemotherapie n = 127 |
|
Anzahl der DFS‑Ereignisse (%) |
14 (12,1) |
45 (39,1) |
15 (11,5) |
50 (39,4) |
Medianes DFS, Monate |
NE |
44,4 |
NE |
41,3 |
Stratifizierte HR |
0,24 |
0,24 |
||
p‑Wert (Log-Rank)* |
< 0,0001 |
< 0,0001 |
||
DFS = krankheitsfreies Überleben (disease-free survival); ITT = Intent-to-Treat; KI = Konfidenzintervall; NE = nicht schätzbar (not estimable); HR = Hazard Ratio
*Stratifiziert nach ethnischer Zugehörigkeit und in Stadium II ‑ IIIA, stratifiziert nach ethnischer Zugehörigkeit in Stadium IB - IIIA.
Abbildung 1: Kaplan-Meier-Kurve des vom Prüfarzt bewerteten DFS in der ITT‑Population
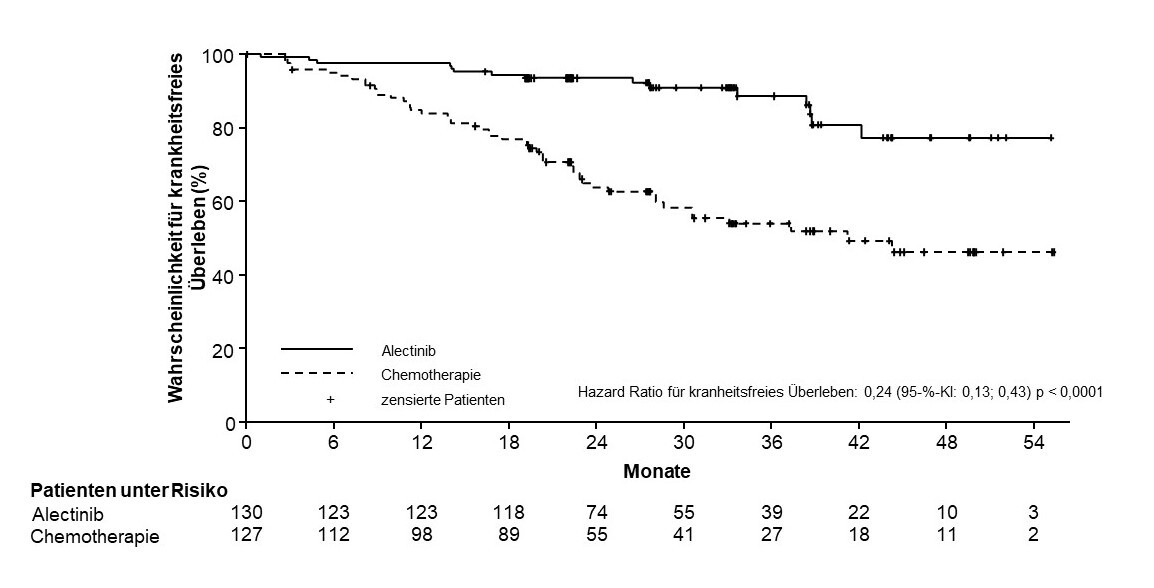
Behandlung des fortgeschrittenen ALK-positiven NSCLC
Behandlungsnaive Patienten
Die Sicherheit und Wirksamkeit von Alecensa wurden in einer globalen, randomisierten, offenen Phase-III-Studie (BO28984, ALEX) an nicht vorbehandelten ALK-positiven NSCLC-Patienten untersucht. Voraussetzung für die Randomisierung in die Studie war der positive Nachweis der ALK-Protein-Expression an Gewebeproben aller Patienten mittels zentraler Testung durch Ventana anti‑ALK (D5F3) Immunhistochemie.
Insgesamt wurden 303 Patienten in die Phase-III-Studie aufgenommen. Davon wurden 151 Patienten in den Crizotinib Arm und 152 Patienten in den Alecensa Arm randomisiert, wobei letztere Alecensa in der empfohlenen oralen Dosis von 600 mg zweimal täglich erhielten.
ECOG PS (Eastern Cooperative Oncology Group-Performance-Status) (0/1 vs. 2), die ethnische Abstammung (asiatisch vs. nicht-asiatisch) und Metastasen im zentralen Nervensystem (ZNS) bei Studienbeginn (ja vs. nein) waren Stratifizierungsfaktoren für die Randomisierung. Der primäre Endpunkt der Studie bestand im Nachweis der Überlegenheit von Alecensa gegenüber Crizotinib basierend auf dem progressionsfreien Überleben (PFS) gemäß Bewertung durch den Prüfarzt anhand der RECIST(Response Evaluation Criteria in Solid Tumors)-Kriterien Version 1.1. Die demographischen Merkmale und die Merkmale der Grunderkrankung bei Studienbeginn für Alecensa waren: medianes Alter von 58 Jahren (54 Jahre für Crizotinib), 55 % Frauen (58 % für Crizotinib), 55 % nicht-asiatisch (54 % für Crizotinib), 61 % negative Raucher-Anamnese (65 % für Crizotinib), 93 % ECOG PS von 0 oder 1 (93 % für Crizotinib), 97 % Krankheitsstadium IV (96 % für Crizotinib), 90 % Adenokarzinom-Histologie (94 % für Crizotinib), 40 % Metastasen im zentralen Nervensystem (ZNS) bei Studienbeginn (38 % für Crizotinib) und 17 % vorherige ZNS-Strahlentherapie (14 % für Crizotinib).
Die Studie erreichte ihren primären Endpunkt zum Zeitpunkt der primären Auswertung und zeigte eine statistisch signifikante Verbesserung des PFS nach Bewertung des Prüfarztes. Die Wirksamkeitsdaten sind in Tabelle 5 zusammengefasst und die Kaplan-Meier-Kurve für das vom Prüfarzt bewertete PFS ist in Abbildung 2 dargestellt. Zusätzlich ist die Kaplan-Meier-Kurve für das Gesamtüberleben aus der finalen OS-Analyse in Abbildung 3 dargestellt.
Tabelle 5: Zusammenfassung der Wirksamkeitsergebnisse aus Studie BO28984 (ALEX)
Crizotinib |
Alecensa |
|
Mediane Dauer der Nachbeobachtung (in Monaten) |
23,3 |
53,5 |
Primärer Wirksamkeitsparameter |
||
PFS (INV) † |
102 (68 %) |
62 (41 %) |
HR |
0,47 |
|
Sekundäre Wirksamkeitsparameter |
||
PFS (IRC)*, † |
92 (61 %) |
63 (41 %) |
HR |
0,50 |
|
Zeit bis zur ZNS-Progression (IRC)*, **, † |
|
|
Ursachen-spezifische HR |
0,16 |
|
12-Monate kumulative Inzidenz der ZNS-Progression (IRC) |
41,4 % |
9,4 % |
ORR (INV)*, ***, † |
114 (75,5 %) |
126 (82,9 %) |
Gesamtüberleben*, ‡ |
73 (48,3 %) |
76 (50,0 %) |
HR |
0,78 |
|
Dauer des Ansprechens (INV) ‡ |
n = 115 |
n = 126 |
|
ZNS-ORR bei Patienten mit messbaren ZNS-Metastasen bei Studienbeginn † ZNS-CR n (%) ZNS-DOR, Median (Monate) |
n = 22 11 (50,0 %) 1 (5 %) 5,5 |
n = 21 17 (81,0 %) 8 (38 %) 17,3 |
|
ZNS-ORR bei Patienten mit messbaren und nicht messbaren ZNS-Metastasen bei Studienbeginn (IRC) † ZNS-CR n (%) ZNS-DOR, Median (Monate) |
n = 58 15 (25,9 %) 5 (9 %) 3,7 |
n = 64 38 (59,4 %) 29 (45 %) NE |
* Wichtigste sekundäre Endpunkte als Teil des hierarchischen Testverfahrens
** Kompetitive Risikoanalyse von ZNS-Progression, systemischer Progression und Tod als konkurrierende Ereignisse
*** 2 Patienten im Crizotinib Arm und 6 Patienten im Alectinib Arm erreichten ein CR
† Daten aus der Primäranalyse
‡ Daten aus der finalen OS-Analyse, die durchgeführt wurde, nachdem 149 Todesfälle aufgetreten waren.
CR = Vollständiges Ansprechen (complete response); DOR = Dauer des Ansprechens (duration of response); HR = Hazard Ratio; IRC = unabhängiges Prüfkomitee (Independent Review Committee); INV = Prüfarzt (investigator); KI = Konfidenzintervall; NE = nicht schätzbar (not estimable); ORR = objektive Ansprechrate (objective response rate); PFS = progressionsfreies Überleben (progression-free survival); ZNS = Zentralnervensystem
Der PFS-Nutzen war bei Patienten mit ZNS-Metastasen bei Studienbeginn (Hazard Ratio [HR] = 0,40; 95-%-Konfidenzintervall [KI]: 0,25 – 0,64, medianes PFS für Alecensa = nicht schätzbar [NE], 95‑%‑KI: 9,2 – NE, medianes PFS für Crizotinib = 7,4 Monate, 95‑%‑KI: 6,6 – 9,6) und ohne ZNS-Metastasen bei Studienbeginn (HR = 0,51; 95‑%‑KI: 0,33 – 0,80, medianes PFS für Alecensa = NE, 95‑%-KI: NE, NE, medianes PFS für Crizotinib = 14,8 Monate, 95‑%‑KI: 10,8 – 20,3) einheitlich und weist auf eine Überlegenheit von Alecensa gegenüber Crizotinib in beiden Untergruppen hin.
Abbildung 2: Kaplan-Meier-Kurve des INV-bewerteten PFS in der Studie BO28984 (ALEX)
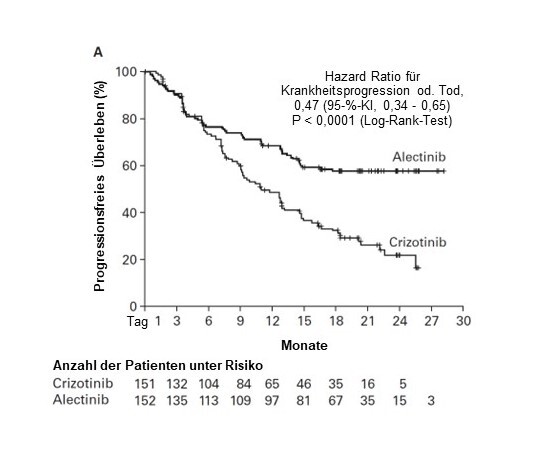
Abbildung 3: Kaplan-Meier-Kurve für das Gesamtüberleben in BO28984 (ALEX)

Mit Crizotinib vorbehandelte Patienten
Die Sicherheit und Wirksamkeit von Alecensa bei mit Crizotinib vorbehandelten Patienten mit ALK‑positivem NSCLC wurde in zwei klinischen Phase-I/II-Studien (NP28673 und NP28761) untersucht.
NP28673
Bei der Studie NP28673 handelt es sich um eine einarmige, multizentrische Studie der Phase I/II mit Patienten mit ALK-positivem fortgeschrittenem NSCLC, die unter einer vorherigen Behandlung mit Crizotinib progredient wurden. Zusätzlich zu Crizotinib konnten die Patienten eine vorherige Chemotherapie erhalten haben. Insgesamt wurden 138 Patienten in die Phase II der Studie eingeschlossen und mit Alecensa in der empfohlenen oralen Dosis von 600 mg zweimal täglich behandelt.
Der primäre Endpunkt war die Bewertung der Wirksamkeit von Alecensa durch die objektive Ansprechrate (ORR) gemäß der Auswertung des zentralen unabhängigen Prüfkomitees (IRC) unter Verwendung der RECIST-Kriterien Version 1.1, in der Gesamtpopulation (mit oder ohne vorherige Exposition mit einer zytotoxischen Chemotherapie). Der ko-primäre Endpunkt war die Bewertung der ORR gemäß der Auswertung des zentralen IRC unter Verwendung der RECIST-Kriterien, v1.1, bei Patienten mit vorheriger Exposition mit einer zytotoxischen Chemotherapie. Eine Untergrenze des Konfidenzintervalls der geschätzten ORR über der prä-spezifizierten Schwelle von 35 % würde ein statistisch signifikantes Ergebnis erzielen.
Die demographischen Patientendaten waren konsistent mit denen einer NSCLC ALK-positiven Population. Die demographischen Charakteristika der Gesamt-Studienpopulation waren 67 % Kaukasier, 26 % Asiaten, 56 % Frauen und das mediane Alter betrug 52 Jahre. Die Mehrzahl der Patienten hatte eine negative Raucheranamnese (70 %). Der Ausgangswert des ECOG PS betrug 0 oder 1 bei 90,6 % der Patienten und 2 bei 9,4 % der Patienten. Zum Zeitpunkt des Studieneinschlusses hatten 99 % der Patienten eine Erkrankung im Stadium IV. 61 % hatten Gehirnmetastasen und bei 96 % der Patienten wurden die Tumoren als Adenokarzinome klassifiziert. Unter den in die Studie eingeschlossenen Patienten waren 20 % unter vorheriger Behandlung mit Crizotinib allein und 80 % unter vorheriger Behandlung mit Crizotinib und mindestens einer Chemotherapie progredient.
Studie NP28761
Bei der Studie NP28761 handelt es sich um eine einarmige, multizentrische Studie der Phase I/II mit Patienten mit ALK-positivem, fortgeschrittenem NSCLC, die unter einer vorherigen Behandlung mit Crizotinib progredient waren. Zusätzlich zu Crizotinib konnten Patienten eine vorherige Behandlung mit einer Chemotherapie erhalten haben. Insgesamt wurden 87 Patienten in die Phase II der Studie eingeschlossen und mit Alecensa, in der empfohlenen oralen Dosis von 600 mg zweimal täglich, behandelt.
Der primäre Endpunkt war die Bewertung der Wirksamkeit von Alecensa durch die ORR, wie durch das zentrale IRC, unter Anwendung der RECIST-Kriterien v1.1, beurteilt. Eine Untergrenze des Konfidenzintervalls der geschätzten ORR über der prä-spezifizierten Schwelle von 35 % würde ein statistisch signifikantes Ergebnis erzielen.
Die demographischen Patientendaten waren konsistent mit denen einer NSCLC ALK-positiven Population. Die demographischen Charakteristika der Gesamt-Studienpopulation waren wie folgt: 84 % Kaukasier, 8 % Asiaten, 55 % Frauen und das mediane Alter betrug 54 Jahre. Die Mehrzahl der Patienten hatte eine negative Raucheranamnese (62 %). Der Ausgangswert des ECOG PS betrug 0 oder 1 bei 89,7 % der Patienten und 2 bei 10,3 % der Patienten. Zum Zeitpunkt des Studieneinschlusses hatten 99 % der Patienten eine Erkrankung im Stadium IV. 60 % hatten Gehirnmetastasen und bei 94 % der Patienten wurden die Tumoren als Adenokarzinome klassifiziert. Von den in die Studie eingeschlossenen Patienten waren 26 % unter vorheriger Behandlung mit Crizotinib allein und 74 % unter vorheriger Behandlung mit Crizotinib und mindestens einer Chemotherapie progredient.
Die wichtigsten Wirksamkeitsergebnisse aus den Studien NP28673 und NP28761 sind in Tabelle 6 zusammengefasst. Eine Zusammenfassung der gepoolten Analyse der ZNS-Endpunkte ist in Tabelle 7 dargestellt.
Tabelle 6: Wirksamkeitsergebnisse der Studien NP28673 und NP28761
Parameter |
NP28673 |
NP28761 |
Mediane Dauer der Nachbeobachtung (Monate) |
21 |
17 |
Primäre Wirksamkeitsparameter |
||
ORR (IRC) in der RE-Population |
n = 122 a n = 96 43 (44,8 %) |
n = 67 b |
|
Sekundäre Wirksamkeitsparameter PFS (IRC) |
n = 62 n = 138 |
n = 35 n = 87 |
DOR = Dauer des Ansprechens (duration of response); IRC = unabhängiges Prüfkomitee (independent review committee); NE = nicht schätzbar (not estimable); KI = Konfidenzintervall; ORR = objektive Ansprechrate (objective response rate); PFS = progressionsfreies Überleben (progression free survival); RE = auswertbares Ansprechen (response evaluable)
a Es gab 16 Patienten, die gemäß IRC keine messbare Erkrankung bei Studienbeginn hatten und nicht in die durch das IRC auswertbare Population in Bezug auf das Ansprechen eingeschlossen wurden.
b Es gab 20 Patienten, die gemäß IRC keine messbare Erkrankung bei Studienbeginn hatten und nicht in die durch das IRC auswertbare Population in Bezug auf das Ansprechen eingeschlossen wurden.
Die ORR-Ergebnisse aus den Studien NP28673 und NP28761 waren in allen Untergruppen im Hinblick auf Ausgangs-Patientencharakteristika, wie Alter, Geschlecht, ethnische Abstammung, ECOG PS, ZNS-Metastasen und vorherige Behandlung mit einer Chemotherapie konsistent, insbesondere unter Berücksichtigung der geringen Anzahl an Patienten in einigen Untergruppen.
Tabelle 7: Zusammenfassung der gepoolten Analyse der ZNS-Endpunkte aus den Studien NP28673 und NP28761
ZNS-Parameter (NP28673 und NP28761) |
Alecensa 600 mg zweimal täglich |
|
Patienten mit messbaren ZNS-Läsionen zu Beginn ZNS DOR (IRC) |
n = 50 32 (64,0 %) n = 32 |
KI = Konfidenzintervall; DOR = Dauer des Ansprechens (duration of response); IRC = unabhängiges Prüfkomitee (independent review committee); ORR = objektive Ansprechrate (objective response rate); NE = nicht schätzbar (not estimable)
Kinder und Jugendliche
Die Europäische Arzneimittel-Agentur hat für Alecensa eine Freistellung von der Verpflichtung zur Vorlage von Ergebnissen zu Studien in allen pädiatrischen Altersklassen in der Indikation Lungenkarzinom (kleinzelliges und nicht-kleinzelliges Karzinom) gewährt (siehe Abschnitt 4.2 bzgl. Informationen zur Anwendung bei Kindern und Jugendlichen).
Die pharmakokinetischen Parameter von Alectinib und seinem aktiven Hauptmetaboliten (M4) wurden bei ALK-positiven NSCLC-Patienten und gesunden Probanden charakterisiert. Basierend auf einer pharmakokinetischen Populationsanalyse lagen die geometrischen Mittel des Steady State Cmax, Cmin und AUC0-12hr (Variationskoeffizient in %) von Alectinib jeweils bei ca. 665 ng/ml (44,3 %), 572 ng/ml (47,8 %) bzw. 7 430 ng x h/ml (45,7 %). Die geometrischen Mittel des Steady State Cmax, Cmin und AUC0-12hr lagen für M4 jeweils bei ca. 246 ng/ml (45,4 %), 222 ng/ml (46,6 %) bzw. 2 810 ng x h/ml (45,9 %).
Resorption
Alectinib wurde bei ALK-positiven NSCLC-Patienten nach oraler Gabe von 600 mg zweimal täglich zusammen mit Nahrungsmitteln resorbiert, wobei Tmax nach etwa 4 bis 6 Stunden erreicht wurde.
Der Steady State von Alectinib wird bei kontinuierlicher Gabe von 600 mg zweimal täglich innerhalb von 7 Tagen erreicht. Das Akkumulationsverhältnis für das Dosisregime von 600 mg zweimal täglich betrug ca. das 6-Fache. Die pharmakokinetische Populationsanalyse weist darüber hinaus auf eine Dosisproportionalität von Alectinib im Dosierungsbereich von 300 mg bis 900 mg bei Einnahme zusammen mit Nahrungsmitteln hin.
Bei gesunden Probanden lag die absolute Bioverfügbarkeit von Alectinib Kapseln bei Einnahme zusammen mit Nahrungsmitteln bei 36,9 % (90‑%-KI: 33,9 %; 40,3 %).
Nach einer oralen Einzeldosis von 600 mg zusammen mit einer sehr fettreichen, hochkalorischen Mahlzeit stieg die Exposition mit Alectinib und M4 im Vergleich zum Nüchternzustand um ca. das 3‑Fache an (siehe Abschnitt 4.2).
Verteilung
Alectinib und sein Hauptmetabolit M4 werden unabhängig von der Wirkstoffkonzentration stark an menschliche Plasmaproteine gebunden (> 99 %). Die mittleren menschlichen In-vitro-Blut/Plasma-Konzentrationsverhältnisse von Alectinib und M4 liegen bei klinisch relevanten Konzentrationen bei 2,64 bzw. 2,50.
Das geometrische Mittel des Steady-State-Verteilungsvolumens (Vss) von Alectinib nach intravenöser Anwendung lag bei 475 l, was auf eine weitgehende Verteilung ins Gewebe hinweist.
Basierend auf In-vitro-Daten ist Alectinib kein P-gp-Substrat. Alectinib und M4 sind keine Substrate von BCRP oder der Organo-Anion-Transporter (OATP) 1B1/B3.
Biotransformation
In-vitro-Metabolismusstudien haben gezeigt, dass CYP3A4 das wesentliche CYP-Isoenzym darstellt, das für den Metabolismus von Alectinib und seines Hauptmetaboliten M4 verantwortlich ist. Es wird geschätzt, dass es zu 40 % – 50 % am Metabolismus von Alectinib beteiligt ist. Ergebnisse einer Massenbilanzierungsstudie am Menschen zeigten, dass Alectinib und M4 die wesentlichen im Plasma zirkulierenden Anteile waren und zusammen 76 % der Gesamtradioaktivität im Plasma ausmachten. Das geometrische Mittel des Metabolit/Ausgangssubstanz-Verhältnisses im Steady State beträgt 0,399.
Metabolit M1b wurde als ein weniger häufig auftretender Metabolit sowohl in vitro als auch im Humanplasma gesunder Probanden entdeckt. Die Bildung des Metaboliten M1b und seines Nebenisomers M1a wird wahrscheinlich durch eine Kombination von CYP-Isozymen (einschließlich anderer Isozyme als CYP3A) und Aldehyd-Dehydrogenase (ALDH)-Enzymen katalysiert.
In-vitro-Studien weisen darauf hin, dass weder Alectinib noch sein aktiver Hauptmetabolit (M4) in klinisch relevanten Konzentrationen CYP1A2, CYP2B6, CYP2C9, CYP2C19 oder CYP2D6 inhibieren. OATP1B1/OATP1B3, OAT1, OAT3 oder OCT2 wurde in vitro durch Alectinib in klinisch relevanten Konzentrationen nicht gehemmt.
Elimination
Nach oraler Gabe einer Einzeldosis von C14-markiertem Alectinib an gesunde Probanden wurde die Radioaktivität größtenteils mit den Faeces ausgeschieden (mittlere Wiederfindungsrate 97,8 %) mit minimaler Ausscheidung im Urin (mittlere Wiederfindungsrate 0,46 %). In den Faeces wurden 84 % bzw. 5,8 % der Dosis als unverändertes Alectinib bzw. als M4 ausgeschieden.
Basierend auf einer pharmakokinetischen Populationsanalyse betrug die scheinbare Clearance (CL/F) von Alectinib 81,9 l/h. Das geometrische Mittel der individuellen Halbwertszeit-Schätzungen für Alectinib betrug 32,5 Stunden. Die entsprechenden Werte für M4 betrugen 217 l/h bzw. 30,7 Stunden.
Pharmakokinetik in speziellen Populationen
Nierenfunktionsstörung
Vernachlässigbare Mengen von Alectinib und seinem aktiven Metaboliten M4 werden unverändert mit dem Urin ausgeschieden (< 0,2 % der Dosis). Basierend auf einer populationspharmakokinetischen Analyse waren die Expositionen mit Alectinib und M4 bei Patienten mit leichter und mittlerer Nierenfunktionsstörung vergleichbar mit denen von Patienten mit normaler Nierenfunktion. Die Pharmakokinetik von Alectinib wurde bei Patienten mit schwerer Nierenfunktionsstörung nicht untersucht.
Leberfunktionsstörung
Da die Elimination von Alectinib hauptsächlich über den Metabolismus in der Leber stattfindet, kann eine Leberfunktionsstörung die Plasmakonzentrationen von Alectinib und/oder seinem Hauptmetaboliten M4 erhöhen. Basierend auf einer populationspharmakokinetischen Analyse waren die Expositionen mit Alectinib und M4 bei Patienten mit leichter Leberfunktionsstörung vergleichbar mit denen bei normaler Leberfunktion.
Nach oraler Gabe einer Einzeldosis von 300 mg Alectinib an Probanden mit schwerer (Child-Pugh C) Leberfunktionsstörung blieb die Alectinib Cmax gleich, die AUCinf war um das 2,2-Fache erhöht, jeweils verglichen mit den gleichen Werten bei entsprechenden gesunden Probanden. M4 Cmax und AUCinf waren um 39 % bzw. 34 % niedriger, was zu einer kombinierten Exposition von Alectinib und M4 (AUCinf) führte, die bei Patienten mit schwerer Leberfunktionsstörung um das 1,8-Fache höher war als bei entsprechenden gesunden Probanden.
In die Studie zur Untersuchung der Leberfunktionsstörung war auch eine Gruppe mit mäßiger (Child-Pugh B) Leberfunktionsstörung eingeschlossen. In dieser Gruppe wurde, verglichen mit entsprechenden gesunden Probanden, eine leicht erhöhte Exposition von Alectinib beobachtet. Die Probanden in der Child-Pugh-B-Gruppe litten in der Regel jedoch nicht an abnormalen Bilirubin- oder Albuminwerten oder einer abnormalen Prothrombinzeit, was darauf hinweist, dass sie möglicherweise nicht vollständig repräsentativ für Patienten mit mäßiger Leberfunktionsstörung mit verringerter metabolischer Kapazität sind.
Auswirkungen von Alter, Körpergewicht, ethnischer Abstammung und Geschlecht
Alter, Körpergewicht, ethnische Abstammung und Geschlecht hatte keine klinisch relevante Auswirkung auf die systemische Exposition mit Alectinib und M4. Das Körpergewicht der Patienten, die an klinischen Studien teilnahmen, lag im Bereich von 36,9 kg – 123 kg. Es liegen keine Daten zu Patienten mit extrem hohem Körpergewicht (> 130 kg) vor (siehe Abschnitt 4.2).
Karzinogenität
Karzinogenitätsstudien zum Nachweis des karzinogenen Potenzials von Alectinib wurden nicht durchgeführt.
Mutagenität
Alectinib war in vitro im bakteriellen Rückmutationstest (Ames-Test) nicht mutagen, verursachte aber einen leichten Anstieg der Anzahl der Aberrationen im zytogenetischen In-vitro-Test an Lungenzellen des Chinesischen Hamsters (CHL) mit metabolischer Aktivierung sowie an Mikronuklei in einem Mikronukleustest mit Knochenmark von Ratten. Der Mechanismus der Mikronukleus-Induktion basiert auf einer fehlerhaften Chromosomentrennung (Aneuploidie), jedoch nicht auf einer klastogenen Wirkung auf Chromosomen.
Fertilitätsstörung
Es wurden keine Fertilitätsstudien an Tieren zur Bewertung der Auswirkung von Alectinib durchgeführt. In allgemeinen Toxizitätsstudien wurden jedoch keine unerwünschten Veränderungen an den männlichen und weiblichen Fortpflanzungsorganen beobachtet. Diese Studien wurden an Ratten und Affen bei Dosierungen durchgeführt, die dem 2,6- bzw. 0,5-Fachen oder mehr der humanen Exposition entsprachen, berechnet anhand der AUC (area under the curve) bei der empfohlenen Dosierung von 600 mg zweimal täglich.
Teratogenität
Alectinib führte zu embryo-fötaler Toxizität bei trächtigen Ratten und Kaninchen. Bei trächtigen Ratten führte Alectinib bei der 4,5‑fach höheren humantherapeutischen Exposition (AUC) zu embryo-fötalem Abort und bei der 2,7‑fach höheren humantherapeutischen Exposition (AUC) zu kleinen Feten mit verzögerter Ossifikation und leichten Organfehlbildungen. Bei trächtigen Kaninchen führte Alectinib beim 2,9-Fachen der humantherapeutischen Expositionen (AUC) bei der empfohlenen Dosierung zu embryo-fötalem Abort, zu kleinen Feten und zu einer erhöhten Inzidenz skelettaler Veränderungen.
Sonstiges
Alectinib absorbiert Ultraviolett(UV)-Licht zwischen 200 nm und 400 nm und zeigt in einem In-vitro-Phototoxizitätstest an kultivierten murinen Fibroblasten nach UVA-Bestrahlung ein phototoxisches Potenzial.
In Toxizitätsstudien mit wiederholter Gabe waren die primären Zielorgane bei Ratten und Affen bei klinisch relevanten Expositionen das erythropoetische System, der Magen-Darm-Trakt und das hepatobiliäre System.
Bei Expositionen, die der humanen Exposition bei empfohlener Dosierung auf AUC-Basis entsprachen oder 10 % – 60 % darüber lagen, wurde eine abnormale Erythrozytenmorphologie beobachtet. Eine Ausdehnung der proliferativen Zone der gastrointestinalen Mukosa wurde in beiden Spezies bei Expositionen, die der humanen AUC-Exposition bei empfohlener Dosierung entsprachen oder 20 % – 120 % darüber lagen, beobachtet. Eine Erhöhung der hepatischen alkalischen Phosphatase (ALP) und des direkten Bilirubins sowie eine Vakuolenbildung/Rückbildung/Nekrose des Gallengangepithels und eine Vergrößerung/fokale Nekrose der Hepatozyten wurde in Ratten und/oder Affen beobachtet bei Expositionen, die der humanen Exposition bei empfohlener Dosierung basierend auf AUC entsprachen oder 20 % – 30 % darüber lagen.
Eine leichte hypotensive Wirkung wurde bei Affen bei klinisch relevanten Expositionen beobachtet.
Kapselinhalt
Lactose-Monohydrat
Hyprolose
Natriumdodecylsulfat
Magnesiumstearat
Carmellose-Calcium
Kapselhülle
Hypromellose
Carrageen
Kaliumchlorid
Titandioxid (E171)
Maisstärke
Carnaubawachs
Drucktinte
Eisen(III)-oxid (E172)
Eisen(III)-hydroxid-oxid x H2O (E172)
Indigocarmin-Aluminiumsalz (E132)
Carnaubawachs
Weißer Schellack
Glycerolmonooleat
Nicht zutreffend.
5 Jahre
Blisterpackung
In der Originalverpackung aufbewahren, um den Inhalt vor Feuchtigkeit zu schützen.
Flaschen
In der Originalverpackung aufbewahren und die Flasche fest verschlossen halten, um den Inhalt vor Feuchtigkeit zu schützen.
Aluminium/Aluminium (PA/Alu/PVC/Alu) Blisterpackung mit 8 Hartkapseln.
Packungsgröße: 224 (4 Packungen mit 56) Hartkapseln.
HDPE-Flasche mit kindergesichertem Verschluss und einem integrierten Trockenmittel.
Packungsgröße: 240 Hartkapseln.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu beseitigen.
Roche Registration GmbH
Emil-Barell-Straße 1
79639 Grenzach-Wyhlen
Deutschland
EU/1/16/1169/001
EU/1/16/1169/002
Datum der Erteilung der Zulassung: 16. Februar 2017
Datum der letzten Verlängerung der Zulassung: 15. Juli 2022
Januar 2026
Verschreibungspflichtig
Roche Pharma AG
Emil-Barell-Straße 1
79639 Grenzach-Wyhlen
Telefon (07624) 14-0
Telefax (07624) 1019
Ausführliche Informationen zu diesem Arzneimittel sind auf den Internetseiten der Europäischen Arzneimittel-Agentur https://www.ema.europa.eu verfügbar.