Emgality® 120 mg Injektionslösung in einem Fertigpen
Jeder Fertigpen enthält 120 mg Galcanezumab in 1 ml.
Galcanezumab ist ein rekombinanter humanisierter monoklonaler Antikörper, der in einer Zelllinie aus Ovarialzellen des chinesischen Hamsters produziert wird.
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
Injektionslösung (Injektion).
Die Lösung ist klar und farblos bis leicht gelblich.
Emgality ist angezeigt zur Migräne-Prophylaxe bei Erwachsenen mit mindestens 4 Migränetagen pro Monat.
Die Behandlung sollte von Ärzten eingeleitet werden, die in der Diagnostik und Behandlung von Patienten mit Migräne erfahren sind.
Dosierung
Die empfohlene Dosis beträgt 120 mg Galcanezumab einmal monatlich mittels subkutaner Injektion, wobei die Behandlung mit einer Anfangsdosis von 240 mg (2 Injektionen zu je 120 mg am selben Tag) eingeleitet wird.
Patienten sollten angewiesen werden, eine versäumte Gabe so bald wie möglich nachzuholen und anschließend die Gabe monatlich - ab dem Tag der nachgeholten Injektion - fortzuführen.
Der Behandlungserfolg sollte 3 Monate nach Behandlungsbeginn beurteilt werden. Jede weitere Entscheidung die Behandlung fortzusetzen, sollte für jeden Patienten individuell erfolgen. Es wird empfohlen, anschließend regelmäßig zu überprüfen, ob eine Weiterbehandlung notwendig ist.
Ältere Patienten (≥ 65 Jahre)
Bei Patienten ≥ 65 Jahren liegen nur begrenzte Informationen vor. Es ist keine Anpassung der Dosis erforderlich, da die Pharmakokinetik von Galcanezumab vom Alter nicht beeinflusst wird.
Eingeschränkte Nierenfunktion/Eingeschränkte Leberfunktion
Es ist keine Dosisanpassung bei Patienten mit leichter bis mittlerer Nierenfunktionsstörung oder Leberfunktionsstörung erforderlich (siehe Abschnitt 5.2).
Kinder und Jugendliche
Die Sicherheit und Wirksamkeit von Galcanezumab bei Kindern im Alter von 6 bis 18 Jahren ist noch nicht erwiesen. Es liegen keine Daten vor.
Es gibt keinen relevanten Nutzen von Galcanezumab bei Kindern unter 6 Jahren zur Migräne-Prophylaxe.
Art der Anwendung
Subkutane Anwendung.
Patienten können sich Galcanezumab selbst injizieren, wobei sie die Bedienungsanleitung befolgen müssen. Galcanezumab kann subkutan in Bauch, Oberschenkel, dorsal am Oberarm oder in den Gesäßbereich injiziert werden. Nach einer entsprechenden Schulung können sich Patienten Galcanezumab selbst injizieren, wenn ein Arzt dies für angebracht hält. Die Anleitungen zur Verabreichung finden sich in der Gebrauchsinformation.
Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
Rückverfolgung
Um die Rückverfolgung biologischer Arzneimittel zu verbessern, sollten der Name und die Chargennummer des verabreichten Produkts dokumentiert werden.
Kardiovaskuläres Risiko
Patienten mit bestimmten schwerwiegenden Herz-Kreislauf-Erkrankungen waren von der Teilnahme an den klinischen Studien ausgeschlossen (siehe Abschnitt 5.1). Es liegen für diese Patienten keine Daten zur Verträglichkeit vor.
Schwere Überempfindlichkeit
Es wurden schwere Überempfindlichkeitsreaktionen einschließlich Fälle von Anaphylaxie, Angioödem und Urtikaria berichtet (siehe Abschnitt 4.8). Schwere Überempfindlichkeitsreaktionen können innerhalb eines Tages nach Anwendung von Galcanezumab auftreten. Es wurden jedoch Fälle mit verzögertem Auftreten (von mehr als einem Tag bis 4 Wochen nach der Verabreichung) berichtet. In einigen Fällen hielten die Überempfindlichkeitsreaktionen länger an. Falls eine schwere Überempfindlichkeitsreaktion auftritt, ist die Behandlung mit Galcanezumab sofort zu beenden und eine geeignete Therapie zu beginnen (siehe Abschnitt 4.3). Die Patienten sind über die Möglichkeit einer verzögert einsetzenden Überempfindlichkeitsreaktion zu informieren und anzuweisen, sich an ihren Arzt zu wenden.
Hilfsstoffe
Dieses Arzneimittel enthält weniger als 1 mmol Natrium (23 mg) pro 120 mg Dosis, d. h. es ist nahezu „natriumfrei“.
Es wurden keine Wechselwirkungsstudien durchgeführt. Basierend auf den Eigenschaften von Galcanezumab sind keine pharmakokinetischen Wechselwirkungen zu erwarten.
Schwangerschaft
Es liegen nur eingeschränkte Daten zur Anwendung von Galcanezumab bei Schwangeren vor. Tierexperimentelle Studien zeigten keine direkten oder indirekten schädlichen Wirkungen in Hinblick auf die Reproduktionstoxizität (siehe Abschnitt 5.3). Es ist aber bekannt, dass humanes Immunglobulin (IgG) die Plazentaschranke passiert. Als Vorsichtsmaßnahme sollte die Anwendung von Galcanezumab während der Schwangerschaft möglichst vermieden werden.
Stillzeit
Es ist nicht bekannt, ob Galcanezumab in die menschliche Muttermilch übergeht. Humanes IgG geht bekanntlich in den ersten Tagen nach der Geburt in die Muttermilch über. Kurz danach sinkt diese Konzentration auf einen niedrigen Spiegel ab. Deshalb kann ein Risiko während dieser Zeitspanne für das gestillte Kind nicht ausgeschlossen werden. Falls es klinisch notwendig sein sollte, könnte danach die Anwendung von Galcanezumab während der Stillzeit in Betracht gezogen werden.
Fertilität
Die Auswirkung von Galcanezumab auf die humane Fertilität wurde nicht untersucht. Tierexperimentelle Studien haben keine negativen Auswirkungen auf die männliche und weibliche Fertilität gezeigt (siehe Abschnitt 5.3).
Galcanezumab könnte einen geringen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen haben. Nach der Verabreichung kann Vertigo auftreten (siehe Abschnitt 4.8).
Zusammenfassung des Verträglichkeitsprofils
Über 2 500 Patienten wurden insgesamt in Studien, die die Erstzulassung von Galcanezumab stützten, zur Migräne-Prophylaxe mit Galcanezumab behandelt. Über 1 400 Patienten wurden in der doppelblinden Behandlungsphase der placebokontrollierten Phase-3-Studien mit Galcanezumab behandelt. 279 Patienten wurden 12 Monate lang behandelt.
Als Nebenwirkungen wurden in den klinischen Studien zu Migräne unter der Gabe von 120 mg bzw. 240 mg von Schmerzen an der Injektionsstelle (10,1 %/11,6 %), Reaktionen an der Injektionsstelle (9,9 %/ 14,5 %), Vertigo (0,7 %/1,2 %), Obstipation (1,0 %/1,5 %), Pruritus (0,7 %/1,2 %) und Urtikaria (0,3 %/0,1 %) berichtet. Die meisten dieser Nebenwirkungen waren leicht oder mittelschwer. Weniger als 2,5 % der Patienten in diesen Studien brachen die Teilnahme aufgrund von Nebenwirkungen ab.
Tabellarische Auflistung der Nebenwirkungen
Tabelle 1. Auflistung von Nebenwirkungen, die in klinischen Studien beobachtet oder nach Markteinführung gemeldet wurden
Geschätzte Häufigkeit: sehr häufig (≥ 1/10), häufig (≥ 1/100, < 1/10), gelegentlich (≥ 1/1 000, < 1/100), selten (≥ 1/10 000, < 1/1 000).
Systemorganklasse |
Sehr häufig |
Häufig |
Gelegentlich |
Selten |
Erkrankungen des Immunsystems |
Anaphylaxie |
|||
Erkrankungen des Ohrs und des Labyrinths |
Vertigo |
|||
Erkrankungen des Gastrointestinaltrakts |
Obstipation |
|||
Erkrankungen der Haut und des Unterhautgewebes |
Pruritus |
Urtikaria |
||
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort |
Schmerzen an der Injektionsstelle, |
a |
Die am häufigsten berichteten Ereignisse (≥ 1 %) waren: Reaktionen an der Injektionsstelle, Erytheme an der Injektionsstelle, Pruritus an der Injektionsstelle, Blutergüsse an der Injektionsstelle, Schwellungen an der Injektionsstelle. |
Beschreibung ausgewählter Nebenwirkungen
Reaktionen oder Schmerz an der Injektionsstelle
Die meisten Reaktionen im Zusammenhang mit der Injektionsstelle waren leicht bis mittelschwer. Weniger als 0,5 % der Patienten, die Galcanezumab während der Phase-3-Studien bekommen hatten, brachen die Behandlung aufgrund einer Reaktion an der Injektionsstelle ab. Die meisten Reaktionen an der Injektionsstelle wurden innerhalb von 1 Tag berichtet und verschwanden im Durchschnitt innerhalb von 5 Tagen. Bei 86 % der Patienten, die von Schmerzen an der Injektionsstelle berichteten, trat die Reaktion innerhalb von 1 Stunde nach der Injektion auf und endete durchschnittlich innerhalb eines Tages. Ein Prozent der Patienten, die Galcanezumab während der Phase-3-Studien erhielten, berichteten über starke Schmerzen an der Injektionsstelle.
Urtikaria
Urtikaria kam gelegentlich vor. In klinischen Studien mit Galcanezumab wurden schwere Fälle von Urtikaria berichtet.
Immunogenität
Die Inzidenz der Bildung von Antikörpern gegen den Wirkstoff lag in den klinischen Studien während des doppelblinden Behandlungszeitraums bei 4,8 % für die Studienteilnehmer, die Galcanezumab einmal monatlich erhielten (bis auf die Antikörper bei einem Patienten hatten die Antikörper aller anderen Patienten neutralisierende Aktivität). Bei 12 Monaten Behandlung mit Galcanezumab entwickelten bis zu 12,5 % der Patienten Antikörper gegen Galcanezumab. Die meisten dieser Antikörper wiesen einen niedrigen Titer auf und waren in vitro nachweislich neutralisierend. Jedoch hatte das Vorhandensein von Antikörpern gegen Galcanezumab keinen Einfluss auf die Pharmakokinetik, Wirksamkeit oder Verträglichkeit von Galcanezumab.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung über das nationale Meldesystem anzuzeigen:
Bundesinstitut für Impfstoffe und
biomedizinische Arzneimittel
Paul-Ehrlich-Institut
Paul-Ehrlich-Str. 51 – 59
63225 Langen
Tel: +49 6103 77 0
Fax: +49 6103 77 1234
Website: https://www.pei.de
Dosierungen von bis zu 600 mg wurden Menschen subkutan verabreicht, ohne dass dosislimitierende Toxizität beobachtet wurde. Im Falle einer Überdosierung wird empfohlen, den Patienten auf Nebenwirkungen zu überwachen und falls erforderlich sofort eine geeignete symptomatische Behandlung einzuleiten.
Pharmakotherapeutische Gruppe: Analgetika, Calcitonin-Gene-Related-Peptide (CGRP) Antagonisten, ATC-Code: N02CD02
Wirkmechanismus
Galcanezumab ist ein humanisierter monoklonaler IgG4-Antikörper, der an Calcitonin Gene-Related Peptide (CGRP) bindet und dessen biologische Aktivität unterbindet. Erhöhte Blutkonzentrationen von CGRP wurden mit Migräneanfällen in Verbindung gebracht. Galcanezumab bindet an CGRP mit hoher Affinität (KD = 31 pM) und hoher Spezifität (> 10 000‑fach im Vergleich zu den verwandten Peptiden Adrenomedullin, Amylin, Calcitonin und Intermedin).
Klinische Wirksamkeit und Sicherheit
Die Wirksamkeit und Sicherheit von Galcanezumab wurde in 3 randomisierten, placebokontrollierten, doppelblinden Phase-3-Studien mit erwachsenen Migräne-Patienten (N = 2 886) untersucht. Die 2 Studien bei episodischer Migräne (EVOLVE-1 und EVOLVE-2) schlossen Patienten ein, die die International Classification of Headache Disorders (ICHD)-Kriterien der Diagnose einer Migräne mit oder ohne Aura mit 4 ‑ 14 Migräne-Kopfschmerztagen pro Monat erfüllten. Die Studie bei chronischer Migräne (REGAIN) schloss Patienten ein, die die ICHD-Kriterien für chronische Migräne mit ≥ 15 Kopfschmerztagen pro Monat, davon mindestens 8 mit Merkmalen einer Migräne, erfüllten. Patienten, bei denen kürzlich akute kardiovaskuläre Ereignisse (einschließlich Myokardinfarkt, instabile Angina pectoris, koronare Bypass-Operation, Schlaganfall, tiefe Venenthrombose) aufgetreten sind, und/oder Patienten mit einem schwerwiegenden kardiovaskulären Risiko waren von den klinischen Studien mit Galcanezumab ausgeschlossen. Patienten > 65 Jahre waren ebenfalls ausgeschlossen.
Die Patienten erhielten Placebo, Galcanezumab 120 mg/Monat (mit einer Initialdosis von 240 mg im ersten Monat) oder Galcanezumab 240 mg/Monat. In allen drei Studien durften Arzneimittel zur Behandlung von akuten Migräneattacken verwendet werden. In den 3 Studien waren die Patienten überwiegend weiblich (> 83 %) mit einem Durchschnittsalter von 41 Jahren und einer durchschnittlichen Migräneanamnese von 20 bis 21 Jahren. Etwa ein Drittel der Patienten in den Studien hatte bei mindestens einer, etwa 16 % der Patienten hatten bei mindestens zwei vorhergehenden prophylaktischen Behandlungen keine ausreichende Wirksamkeit.
In allen drei Studien war die durchschnittliche Gesamtveränderung der monatlichen Migräne-Kopfschmerztage (MKT) gegenüber dem Ausgangswert zu Studienbeginn das primäre Wirksamkeitskriterium. Die Ansprechrate ist definiert als der mittlere Prozentsatz der Patienten, die einen definierten Schwellenwert der Reduzierung der Anzahl monatlicher Migräne-Kopfschmerztage (≥ 50 %, ≥ 75 % und 100 %) während der doppelblinden Behandlungsphase erreichten. Der Einfluss der Migräne auf die Funktionsfähigkeit wurde mit dem Role Function-Restrictive-Score im Migraine-Specific Quality of Life Questionnaire (MSQ) Version 2.1 sowie mit dem MIDAS (MIgraine Disability ASsessment) erhoben. Der MSQ misst die Auswirkungen der Migräne auf Arbeit oder Aktivitäten des täglichen Lebens, Beziehungen zu Familie und Freunden, Freizeit, Leistungsfähigkeit, Konzentrationsfähigkeit, Energie und Müdigkeit. Die Domäne des Fragebogens hat einen Wertebereich von 0 bis 100, wobei höhere Werte eine geringere Einschränkung anzeigen, d. h. Patienten weniger Einschränkungen bei der Durchführung alltäglicher Aktivitäten haben. Im MIDAS weisen höhere Werte auf eine schlechtere Funktionsfähigkeit hin. Die Ausgangswerte des MIDAS zu Studienbeginn spiegelten eine schwere Migräne-bedingte Einschränkung der Patienten in EVOLVE-1 und EVOLVE-2 (Mittel von 33,1) und eine sehr schwer eingeschränkte Population (Mittel von 67,2) in REGAIN wider.
Episodische Migräne
Die Studien EVOLVE-1 und EVOLVE-2 hatten eine 6-monatige, doppelblinde, placebokontrollierte Behandlungsphase. Zwischen 82,8 % und 87,7 % der Patienten, die mit Galcanezumab behandelt wurden, schlossen die doppelblinde Behandlungsphase vollständig ab.
Beide Behandlungsgruppen mit Galcanezumab 120 mg und 240 mg zeigten bei der mittleren Veränderung der MKT statistisch signifikante und klinisch relevante Verbesserungen gegenüber dem Ausgangswert im Vergleich zu Placebo (siehe Tabelle 2). Patienten, die mit Galcanezumab behandelt wurden, zeigten im Vergleich zu Patienten, die Placebo erhielten, höhere Ansprechraten und eine größere Abnahme der Anzahl an monatlichen MKT mit Einnahme von Akutmedikation. Ab dem ersten Monat zeigten Patienten, die mit Galcanezumab behandelt wurden, eine deutlichere Verbesserung hinsichtlich der Funktionalität (gemessen am MSQ Role Function-Restrictive-Score) verglichen mit den Patienten, die Placebo erhielten. Mehr Patienten, die Galcanezumab erhielten, erreichten eine klinisch signifikante Verbesserung der Funktionalität (Ansprechrate gemessen am MSQ Role Function-Restrictive-Score) verglichen mit denen, die Placebo erhielten. Die Gabe von Galcanezumab war mit einer statistisch signifikanten Verringerung der Einschränkungen im Vergleich zu Placebo verbunden.
Patienten mit Galcanezumab 120 mg und 240 mg hatten im Vergleich zu Patienten mit Placebo während des ersten Monates und in allen folgenden Monaten bis zum 6. Monat im Mittel signifikant weniger monatliche MKT im Vergleich zu Studienbeginn (siehe Abbildung 1). Außerdem hatten Patienten mit Galcanezumab (Anfangsdosis von 240 mg) im Vergleich zu Placebo bereits während des ersten Monates in Woche 1 und in allen folgenden Wochen signifikant weniger wöchentliche MKT.
Abbildung 1 Abnahme der monatlichen Migräne-Kopfschmerztage im zeitlichen Verlauf in den Studien EVOLVE-1 und EVOLVE-2
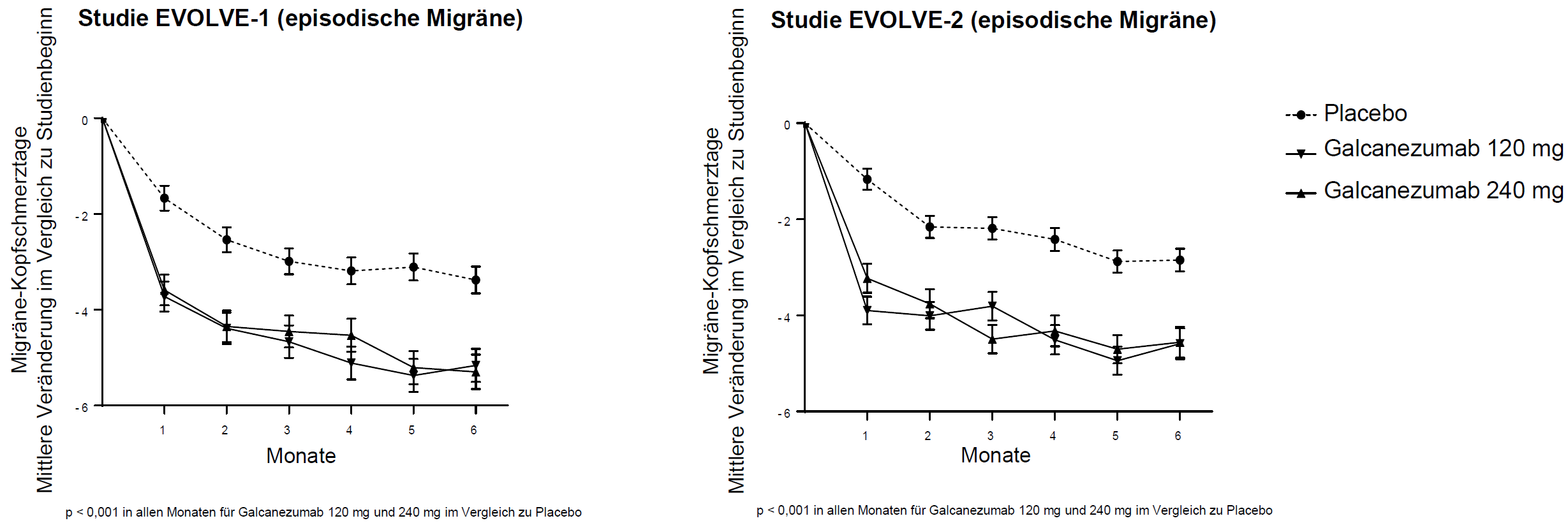
Tabelle 2. Wirksamkeit und Behandlungsergebnis aus Patientensicht (patientenbezogene Endpunkte)
|
EVOLVE 1 – Episodische Migräne |
EVOLVE 2 – Episodische Migräne |
|||||||
Emgality |
Placebo |
Emgality |
Placebo |
||||||
120 mg |
240 mg |
120 mg |
240 mg |
||||||
n = 210 |
n = 208 |
n = 425 |
n = 226 |
n = 220 |
n = 450 |
||||
Wirksamkeitsendpunkte a | |||||||||
MKT |
|
||||||||
Ausgangswert |
9,21 |
9,14 |
9,08 |
9,07 |
9,06 |
9,19 |
|||
Mittlere Änderung |
- 4,73 |
- 4,57 |
- 2,81 |
- 4,29 |
- 4,18 |
- 2,28 |
|||
Unterschied |
- 1,92 |
- 1,76 |
- 2,02 |
- 1,90 |
|||||
Verum/Placebo |
|||||||||
CI95 % |
(- 2,28, - 1,33) |
(- 2,09, - 1,14) |
(- 2,29, - 1,36) |
(- 2,25, - 1,31) |
|||||
p-Wert |
< 0,001 d |
< 0,001 d |
|
< 0,001 d |
< 0,001 d |
|
|||
≥ 50 % MKT-Responder |
|
|
|
|
|
|
|||
Prozent, % |
62,3 |
60,9 |
38,6 |
59,3 |
56,5 |
36,0 |
|||
p-Wert |
< 0,001 d |
< 0,001 d |
|
< 0,001 d |
< 0,001 d |
|
|||
≥ 75 % MKT-Responder |
|
|
|
|
|
|
|||
Prozent, % |
38,8 |
38,5 |
19,3 |
33,5 |
34,3 |
17,8 |
|||
p-Wert |
< 0,001 d |
< 0,001 d |
|
< 0,001 d |
< 0,001 d |
|
|||
100 % MKT-Responder |
|
|
|
|
|
|
|||
Prozent, % |
15,6 |
14,6 |
6,2 |
11,5 |
13,8 |
5,7 |
|||
p-Wert |
< 0,001 d |
< 0,001 d |
|
< 0,001 d |
< 0,001 d |
|
|||
MKT mit Akutmedikation |
|
|
|
|
|
|
|||
Ausgangswert |
7,42 |
7,34 |
7,38 |
7,47 |
7,47 |
7,62 |
|||
Mittlere Änderung |
- 3,96 |
- 3,76 |
- 2,15 |
- 3,67 |
- 3,63 |
- 1,85 |
|||
Unterschied |
- 1,81 |
- 1,61 |
- 1,82 |
- 1,78 |
|||||
Verum/Placebo |
|||||||||
CI95 % |
(- 2,28, - 1,33) |
(- 2,09, - 1,14) |
(- 2,29, - 1,36) |
(- 2,25, - 1,31) |
|||||
p-Wert |
< 0,001 d |
< 0,001 d |
|
< 0,001 d |
< 0,001 d |
|
|||
Patientenbezogene Endpunkte | |||||||||
MSQ Role Function-Restrictive Domain b |
|
|
|
|
|
|
|||
n |
189 |
184 |
377 |
213 |
210 |
396 |
|||
Ausgangswert |
51,39 |
48,76 |
52,92 |
52,47 |
51,71 |
51,35 |
|||
Mittlere Änderung |
32,43 |
32,09 |
24,69 |
28,47 |
27,04 |
19,65 |
|||
Unterschied |
7,74 |
7,40 |
8,82 |
7,39 |
|||||
Verum/Placebo |
|||||||||
CI95 % |
(5,20, 10,28) |
(4,83, 9,97) |
(6,33, 11,31) |
(4,88, 9,90) |
|||||
p-Wert |
< 0,001 d |
< 0,001 d |
|
< 0,001 d |
< 0,001 d |
|
|||
MSQ Role Function Restrictive Domain Responders c |
|
|
|
|
|
|
|||
n |
189 |
184 |
377 |
213 |
210 |
396 |
|||
Prozent, % |
63,5 |
69,6 |
47,2 |
58,2 |
60,0 |
43,4 |
|||
p-Wert |
< 0,001 f |
< 0,001 f |
|
< 0,001 f |
< 0,001 f |
|
|||
MIDAS Total Score e |
|
|
|
|
|
|
|||
n |
177 |
170 |
345 |
202 |
194 |
374 |
|||
Ausgangswert |
32,93 |
36,09 |
31,84 |
30,87 |
32,75 |
34,25 |
|||
Mittlere Änderung |
- 21,16 |
- 20,06 |
- 14,87 |
- 21,17 |
- 20,24 |
- 12,02 |
|||
Unterschied |
- 6,29 |
- 5,19 |
- 9,15 |
- 8,22 |
|||||
Verum/Placebo |
|||||||||
CI95 % |
(- 9,45, - 3,13) |
(- 8,39, - 1,98) |
(- 12,61, - 5,69) |
(- 11,71, - 4,72) |
|||||
p-Wert |
< 0,001 f |
0,002 f |
|
< 0,001 f |
< 0,001 f |
|
|||
n = Anzahl der Patienten, CI95 % = 95 % Konfidenzintervall (confidence interval). | |||||||||
a |
Änderungen hinsichtlich der Wirksamkeit gemessen über die Monate 1 bis 6. |
b |
Gemessen über die Monate 4 bis 6. |
c |
Definiert als eine Verbesserung ≥ 25 Punkte für episodische Migräne im Durchschnitt über die Monate 4 bis 6 |
d |
Statistisch signifikant nach Adjustierung für multiples Testen. |
e |
Erhoben in Monat 6. |
f |
Nicht adjustiert für multiples Testen. |
Gemäß gepoolter Daten aus den Studien EVOLVE-1- und EVOLVE-2 wurde gezeigt, dass Patienten, die vorher eine oder mehrere prophylaktische Behandlungen aufgrund fehlender oder mangelnder Wirkung abgebrochen hatten, die Unterschiede der Abnahme der mittleren monatlichen MKT zwischen Galcanezumab 120 mg und Placebo - 2,69 Tage (p < 0,001) und zwischen Galcanezumab 240 mg und Placebo - 2,78 Tage (p < 0,001) betrugen. Bei Patienten, die zwei oder mehr prophylaktische Behandlungen aufgrund fehlender oder mangelnder Wirkung abgebrochen hatten, betrugen die Unterschiede - 2,64 Tage (p < 0,001) zwischen 120 mg und Placebo und - 3,04 Tage (p < 0,001) zwischen 240 mg und Placebo.
Chronische Migräne
Die Studie REGAIN hatte eine 3-monatige, doppelblinde, placebokontrollierte Behandlungsphase gefolgt von einer 9-monatigen offenen Verlängerung. Etwa 15 % der Patienten setzten die gleichzeitige Behandlung mit Topiramat oder Propranolol zur Migräne-Prophylaxe fort, was gemäß dem Studienprotokoll erlaubt war. 95,3 % der Patienten, die Galcanezumab erhielten, schlossen die doppelblinde Behandlungsphase vollständig ab.
Beide Behandlungsgruppen, die Galcanezumab 120 mg und 240 mg erhielten, zeigten im Vergleich zum Ausgangswert eine statistisch signifikante und klinisch relevante Abnahme der mittleren MKT verglichen mit Placebo (siehe Tabelle 3). Patienten, die mit Galcanezumab behandelt wurden, zeigten im Vergleich zu Patienten, die Placebo erhielten, höhere Ansprechraten. Weiterhin reduzierte sich die Anzahl der monatlichen MKT mit Einnahme von Akutmedikation. Die Behandlung mit Galcanezumab war mit einer statistisch signifikanten Verbesserung hinsichtlich der Funktionalität (gemessen am MSQ Role Function-Restrictive-Domain-Score) verglichen mit Patienten, die Placebo erhielten, verbunden. Ab dem ersten Monat wurde eine Reduktion der Migräne-bedingten Beeinträchtigung der Funktionalität beobachtet. Mehr Patienten, die Galcanezumab erhielten, erreichten eine klinisch signifikante Verbesserung der Funktionalität (Ansprechrate gemessen am MSQ Role Function-Restrictive-Domain-Score) verglichen mit denen, die Placebo erhielten. Die 120 mg Dosis war mit einer statistisch signifikanten Abnahme der Einschränkungen im Vergleich zu Placebo verbunden.
Patienten mit Galcanezumab 120 mg oder 240 mg hatten im Vergleich zu Placebo während des ersten Monats und in allen folgenden Monaten bis zum 3. Monat im Mittel signifikant weniger monatliche MKT im Vergleich zu Studienbeginn (siehe Abbildung 2). Außerdem hatten Patienten mit Galcanezumab (Anfangsdosis von 240 mg) im Vergleich zu Placebo während der 1. Woche des ersten Monats und in allen folgenden Wochen signifikant weniger wöchentliche MKT.
Abbildung 2 Abnahme der monatlichen Migräne-Kopfschmerztage im zeitlichen Verlauf in der Studie REGAIN
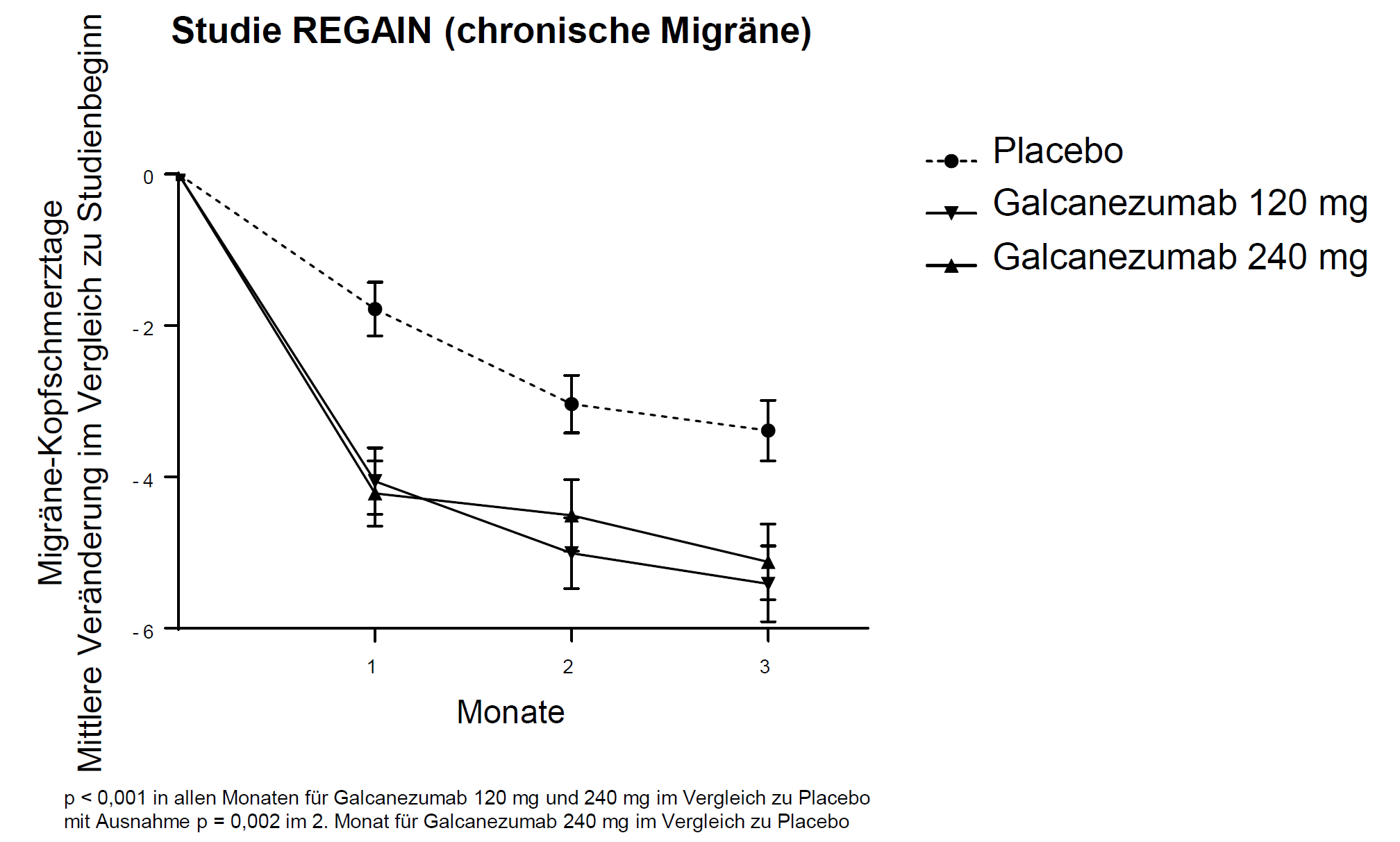
Tabelle 3. Wirksamkeit und Behandlungsergebnis aus Patientensicht (patientenbezogene Endpunkte)
|
REGAIN – Chronische Migräne |
||||||
|
Emgality |
Placebo |
|||||
|
120 mg |
240 mg |
|||||
|
n = 273 |
n = 274 |
n = 538 |
||||
Wirksamkeitsendpunkte a |
|
|
|
||||
MKT |
|
|
|
||||
Ausgangswert |
19,36 |
19,17 |
19,55 |
||||
Mittlere Änderung |
- 4,83 |
- 4,62 |
- 2,74 |
||||
Unterschied Verum/Placebo |
- 2,09 |
- 1,88 |
|||||
CI95 % |
(- 2,92, - 1,26) |
(- 2,71, - 1,05) |
|||||
p-Wert |
< 0,001 c |
< 0,001 c |
|
||||
≥ 50 % MKT Responder |
|
|
|
||||
Prozent, % |
27,6 |
27,5 |
15,4 |
||||
p-Wert |
< 0,001 c |
< 0,001 c |
|
||||
≥ 75 % MKT Responder |
|
|
|
||||
Prozent, % |
7,0 |
8,8 |
4,5 |
||||
p-Wert |
0,031 d |
< 0,001 c |
|
||||
100 % MKT-Responder |
|
|
|
||||
Prozent, % |
0,7 |
1,3 |
0,5 |
||||
p-Wert |
> 0,05 d |
> 0,05 d |
|
||||
MKT mit Akutmedikation |
|
|
|
||||
Ausgangswert |
15,12 |
14,49 |
15,51 |
||||
Mittlere Änderung |
- 4,74 |
- 4,25 |
- 2,23 |
||||
Unterschied Verum/Placebo |
- 2,51 |
- 2,01 |
|||||
CI95 % |
(- 3,27, - 1,76) |
(- 2,77, - 1,26) |
|||||
p-Wert |
< 0,001 d |
< 0,001 c |
|
||||
Patientenbezogene Endpunkte b |
|||||||
MSQ Role Function-Restrictive Domain |
|
|
|
||||
n |
252 |
253 |
494 |
||||
Ausgangswert |
39,29 |
38,93 |
38,37 |
||||
Mittlere Änderung |
21,81 |
23,05 |
16,76 |
||||
Unterschied Verum/Placebo |
5,06 |
6,29 |
|||||
CI95 % |
(2,12, 7,99) |
(3,03, 9,55) |
|||||
p-Wert |
< 0,001 d |
< 0,001 c |
|
||||
MSQ Role Function Restrictive Domain Responders |
|
|
|
||||
n |
252 |
253 |
494 |
||||
Prozent, % |
64,3 |
64,8 |
54,1 |
||||
p-Wert |
0,003 e |
0,002 e |
|
||||
MIDAS Gesamtwert |
|
|
|
||||
n |
254 |
258 |
504 |
||||
Ausgangswert |
62,46 |
69,17 |
68,66 |
||||
Mittlere Änderung |
- 20,27 |
- 17,02 |
- 11,53 |
||||
Unterschied Verum/Placebo |
- 8,74 |
- 5,49 |
|||||
CI95 % |
(- 16,39, - 1,08) |
(- 13,10, 2,12) |
|||||
p-Wert |
0,025 e |
> 0,05 e |
|||||
n = Anzahl an Patienten; CI95 % = 95 % Konfidenzintervall (confidence interval). | |||||||
a |
Änderungen hinsichtlich der Wirksamkeit gemessen in den Monaten 1 bis 3. |
b |
Wirksamkeit aus Patientensicht wurde im Monat 3 gemessen. MSQ role function restrictive domain responders waren definiert als diejenigen mit einer Verbesserung von ≥ 17,14 Punkten für die chronische Migräne in Monat 3. |
c |
Statistisch signifikant nach Adjustierung für multiples Testen. |
d |
Nicht statistisch signifikant nach Adjustierung für multiples Testen. |
e |
Nicht adjustiert für multiples Testen. |
Bei Patienten, die eine oder mehrere prophylaktische Behandlungen aufgrund fehlender oder mangelnder Wirkung abgebrochen hatten, betrug der Unterschied in der Abnahme der mittleren monatlichen MKT zwischen Galcanezumab 120 mg und Placebo - 3,54 Tage (p < 0,001) und zwischen Galcanezumab 240 mg und Placebo - 1,37 Tage (p < 0,05). Bei Patienten, die zwei oder mehr prophylaktische Behandlungen aufgrund fehlender oder mangelnder Wirkung abgebrochen hatten, betrug der Unterschied zwischen 120 mg und Placebo - 4,48 Tage (p < 0,001) und zwischen 240 mg und Placebo - 1,86 Tage (p < 0,01).
Bei Studienbeginn hatten 64 % der Patienten einen Übergebrauch von Akutmedikation gegen Kopfschmerzen. Der Behandlungsunterschied bezüglich der Abnahme der MKT betrug bei diesen Patienten zwischen Galcanezumab 120 mg und Placebo - 2,53 Tage (p < 0,001) sowie zwischen Galcanezumab 240 mg und Placebo - 2,26 Tage (p < 0,001).
Langzeitwirkung
Die Wirksamkeit hielt für bis zu 1 Jahr in einer offenen Studie an, in der Patienten mit episodischer oder chronischer Migräne (mit einem durchschnittlichen Ausgangswert von 10,6 monatlichen MKT) Galcanezumab 120 mg/Monat (mit einer Anfangsdosis von 240 mg im ersten Monat) oder Galcanezumab 240 mg/Monat erhielten. 77,8 % der Patienten durchliefen den gesamten Behandlungszeitraum. Über den gesamten Behandlungszeitraum betrug die mittlere Abnahme der monatlichen MKT im Durchschnitt 5,6 Tage für die Patienten, die 120 mg und 6,5 Tage für die Patienten, die 240 mg erhielten. Über 72 % der Patienten, die die Studie abschlossen haben, berichteten eine 50 %ige Abnahme der MKT zu Monat 12. Gemäß gepoolter Daten aus den Studien EVOLVE-1 und EVOLVE-2 hielt bei mehr als 19 % der mit Galcanezumab behandelten Patienten eine ≥ 50 %ige Ansprechrate während der Monate 1 bis 6 durchgehend an, versus 8 % der Patienten mit Placebo (p < 0,001).
Phase-3-Studie in einer Population, bei der 2 bis 4 vorhergehende prophylaktische Behandlungen der Migräne keine ausreichende Wirksamkeit oder nicht vertretbare Nebenwirkungen gezeigt haben
Die Studie CONQUER untersuchte Patienten mit episodischer und chronischer Migräne, bei denen in den letzten 10 Jahren 2 bis 4 vorhergehende prophylaktische Behandlungen der Migräne keine ausreichende Wirksamkeit oder nicht vertretbare Nebenwirkungen gezeigt hatten. Diese Studie unterstützt die wichtigsten Ergebnisse der bisherigen Migräne-Wirksamkeitsstudien, d. h. die Behandlung mit Galcanezumab führte zu einer mittleren Reduktion der monatlichen Migräne-Kopfschmerztage in der Gesamtgruppe (4,1 Tage verglichen zu 1,0 Tag bei Patienten, die Placebo erhielten; p < 0,0001). Eine mittlere Reduktion der monatlichen Migräne-Kopfschmerztage wurde auch innerhalb der Subpopulationen der episodischen Migräne (2,9 Tage für Galcanezumab verglichen zu 0,3 Tagen für Placebo; p < 0,0001) und der chronischen Migräne (5,9 Tage für Galcanezumab im Vergleich zu 2,2 Tagen für Placebo; p < 0,0001) beobachtet.
Kinder und Jugendliche
Die Europäische Arzneimittel-Agentur hat für Galcanezumab eine Zurückstellung von der Verpflichtung zur Vorlage von Ergebnissen zu Studien in einer oder mehreren pädiatrischen Altersklassen zur Migräne-Prophylaxe gewährt (siehe Abschnitt 4.2 bzgl. Informationen zur Anwendung bei Kindern und Jugendlichen).
Resorption
Basierend auf der Populations-Pharmakokinetischen Analyse betrug die maximale Serumkonzentration (Cmax) von Galcanezumab nach einer Anfangsdosis von 240 mg circa 30 µg/ml (27 % Variationskoeffizient (CV = coefficient of variation)) und die Zeit bis Cmax betrug 5 Tage nach der Verabreichung.
Monatliche Dosierungen von 120 mg bzw. 240 mg erreichten einen Steady-State Cmax (Cmax, ss) von circa 28 µg/ml (35 % CV) bzw. 54 µg/ml (31 % CV). Die Galcanezumab Cmax, ss bei monatlicher Gabe von 120 mg wird nach der 240 mg Anfangsdosis erreicht.
Die Wahl der Injektionsstelle wie Bauch, Oberschenkel, Rückseite des Oberarms und Gesäß hatte keinen signifikanten Einfluss auf die Resorption von Galcanezumab.
Verteilung
Basierend auf der Populations-Pharmakokinetischen Analyse betrug das berechnete Verteilungsvolumen von Galcanezumab 7,3 l.
Biotransformation
Es ist davon auszugehen, dass Galcanezumab als humanisierter monoklonaler IgG4-Antikörper auf die gleiche Art und Weise wie endogenes IgG abgebaut wird, nämlich über katabole Stoffwechselwege zu kleinen Peptiden und Aminosäuren.
Elimination
Basierend auf der Populations-Pharmakokinetischen Analyse betrug die berechnete Clearance von Galcanezumab etwa 0,008 l/Stunde und die Halbwertszeit von Galcanezumab 27 Tage.
Linearität/Nicht-Linearität
Die Galcanezumab-Exposition erhöht sich proportional zur Dosis.
Basierend auf der Populations-Pharmakokinetischen Analyse, die Dosierungen von 5 bis 300 mg enthielt, waren die Resorptionsrate, die berechnete Clearance und das berechnete Verteilungsvolumen unabhängig von der Dosis.
Alter, Geschlecht, Gewicht, Rasse, ethnische Zugehörigkeit
Es ist keine Dosisanpassung aufgrund des Alters (von 18 bis 65 Jahren), Geschlechts, Gewichts, der Rasse oder der ethnischen Zugehörigkeit erforderlich, da diese Faktoren keinen klinisch relevanten Effekt auf das berechnete Verteilungsvolumen von Galcanezumab hatten.
Nieren- oder Leberinsuffizienz
Es wurden keine spezifischen klinisch-pharmakologischen Studien zur Beurteilung der Auswirkungen von Nierenfunktionsstörungen und Leberfunktionsstörungen auf die Pharmakokinetik von Galcanezumab durchgeführt. Die renale Elimination von monoklonalen IgG-Antikörpern ist gering. Außerdem werden monoklonale IgG-Antikörper hauptsächlich über intrazellulären Katabolismus eliminiert. Daher ist nicht zu erwarten, dass eine Leberinsuffizienz die Clearance von Galcanezumab beeinflusst. Basierend auf der Populations-Pharmakokinetischen Analyse hatten die Bilirubinkonzentration oder die Cockcroft-Gault Kreatinin-Clearance (Bereich: 24 bis 308 ml/min) keinen relevanten Einfluss auf die berechnete Clearance von Galcanezumab.
Die präklinischen Daten zeigten keine besonderen Gefahren für den Menschen auf der Grundlage von Toxizitätsstudien mit Mehrfachgaben bei Ratten und Cynomolgus-Affen sowie von pharmakologischen Verträglichkeitsstudien bei Cynomolgus-Affen mit Expositionen, die etwa 10- bis 80-mal höher waren als bei Patienten, die 240 mg Galcanezumab erhielten.
Es wurden keine präklinischen Studien zur Bewertung des kanzerogenen oder mutagenen Potentials von Galcanezumab durchgeführt. Basierend auf Daten aus pharmakologischen und längerdauernden Studien zur Bestimmung der Toxizität von Galcanezumab sowie einer Bewertung der Literatur zu CGRP gibt es keine Hinweise darauf, dass eine dauerhafte Behandlung mit Galcanezumab das Risiko einer Karzinogenese erhöhen würde.
Bei Ratten, denen Galcanezumab verabreicht wurde (circa 4- bis 20‑fache Exposition gegenüber einer humanen Dosis von 240 mg), wurden keine Auswirkungen auf Fertilitätsparameter wie Östruszyklus, Spermienanalyse oder Paarung und Fruchtbarkeit beobachtet. In einer Studie zur männlichen Fertilität war das Gewicht des rechten Hodens bei Gabe einer vierfach höheren Dosis im Vergleich zur humanen Dosis von 240 mg signifikant reduziert.
Am 20. Gestationstag kam es bei Ratten in der embryofetalen Toxizitätsentwicklungsstudie mit einer 20‑fachen Exposition gegenüber der humanen Dosis von 240 mg zu einer Erhöhung der Anzahl von Föten und Würfen mit kurzen Rippen und zu einer Abnahme der mittleren Anzahl von verknöcherten Schwanzwirbeln. Diese Befunde wurden erhoben ohne Hinweise auf maternale Toxizität und wurden als mit Galcanezumab in Verbindung stehend, jedoch nicht als nachteilig angesehen.
Am 29. Gestationstag wurde in der embryofetalen Toxizitätsentwicklungsstudie an Kaninchen eine Schädelanomalie bei einem männlichen Fötus von einer mit Galcanezumab behandelten Mutter bei einer Exposition von etwa dem 33‑fachen der humanen Dosis von 240 mg gefunden.
In einer Studie zur Bestimmung der juvenilen Toxizität, bei der Ratten vom 21. bis zum 90. postnatalen Tag Galcanezumab zweimal wöchentlich verabreicht bekamen, beschränkten sich die systemischen Effekte auf reversible, minimale, nicht nachteilige Verringerungen des Mineralgehaltes der Gesamtknochen und der Knochenmineraldichte, wobei die Expositionen beim circa 50–fachen einer humanen Dosis von 240 mg lagen.
Histidin
Histidinhydrochlorid-Monohydrat
Polysorbat 80
Natriumchlorid
Wasser für Injektionszwecke
Nicht zutreffend.
2 Jahre
Im Kühlschrank lagern (2 °C - 8 °C).
Nicht einfrieren.
In der Originalverpackung aufbewahren, um vor Licht zu schützen.
Emgality kann ungekühlt bis zu 7 Tage bei bis zu 30 °C gelagert werden. Wenn diese Bedingungen nicht eingehalten werden, muss der Fertigpen entsorgt werden.
Typ I Klarglasspritze. Die Spritze ist mit einem Pen zum einmaligen Gebrauch ummantelt. Packungsgrößen zu 1, 2 oder 3 Fertigpens. Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
Art der Anwendung
Die Bedienungsanleitung für den Pen ist in der Packungsbeilage enthalten und muss genau befolgt werden. Der Fertigpen muss immer vollständig verabreicht werden.
Das Aussehen des Fertigpens sollte vor der Anwendung überprüft werden. Emgality darf nicht verwendet werden, wenn die Lösung milchig oder verfärbt aussieht, oder wenn es Partikel enthält oder wenn irgendein Teil des Produkts beschädigt aussieht.
Nicht schütteln.
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu beseitigen.
Eli Lilly Nederland B.V.
Orteliuslaan 1000
3528 BD Utrecht
Niederlande
EU/1/18/1330/001
EU/1/18/1330/002
EU/1/18/1330/005
Datum der Erteilung der Zulassung: 14. November 2018
Datum der letzten Verlängerung der Zulassung: 01. September 2023
Januar 2026
Ausführliche Informationen zu diesem Arzneimittel sind auf der Internetseite der Europäischen Arzneimittel-Agentur https://www.ema.europa.eu verfügbar.
Verschreibungspflichtig
Emgality® 120 mg Injektionslösung in einem Fertigpen
Inhalt |
PZN |
2 Fertigpens |
14445697 |
3 Fertigpens |
14445728 |
Organon Healthcare GmbH
Tel. + 0800 3384 726
(+49 (0) 8920 400 2210)
dpoc.germany@organon.com