metodura 50 mg, Tabletten
metodura 100 mg, Tabletten
metodura 50 mg
Jede Tablette enthält 50 mg Metoprololtartrat.
Sonstiger Bestandteil mit bekannter Wirkung:
Jede Tablette enthält 24,88 mg Lactose-Monohydrat.
metodura 100 mg
Jede Tablette enthält 100 mg Metoprololtartrat.
Sonstiger Bestandteil mit bekannter Wirkung:
Jede Tablette enthält 49,75 mg Lactose-Monohydrat.
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
Tablette
metodura 50 mg sind weiße, runde, beidseitig gewölbte Tabletten mit Bruchkerbe auf einer Seite. Die Tablette kann in gleiche Hälften geteilt werden.
metodura 100 mg sind weiße, runde, beidseitig gewölbte Tabletten mit Bruchkerbe auf einer Seite. Die Tablette kann in gleiche Hälften geteilt werden.
Arterielle Hypertonie
Koronare Herzkrankheit
Hyperkinetisches Herzsyndrom (funktionelle Herzbeschwerden)
Tachykarde Herzrhythmusstörungen
Reinfarktprophylaxe
Migräneprophylaxe
Akutbehandlung des Herzinfarktes
Dosierung
Die Dosierung sollte individuell - vor allem nach dem Behandlungserfolg - festgelegt werden. Die Dauer der Anwendung ist zeitlich nicht begrenzt.
Es gelten folgende Richtdosen:
Arterielle Hypertonie:
Bei der Verordnung von metodura 50 mg:
Ein- bis zweimal täglich 1 Tablette bzw. einmal täglich 1 bis 2 Tabletten (entsprechend 50-100 mg Metoprololtartrat täglich).
Falls erforderlich kann die Tagesdosis auf zweimal 2 Tabletten (entsprechend 200 mg Metoprololtartrat täglich) erhöht werden.
Bei der Verordnung von metodura 100 mg:
Ein- bis zweimal täglich ½ Tablette bzw. einmal täglich ½ bis 1 Tablette (entsprechend 50-100 mg Metoprololtartrat täglich).
Falls erforderlich kann die Tagesdosis auf zweimal 1 Tablette (entsprechend 200 mg Metoprololtartrat täglich) erhöht werden.
Koronare Herzkrankheit:
Bei der Verordnung von metodura 50 mg:
Ein- bis zweimal täglich 1 Tablette bzw. einmal täglich 1 bis 2 Tabletten (entsprechend 50-100 mg Metoprololtartrat täglich).
Falls erforderlich kann die Tagesdosis unter Kontrolle des Blutdruckes auf zweimal 2 Tabletten (entsprechend 200 mg Metoprololtartrat täglich) erhöht werden.
Bei der Verordnung von metodura 100 mg:
Ein- bis zweimal täglich ½ Tablette bzw. einmal täglich ½ bis 1 Tablette (entsprechend 50 – 100 mg Metoprololtartrat täglich).
Falls erforderlich kann die Tagesdosis unter Kontrolle des Blutdruckes auf zweimal 1 Tablette (entsprechend 200 mg Metoprololtartrat täglich) erhöht werden.
Hyperkinetisches Herzsyndrom (sog. funktionelle Herzbeschwerden):
Bei der Verordnung von metodura 50 mg:
Ein- bis zweimal täglich 1 Tablette bzw. einmal täglich 1 bis 2 Tabletten (entsprechend 50-100 mg Metoprololtartrat täglich).
Falls erforderlich kann die Tagesdosis unter Kontrolle des Blutdruckes auf zweimal 2 Tabletten (entsprechend 200 mg Metoprololtartrat täglich) erhöht werden.
Bei der Verordnung von metodura 100 mg:
Ein- bis zweimal täglich ½ Tablette bzw. einmal täglich ½ bis 1 Tablette (entsprechend 50-100 mg Metoprololtartrat täglich).
Falls erforderlich kann die Tagesdosis unter Kontrolle des Blutdruckes auf zweimal 1 Tablette (entsprechend 200 mg Metoprololtartrat täglich) erhöht werden.
Tachykarde Herzrhythmusstörungen:
Bei der Verordnung von metodura 50 mg:
Ein- bis zweimal täglich 2 Tabletten (entsprechend 100-200 mg Metoprololtartrat täglich).
Bei der Verordnung von metodura 100 mg:
Ein- bis zweimal täglich 1 Tablette (entsprechend 100-200 mg Metoprololtartrat täglich).
Akutbehandlung des Herzinfarktes und Reinfarktprophylaxe:
metodura wird eingesetzt bei Patienten, für die keine Gegenanzeigen für eine Behandlung mit Beta-Rezeptorenblockern bestehen.
a) Akutbehandlung
Bei der Verordnung von metodura 50 mg bzw. metodura 100 mg:
Bei akutem Herzinfarkt erfolgt die Behandlung möglichst umgehend nach Krankenhauseinweisung unter kontinuierlicher EKG- und Blutdruckkontrolle. Die Behandlung wird mit 5 mg Metoprololtartrat i.v. begonnen. Je nach Verträglichkeit können in Abständen von 2 Minuten weitere Einzeldosen von 5 mg Metoprololtartrat i.v. bis zu einer maximalen Gesamtdosis von bis zu 15 mg Metoprololtartrat verabreicht werden.
Wird die volle Dosis von 15 mg i.v. vertragen, gibt man beginnend 15 Minuten nach der letzten intravenösen Injektion einmal 1 Tablette metodura 50 mg bzw. einmal ½ Tablette metodura 100 mg (entsprechend 50 mg Metoprololtartrat).
In den folgenden 48 Stunden wird alle 6 Stunden 1 Tablette metodura 50 mg bzw. ½ Tablette metodura 100 mg verabreicht.
Bei Patienten, die weniger als 15 mg Metoprololtartrat i.v. vertragen haben, sollte die orale Anschlussbehandlung vorsichtig mit einmal ½ Tablette metodura 50 mg (entsprechend 25 mg Metoprololtartrat) begonnen werden.
b) Erhaltungsdosis
Bei der Verordnung von metodura 50 mg bzw. metodura 100 mg:
Anschließend an die Akuttherapie werden zweimal 2 Tabletten metodura 50 mg bzw. zweimal 1 Tablette metodura 100 mg (entsprechend 200 mg Metoprololtartrat täglich) gegeben.
Bei behandlungsbedürftigem Abfall von Herzfrequenz und/oder Blutdruck oder anderen Komplikationen ist metodura 50 mg /- 100 mg sofort abzusetzen.
Migräneprophylaxe:
Bei der Verordnung von metodura 50 mg:
Ein- bis zweimal täglich 2 Tabletten (entsprechend 100-200 mg Metoprololtartrat täglich).
Bei der Verordnung von metodura 100 mg:
Ein- bis zweimal täglich 1 Tablette (entsprechend 100-200 mg Metoprololtartrat täglich).
Patienten mit Leberfunktionsstörungen
Bei stark eingeschränkter Leberfunktion ist die Elimination von metodura vermindert, so dass unter Umständen eine Dosisreduktion erforderlich ist.
Art der Anwendung
Die Tabletten sind unzerkaut mit ausreichend Flüssigkeit nach einer Mahlzeit einzunehmen.
Die Tabletten sollten bei Einmalgabe morgens bzw. bei zweimaliger Gabe morgens und abends eingenommen werden.
Sollte die Behandlung mit metodura nach längerer Anwendung unterbrochen oder abgesetzt werden, sollte dies, da abruptes Absetzen zur Herzischämie mit Exazerbation einer Angina pectoris oder zu einem Herzinfarkt oder zur Exazerbation einer Hypertonie führen kann, grundsätzlich langsam ausschleichend erfolgen.
metodura darf nicht eingenommen werden bei:
Überempfindlichkeit gegen den Wirkstoff, einen anderen Beta-Rezeptorenblocker oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile
manifester Herzinsuffizienz
Schock
AV-Block 2. oder 3. Grades
Sinusknoten-Syndrom (sick sinus syndrome)
sinuatrialem Block
Bradykardie (Ruhepuls kleiner als 50 Schläge pro Minute vor Behandlungsbeginn)
Hypotonie (systolisch kleiner als 90 mm Hg)
Azidose
bronchialer Hyperreagibilität (z. B. bei Asthma bronchiale)
Spätstadien peripherer Durchblutungsstörungen
gleichzeitiger Gabe von MAO-Hemmstoffen (Ausnahme MAO-B-Hemmstoffe)
Die intravenöse Applikation von Calciumantagonisten vom Verapamil- und Diltiazem-Typ oder anderen Antiarrhythmika (wie Disopyramid) bei Patienten, die mit metodura behandelt werden, ist kontraindiziert (Ausnahme Intensivmedizin).
Eine besonders sorgfältige ärztliche Überwachung ist erforderlich bei:
AV-Block 1. Grades
Diabetikern mit stark schwankenden Blutzuckerwerten (wegen möglicher schwerer hypoglykämischer Zustände)
längerem strengen Fasten und schwerer körperlicher Belastung (wegen möglicher schwerer hypoglykämischer Zustände)
Patienten mit Phäochromozytom (Nebennierenmarktumor) (metodura erst nach vorheriger alpha-Blockade verabreichen)
Patienten mit eingeschränkter Leberfunktion (siehe Dosierung).
Bei Patienten mit einer Psoriasis in der Eigen- oder Familienanamnese sollte die Verordnung von Beta-Rezeptorenblockern nur nach sorgfältiger Nutzen-Risiko-Abwägung erfolgen.
Beta-Rezeptorenblocker können die Empfindlichkeit gegenüber Allergenen und die Schwere anaphylaktischer Reaktionen erhöhen. Deshalb ist eine strenge Indikationsstellung bei Patienten mit schweren Überempfindlichkeitsreaktionen in der Vorgeschichte und bei Patienten unter Desensibilisierungstherapie (Vorsicht, überschießende anaphylaktische Reaktionen) geboten.
Die Anwendung von metodura kann bei Dopingkontrollen zu positiven Ergebnissen führen. Die Anwendung von metodura als Dopingmittel kann zu einer Gefährdung der Gesundheit führen.
Patienten mit der seltenen hereditären Galactose-Intoleranz, Lactase-Mangel oder Glucose-Galactose-Malabsorption sollten metodura nicht einnehmen.
Folgende Wechselwirkungen zwischen den vorliegenden und anderen Arzneimitteln sind zu beachten:
Bei gleichzeitiger Anwendung von metodura und Insulin oder oralen Antidiabetika kann deren Wirkung verstärkt, verlängert oder abgeschwächt werden. Warnzeichen einer Hypoglykämie - insbesondere Tachykardie und Tremor - sind verschleiert oder abgemildert. Daher sind regelmäßige Blutzuckerkontrollen erforderlich.
Bei gleichzeitiger Anwendung von metodura und trizyklischen Antidepressiva, Barbituraten, Phenothiazinen und Nitroglycerin sowie Diuretika, Vasodilatatoren und anderen blutdrucksenkenden Mitteln kann es zu einem verstärkten Blutdruckabfall kommen.
Bei gleichzeitiger Anwendung von metodura und Calciumantagonisten vom Nifedipin-Typ kann es zu einer verstärkten Blutdrucksenkung und in Einzelfällen zur Ausbildung einer Herzinsuffizienz kommen.
Die kardiodepressiven Wirkungen von metodura und Antiarrhythmika können sich addieren.
Bei gleichzeitiger Anwendung von metodura und Calciumantagonisten vom Verapamil- oder Diltiazem-Typ oder anderen Antiarrhythmika (wie Disopyramid) ist eine sorgfältige Überwachung der Patienten angezeigt, da es zu Hypotension, Bradykardie oder anderen Herzrhythmusstörungen kommen kann.
Hinweis:
Die intravenöse Applikation von Calciumantagonisten vom Verapamil- und Diltiazem-Typ oder anderen Antiarrhythmika (wie Disopyramid) bei Patienten, die mit metodura behandelt werden, ist kontraindiziert (Ausnahme Intensivmedizin).
Bei gleichzeitiger Anwendung von metodura und Herzglykosiden, Reserpin, alpha-Methyldopa, Guanfacin oder Clonidin kann es zu einem stärkeren Absinken der Herzfrequenz bzw. zu einer Verzögerung der Überleitung kommen.
Nach abruptem Absetzen von Clonidin bei gleichzeitiger Anwendung von metodura kann der Blutdruck überschießend ansteigen. Clonidin darf daher erst abgesetzt werden, wenn einige Tage zuvor die Verabreichung von metodura beendet wurde. Anschließend kann Clonidin stufenweise (siehe Fachinformation Clonidin) abgesetzt werden.
Bei gleichzeitiger Anwendung von metodura und Noradrenalin, Adrenalin oder anderen sympathomimetisch wirkenden Substanzen (z. B. enthalten in Hustenmitteln, Nasen- und Augentropfen) ist ein beträchtlicher Blutdruckanstieg möglich.
Unter metodura-Therapie kann es zu einer verminderten Ansprechbarkeit auf die zur Behandlung der allergischen Reaktion gewöhnlich eingesetzten Adrenalin-Dosis kommen.
Monoaminooxidase(MAO)-Hemmer sollten wegen möglicher überschießender Hypertension nicht zusammen mit metodura eingenommen werden.
Indometacin und Rifampicin können die blutdrucksenkende Wirkung von metodura vermindern.
Die Wirkung von metodura kann durch Cimetidin verstärkt werden.
metodura kann die Ausscheidung von Lidocain vermindern.
Die gleichzeitige Anwendung von metodura und Narkotika kann eine verstärkte Blutdrucksenkung zur Folge haben. Die negativ inotrope Wirkung der beiden vorgenannten Arzneimittel kann sich addieren.
Die neuromuskuläre Blockade durch periphere Muskelrelaxantien (z. B. Suxamethonium, Tubocurarin) kann durch die Beta-Rezeptorenhemmung von metodura verstärkt werden.
Für den Fall, dass metodura vor Eingriffen in Allgemeinnarkose oder vor der Anwendung peripherer Muskelrelaxantien nicht abgesetzt werden kann, muss der Narkosearzt über die Behandlung mit metodura informiert werden.
Schwangerschaft
Metoprolol darf in der Schwangerschaft nur nach strenger Nutzen-Risiko-Abwägung angewendet werden, da bislang keine ausreichend gut dokumentierte Studien zu einer Anwendung an schwangeren Frauen existieren.
Metoprolol zeigte in Tierversuchen keine teratogenen Eigenschaften (siehe Abschnitt 5.3). Metoprolol passiert die Plazenta und kann im Fötus zu Bradykardie, Hypotonie und Hypoglykämie führen.
Betablocker reduzieren die plazentare Durchblutung, was zu Frühgeburten oder zum intrauterinen Fruchttod führen kann. Das Risiko von kardialen und pulmonalen Komplikationen bei pränatal Metoprolol-exponierten Neugeborenen ist in der Postpartalperiode erhöht.
Metoprolol sollte 48-72 Stunden vor dem errechneten Geburtstermin abgesetzt werden. Wenn dies nicht möglich ist, müssen die Neugeborenen für die Dauer von 48-72 Stunden nach der Geburt sorgfältig auf Anzeichen einer β-Blockade überwacht werden.
Stillzeit
Metoprolol geht in die Muttermilch über. In der Muttermilch erreicht Metoprolol in etwa das Dreifache der bei der Mutter gemessenen Serumkonzentration. Obwohl nach therapeutischen Dosierungen nicht mit unerwünschten Wirkungen zu rechnen ist (Ausnahme sind „slow metabolizer“), sollten gestillte Säuglinge auf Anzeichen einer β-Blockade hin beobachtet werden.
Um die mit der Muttermilch aufgenommene Wirkstoffmenge gering zu halten, sollte 3-4 Stunden nach der Einnahme des Medikamentes nicht gestillt werden.
Die Behandlung mit diesen Arzneimitteln bedarf der regelmäßigen ärztlichen Kontrolle. Durch individuell auftretende unterschiedliche Reaktionen kann das Reaktionsvermögen soweit verändert sein, dass die Fähigkeit zur aktiven Teilnahme am Straßenverkehr, zum Bedienen von Maschinen oder zum Arbeiten ohne sicheren Halt beeinträchtigt wird. Dies gilt in verstärktem Maße bei Behandlungsbeginn, Dosiserhöhung und Präparatewechsel sowie im Zusammenwirken mit Alkohol.
Bei der Bewertung von Nebenwirkungen werden folgende Häufigkeiten zugrunde gelegt: Sehr häufig (≥1/10), Häufig (≥1/100 bis <1/10), Gelegentlich (≥1/1.000 bis <1/100), Selten (≥1/10.000 bis <1/1.000), Sehr selten (<1/10.000).
Erkrankungen des Nervensystems
Insbesondere zu Beginn der Behandlung kann es gelegentlich zu zentralnervösen Störungen wie Müdigkeit, depressiven Verstimmungen, Schwindelgefühl, Verwirrtheit, Kopfschmerzen, Schwitzen, Alpträumen oder verstärkter Traumaktivität, Schlafstörungen und Halluzinationen kommen.
Erkrankungen des Gastrointestinaltrakts
Vorübergehend kann es gelegentlich zu Magen-Darm-Beschwerden (Übelkeit, Erbrechen, Bauchschmerzen, Obstipation, Diarrhoe) kommen. Selten wurde Mundtrockenheit beobachtet.
Erkrankungen der Haut
Gelegentlich können allergische Hautreaktionen (Rötung, Juckreiz, Exantheme, Photosensitivität) auftreten.
Erkrankungen des Herz-Kreislauf- und Gefäßsystems
Gelegentlich kann es zu Parästhesien und Kältegefühl an den Extremitäten kommen. Auch eine Verstärkung der Beschwerden bei Patienten mit peripheren Durchblutungsstörungen (einschließlich Patienten mit Raynaud-Syndrom) sowie kardiogener Schock bei Patienten mit akutem Myokardinfarkt wurde beobachtet.
Die Behandlung mit metodura kann in seltenen Fällen zu verstärktem Blutdruckabfall, Synkopen, Palpitationen, Bradykardie, atrioventrikulären Überleitungsstörungen oder Verstärkung einer Herzinsuffizienz mit peripheren Ödemen und/oder Belastungsdyspnoe führen.
In vereinzelten Fällen ist bei Patienten mit Angina pectoris eine Verstärkung der Anfälle nicht auszuschließen.
Atemwegserkrankungen
Infolge einer möglichen Erhöhung des Atemwegswiderstandes kann es bei Patienten mit Neigung zu bronchospastischen Reaktionen (insbesondere bei obstruktiven Atemwegserkrankungen) zu Atemnot kommen.
Augenerkrankungen
Selten wurden Konjunktivitis oder verminderter Tränenfluss (dies ist beim Tragen von Kontaktlinsen zu beachten) sowie in Einzelfällen Sehstörungen beobachtet.
Stoffwechsel- und Ernährungsstörungen
In seltenen Fällen kann ein latenter Diabetes mellitus in Erscheinung treten oder ein manifester Diabetes mellitus sich verschlechtern. Nach längerem strengen Fasten oder schwerer körperlicher Belastung kann es bei gleichzeitiger metodura-Therapie zu hypoglykämischen Zuständen kommen.
Warnzeichen einer Hypoglykämie (insbesondere Tachykardie und Tremor) können verschleiert werden.
Unter der Therapie mit metodura kann es zu Störungen im Fettstoffwechsel kommen. Bei meist normalem Gesamtcholesterin wurden eine Verminderung des HDL-Cholesterins und eine Erhöhung der Triglyzeride im Plasma beobachtet.
Erkrankungen des Urogenitaltrakts
Vereinzelt wurden Libido- und Potenzstörungen beobachtet.
Erkrankungen des Muskel- und Skelettsystems
Selten kann es zu Muskelschwäche oder Muskelkrämpfen kommen. Bei Langzeittherapie mit metodura wurde in Einzelfällen eine Arthropathie (Mono- und Polyarthritis) beobachtet.
Leber- und Gallenerkrankungen
In Einzelfällen kann es zu einer Erhöhung der Transaminasen (GOT, GPT) im Serum oder zum Auftreten einer Hepatitis kommen.
Sonstiges
Des Weiteren wurden in Einzelfällen Haarausfall, Hörstörungen oder Ohrensausen, Gewichtszunahme, Persönlichkeitsveränderungen (z. B. Gefühlsschwankungen, kurzdauernder Gedächtnisverlust), eine Thrombozytopenie oder Leukopenie, eine Rhinitis allergica oder eine Induratio penis plastica (Peyronie`s disease) beobachtet.
Beta-Rezeptorenblocker können in Einzelfällen eine Psoriasis auslösen, die Symptome dieser Erkrankung verschlechtern oder zu psoriasiformen Exanthemen führen.
Besondere Hinweise:
Beta-Rezeptorenblocker können die Empfindlichkeit gegenüber Allergenen und die Schwere anaphylaktischer Reaktionen erhöhen. Bei Patienten mit schweren Überempfindlichkeitsreaktionen in der Vorgeschichte und bei Patienten unter Desensibilisierungstherapie kann es daher zu überschießenden anaphylaktischen Reaktionen kommen.
Bei schweren Nierenfunktionsstörungen wurde in Einzelfällen über eine Verschlechterung der Nierenfunktion unter Therapie mit Beta-Rezeptorenblockern berichtet. Eine Anwendung von metodura sollte in diesen Fällen unter entsprechender Überwachung der Nierenfunktion erfolgen.
metodura kann die Symptome einer Thyreotoxikose maskieren.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger-Allee 3, D-53175 Bonn, Website: https://www.bfarm.de , anzuzeigen.
Symptome
Das klinische Bild ist in Abhängigkeit vom Ausmaß der Intoxikation im Wesentlichen von kardiovaskulären und zentralnervösen Symptomen geprägt. Überdosierung kann zu schwerer Hypotonie, Bradykardie bis zum Herzstillstand, Herzinsuffizienz und kardiogenem Schock führen. Zusätzlich können Atembeschwerden, Bronchospasmen, Erbrechen, Bewusstseinsstörungen, gelegentlich auch generalisierte Krampfanfälle auftreten.
Therapiemaßnahmen
Bei Überdosierung oder bedrohlichem Abfall der Herzfrequenz und/oder des Blutdrucks muss die Behandlung mit metodura abgebrochen werden.
Neben allgemeinen Maßnahmen der primären Giftelimination müssen unter intensivmedizinischen Bedingungen die vitalen Parameter überwacht und gegebenenfalls korrigiert werden. Als Gegenmittel können gegeben werden:
Atropin: 0,5-2 mg intravenös als Bolus
Glukagon: initial 1-10 mg intravenös
anschließend 2-2,5 mg pro Std. als Dauerinfusion
Sympathomimetika in Abhängigkeit von Körpergewicht und Effekt: Dopamin, Dobutamin, Isoprenalin, Orciprenalin oder Adrenalin.
Bei therapierefraktärer Bradykardie sollte eine temporäre Schrittmachertherapie durchgeführt werden.
Bei Bronchospasmus können β2-Sympathomimetika als Aerosol (bei ungenügender Wirkung auch intravenös) oder Aminophyllin intravenös gegeben werden.
Bei generalisierten Krampfanfällen empfiehlt sich die langsame intravenöse Gabe von Diazepam.
Pharmakotherapeutische Gruppe: Beta-Rezeptorenblocker
ATC-Code: C07AB02
Metoprolol ist ein schwach lipophiler Beta-Rezeptorenblocker mit relativer β1-Selektivität („Kardioselektivität“), ohne intrinsische sympathomimetische Aktivität (ISA) und nur schwach ausgeprägter membranstabilisierender Wirkung.
Die Substanz senkt in Abhängigkeit von der Höhe des Sympathikotonus die Frequenz und die Kontraktionskraft des Herzens, die AV-Überleitungsgeschwindigkeit und die Plasma-Renin-Aktivität. Metoprolol kann durch Hemmung von β2-Rezeptoren eine Erhöhung des Tonus der glatten Muskulatur bewirken.
Nach oraler Applikation wird Metoprolol nahezu vollständig (ca. 95 %) aus dem Gastrointestinaltrakt resorbiert. Da Metoprolol einem ausgeprägten First-Pass-Metabolismus unterliegt, beträgt die systemische Verfügbarkeit nur ca. 50 %. Maximale Plasmaspiegel werden nach 1,5-2 Stunden erreicht.
Die Plasmaproteinbindung liegt bei ca. 12 %; das relative Verteilungsvolumen beträgt 5,6 l/kg.
Metoprolol wird fast vollständig in der Leber metabolisiert. Zwei der drei Hauptmetaboliten zeigen schwach betablockierende Eigenschaften, sind jedoch klinisch nicht relevant. Bei Leberzirrhose muss wegen der dann verminderten Metabolisierungsrate mit erhöhten Plasmaspiegeln an unverändertem Metoprolol gerechnet werden.
Metoprolol und seine Metabolite werden zu ca. 95 % - davon ca. 10 % unverändert - renal eliminiert. Die Eliminationshalbwertszeit von Metoprolol beträgt 3-5 Stunden.
a) Akute Toxizität
Siehe Abschnitt 4.9.
b) Chronische Toxizität
Untersuchungen zur chronischen Toxizität an verschiedenen Tierspezies erbrachten keine Hinweise auf substanzbedingte toxische Effekte.
c) Tumorerzeugendes und mutagenes Potential
Es liegen Ergebnisse von Kanzerogenitätsstudien an Ratten und Mäusen vor, aus denen sich kein tumorerzeugendes Potential ableiten lässt.
Metoprolol wurde keiner ausführlichen Mutagenitätsprüfung unterzogen; bisherige Untersuchungen ergaben keine Hinweise auf ein mutagenes Potential.
d) Reproduktionstoxizität
Untersuchungen an zwei Tierspezies (Ratte und Kaninchen) haben keine Hinweise auf teratogene Eigenschaften von Metoprolol ergeben. Für den Menschen liegen keine ausreichenden Erkenntnisse über die Sicherheit der Anwendung im ersten und zweiten Schwangerschaftsdrittel vor. Berichte über Geburtsschädigungen durch Metoprolol wurden nicht gefunden.
Humanstudien ergaben Hinweise auf eine Beeinträchtigung der Plazentaperfusion durch Metoprolol. Zum Zeitpunkt der Geburt sind die Serumkonzentrationen von Mutter und Kind vergleichbar. In der Muttermilch erreicht Metoprolol in etwa das Dreifache der bei der Mutter gemessenen Serumkonzentration. Bei einer täglichen Einnahme von 200 mg Metoprolol werden ca. 225 µg pro Liter Milch ausgeschieden.
Calciumhydrogenphosphat
Hyprolose
Lactose-Monohydrat
Magnesiumstearat (Ph. Eur.)
Maisstärke
mikrokristalline Cellulose
hochdisperses Siliciumdioxid
Crospovidon (Typ A)
Nicht zutreffend.
5 Jahre
Für diese Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
PP/Aluminium-Blister mit 20, 30, 50 oder 100 Tabletten.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
Keine besonderen Anforderungen.
Mylan Germany GmbH
Lütticher Straße 5
53842 Troisdorf
Mitvertrieb:
Viatris Healthcare GmbH
Lütticher Straße 5
53842 Troisdorf
metodura 50 mg: 9068.00.00
metodura 100 mg: 9068.01.00
Datum der Erteilung der Zulassungen: 18. November 1991
Datum der letzten Verlängerung der Zulassungen: 7. März 2005
August 2024
Verschreibungspflichtig
Zusätzliche Angaben der Firma Mylan Germany GmbH zur Bioverfügbarkeit von metodura 100 mg
Bioverfügbarkeit
metodura 100 mg
Eine im Jahr 1991 durchgeführte Bioverfügbarkeitsuntersuchung (single-dose) an 24 Probanden ergab im Vergleich zum Referenzpräparat:
metodura 100 mg | Referenzpräparat | |
maximale Plasmakonzentration | 185 ± 112 | 179 ± 125 |
Zeitpunkt der maximalen Plasmakonzentration | 1,20 ± 0,58 | 1,48 ± 0,63 |
Fläche unter der Konzentrations-Zeit-Kurve | 905,7 ± 958,9 | 899,9 ± 969,8 |
Fläche unter der Konzentrations-Zeit-Kurve | 999,4 ± 1103,4 | 999,5 ± 1136,1 |
Angabe der Werte als Mittelwert und Streubreite
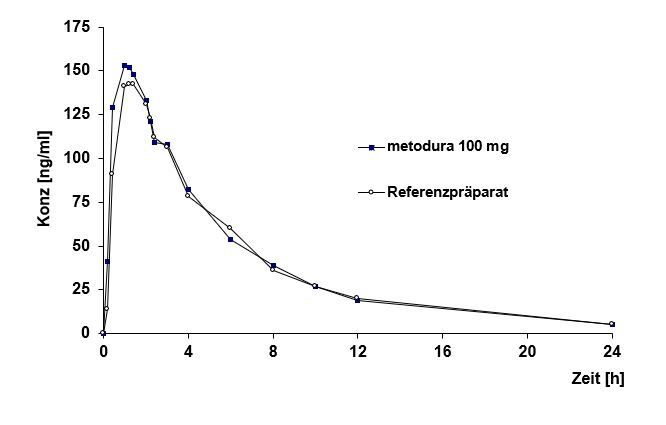
Mittlere Plasmaspiegelverläufe im Vergleich zu einem Referenzpräparat in einem Konzentrations-Zeit-Diagramm: