▼Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung zu melden. Hinweise zur Meldung von Nebenwirkungen, siehe Abschnitt 4.8.>
HD-CAR-19; 0,5-2,0 x108/m2 KOF; Dispersion für Infusion
HD-CAR-19 (Heidagen-lecleucel) ist ein Arzneimittel, welches auf genetisch modifizierten, autologen Zellen basiert. Dieses enthält T-Zellen, die ex vivo mit einem retroviralen Vektor transduziert wurden, der einen gegen CD19 gerichteten chimären Antigenrezeptor (CAR) exprimiert, welcher ein variables Maus-Anti-CD19-Einzelkettenfragment (scFv) umfasst, dass mit den kostimulatorischen Domänen CD28 und 4-1bb verbunden sind. Zudem ist die Signaldomäne CD3-zeta damit verbunden.
Jeder patientenspezifische HD-CAR-19 Infusionsbeutel enthält Heidagen-lecleucel in einer Konzentration von 1 x107 viablen Zellen/ml einen chargenspezifischen Anteil an autologen T-Zellen, die genetisch modifiziert wurden, um einen gegen CD19 gerichteten CAR zu exprimieren (CAR-positive lebensfähige Zellen). Das Arzneimittel ist in einem Infusionsbeutel abgepackt, der eine Zell-Infusionsdispersion mit 0,5-2,0 x108 CAR-T-Zellen pro m2 Körperoberfläche (KOF) enthält. Das maximale Volumen, das ein Patient/eine Patientin erhalten wird, beträgt 100 ml. Ein Infusionsbeutel enthält maximal 70 ml Zellsuspension. Gegebenenfalls müssen zwei Beutel verabreicht werden. Es werden insgesamt nicht mehr als zwei Beutel verabreicht. Die Dosis wird speziell für jeden Patienten berechnet und ist abhängig von der Körperoberfläche des Patienten und das Volumen von der Anzahl an CD19-CAR transduzierten T-Zellen im Präparat.
Die genaue Zusammensetzung des Arzneimittels ist in Tabelle 1 dargestellt.
Tabelle 1: Zusammensetzung des Arzneimittels
Komponente |
Funktion |
Menge |
Nicht-transduzierte Zellen |
Enthält aktive Zellpopulation |
< 85% der T-Zellen |
Viable CAR T-Zellen |
Aktiver Bestandteil |
≥ 15% der T-Zellen |
DMSO |
Teil des Einfriermediums zum Schutz der Zellen |
10% des Volumens |
PBS |
Teil des Einfriermediums |
40% des Volumens |
Humanes Serum Albumin (HSA) |
Teil des Einfriermediums zum Schutz der Zellen |
50% des Volumens |
Sonstige(r) Bestandteil(e) mit bekannter Wirkung:
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
Dispersion zur Infusion.
Erwachsene Patienten mit rezidivierten oder refraktären CD19+- Erkrankungen des lymphatischen Systems: chronische lymphatische Leukämie (CLL)
CLL: C91.1
HD-CAR-19 muss in einem qualifizierten Behandlungszentrum von einem Arzt angewendet werden, der über Erfahrung in der Behandlung von hämatologischen Erkrankungen verfügt und der in der Verabreichung von CAR-T-Zellpräparaten sowie dem Management dieser Patienten, geschult ist.
Besondere Patientengruppen
Ältere Patienten
Bei Patienten im Alter von > 65 Jahren ist keine Dosisanpassung erforderlich.
Kinder und Jugendliche
Die Sicherheit und Wirksamkeit von HD-CAR-19 bei Kindern und Jugendlichen unter 18 Jahren ist bisher noch nicht erwiesen. Es liegen keine Daten vor.“
Für den Fall des Auftretens eines Zytokin-Freisetzungs-Syndroms (Cytokine Release Syndrome, CRS) muss mindestens 1 Dosis Tocilizumab zur Verfügung stehen. Das Behandlungszentrum muss innerhalb von 8 Stunden nach jeder vorangegangenen Dosis Zugang zu einer weiteren Dosis Tocilizumab haben. Sollte Tocilizumab aufgrund von Lieferengpässen nicht verfügbar sein, müssen vor der Infusion geeignete alternative Maßnahmen zur Behandlung eines CRS zur Verfügung stehen.
Dosierung
Die Behandlung besteht aus einer Einzeldosis zur Infusion, die eine Infusionsdispersion von CAR-positiven, lebensfähigen T-Zellen enthält. Eine Dosis besteht aus maximal 2 Infusionsbeuteln, die nacheinander gegeben werden.
Die Dosis von HD-CAR-19 muss auf der Grundlage des der Körperoberfläche des Patienten während der Herstellung festgelegt werden.
Die Zieldosis beträgt 0,5-2,0 x108/m2 KOF i.v. zur autologen Anwendung bei CLL-Patienten.
Die genaue Dosis ist für jeden Patienten in der jeweiligen Begleit-Dokumentation aufgeführt.
Vorbehandlung (Chemotherapie zur Lymphozytendepletion)
Ein Chemotherapie-Schema zur Lymphodepletion, das aus intravenös verabreichtem Cyclophosphamid 500mg/m2 und intravenös verabreichtem Fludarabin 30 mg/m2 besteht, muss vor der Infusion von HD-CAR-19 verabreicht werden. Die hierfür empfohlenen Tage sind der 4., 3. und 2. Tag vor der Infusion von HD-CAR-19.
Überwachung
Die Patienten müssen in den ersten 10 Tagen nach der Infusion täglich auf Anzeichen und Symptome eines potenziellen CRS (cytokine release syndrome, Zytokin-Freisetzungs-Syndrom), neurologischer Ereignisse und anderer Toxizitäten überwacht werden. Ärzte sollen eine Hospitalisierung für die ersten 10 Tage nach der Infusion, oder bei ersten Anzeichen/Symptomen eines CRS und/oder neurologischer Ereignisse, in Erwägung ziehen. Nach Ablauf der ersten 10 Tage nach der Infusion ist der Patient nach Ermessen des Arztes zu überwachen. Die Patienten sind anzuweisen, sich nach der Infusion mindestens 4 Wochen lang in der Nähe eines qualifizierten Behandlungszentrums aufzuhalten und sich unverzüglich in ärztliche Behandlung zu begeben, wenn Anzeichen oder Symptome eines CRS oder neurologischer Nebenwirkungen auftreten. Die Vitalzeichen und Organfunktionen müssen in Abhängigkeit von der Schwere der Nebenwirkung überwacht werden.
Art der Anwendung
HD-CAR-19 ist ausschließlich zur autologen Anwendung vorgesehen. Vor der Infusion muss die Identität des Patienten mit den Patienten-Identifizierungsmerkmalen auf dem Infusionsbeutel und der Kassette abgeglichen werden („Chain of Identity“, Prüfung auf Identität des Präparates).
HD-CAR-19 ist mittels intravenöser Infusion zu verabreichen.
HD-CAR-19 darf nicht bestrahlt werden. Es darf KEIN leukozytendepletierender Filter verwendet werden.
Vor der Verabreichung muss bestätigt werden, dass die Identität des Patienten mit den eindeutigen
Patientenangaben auf dem HD-CAR-19 -Infusionsbeutel und der Kassette übereinstimmt.
Ausführliche Anweisungen zu Zubereitung, Anwendung, Maßnahmen im Falle einer versehentlichen Exposition und Beseitigung von HD-CAR-19, siehe Abschnitt 6.6.
Überempfindlichkeit gegen den Wirkstoff oder gegen einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
Rückverfolgbarkeit
Es müssen die Anforderungen an die Rückverfolgbarkeit zellbasierter Arzneimittel für neuartige Therapien eingehalten werden. Um die Rückverfolgbarkeit zu gewährleisten, sind die Bezeichnung des angewendeten Arzneimittels, die Chargenbezeichnung und der Name des behandelten Patienten für einen Zeitraum von 30 Jahren nach dem Verfalldatum des Arzneimittels aufzubewahren.
Autologe Anwendung
HD-CAR-19 ist ausschließlich für die autologe Anwendung bestimmt und darf unter keinen Umständen an andere Patienten verabreicht werden. Das Präparat darf nicht angewendet werden, wenn die Angaben auf den Produktetiketten und der Begleitdokumentation nicht mit der Identität des Patienten übereinstimmen.
Allgemein
Die Warnhinweise und Vorsichtsmaßnahmen für die Chemotherapie zur Lymphodepletion müssen berücksichtigt werden.
Überwachung nach der Infusion
Die Patienten müssen in den ersten 10 Tagen nach der Infusion täglich auf Anzeichen und Symptome eines potenziellen CRS (cytokine release syndrome, Zytokin-Freisetzungs-Syndrom), neurologischer Ereignisse und anderer Toxizitäten überwacht werden. Ärzte sollen eine Hospitalisierung für die ersten 10 Tage nach der Infusion, oder bei ersten Anzeichen/Symptomen eines CRS und/oder neurologischer Ereignisse, in Erwägung ziehen. Nach Ablauf der ersten 10 Tage nach der Infusion ist der Patient nach Ermessen des Arztes zu überwachen. Die Patienten sind anzuweisen, sich nach der Infusion mindestens 4 Wochen lang in der Nähe eines qualifizierten Behandlungszentrums aufzuhalten und sich unverzüglich in ärztliche Behandlung zu begeben, wenn Anzeichen oder Symptome eines CRS oder neurologischer Nebenwirkungen auftreten. Die Vitalzeichen und Organfunktionen müssen in Abhängigkeit von der Schwere der Nebenwirkung überwacht werden.
Gründe für einen Aufschub der Behandlung
Aufgrund der Risiken, die mit der HD-CAR-19 -Behandlung verbunden sind, muss die Infusion verschoben werden, wenn auf den Patienten einer der folgenden Zustände zutrifft:
Bestehende schwerwiegende Nebenwirkungen (insbesondere Reaktionen bezüglich der Lunge oder des Herzens, oder Hypotonie), einschließlich jener, die durch vorangegangene Chemotherapien entstanden sind.
Aktive unkontrollierte Infektion.
Aktive Graft-versus-host-disease (GVHD).
In manchen Fällen kann die Behandlung nach der Anwendung des Chemotherapie-Schema zur Lymphodepletion verschoben werden. Wird die Behandlung um mehr als 2 Woche, nachdem der Patient die Chemotherapie zur Lymphodepletion erhalten hat, aufgeschoben wird, muss das Chemotherapie-Schema zur Lypmhodepletion erneut angewendet werden (siehe Abschnitt 4.2).
Serologische Untersuchung
Vor der Entnahme der Zellen für die Herstellung von HD-CAR-19 muss ein Screening auf HBV, HCV und HIV durchgeführt werden.
Spende von Blut, Organen, Geweben und Zellen
Patienten, die mit HD-CAR-19 behandelt werden, dürfen kein Blut, keine Organe, kein Gewebe und keine Zellen für eine Transplantation spenden.
Aktives Lymphom des zentralen Nervensystems (ZNS)
Es liegen keine Erfahrungen zur Anwendung dieses Arzneimittels bei Patienten mit aktivem ZNS-Lymphom, definiert als mittels Bildgebung bestätigte Hirnmetastasen, vor. In bereits durchgeführten Studien wurden bisher nur asymptomatische Patienten mit Heidagen-lecleucel behandelt, mit ZNS-2-Status (definiert als weiße Blutkörperchen < 5/μl in der Zerebrospinalflüssigkeit bei Vorhandensein von Lymphoblasten) und ohne klinisch ersichtliche neurologische Veränderungen. Die Daten in dieser Population sind jedoch begrenzt. Daher ist das Nutzen-Risiko-Verhältnis von Heidagen-lecleucel bei diesen Patientengruppen nicht bekannt.
Begleiterkrankung
Patienten mit einer aktiven Erkrankung des ZNS in der Anamnese oder unzureichender Nieren-, Leber-, Lungen- oder Herzfunktion waren von den Studien ausgeschlossen. Es ist davon auszugehen, dass diese Patienten anfälliger für die Folgen der nachstehend beschriebenen Nebenwirkungen sind und engmaschiger überwacht werden müssen.
Zytokin-Freisetzungs-Syndrom
Bei 12/38 Patienten (32%) ist bisher ein CRS aufgetreten. Es wurden Grad 1-2 CRS (29%), sowie ein einziges Mal (3%) Grad 3 beobachtet. Die Zeit bis zum Einsetzen des Syndroms betrug in allen Fällen nur wenige Tage. Um diesen in Studien erreichten Sicherheitsstandard zu ermöglichen, müssen Patienten engmaschig auf Anzeichen oder Symptome dieser Ereignisse überwacht werden, wie z. B. hohes Fieber, Hypotonie, Hypoxie, Schüttelfrost, Tachykardie und Kopfschmerzen (siehe Abschnitt 4.8). Ein CRS ist nach Ermessen des Arztes zu behandeln, basierend auf dem klinischen Zustand des Patienten und entsprechend des in Tabelle 1 aufgeführten Behandlungsalgorithmus für CRS.
Für die Diagnose des CRS müssen alternative Ursachen einer systemischen inflammatorischen Reaktion, einschließlich Infektion, ausgeschlossen werden.
Behandlung des Heidagen-lecleucel-assoziierten Zytokin-Freisetzungs-Syndroms (CRS)
Vor der Heidagen-lecleucel-Infusion muss mindestens 1 Dosis Tocilizumab, ein Interleukin-6 (IL-6)- Rezeptor-Blocker, pro Patient vor Ort sein und zur Verabreichung zur Verfügung stehen. Das qualifizierte Behandlungszentrum muss innerhalb von 8 Stunden nach jeder vorangegangenen Dosis Zugang zu einer weiteren Dosis Tocilizumab haben. In dem Ausnahmefall, in dem Tocilizumab aufgrund eines Lieferengpasses, der im Lieferengpasskatalog der Europäischen Arzneimittel-Agentur aufgeführt ist, nicht verfügbar ist, muss das Behandlungszentrum Zugang zu geeigneten alternativen Maßnahmen anstelle von Tocilizumab zur Behandlung eines CRS haben.
Es wurden Behandlungsalgorithmen entwickelt, um einige der CRS-Symptome, die bei Patienten unter Heidagen-lecleucel aufgetreten sind, zu lindern. Diese schließen die Anwendung von Tocilizumab bzw. Tocilizumab und Kortikosteroiden ein. Patienten mit CRS vom Schweregrad 2 oder höher (z. B. nicht auf Flüssigkeitsgabe ansprechende Hypotonie, oder Hypoxie, die eine ergänzende Sauerstoffgabe erfordert) müssen durch kontinuierliches telemetrisches Monitoring des Herzens sowie Pulsoxymetrie überwacht werden. Bei Patienten mit schwerem CRS sollte die Durchführung eines Echokardiogramms zur Überwachung der Herzfunktion erwogen werden. Bei schwerem oder lebensbedrohlichem CRS ist eine intensiv-medizinische supportive Behandlung indiziert.
CRS ist bekanntermaßen mit Endorgan-Dysfunktion (z. B. Leber, Nieren, Herz und Lunge) assoziiert. Darüber hinaus kann im Zusammenhang mit CRS eine Verschlechterung zugrunde liegender Organpathologien auftreten. Patienten mit einer medizinisch signifikanten kardialen Dysfunktion müssen entsprechend intensiv-medizinischer Standards überwacht werden und Maßnahmen wie Echokardiographie sind zu erwägen.
Tabelle 2: Schweregrade eines Zytokin-Freisetzungs-Syndroms (cytokine release syndrome (CRS))
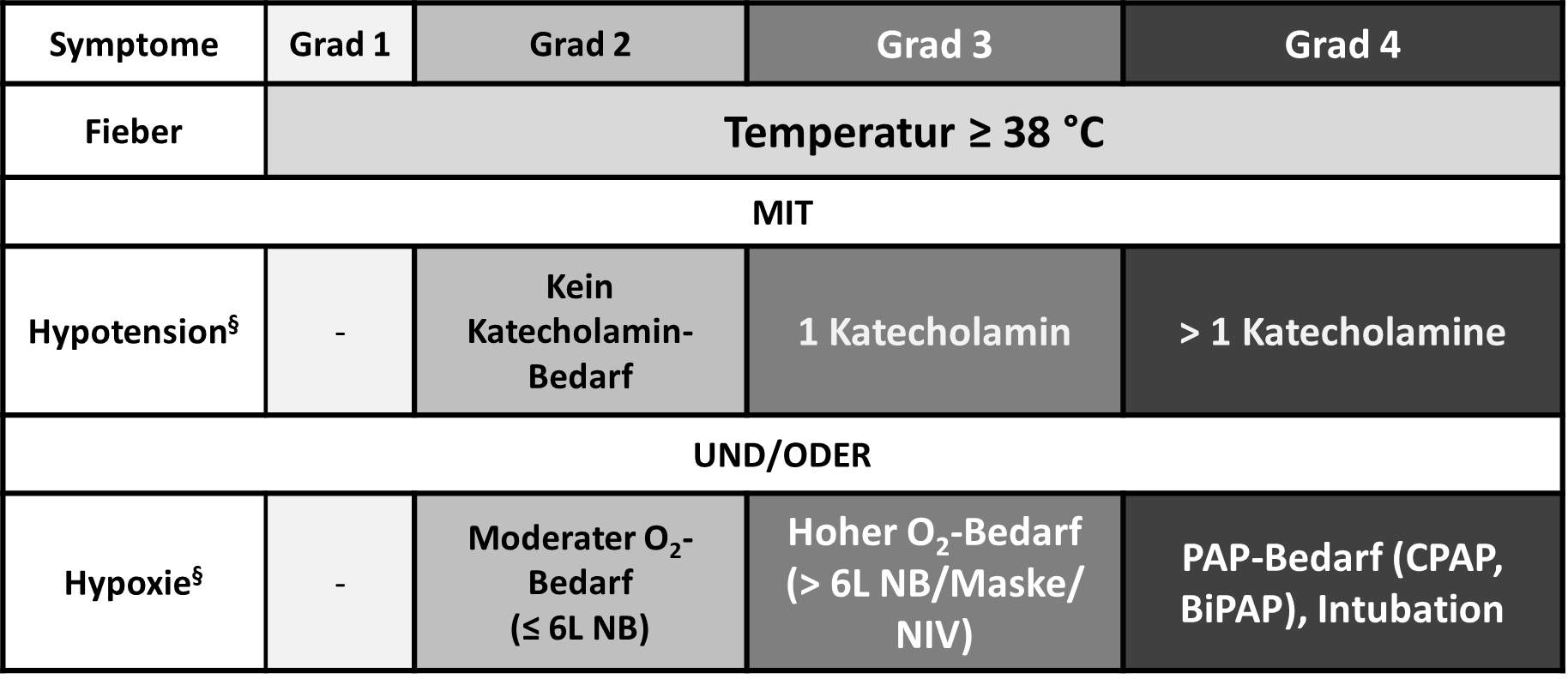
Abbildung 1: Behandlung des Zytokine-Freisetzungs-Syndroms (CRS):

Neurotoxizität
Bis dato ist bei allen Anwendungen von Heidagen-lecleucel keine Produkt-spezifische Neurotoxizität als so genanntes Immune cell associated neuropathy syndrome (ICANS) aufgetreten.
Sollte ICANS auftreten, wäre das Grading-System und die therapeutische Vorgehensweise wie untenstehend:
Tabelle 3: Einteilung des Schweregrades einerNeurotoxizität (Immune cell associated neuropathy syndrome (ICANS)

Abbildung 2: Behandlung bei Neurotoxizität (ICANs)


Infektionen und febrile Neutropenie
Schwerwiegende Infektionen, die lebensbedrohlich verlaufen konnten, wurden sehr häufig im Zusammenhang mit Heidagen-lecleucel beobachtet (siehe Abschnitt 4.8).
Patienten müssen vor, während und nach der Infusion auf Anzeichen und Symptome einer Infektion überwacht und entsprechend behandelt werden. Prophylaktische Antibiotika müssen gemäß den Standardleitlinien der Einrichtung angewendet werden.
Nach Heidagen-lecleucel-Infusion sind bei Patienten febrile Neutropenien beobachtet worden (siehe Abschnitt 4.8). Diese können gleichzeitig mit einem CRS auftreten. Im Falle einer febrilen Neutropenie ist eine Infektionsdiagnostik durchzuführen und eine Behandlung mit Breitbandantibiotika, Flüssigkeiten und anderen supportiven Maßnahmen, je nach medizinischer Indikation, einzuleiten.
Bei immunsupprimierten Patienten wurden lebensbedrohliche und tödlich verlaufende opportunistische Infektionen berichtet, einschließlich
disseminierter Pilzinfektionen und Virusreaktivierung (z. B. HHV-6 und progressive multifokale Leukoenzephalopathie). Bei Patienten mit neurologischen Ereignissen sollte die Möglichkeit solcher Infektionen in Betracht gezogen werden und es müssen entsprechende diagnostische Abklärungen durchgeführt werden.
Virusreaktivierung
Eine Virusreaktivierung, z. B. eine Reaktivierung des Hepatitis-B-Virus (HBV), kann bei Patienten, die mit gegen B-Zellen gerichteten Arzneimitteln behandelt werden, auftreten und kann zu einer fulminanten Hepatitis, Leberversagen und zum Tod führen. Bei länger anhaltenden Lymphopenien (s.u.) muss auch eine Diagnostik auf myelotrope Viren wie CMV, EBV, HSV oder Parvovirus B19 durchgeführt werden.
Länger anhaltende Zytopenien
Nach Chemotherapie zur Lymphodepletion und Heidagen-lecleucel -Infusion können die Patienten über mehrere Wochen anhaltende Zytope-nien entwickeln und diese müssen gemäß
den Standardleitlinien behandelt werden. Nach Heidagen-lecleucel -Infusion traten sehr häufig länger anhaltende Zytopenien 3. oder höheren Grades auf, einschließlich Thrombozytopenie, Neutropenie und Anämie (siehe Abschnitt 4.8). Das Blutbild des Patienten muss nach der Heidagen-lecleucel-Infusion überwacht werden.
Hypogammaglobulinämie
Bei Patienten, die mit Heidagen-lecleucel behandelt werden, kann eine B-Zell-Aplasie auftreten, welche zu einer Hypogammaglobulinämie führt. Hypogammaglobulinämie wurde bei mit Heidagen-lecleucel behandelten Patienten beobachtet (siehe Abschnitt 4.8). Eine Hypogammaglobulinämie macht Patienten
anfälliger für Infektionen. Die Immunglobulin-Konzentrationen sind nach der Behandlung mit Heidagen-lecleucel zu überwachen und müssen im Falle rezidivierender Infektionen durch Vorbeugung von Infektionen, antibiotische Prophylaxe und Substitution mit Immunglobulinen und gemäß den Standardleitlinien gehandhabt werden.
Überempfindlichkeitsreaktionen
Schwerwiegende Überempfindlichkeitsreaktionen, einschließlich Anaphylaxie, können aufgrund von DMSO in Heidagen-lecleucel auftreten.
Sekundäre Malignome
Patienten, die mit Heidagen-lecleucel behandelt werden, können sekundäre Malignome entwickeln. Nach der Behandlung hämatologischer Malignome mit einer BCMA- oder CD19-gerichteten CAR-T-Zelltherapie wurden T-Zell-Malignome gemeldet. T-Zell-Malignome, einschließlich CAR-positiver Malignome, wurden innerhalb von Wochen bis zu mehreren Jahren nach Verabreichung einer CD19- oder BCMA-gerichteten CAR-T-Zelltherapie gemeldet. Es gab Fälle mit tödlichem Ausgang. Die Patienten müssen lebenslang auf sekundäre Malignome überwacht werden. Wenn ein sekundäres Malignom auftritt, ist der pharmazeutische Hersteller zu kontaktieren, um Anweisungen zur Entnahme von Patientenproben für eine Untersuchung zu erhalten.
Tumorlysesyndrom (TLS)
TLS, das schwerwiegend sein kann, wurde gelegentlich beobachtet. Um das TLS-Risiko zu minimieren, sollten Patienten mit erhöhten Harnsäurewerten oder einer hohen Tumorlast vor der Heidagen-lecleucel -Infusion Allopurinol oder eine alternative Prophylaxe erhalten. Anzeichen und Symptome eines TLS müssen überwacht und bei einem Auftreten gemäß Standardleitlinien behandelt werden.
Vorherige Stammzelltransplantation (GVHD)
Patienten, die sich einer allogenen Stammzelltransplantation unterzogen haben und an einer aktiven akuten oder chronischen GVHD leiden, sollten keine Heidagen-lecleucel Behandlung erhalten, da das potenzielle Risiko einer Verschlimmerung der GVHD besteht.
Überempfindlichkeitsreaktionen
Schwerwiegende Überempfindlichkeitsreaktionen, einschließlich Anaphylaxie, können auf das Kryokonservierungsmittel DMSO im Präparat zurückzuführen sein.
Langzeitnachbeobachtung
Die Patienten mit einer Heidagen-lecleucel Behandlung können / haben die Möglichkeit in das europäische EBMT-Register, sowie in einem Produkt-spezifischen Register des Herstellers aufgenommen zu werden. Damit kann die langfristige Wirksamkeit und Sicherheit der Behandlung genauer erfasst werden.
Es wurden keine pharmakokinetischen oder pharmakodynamischen Studien zur Erfassung von Arzneimittelwechselwirkungen mit HD-CAR-19 durchgeführt. Die gleichzeitige Anwendung von Arzneimitteln, von denen bekannt ist, dass sie die Funktion von T-Zellen hemmen, wurde nicht untersucht.
Lebendimpfstoffe
Die Sicherheit einer Immunisierung mit viralen Lebendimpfstoffen während oder nach der Behandlung mit HD-CAR-19 wurde nicht untersucht. Als Vorsichtsmaßnahme wird für mindestens 6 Wochen lang vor Beginn der Chemotherapie zur Lymphozytendepletion, während der Behandlung mit HD-CAR-19 und bis zur Wiederherstellung des Immunsystems nach der Behandlung HD-CAR-19 nicht empfohlen.
Eine Anwendung während der Schwangerschaft und Stillzeit ist nicht vorgesehen.
Frauen im gebärfähigen Alter/Empfängnisverhütung bei Männern und Frauen
Vor Beginn der HD-CAR-19 -Therapie muss bei Frauen im gebärfähigen Alter der Schwangerschaftsstatus erhoben werden.
Informationen zur Notwendigkeit der Anwendung einer zuverlässigen Verhütungsmethode bei Patientinnen, die eine Chemotherapie zur Lymphodepletion erhalten, sind den Fachinformationen der Chemotherapeutika zur Lymphodepletion zu entnehmen.
Es liegen unzureichende Expositionsdaten vor, um eine Empfehlung bezüglich der Dauer der Verhütung nach einer Behandlung mit HD-CAR-19 auszusprechen.
Schwangerschaft
Es liegen keine Daten zur Anwendung von HD-CAR-19 bei Schwangeren vor. Es wurden keine tierexperimentellen Studien zur Reproduktions- und Entwicklungstoxizität mit HD-CAR-19 durchgeführt, um zu beurteilen, ob die Verabreichung an eine Schwangere schädlich für den Fötus sein kann.
Es ist nicht bekannt, ob HD-CAR-19 potenziell auf den Fötus übergehen kann. Basierend auf dem Wirkmechanismus können die transduzierten Zellen, wenn sie plazentagängig sind, zu einer fötalen Schädigung, einschließlich einer B-Zell-Lymphozytopenie, führen. Die Anwendung von HD-CAR-19 bei Schwangeren oder bei Frauen im gebärfähigen Alter, die nicht verhüten, wird daher nicht empfohlen.
Schwangere müssen hinsichtlich der potenziellen Risiken für den Fötus beraten werden. Eine Schwangerschaft nach der HD-CAR-19 -Therapie muss mit dem behandelnden Arzt besprochen werden.
Bei Neugeborenen von mit HD-CAR-19 -behandelten Müttern muss die Untersuchung der Immunglobulinkonzentrationen sowie der Anzahl der B-Zellen in Erwägung gezogen werden.
Stillzeit
Es ist nicht bekannt, ob das HD-CAR-19-Präparat in die Muttermilch oder auf das gestillte Kind übergeht. Stillende Frauen müssen über das potenzielle Risiko für das gestillte Kind informiert werden.
Fertilität
Es sind keine klinischen Daten über die Auswirkung von HD-CAR-19 auf die Fertilität verfügbar. Die Auswirkungen auf die männliche und weibliche Fertilität wurden nicht in tierexperimentellen Studien untersucht.
HD-CAR-19 hat großen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen. Aufgrund des Potenzials neurologischer Ereignisse, einschließlich veränderter mentaler Fähigkeiten oder Krampfanfälle, müssen Patienten nach der Infusion mindestens 8 Wochen lang oder bis zum Abklingen neurologischer Nebenwirkungen vom Führen eines Fahrzeugs oder dem Bedienen schwerer oder potenziell gefährlicher Maschinen absehen.
Nach CAR-T-Zell-Gabe können als klassische Nebenwirkung das Zytokin-Freisetzungs-Syndrom (cytokine release syndrome; CRS) und Neurotoxizität (immune effector cell associated neurotoxicity syndrome; ICANS) auftreten. Längerfristig können zusätzlich eine Anfälligkeit für bakterielle, viral und Pilz-Infektionen bestehen. Dies ist durch die unter Umständen verlängerte Zeit der hämatopoetischen Rekonstitution und damit auch der Rekonstitution des Immunsystems bedingt.
Die häufigste Nebenwirkung der Behandlung mit CAR T-Zellen ist das Zytokin-Freisetzungs-Syndrom (cytokine release syndrome (CRS)). Dabei handelt sich um eine sehr häufige (mehr als 1 von 10 Behandelten) Reaktion des Immunsystems, die sich mit Fieber, Schüttelfrost, Blutdruckabfällen, Luftnot, oder Kopfschmerz äußern kann. In etwa 30% der Patienten mit CRS können schwerwiegende bis lebensbedrohliche Nebenwirkungen (Nierenversagen, Krampfanfall, Kreislaufstillstand) auftreten.
Die Symptome sind jedoch bei der rechtzeitigen Behandlung mit Kortison und/oder einem bestimmten Antikörper (Tocilizumab) gut behandelbar.
Ein schweres CRS kann sich mit einer überschießenden Immunaktivierung, die als hämophagozytische Lymphohistiozytose (HLH) bzw. Makrophagenaktivierungssyndrom (MAS) bezeichnet wird, einhergehen bzw. überlappen. Bisher konnte nicht geklärt werden, ob es sich bei HLH/MAS um die Endstrecke des CRS oder um eine eigenständige Nebenwirkung der CAR-T-Zell-Therapie handelt. Bemerkbar macht sich HLH/MAS durch Fieber, Vergrößerung der Leber, Milz und/oder Lymphknoten, Abfall der weißen oder roten Blutkörperchen sowie Blutplättchen, Blutungszeichen, Krampfanfälle, Hirnnervenausfälle oder Bewusstseinstrübung. Neben Blutanalysen kann eine Knochenmarkpunktion mit Nachweis einer Hämophagozytose die Diagnose stützen. Die Behandlung entspricht jedoch weitgehend der CRS-Behandlung, worunter sich die Symptome in den meisten Fällen zurückbilden.
Als weitere Nebenwirkung können häufig (bis zu 1 von 10 Behandelten) neurotoxische Effekte auftreten, die sich u.a. durch Verwirrtheit, Krämpfe, Zittern, Gangstörungen, Wortfindungsstörungen oder Halluzinationen äußern. Bei den meisten betroffenen Patienten endeten die Symptome spontan und waren vollständig rückläufig. Es sind weiterhin Fälle von CAR-T-Zell behandelten Patienten beschrieben worden, bei denen ein Hirnödem mit lebensbedrohlichen Konsequenzen auftrat. Diese neurologischen Nebenwirkungen sind bisher bei keinem der Studien-Teilnehmer mit einer Heidagen-lecleucel Behandlung beobachtet worden.
Tabelle zeigt zusammengefasst die Daten zu CRS und neurotoxischen Nebenwirkungen (ICANS) der in der HD-CAR-1 Studie behandelten Patienten. Es wurden bei keinem Patienten Neurotoxizitäten (ICANS) beobachtet. CRS gab es nur bei einem kleinen Teil der Patienten und es waren nur milde Symptome (CRS Grade I) in den meisten Fällen zu beobachten.
Tabelle 5: Zusammenfassung der in der HD-CAR-1-Studie beobachteten Nebenwirkungen CRS und ICANS.
Stratum |
CRS |
ICANS |
|||
Grad |
I |
II |
III |
IV |
0 – 4 |
ALL (n=17) |
5 |
2 |
0 |
0 |
0 |
alle NHL (n=20) |
4 |
3 |
1 |
0 |
0 |
davon CLL (n=8) |
2 |
2 |
1 |
0 |
0 |
Bei dem Auftreten eines sog. Tumorlysesyndrom (TLS) kann es zu Elektrolytentgleisungen, Stoffwechselstörungen und einer eingeschränkten Nierenfunktion kommen. TLS tritt meistens nach einer Chemotherapie vor der CAR-T-Zell-Gabe (s. unten „Konditionierungs-Chemotherapie“) bei hoher Tumorlast häufig (bis zu 1 von 10 Behandelten) auf. Ein TLS, dass isoliert durch CAR T-Zellen hervorgerufen wird, ist selten (1 von 1.000 Behandlungen). Um ein TLS zu verhindern, werden wir Ihnen intravenöse Flüssigkeit, Elektrolyte und Medikamente zur Senkung des Harnsäurespiegels verabreichen. Durch Überwachung der Elektrolyte und Nierenwerte mittels Blutentnahmen kann ein TLS meist sicher diagnostiziert werden. In seltenen Fällen kann ein TLS zu einer solchen Schädigung der Nieren führen, so dass eine Nierenersatztherapie mittels Hämodialyse notwendig wird.
Obwohl in einigen Fällen zunächst ein gutes Ansprechen auf die T-Zell-Therapie gegen CD19-positive bösartige Zellen beobachtet werden konnte, hat sich gezeigt, dass im Verlauf der Therapie ein Verlust des CD19-Markers auf der Oberfläche maligner Zellen auftreten kann. In diesem Falle ist die Therapie mit dem Prüfpräparat nicht mehr wirksam und es muss auf andere Therapien zurückgegriffen werden.
Im Vorfeld der CAR T-Zell-Behandlung finden zum einen die Leukapherese sowie die Konditionierung mit Chemotherapie statt. Die Risiken werden im Folgenden aufgeführt:
Bei der Leukapherese werden die Venen beider Armbeugen punktiert. Bei ungenügenden peripheren Venen kann die Anlage eines zentralen Venenkatheters notwendig werden. Unter örtlicher Betäubung wird eine große Vene des Körperstammes, in der Regel eine Halsvene, punktiert. Durch die Punktion von peripheren und zentralen Venen kann es selten (1 von 1.000 Behandlungen) zu Komplikationen kommen, wie Blutung und Infektion an der Einstichstelle, Thrombose oder Entzündungen der punktierten Vene. Es können sich gelegentlich (1 von 100 Behandelten) örtliche Blutergüsse bilden. In äußerst seltenen Fällen (1 von 10.000 Behandelten) kann es zu Verletzungen von Nervenästen und Arterien kommen, die zu chronischen Beeinträchtigungen führen können. Äußerst selten (1 von 10.000 Behandelten) können technische Komplikationen auftreten, wie z.B. eine Luftembolie (Ansaugen von Luft in die Vene) durch Ausfall von Sicherheitssystemen. Während der Leukapherese selbst kann es gelegentlich (1 von 100 Behandelten) zu Kreislaufschwäche kommen, die sich etwa wie bei der herkömmlichen Blutspende mit Schweißausbruch, Erbrechen, Übelkeit und Ohnmacht zeigen kann. Es können gelegentlich (1 von 100 Behandelten) vorübergehende Reaktionen durch Mittel mit Blutgerinnung hemmender Wirkung auftreten; und zwar Citrat-abhängige Reaktionen, wie das Gefühl von „Ameisenlaufen“ an den Fingerspitzen und Zehen, dem Mund sowie der Zunge und sehr selten (1 von 10.000 Behandelten) bei stärkerer Ausprägung Muskelverkrampfungen und Unregelmäßigkeiten des Herzschlages. In sehr seltenen Fällen (1 von 10.000 Behandelten) kann es infolge technischer Fehler, z.B. zu Blutverlusten oder Infektionen durch Reißen der Schlauch-/Beutelsysteme oder zum Zerfall von Blutzellen durch außergewöhnliche Druckveränderungen kommen. Zur Vermeidung der Nebenwirkungen werden alle erforderlichen Sicherheitsvorkehrungen getroffen.
Die Konditionierungschemotherapie im Vorfeld der CAR T-Zell-Gabe wird Fludarabin (3x30 mg/m2) und Cyclophosphamid (3x500mg/m2) umfassen. Bei der Behandlung mit Fludarabin sind die häufigsten Nebenwirkungen (1 von 10 Behandelten) die Hemmung des Knochenmarks, welches zu einer verminderten Bildung der Blutzellen führt, Immunsuppression (verminderte Funktionen des Immunsystems), Übelkeit, Erbrechen und Durchfall. Häufig (1 von 100 Behandelten) treten Sehstörungen auf. Gelegentlich (1 von 1.000 Behandelten) kommt es zu Veränderungen der Leberwerte und Verwirrtheit. In seltenen Fällen (1 von 10.000 Behandelten) treten Koma, Krampfanfälle oder Agitiertheit auf.
Bei der Behandlung mit Cyclophosphamid sind akute dosislimitierende und sehr häufige Nebenwirkungen (1 von 10 Behandelten) die Hemmung des Knochenmarks, sowie Immunsuppression, Harnwegsinfektionen und Haarausfall. Häufig (1 von 100 Behandelten) treten Übelkeit, Erbrechen, Durchfall, Gewichtsverlust und eine Störung der Spermatogenese auf. Bei den in hier angewandten Dosen sind diese Nebenwirkungen jedoch unwahrscheinlich.
Systemorganklasse (SOC) |
Häufigkeit |
Nebenwirkungen |
Infektionen | ||
Sehr häufig |
Infektionen mit nicht spezifizierten Erregern |
|
Erkrankungen des Blutes und des Lymphsystems | ||
Sehr häufig |
Leukopenie# |
|
Erkrankungen des Immunsystems | ||
Sehr häufig |
Zytokin-Freisetzungssyndrom## |
|
Häufig |
Allergie |
|
Stoffwechsel- und Ernährungsstörungen | ||
Häufig |
Hypophosphatämie |
|
Psychiatrische Erkrankungen | ||
Häufig |
Delirium |
|
Erkrankungen des Nervensystems | ||
Häufig |
Kopfschmerzen |
|
Herzerkrankungen | ||
Häufig |
Tachykardie |
|
Gefäßerkrankungen | ||
Sehr häufig |
Hypotonie |
|
Häufig |
Thrombose |
|
Erkrankungen der Atemwege, des Brustraums und Mediastinums | ||
Sehr häufig |
Husten |
|
Häufig |
Respiratorische Insuffizienz |
|
Erkrankungen des Gastrointestinaltrakts | ||
Sehr häufig |
Übelkeit |
|
Häufig |
Mundtrockenheit |
|
Erkrankungen der Haut und des Unterhautgewebes | ||
Sehr häufig |
Ausschlag |
|
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen | ||
Sehr häufig |
Schmerzen des Muskel- und Skelettsystems |
|
Erkrankungen der Nieren und Harnwege | ||
Sehr häufig |
Niereninsuffizienz |
|
Häufig |
Verminderte Urinausscheidung |
|
Allgemeine Erkrankungen | ||
Sehr häufig |
Ödem |
|
Häufig |
Reaktion im Zusammenhang mit einer Infusion |
|
Augenerkrankungen | ||
Häufig |
Sehstörung |
|
Untersuchungen | ||
Sehr häufig |
Alanin-Aminotransferase erhöht# |
|
Häufig |
Bilirubin erhöht# |
|
Stand: 28.02.2025 | ||
Tabelle 6: Zusammenfassung der möglichen Nebenwirkungen und der Häufigkeit des Auftretens.
Die Häufigkeiten sind wie folgt definiert: sehr häufig (≥ 1/10); häufig (≥ 1/100, < 1/10). Innerhalb der einzelnen Häufigkeitsgruppen werden die Nebenwirkungen nach abnehmendem Schweregrad angegeben.
In der Tabelle sind nur Zytopenien enthalten, die (i) zu neuen oder sich verschlechternden klinischen Folgeerscheinungen führten, oder (ii) eine Therapie erforderten oder (iii) eine Anpassung der aktuellen Therapie erforderten.
# Die Häufigkeit basiert auf Laborparametern 3. oder höheren Grades.
## Siehe Abschnitt „Beschreibung ausgewählter Nebenwirkungen“.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung über
das nationale Meldesystem anzuzeigen:
Bundesinstitut für Impfstoffe und biomedizinische Arzneimittel
Paul-Ehrlich-Institut
Paul-Ehrlich-Str. 51 – 59
63225 Langen
Tel: +49 6103 77 0
Fax: +49 6103 77 1234
E-Mail: biovigilance@pei.de
Website: www.pei.de
Es liegen keine Daten bezüglich der Anzeichen einer Überdosierung mit HD-CAR-19 vor.
Pharmakotherapeutische Gruppe: Antineoplastische Mittel, sonstige antineoplastische
Mittel, ATC-Code: noch nicht vergeben.
Wirkmechanismus
HD-CAR-19, ein Arzneimittel zur Immuntherapie mit genetisch modifizierten autologen T-Zellen, bindet an CD19-exprimierende Krebszellen und normale B-Zellen. Nach der Bindung der Anti-CD19-CART-Zellen an die CD19-exprimierenden Zielzellen aktivieren die kostimulierenden Domänen CD28, 41bb und CD3-zeta nachgeschaltete Signalkaskaden, die bei den T-Zellen zu Aktivierung, Proliferation, Erlangung von Effektor-Funktionen und Sekretion von inflammatorischen Zytokinen und Chemokinen führen. Diese Abfolge von Ereignissen führt zur Apoptose und Nekrose der CD19-exprimierenden Zielzellen.
Pharmakodynamische Wirkungen
Nach der HD-CAR-19 -Transfusion wurde das pharmakodynamische Ansprechen evaluiert, indem der vorübergehende Anstieg von Zytokinen und anderen Molekülen im Blut über einen 3-monatigen Zeitraum gemessen wurde. Konzentrationen von Zytokinen wie IL-6 und CRP wurden analysiert.
Der maximale Anstieg wurde in den ersten 7-8 Tagen nach der Infusion beobachtet, und die Konzentrationen erreichten in der Regel innerhalb von 14 Tagen wieder den Ausgangswert. Analysen, die durchgeführt wurden, um Zusammenhänge zwischen Zytokinkonzentrationen und der Inzidenz von CRS festzustellen, zeigten, dass höhere Konzentrationen nach der Transfusion (Spitzenkonzentration und AUC nach 1 Monat) von mehreren und proinflammatorischen Molekülen in der Studie HD-CAR-1 mit einem CRS 1. oder 2. assoziiert waren. Aufgrund der on-target-, off-tumor-Wirkung der CD19-CAR-T-Zellen ist für einen gewissen Zeitraum nach der Behandlung eine B-Zell-Aplasie zu erwarten. Von 13 Patienten in HD-CAR-1 mit auswertbaren Proben zu Studienbeginn hatten 10/13 nachweisbare B-Zellen; die bei der Mehrheit der Patienten zu Studienbeginn beobachtete B-Zell-Aplasie wurde auf frühere Antikörper- und/oder Chemo-Therapien zurückgeführt. Nach der Behandlung mit CD19-CAR-T-Zellen verringerte sich der Anteil der Patienten mit nachweisbaren B-Zellen: In gesamten Studienverlauf von Monat 1 bis 3 hatten alle Patienten keine nachweisbaren B-Zellen mehr, ohne dass dies mit einer Infekt-Häufung einherging. Eine B-Zell-Aplasie wir ja von vielen Experten im Feld als Indiz für eine persistierende CAR-T-Zell-Population gewertet. Klinisch haben wir parallel zum Immunstatus auch die Konzentration an Immunglobulinen der Klasse G (IgG) bestimmt. Bei einem Serumwert von unter 4 g/l wurden dann Immunglobuline substituiert.
Klinische Wirksamkeit und Sicherheit
Im Rahmen der HD-CAR-1 Studie wurden bisher 44 Patienten untersucht. 41 wurden in die Studie aufgenommen. Drei Patienten waren nach dem Screening nicht für die Studie geeignet. Die Gründe für den Ausschluss aus der Studie waren eine Hepatitis-B-Reaktivität bzw. ein rasches Fortschreiten der Krankheit. Die Leukapherese wurde bei allen eingeschlossenen Patienten erfolgreich durchgeführt. Es wurden immer genügend Zellen isoliert, um die Produktion von CAR-T-Zellen zu starten. Die CAR-T-Zell-Produktion war bei allen 41 Patienten erfolgreich. Davon konnten 35 Produkte den Patienten verabreicht werden. Fünf Patienten erhielten keine CAR-T-Zell-Produkte: Drei von ihnen starben während des Produktionszeitraums aufgrund eines massiven Fortschreitens der Krankheit. Ein Patient wurde kurz vor der Verabreichung aufgrund des schnellen Fortschreitens der Grunderkrankung aus der Studie ausgeschlossen. Ein Patient entwickelte während des Herstellungszeitraums des CAR-T-Zell-Produkts überraschend einen Zustand der MRD-Negativität. Daher qualifizierte sich der Patient nicht mehr für die Studie. Von den 35 Patienten, die ihr Produkt erhielten, erreichten 31 das Ende der Studie (EOS) am Tag 90 nach der Verabreichung. Vier Patienten erreichten das EOS nicht. Drei Patienten starben vor dem 90. Tag aufgrund eines raschen Fortschreitens der Grunderkrankung und ein Patient aufgrund von septischem Organversagen.
Die HD-CAR-1-Studie umfasst zwei Patientengruppen für erwachsene Patienten. Diese sind die ALL-Kohorte (Stratum I) und die NHL-Kohorte (Stratum II). Zur NHL-Kohorte gehören verschiedene CD19-positive Erkrankungen wie CLL, FL, DLBCL oder MCL. In beiden Gruppen sind durch die Änderung sechs Dosisstufen vorgesehen. Insgesamt sind für beiden Patientengruppen drei Dosisstufen vorgesehen.
Fünfundzwanzig männliche und 16 weibliche Patienten wurden in die Studie aufgenommen. Das Durchschnittsalter betrug 54 Jahre (Spanne 20 bis 76 Jahre). In der NHL-Kohorte wurden acht CLL-Patienten und ein Patient mit BCL aus CLL behandelt.
Ohne Berücksichtigung der beiden Patienten, die mit DL 1 oder 2 behandelt wurden (P2-02 und P2-07), lag die ORR- und CR-Rate bei EOS bei den sechs Patienten mit CLL, die mit höheren DL behandelt wurden, bei 100%. Eine MRD-Clearance wurde bei 5 der 6 Responder erreicht (83 %). Da keiner dieser sechs Patienten an nicht-CLL-bedingten Ursachen starb und alle bereits am Tag +28 ein Ansprechen erreicht hatten, kann die Dauer des Ansprechens (DOR) als gleichwertig mit dem PFS angesehen werden. Das mediane PFS der 6 Patienten, die mit höherer DL behandelt wurden, betrug 12,1 Monate, und das mediane OS wurde mit einer 2-Jahres-Wahrscheinlichkeit von 80 % der Patienten ohne Ereignis nicht erreicht (Abbildung 3).
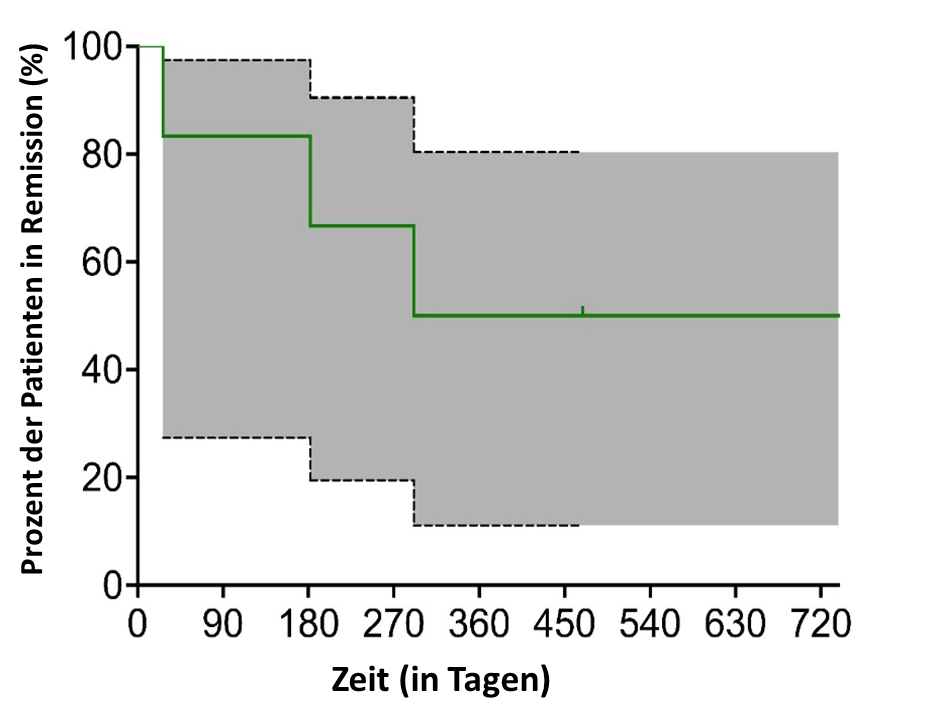
Abbildung 3: Dauer des Ansprechens (DOR) der 6 CLL-Patienten, die eine CR als bestes Ansprechen erreichten.
Die DOR (rote Linie) der 6 CLL-Patienten, die mit einer höheren Dosis behandelt wurden und auf HD-CAR-1 ansprachen, ist dargestellt.
Die Pharmakokinetik wird mittels quantitativer „Single-Copy-Gene PCR“ überwacht.
Im Rahmen der HD-CAR-1 Studie wurde bei allen behandelten Patienten im Rahmen der Follow-Up Besuche peripheres Blut abgenommen und die enthaltenen PBMCS asserviert. Hiervon wurde für die PCR DNA aus den Proben extrahiert und analysiert.
In Abbildung 4 ist die Analyse für die 6 CLL-Patienten dargestellt. Die PB-CART-Expansion wurde bei allen Patienten unmittelbar nach der CART-Verabreichung beobachtet. Der Höhepunkt der Kurve wird immer an den Tagen 10-14 erreicht.
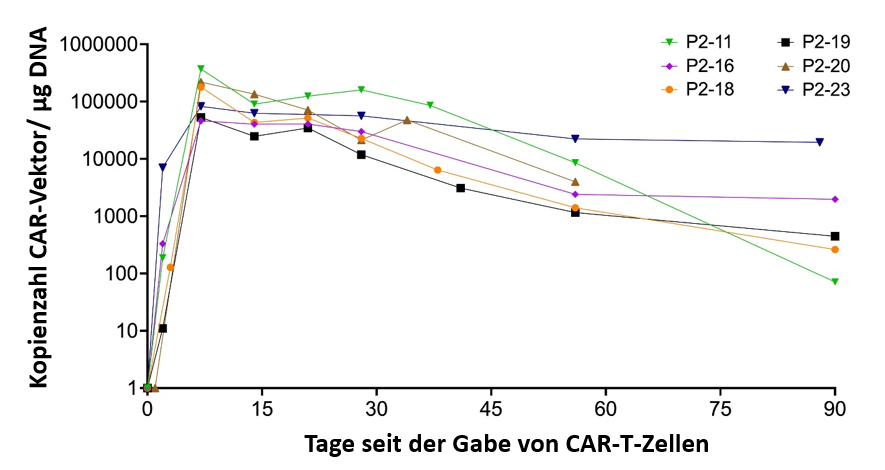
Abbildung 4: Expansion von HD-CAR-1 T Zellen in CLL-Patienten (n=6).
Expansion von CARTs im peripheren Blut (PB) einzelner HD-CAR-1-Patienten, die höhere Dosen erhalten haben, für die wir hier eine Ausnahmegenehmigung für das Krankenhaus beantragen (n=6), bewertet mittels quantitativer Einzelkopie-Gen-Duplex-PCR (SCG-DP-PCR). Die DNA wurde dafür aus mononukleären Zellen des peripheren Blutes der Patienten gewonnen, nach Verabreichung der CAR-T-Zellen und bis zum Ende der Studie (EOS) an Tag 90. (DL: DL3: 20×106 CARTs/m2, DL4: 5×107 CARTs/m2).
Zelluläre Kinetik
Nach der Infusion von HD-CAR-19 zeigten die Anti-CD19-CAR-T-Zellen eine initial schnelle Expansion, gefolgt von einem Rückgang auf einen kaum messbaren Bereich nach 90 Tagen bei den meisten Patienten. Die Spitzenkonzentrationen von Anti-CD19-CAR-T-Zellen traten innerhalb der ersten 7 bis 14 Tage nach dem Tag der CAR-T-Zell-Infusion auf. Höhere CART-Dosen (DL3, DL4) führten zu höheren und längeren Expansionswerten, während bei Patienten, die niedrigere CART-Dosen (DL1, DL2) erhalten hatten, kein Nachweis mehr möglich war.
HD-CAR-19 enthält genetisch modifizierte humane T-Zellen; daher existieren keine repräsentativen In-vitro-Assays, Ex-vivo-Modelle oder In-vivo-Modelle, die die toxikologischen Eigenschaften des humanen Produkts adäquat abbilden könnten. Folglich wurden keine traditionellen toxikologischen Studien, die bei einer Arzneimittel-Entwicklung eingesetzt werden, durchgeführt.
Mit HD-CAR-19 wurden keine Studien zur Karzinogenität oder Genotoxizität durchgeführt.
Es wurden keine Studien durchgeführt, um die Auswirkungen von HD-CAR-19 auf die Fertilität, Reproduktion und Entwicklung zu bewerten.
Die Patienten wurden nach der Behandlung mit CAR-T-Zellen 14 Tage lang stationär behandelt. Die Nachbeobachtung wurde bis 90 Tage nach der CAR-Verabreichung durchgeführt. Während der Studie wurden nur sehr wenige Nebenwirkungen beobachtet, sowohl kurz nach der Verabreichung als auch über den Zeitraum von 90 Tagen. Insgesamt wurde die Verabreichung von allen Patienten sehr gut vertragen. Bei 15 ausgewerteten ALL-Patienten wurden zweimal CRS Grad II beobachtet und dreimal ein CRS Grad 1. Bei allen Patienten traten keine ICANS und nur vereinzelte CRS-Ereignisse auf. In der NHL Kohorte wurde bei 20 ausgewerteten Patienten ein CRS Grad III, 2 CRS Grad II und viermal ein CRS Grad I beobachtet.
DMSO (Dimetylsulfoxid)
HSA (Humanalbumin)
PBS (Phosphate buffered saline)
Da keine Kompatibilitätsstudien durchgeführt wurden, darf dieses Arzneimittel nicht mit anderen
Arzneimitteln gemischt werden.
90 Tage in der Gasphase im Stickstoff (N2) bei unter -130°C.
Nach vollständigem Auftauen ist das Präparat für 2h bei gekühlter Lagerung (2-8°C) haltbar. Die Infusion soll zügig nach dem Auftauen erfolgen und das eine Infusionsdauer von 30min nicht überschreiten.
Lagerung nur in den dafür vorgesehenen Kryo-Kassetten in der Gasphase im Stickstoff (N2) bei unter -130°C. Das Präparat muss in gefrorenem Zustand bleiben, bis der Patient für die Behandlung bereit ist, um sicherzustellen, dass lebensfähige Zellen für die Gabe an den Patienten zur Verfügung stehen. Aufgetautes Arzneimittel darf nicht wieder eingefroren werden.
Aufbewahrungsbedingungen nach Auftauen des Arzneimittels, siehe Abschnitt 6.3.
Ethylenvinylacetat-Beutel für die Kryokonservierung mit versiegeltem Zuführschlauch und zwei verfügbaren Spikeports. Inhalt ist die Zellsuspension (max. 70ml in einem Beutel). Diese wird vor der Gabe aufgetaut. Bei Dosen <10ml Röhrchen, die aufgetaut und in einer Spritze aufgezogen werden.
Ein Beutel wird für die Kryolagerung einzeln in einer Kassette verpackt.
Die Lösung ist vor Gebrauch visuell zu prüfen und nur dann zu verwenden, wenn sie klar und ohne Aggregate ist.
Der leere Beutel, sowie nicht verwendete Zellen müssen vor der Entsorgung inaktiviert werden. Vorzugsweise durch Hitzeinaktivierung mittels Autoklavieren.
Vorsichtsmaßnahmen vor/bei der Handhabung bzw. vor/während der Anwendung des Arzneimittels
HD-CAR-19 im Beutel muss innerhalb der Einrichtung in geschlossenen, bruchsicheren und austrittsicheren Behältnissen transportiert werden.
Dieses Arzneimittel enthält menschliche Zellen Angehörige der Gesundheitsberufe müssen daher bei der Handhabung von HD-CAR-19 angemessene Vorsichtsmaßnahmen treffen (Schutzhandschuhe, Schutzkleidung und Augenschutz (bei Einlagerung bzw. Entnahme aus der LN2 Gasphase tragen), um eine mögliche Übertragung von Infektionskrankheiten zu vermeiden.
Vorbereitung vor der Anwendung
Verifizieren Sie, dass die Identität des Patienten mit den Patienten-Identifizierungsmerkmalen auf der HD-CAR-19 -Kassette übereinstimmt.
Der HD-CAR-19 -Beutel darf nicht aus der Metallkassette genommen werden, wenn die Informationen auf dem patientenspezifischen Etikett nicht mit dem vorgesehenen Patienten übereinstimmen.
Nehmen Sie den HD-CAR-19 -Beutel, nachdem die Patienten-Idenitifizierungsmerkmale bestätigt wurde, aus der Metallkassette.
Stellen Sie sicher, dass die Patienteninformationen auf dem Etikett der Metallkassette mit denen auf dem Etikett des Beutels übereinstimmen.
Untersuchen Sie den Beutel mit dem Arzneimittel vor dem Auftauen auf Unversehrtheit. Wenn der Beutel beschädigt ist, halten Sie die lokal geltenden Bestimmungen zum Umgang mit Abfallmaterialien humanen Ursprungs ein (oder nehmen Sie direkt Kontakt mit der GMP Core Facility UKHD auf).
Auftauen
Verpacken Sie den Infusionsbeutel in einen zweiten Beutel.
Tauen Sie das HD-CAR-19 -Zellprodukt bei ca. 37 °C unter Verwendung eines Plasmathermgerätes oder einer Methode zum trockenen Auftauen auf, bis im Infusionsbeutel kein Eis mehr sichtbar ist. Mischen Sie den Beutelinhalt vorsichtig durch, um Klumpen von Zellmaterial aufzulösen. Wenn weiterhin Zellklumpen sichtbar sind, mischen Sie den Beutelinhalt weiter vorsichtig durch. Kleine Klumpen von Zellmaterial sollten sich durch vorsichtiges manuelles Durchmischen auflösen lassen. HD-CAR-19 darf vor der Infusion nicht gewaschen, zentrifugiert und/oder in einem neuen Medium resuspendiert werden. Das Auftauen dauert ca. 3 bis 5 Minuten.
Nach dem Auftauen ist HD-CAR-19 bis zu 2 Stunden bei Raumtemperatur (2 °C–8 °C) stabil.
Anwendung
Es darf kein Leukozyten-depletierender Filter verwendet werden.
Vor der Infusion und während der Nachbeobachtung müssen Tocilizumab und eine Notfallausrüstung zur Verfügung stehen. In dem Ausnahmefall, in dem Tocilizumab aufgrund eines Lieferengpasses, der im Lieferengpasskatalog der Europäischen Arzneimittel-Agentur aufgeführt ist, nicht verfügbar ist, müssen vor der Infusion geeignete alternative Maßnahmen anstelle von Tocilizumab zur Behandlung eines CRS zur Verfügung stehen.
Für die Gabe von HD-CAR-19 wird ein zentralvenöser Zugang empfohlen.
Nur zur autologen Anwendung.
Verifizieren Sie die Patienten-Identifizierungsmerkmale erneut, um sie mit den Patienten-Identifizierungsmerkmalen auf dem HD-CAR-19 -Beutel abzugleichen.
Spülen Sie die Schläuche vor der Infusion mit 0,9 % Natriumchloridlösung (0,154 mmol Natrium pro ml).
Infundieren Sie den gesamten Inhalt des HD-CAR-19 -Beutels innerhalb von 30 Minuten, entweder mittels Schwerkraft oder über eine peristaltische Pumpe.
Schütteln Sie den Beutel sanft während der HD-CAR-19 -Infusion, um ein Verklumpen der Zellen zu vermeiden.
Spülen Sie die Schläuche, nachdem der gesamte Inhalt des Beutels infundiert wurde, mit derselben Infusionsrate mit 0,9 % Natriumchloridlösung (0,154 mmol Natrium pro ml) durch, um sicherzustellen, dass die gesamte HD-CAR-19 -Dosis verabreicht wurde.
Im Falle einer versehentlichen Exposition zu ergreifende Maßnahmen
Im Falle einer versehentlichen Exposition sind die vor Ort geltenden Richtlinien für den Umgang mit Material menschlicher Herkunft zu befolgen. Arbeitsflächen und Materialien, die möglicherweise mit HD-CAR-19 in Kontakt gekommen sind, müssen mit einem geeigneten Desinfektionsmittel dekontaminiert werden.
Vorsichtsmaßnahmen für die Beseitigung des Arzneimittels
Nicht verwendetes Arzneimittel und sämtliches Material, das mit HD-CAR-19 in Kontakt gekommen ist (feste und flüssige Abfälle), sind gemäß den vor Ort geltenden Richtlinien für den Umgang mit Material menschlicher Herkunft als potenziell infektiöser Abfall zu behandeln und zu entsorgen.
NACH §4b AMG
Universitätsklinikum Heidelberg
Medizinische Klinik V – GMP Core Facility
Im Neuenheimer Feld 410
69120 Heidelberg
PEI.A.12181.01.1
/VERLÄNGERUNG DER ZULASSUNG
Datum der Erteilung der Zulassung: 18.09.2025
Januar 2026
Ausführliche Informationen sind beim Hersteller erhältlich.
Verschreibungspflichtig.
Die Anwendung von HD-CAR-19 (Heidagen-lecleucel) darf nur gerichtet erfolgen und muss in der Bundesrepublik Deutschland vorgenommen werden (Arzneimittel nur zur Anwendung gemäߧ 4b AMG).
Univ.-Prof. Dr. med. Michael Schmitt, MHBA
Siebeneicher-Professor für Zelluläre Immuntherapie
Leiter der GMP Core Facility
Sachkundige Person gem. §14 AMG
Medizinische Klinik (Krehl-Klinik) | Zentrum für Innere Medizin
Klinik für Hämatologie, Onkologie und Rheumatologie | Innere Medizin V
Universitätsklinikum Heidelberg | Im Neuenheimer Feld 410 | 69120 Heidelberg
Tel.: +49 6221 56-6614 | Fax: +49 6221 56-5740 | E-Mail: michael.schmitt@med.uni-heidelberg.de