NUCEIVA 50 Einheiten Pulver zur Herstellung einer Injektionslösung
NUCEIVA 100 Einheiten Pulver zur Herstellung einer Injektionslösung
Jede Durchstechflasche enthält 50 Einheiten Botulinum-Toxin Typ A zur Injektion (Ph.Eur.), hergestellt von Clostridium botulinum.
Jede Durchstechflasche enthält 100 Einheiten Botulinum-Toxin Typ A zur Injektion (Ph.Eur.), hergestellt von Clostridium botulinum.
Nach der Rekonstitution enthält 0,1 ml der Lösung 4 Einheiten.
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
Pulver zur Herstellung einer Injektionslösung.
Weißes Pulver.
NUCEIVA wird angewendet bei Erwachsenen im Alter unter 65 Jahren zur vorübergehenden Verbesserung des Aussehens von mittelstarken bis starken vertikalen Falten zwischen den Augenbrauen, sichtbar bei maximalem Stirnrunzeln (Glabellafalten), wenn das Ausmaß dieser Falten eine erhebliche psychologische Belastung darstellt.
NUCEIVA darf nur von Ärzten mit geeigneter Qualifikation und der erforderlichen Fachkenntnis in der Behandlung von Glabellafalten und unter Verwendung der erforderlichen Ausstattung angewendet werden.
Dosierung
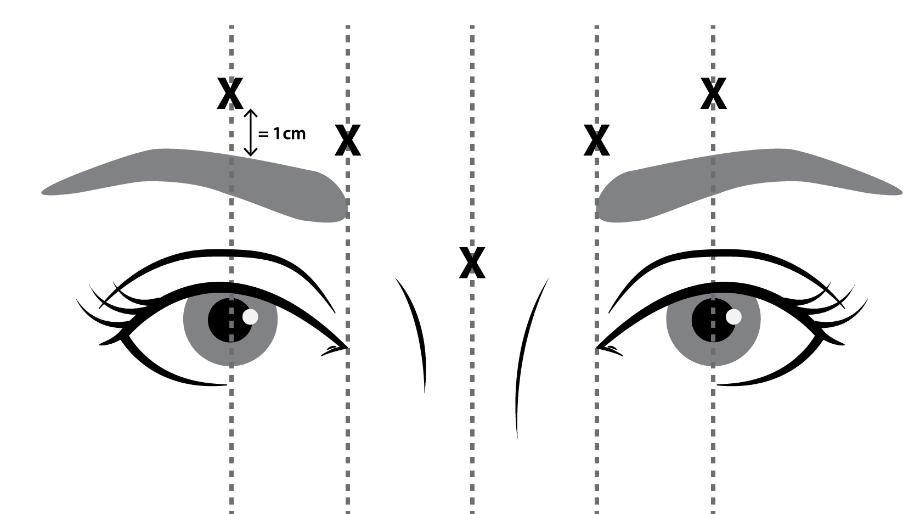
Das empfohlene Injektionsvolumen pro Muskelstelle beträgt 4 Einheiten/0,1 ml. Fünf Injektionsstellen (siehe Abbildung 1): 2 Injektionen in jeden M. corrugator (untere Medialseite und obere Medialseite) und 1 Injektion in den M. procerus, dies entspricht einer Gesamtdosis von 20 Einheiten.
Die Botulinumtoxin-Einheiten verschiedener Arzneimittel sind nicht austauschbar. Die empfohlenen Dosierungen unterscheiden sich von denen anderer Botulinumtoxin-Arzneimittel.
Wenn während der Erstbehandlung keine Nebenwirkungen auftreten, kann eine weitere Behandlung durchgeführt werden, wobei zwischen der Erst- und der Wiederholungsbehandlung ein Mindestabstand von 3 Monaten eingehalten werden muss.
Wenn einen Monat nach der ersten Behandlung kein therapeutischer Effekt (keine sichtbare Verbesserung der Glabellafalten bei maximalem Stirnrunzeln) eingetreten ist, können die folgenden Vorgehensweisen in Betracht gezogen werden:
Analyse der Gründe für das Therapieversagen, z. B. falsche Injektionstechnik, Injektion in die falschen Muskeln sowie mögliche Bildung Botulinumtoxin-neutralisierender Antikörper.
Überprüfung, ob die Behandlung mit Botulinum-Toxin Typ A die angemessene Therapieform ist.
Die Wirksamkeit und Sicherheit von Wiederholungsinjektionen über den Zeitraum von 12 Monaten hinaus wurde nicht untersucht.
Ältere Patienten
Es liegen begrenzte klinische Daten zur Anwendung dieses Arzneimittels bei Patienten über 65 Jahren vor (siehe Abschnitt 5.1). Dieses Arzneimittel wird nicht zur Behandlung von Patienten über 65 Jahren empfohlen.
Kinder und Jugendliche
Es gibt keinen relevanten Nutzen dieses Arzneimittels bei Kindern und Jugendlichen.
Art der Anwendung
Intramuskuläre Anwendung.
NUCEIVA darf nach der Rekonstitution nur für die Behandlung eines einzigen Patienten während einer einzigen Sitzung angewendet werden.
Vorsichtsmaßnahmen vor/bei der Handhabung bzw. vor/während der Anwendung des Arzneimittels
Hinweise zur Anwendung, zu Vorsichtsmaßnahmen vor/bei der Handhabung oder vor/während der Anwendung des Arzneimittels sowie zur Handhabung und Beseitigung der Durchstechflaschen, siehe Abschnitt 6.6.
Es ist darauf zu achten, dass dieses Arzneimittel nicht in ein Blutgefäß injiziert wird, wenn die Injektion in die vertikalen Falten zwischen den Augenbrauen, die bei maximalem Stirnrunzeln sichtbar sind (auch Glabellafalten genannt), erfolgt (siehe Abschnitt 4.4).
Die physische Manipulation (z. B. Reiben) der Injektionsstelle in der Phase unmittelbar nach der Anwendung sollte vermieden werden.
Anweisungen für die Anwendung bei Glabellafalten, die bei maximalem Stirnrunzeln sichtbar sind
Rekonstituiertes NUCEIVA (50 Einheiten/1,25 ml; 100 Einheiten/2,5 ml) wird mit einer sterilen 30-Gauge-Kanüle injiziert.
Um Komplikationen durch das Auftreten einer Ptosis des Augenlids zu reduzieren, sollten die folgenden Schritte durchgeführt werden:
Zwei Injektionen sollten in jeden M. corrugator (untere und obere Medialseite) und eine Injektion in den M. procerus verabreicht werden, dies entspricht einer Gesamtdosis von 20 Einheiten.
Injektionen in der Nähe des M. levator palpebrae superioris müssen vermieden werden, insbesondere bei Patienten mit größeren Brauendepressorkomplexen.
Injektionen in den M. corrugator lateralis sollten mindestens 1 cm oberhalb des oberen knöchernen Orbitarandes erfolgen.
Abbildung 1: Injektionsstellen
Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
Generalisierte Störungen der Muskelaktivität (z. B. Myasthenia gravis oder Lambert-Eaton-Syndrom)
Infektion oder Entzündung an der vorgesehenen Injektionsstelle.
Allgemeines
Bevor der Arzt dieses Arzneimittel anwendet, muss er mit der Anatomie und den anatomischen Orientierungspunkten des Musculus procerus und des Musculus corrugator supercilii sowie den umgebenden Gefäß- und Nervenstrukturen im Glabellabereich vertraut sein. Injektionen in verletzliche anatomische Strukturen wie Nerven und Blutgefäße müssen vermieden werden.
Lokaler Schmerz, Entzündung, Parästhesie, Hypoästhesie, Empfindlichkeit, Schwellung/Ödem, Erythem, lokalisierte Infektion, Blutungen und/oder Blutergüsse wurden mit der Injektion in Verbindung gebracht. Durch den Einstich der Nadel bedingte Schmerzen und/oder Angstzustände haben zu vasovagalen Reaktionen geführt, einschließlich vorübergehender symptomatischer Hypotonie und Synkope.
Vorsicht ist geboten, wenn der Zielmuskel eine ausgeprägte Schwäche oder Atrophie aufweist.
Es ist darauf zu achten, dass dieses Arzneimittel nicht in ein Blutgefäß injiziert wird, wenn die Injektion in die Glabellafalten, die bei maximalem Stirnrunzeln sichtbar sind, erfolgt (siehe Abschnitt 4.2).
Es besteht das Risiko einer Ptosis des Augenlids nach der Behandlung (siehe Abschnitt 4.2).
Vorsicht ist geboten, wenn bereits bei früheren Botulinumtoxin-Injektionen Komplikationen aufgetreten sind.
Blutgerinnungsstörungen
Bei der Anwendung dieses Arzneimittels bei Patienten mit Blutgerinnungsstörungen ist Vorsicht geboten, da die Injektion zu Blutergüssen führen kann.
Lokale und von der Injektionsstelle entfernte Ausbreitung der Toxinwirkung
Nebenwirkungen, die möglicherweise mit der Ausbreitung des Toxins an vom Verabreichungsort entfernte Stellen in Zusammenhang stehen, wurden für Botulinumtoxin sehr selten berichtet (siehe Abschnitt 4.8). Schluck- und Atemstörungen sind schwerwiegend und können zum Tode führen. Die Injektion dieses Arzneimittels wird bei Patienten mit einer Vorgeschichte von Aspiration oder Dysphagie nicht empfohlen.
Patienten oder pflegende Personen sind darauf hinzuweisen, unverzüglich einen Arzt zu verständigen, wenn Schluck-, Sprech- oder Atemstörungen auftreten.
Bereits bestehende neuromuskuläre Erkrankungen
Patienten mit nicht erkannten neuromuskulären Erkrankungen können nach der Injektion von Botulinum-Toxin Typ A in der normalen Dosierung einem erhöhten Risiko für klinisch signifikante systemische Wirkungen ausgesetzt sein, darunter schwere Dysphagie und Beeinträchtigung der Atmung. In einigen dieser Fälle hielt die Dysphagie mehrere Monate an und erforderte das Legen einer Ernährungssonde (siehe Abschnitt 4.3).
Vorsicht ist außerdem geboten, wenn Botulinum-Toxin Typ A zur Behandlung von Patienten mit amyotropher Lateralsklerose oder mit peripheren neuromuskulären Erkrankungen angewendet wird.
Überempfindlichkeitsreaktionen
Sehr selten wurden nach der Injektion von Botulinumtoxin anaphylaktische Reaktionen beobachtet. Deshalb sollten Epinephrin (Adrenalin) und andere antianaphylaktische Maßnahmen verfügbar sein.
Antikörperbildung
Während der Behandlung mit Botulinumtoxin kann es zur Bildung von Antikörpern gegen Botulinum-Toxin Typ A kommen. Einige der gebildeten Antikörper sind neutralisierend, was zu einem Therapieversagen von Botulinum-Toxin Typ A führen kann.
Es wurden keine Studien zur Erfassung von Wechselwirkungen durchgeführt.
Theoretisch kann die Wirkung von Botulinumtoxin durch Aminoglykosidantibiotika, Spectinomycin oder andere Arzneimittel, die auf die neuromuskuläre Reizleitung wirken (z. B. neuromuskulär blockierende Arzneimittel), verstärkt werden.
Die Wirkung einer gleichzeitigen Anwendung verschiedener Botulinumneurotoxin-Serotypen bzw. deren Anwendung innerhalb weniger Monate ist nicht bekannt. Eine ausgeprägte neuromuskuläre Schwäche kann sich noch verstärken, wenn ein anderes Botulinumtoxin angewendet wird, bevor die Wirkungen eines zuvor injizierten Botulinumtoxins abgeklungen sind.
Schwangerschaft
Es liegen keine hinreichenden Daten zur Anwendung von Botulinum-Toxin Typ A bei Schwangeren vor. Es liegen keine ausreichenden tierexperimentellen Studien in Bezug auf eine Reproduktionstoxizität vor (siehe Abschnitt 5.3). Die Anwendung dieses Arzneimittels während der Schwangerschaft und bei Frauen im gebärfähigen Alter, die nicht verhüten, wird nicht empfohlen.
Stillzeit
Es ist nicht bekannt, ob Botulinum-Toxin Typ A in die Muttermilch übergeht. Dieses Arzneimittel soll während der Stillzeit nicht angewendet werden.
Fertilität
Die Auswirkung dieses Arzneimittels auf die menschliche Fertilität ist nicht bekannt. Es hat sich jedoch gezeigt, dass ein anderes Botulinum-Toxin Typ A die Fertilität von männlichen und weiblichen Tieren beeinträchtigt.
Dieses Arzneimittel hat einen geringen oder mäßigen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen. Es besteht ein potenzielles Risiko von Asthenie, Muskelschwäche, Schwindel und Sehstörungen, was zu einer Beeinträchtigung der Fähigkeit, Fahrzeuge zu führen und Maschinen zu bedienen, führen kann.
Zusammenfassung des Sicherheitsprofils
Zu den schwerwiegenden Nebenwirkungen, die nach der Behandlung mit diesem Arzneimittel auftreten können, gehören Augenlidptosis, eine Immunreaktion, die Ausbreitung von Toxin an vom Verabreichungsort entfernte Stellen, die Entwicklung oder Verschlimmerung einer neuromuskulären Störung und Überempfindlichkeitsreaktionen. Die am häufigsten berichteten Nebenwirkungen während der Behandlung sind Kopfschmerzen, die bei 9 % der Patienten auftreten, gefolgt von Augenlidptosis, die bei 1 % der Patienten auftritt.
Tabellarische Auflistung der Nebenwirkungen
Tabelle 1 Die Nebenwirkungen im Zusammenhang mit NUCEIVA werden nach Systemorganklasse und Häufigkeit klassifiziert. Die Häufigkeiten sind wie folgt definiert: Sehr häufig (≥ 1/10), häufig (≥ 1/100, < 1/10), gelegentlich (≥ 1/1.000, < 1/100), selten (≥ 1/10.000, < 1/1.000) und sehr selten (< 1/10.000).
Systemorganklasse |
Bevorzugte Bezeichnung |
Häufigkeit |
Infektionen und parasitäre Erkrankungen |
Infektionen der oberen Atemwege |
Selten |
Psychiatrische Erkrankungen |
Depression |
Selten |
Erkrankungen des Nervensystems |
Kopfschmerzen |
Häufig |
Schwindelgefühl, Migräne, Störung des Muskeltonus, Sprechstörung |
Gelegentlich |
|
Dysästhesie, Kopfbeschwerden, Hypoästhesie, Parästhesie, sensorische Störung |
Selten |
|
Augenerkrankungen |
Augenlidptosis |
Häufig |
Asthenopenie, Blepharospasmus, Brauenptosis, Augenlidödem, Schwellung des Auges, verschwommenes Sehen |
Gelegentlich |
|
Doppeltsehen, trockenes Auge, sensorische Störung des Augenlids |
Selten |
|
Erkrankungen des Ohrs und des Labyrinths |
Vertigo |
Selten |
Gefäßerkrankungen |
Gesichtsrötung |
Selten |
Erkrankungen der Atemwege, des Brustraums und Mediastinums |
Epistaxis |
Selten |
Erkrankungen des Gastrointestinaltrakts |
Diarrhö |
Selten |
Erkrankungen der Haut und des Unterhautzellgewebes |
Pruritus |
Gelegentlich |
Hautzyste, Erythem, Lichtempfindlichkeitsreaktion, Raumforderung der Haut, Hautspannen |
Selten |
|
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen |
Muskelzucken, Schmerzen des Muskel- und Skelettsystems, Myalgie, Nackenschmerzen |
Selten |
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort |
Bluterguss an der Applikationsstelle, grippeähnliche Erkrankung, Bluterguss an der Injektionsstelle, Schmerzen an der Injektionsstelle, Schwellung an der Injektionsstelle |
Häufig |
Injektionsstelle: Erythem, Parästhesie an der Injektionsstelle, Pruritus an der Injektionsstelle, Schmerz, Druckschmerz |
Selten |
|
Untersuchungen |
Augendruckmessung |
Selten |
Verletzung, Vergiftung und durch Eingriffe bedingte Komplikationen |
Kontusion |
Gelegentlich |
Schwellung nach einem Eingriff, Kopfschmerz im Zusammenhang mit dem Verfahren |
Selten |
Hinweis: Nur bei einem der 1 659 mit NUCEIVA behandelten Personen traten seltene Ereignisse auf. Gelegentliche Ereignisse traten bei 2 bis 7 Personen auf.
Beschreibung ausgewählter Nebenwirkungen
Anwendungsbezogene Nebenwirkungen
Anwendungsbezogene Nebenwirkungen, die nach der Anwendung dieses Arzneimittels berichtet wurden, sind einzeln betrachtet gelegentliche Ereignisse und häufige Ereignisse, wenn sie addiert werden. Dazu gehören Bluterguss an der Applikationsstelle und an der Injektionsstelle, Schmerz an der Injektionsstelle und Schwellung an der Injektionsstelle. Selten auftretende Ereignisse an der Injektionsstelle, von denen berichtet wurde, umfassen Erythem, Parästhesie, Pruritus, Schmerz und Druckschmerz.
Nebenwirkungen der Substanzklasse Botulinum-Toxin Typ A
Muskelatrophie
Muskelatrophie wird nach wiederholter Behandlung mit Botulinum als Folge der schlaffen Lähmung der behandelten Muskeln erwartet.
Ausbreitung des Toxins
Nebenwirkungen, die möglicherweise mit der Ausbreitung des Toxins an vom Anwendungsort entfernte Stellen in Zusammenhang stehen, wurden für Botulinumtoxin sehr selten berichtet (z. B. Muskelschwäche, Atembeschwerden, Dysphagie oder Obstipation) (siehe Abschnitt 4.4).
Überempfindlichkeitsreaktionen
Nach der Injektion von Botulinumtoxin kann sehr selten eine anaphylaktische Reaktion auftreten. Deshalb sollten Epinephrin (Adrenalin) und andere antianaphylaktische Maßnahmen verfügbar sein.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung über die nachstehend aufgeführten nationalen Meldesystemen anzuzeigen:
Deutschland
Bundesinstitut für Arzneimittel und Medizinprodukte
Abt. Pharmakovigilanz
Kurt-Georg-Kiesinger-Allee 3
D-53175 Bonn
Website: http://www.bfarm.de
Österreich
Bundesamt für Sicherheit im Gesundheitswesen
Traisengasse 5
1200 WIEN
ÖSTERREICH
Fax: +43 (0) 50 555 36207
Website: http://www.basg.gv.at/
Symptome einer Überdosierung
Symptome einer Überdosierung treten möglicherweise nicht unmittelbar nach einer Injektion auf. Nach versehentlicher Injektion oder Einnahme muss der Patient mehrere Tage medizinisch auf Anzeichen und Symptome einer allgemeinen Muskelschwäche oder Muskellähmung überwacht werden. Eine Einweisung in ein Krankenhaus sollte bei Patienten mit Symptomen einer Vergiftung mit Botulinum-Toxin Typ A (allgemeine Schwäche, Ptosis, Diplopie, Schluck- und Sprechstörungen oder Lähmung der Atemmuskulatur) erwogen werden.
Eine zu häufige Anwendung oder eine zu hohe Dosierung können das Risiko der Antikörperbildung erhöhen. Die Bildung von Antikörpern kann zu Therapieversagen führen.
Die Überdosierung dieses Arzneimittels ist abhängig von der Dosis, der Injektionsstelle und den Eigenschaften der tiefer liegenden Gewebeschichten. Es wurden bisher keine Fälle von systemischer Toxizität infolge einer versehentlichen Injektion von Botulinum-Toxin Typ A beobachtet. Zu hohe Dosen können zu lokalen oder von der Injektionsstelle entfernten, generalisierten und tiefen neuromuskulären Lähmungen führen. Es wurden bisher keine Fälle einer Einnahme von Botulinum-Toxin Typ A berichtet.
Maßnahmen bei Überdosierung
Im Falle einer Überdosierung muss der Patient medizinisch auf Symptome übermäßiger Muskelschwäche oder Muskellähmung überwacht werden. Bei Bedarf sollte eine symptomatische Behandlung eingeleitet werden.
Pharmakotherapeutische Gruppe: Muskelrelaxanzien, andere Muskelrelaxanzien, peripher wirkende Mittel,
ATC-Code: M03AX01.
Wirkmechanismus
Botulinum-Toxin Typ A blockiert durch Spaltung von SNAP-25 die periphere Acetylcholinfreisetzung an den präsynaptischen, cholinergen Nervenendigungen. SNAP-25 ist ein Protein, das für die erfolgreiche Bindung und Freisetzung von Acetylcholin aus den Vesikeln, die sich in den Nervenendigungen befinden, wesentlich ist. Daher kommt es zu einer Denervierung des Muskels und zu einer schlaffen Lähmung.
Nach der Injektion erfolgt initial eine schnelle, hochaffine Bindung des Toxins an spezifische Rezeptoren der Zelloberfläche. Daraufhin wird das Toxin mittels rezeptorvermittelter Endozytose durch die Plasmamembran transportiert. Schließlich wird das Toxin in das Zytosol abgegeben, wobei es zu einer progressiven Hemmung der Acetylcholinfreisetzung kommt. Klinische Anzeichen treten innerhalb von 2 bis 3 Tagen auf, wobei die maximale Wirkung 4 Wochen nach der Injektion zu beobachten ist.
Die Wiederherstellung der Impulsübertragung nach intramuskulärer Injektion erfolgt normalerweise innerhalb von 12 Wochen nach der Injektion, wenn sich neue Nervenendigungen bilden und mit den motorischen Endplatten verbinden.
Klinische Wirksamkeit und Sicherheit
Glabellafalten
540 Patienten mit mittelstarken bis starken, bei maximalem Stirnrunzeln sichtbaren Glabellafalten, für die ihre Glabellafalten eine erhebliche psychologische Belastung darstellten (in Bezug auf Stimmung, Angstzustände oder depressive Symptome), wurden in die europäisch-kanadische klinische Studie aufgenommen.
Injektionen mit NUCEIVA reduzierten die Ausprägung der bei maximalem Stirnrunzeln sichtbaren Glabellafalten signifikant um mindestens 1 Punkt über einen Zeitraum von bis zu 139 Tagen. Dabei wurde die Ausprägung der Glabellafalten bei maximalem Stirnrunzeln vom Prüfarzt bewertet.
Tabelle 2 — Primärer Wirksamkeitsendpunkt — Glabellafalten-Skalenscore von 0 (keine Falten) oder 1 (leichte Falten) an Tag 30, basierend auf der Beurteilung des Prüfarztes bei maximaler Kontraktion, PP-Population
Responder für den primären Wirksamkeitsendpunkt |
Placebo |
BOTOX |
NUCEIVA |
Absolute Differenz |
||
BOTOX vs. Placebo |
NUCEIVA vs. |
NUCEIVA vs. |
||||
Anzahl |
2/48 |
202/244 |
205/235 |
|||
Prozentsatz |
4,2 % |
82,8 % |
87,2 % |
78,6 % |
83,1 % |
4,4 % |
(% KI) |
(0,0; 9,8) |
(78,1; 87,5) |
(83,0; 91,5) |
(66,5; 85,5) |
(70,3; 89,4) |
(-1,9; 10,8) |
p-Wert |
< 0,001 |
< 0,001 |
||||
Glabellafalten-Skala (Glabellar Line Scale — GLS); 0 = keine Falten, 1 = leichte Falten, 2 = mittelstarke Falten, 3 = starke Falten
Zwei Tage nach der Injektion wurden 12,2 % (6/49) der mit Placebo behandelten Patienten, 57,0 % (139/244) der mit Botox und 54,2 % (130/240) der mit NUCEIVA behandelten Patienten von den Prüfärzten als Responder eingestuft (keine oder leicht ausgeprägte Falten bei maximalem Stirnrunzeln).
Tabelle 3 — Explorativer Wirksamkeitsendpunkt — Glabellafalten-Skalenscore von 0 (keine Falten) oder 1 (leichte Falten) an Tag 30, basierend auf der Beurteilung der mit NUCEIVA behandelten Studienteilnehmer durch den Prüfarzt bei maximaler Kontraktion, basierend auf dem GLS-Score bei Studienbeginn bei maximaler Kontraktion, ITT-Population
GLS-Score bei Studienbeginn bei maximaler Kontraktion |
NUCEIVA (N = 245) |
|
GLS = 0 an Tag 30 bei maximaler Kontraktion |
GLS = 1 an Tag 30 bei maximaler Kontraktion |
|
2 (mittelstarke Falten) |
||
Anzahl |
35/62 |
25/62 |
Prozentsatz |
56,5 % |
40,3 % |
3 (starke Falten) |
||
Anzahl |
41/179 |
108/179 |
Prozentsatz |
22,9 % |
60,3 % |
Glabellafalten-Skala (GLS); 0 = keine Falten, 1 = leichte Falten, 2 = mittelstarke Falten, 3 = starke Falten. Die Nenner basieren auf der Anzahl der Studienteilnehmer mit dem angegebenen Schweregrad bei Studienbeginn bei maximaler Kontraktion, die sowohl GSL-Scores bei Studienbeginn als auch an Tag 30 bei maximaler Kontraktion, beurteilt durch den Prüfarzt, aufwiesen.
Tabelle 4 — Explorativer Wirksamkeitsendpunkt — Glabellafalten-Skalenscore von 0 (keine Falten) oder 1 (leichte Falten) an Tag 30, basierend auf der Beurteilung der mit NUCEIVA behandelten Studienteilnehmer durch den Prüfarzt bei maximaler Kontraktion, basierend auf den GLS-Kategorien bei Studienbeginn im Ruhezustand, ITT-Population
GLS-Kategorie bei Studienbeginn im Ruhezustand |
NUCEIVA (N = 245) |
|
GLS = 0 an Tag 30 bei maximaler Kontraktion |
GLS = 1 an Tag 30 bei maximaler Kontraktion |
|
≤ 1 (d. h. keine oder leichte Falten) |
||
Anzahl |
61/103 |
40/103 |
Prozentsatz |
59,2 % |
38,8 % |
> 1 (d. h. mittelstarke oder starke Falten) |
||
Anzahl |
15/138 |
93/138 |
Prozentsatz |
10,9 % |
67,4 % |
Glabellafalten-Skala (GLS); 0 = keine Falten, 1 = leichte Falten, 2 = mittelstarke Falten, 3 = starke Falten. Die Nenner basieren auf der Anzahl der Studienteilnehmer mit dem angegebenen Schweregrad bei Studienbeginn im Ruhezustand, die außerdem sowohl GSL-Scores bei Studienbeginn als auch an Tag 30 bei maximaler Kontraktion, beurteilt durch den Prüfarzt, aufwiesen.
NUCEIVA-Injektionen reduzierten auch den Schweregrad der Glabellafalten im Ruhezustand, einem explorativen Endpunkt.
Tabelle 5 — Explorativer Wirksamkeitsendpunkt — Verbesserung des Glabellafalten-Skalenscores um >/=2 Punkte an Tag 30, basierend auf der Beurteilung des Prüfarztes im Ruhezustand, PP-Population
Responder für den explorativen Wirksamkeitsendpunkt |
Placebo |
BOTOX |
NUCEIVA |
Absolute Differenz |
||
BOTOX vs. Placebo |
NUCEIVA vs. Placebo |
NUCEIVA vs. BOTOX |
||||
Anzahl |
0/27 |
36/149 |
32/133 |
|||
Prozentsatz |
0 % |
24,2 % |
24,1 % |
24,2 % |
24,1 % |
-0,1 % |
(% KI) |
(0,0; 12,8) |
(17,5; 31,8) |
(17,1; 32,2) |
(11,4; 32,3) |
(11,3; 32,4) |
(-10,1; 9,9) |
p-Wert |
0,003 |
0,003 |
0,984 |
|||
Es liegen begrenzte klinische Daten aus einer Phase-III-Studie zur Anwendung von NUCEIVA bei Patienten über 65 Jahren vor.
Die Dauer des Ansprechens in der Phase-III-Studie betrug 139 Tage, basierend auf einer GLS-Verbesserung um 1 Punkt.
Insgesamt 922 Patienten nahmen an zwei einjährigen offenen, unkontrollierten Studien teil, und im Laufe dieser Studien erhielten die Patienten im Durchschnitt drei Behandlungen.
Die psychologische Auswirkung der Glabellafalten wurde bei Studienbeginn bestätigt, und obwohl keine positive Wirkung auf das psychische Wohlbefinden nachgewiesen werden konnte, wurden im Vergleich zu Placebo signifikante Auswirkungen auf Patientenberichte bezüglich der Ergebnisse nachgewiesen. Darüber hinaus waren die Auswirkungen von NUCEIVA auf das psychische Wohlbefinden und die von den Patienten berichteten Ergebnisse vergleichbar mit BOTOX, der aktiven Kontrolle, die in der Zulassungsstudie verwendet wurde.
Dieses Arzneimittel wurde nach intramuskulärer Injektion in der empfohlenen Dosierung nicht im peripheren Blut nachgewiesen.
Studien zur Resorption, Verteilung, Biotransformation und Elimination (ADME) des Wirkstoffs wurden aufgrund der Art dieses Arzneimittels nicht durchgeführt.
Basierend auf den konventionellen Studien zur akuten Toxizität und zur Toxizität bei wiederholter Gabe lassen die präklinischen Daten keine besonderen Gefahren für den Menschen erkennen.
Reproduktionstoxizität
Die möglichen Auswirkungen dieses Arzneimittels auf die Fertilität wurden bei Tieren nicht untersucht. Bei trächtigen Ratten hatten tägliche intramuskuläre Injektionen von 0,5 Einheiten/kg, 1 Einheit/kg oder 4 Einheiten/kg während der Organogenese (zwischen dem 6. und 16. Trächtigkeitstag) keine durch das Prüfprodukt bedingten, signifikanten toxikologischen Wirkungen auf die Muttertiere und die embryofetale Entwicklung. Die Auswirkungen auf die peri-/postnatale Entwicklung wurden nicht untersucht.
Albuminlösung vom Menschen
Natriumchlorid
Da keine Kompatibilitätsstudien durchgeführt wurden, darf dieses Arzneimittel nicht mit anderen Arzneimitteln gemischt werden.
Ungeöffnete Durchstechflasche
50 Einheiten
30 Monate
100 Einheiten
30 Monate
Rekonstituierte Lösung
Die chemische und physikalische Stabilität der gebrauchsfertigen Zubereitung wurde über 72 Stunden bei 2 °C bis 8 °C nachgewiesen.
Aus mikrobiologischer Sicht sollte die gebrauchsfertige Zubereitung sofort verwendet werden. Wenn die gebrauchsfertige Zubereitung nicht sofort verwendet wird, ist der Anwender für die Dauer und die Bedingungen der Aufbewahrung verantwortlich. Sofern die Herstellung der gebrauchsfertigen Zubereitung nicht unter kontrollierten und validierten aseptischen Bedingungen erfolgt, ist diese nicht länger als 24 Stunden bei 2°C bis 8°C aufzubewahren.
Im Kühlschrank lagern (2° C – 8° C).
Aufbewahrungsbedingungen nach Rekonstitution des Arzneimittels, siehe Abschnitt 6.3.
Durchstechflasche (Glas Typ I) mit einem Stopfen (Chlorobutylgummi) und einer Versiegelung (Aluminium).
Nuceiva 100 Einheiten:
Packungen mit einer Durchstechflasche.
Nuceiva 50 Einheiten:
Packungen mit einer Durchstechflasche.
Mehrfachpackung enthält 4 (4 x 1) Durchstechflaschen.
Mehrfachpackung enthält 10 (10 x 1) Durchstechflaschen.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
Die Rekonstitution muss unter Einhaltung geeigneter aseptischer Verfahren durchgeführt werden. Dieses Arzneimittel wird mit Natriumchlorid-Injektionslösung 9 mg/ml (0,9%) rekonstituiert. Die benötigte Menge an Natriumchlorid-Injektionslösung 9 mg/ml (0,9%) ist gemäß nachstehender Verdünnungstabelle in eine Spritze aufzuziehen, um eine rekonstituierte Lösung mit einer Konzentration von 4 Einheiten/0,1 ml zu erhalten.
Durchstechflasche mit 50 Einheiten |
Durchstechflasche mit 100 Einheiten |
|
Menge an Lösungsmittel (Natriumchlorid-Injektionslösung 9 mg/ml (0,9%)), die hinzugefügt wird |
1,25 ml |
2,5 ml |
Resultierende Dosis (Einheiten pro 0,1 ml) |
4 Einheiten |
4 Einheiten |
Der Mittelteil des Gummistopfens muss mit Alkohol gereinigt werden.
Die Lösung wird hergestellt, indem das Lösungsmittel langsam mit einer Kanüle durch den Gummistopfen in die Durchstechflasche injiziert wird. Anschließend wird die Durchstechflasche vorsichtig geschwenkt, um Blasenbildung zu vermeiden. Die Durchstechflasche ist zu verwerfen, wenn in der Flasche kein Unterdruck vorhanden ist, der das Lösungsmittel aus der Spritze ansaugt. Nach der Rekonstitution ist die Lösung vor Anwendung visuell zu prüfen. Es darf nur eine klare, farblose Lösung ohne Partikel verwendet werden.
Vorgehensweise zur sicheren Entsorgung der Durchstechflaschen, Spritzen und verwendeten Materialien:
Unmittelbar nach der Anwendung und vor der Entsorgung muss nicht benutzte rekonstituierte NUCEIVA-Lösung in der Durchstechflasche und/oder der Spritze inaktiviert werden. Hierzu 2 ml verdünnte Natriumhypochloritlösung (0,5%ig oder 1%ig, Javelwasser) zusetzen und entsprechend den nationalen Anforderungen beseitigen.
Gebrauchte Durchstechflaschen, Spritzen oder Materialien dürfen nicht entleert werden, sondern müssen in entsprechenden Behälter geworfen und entsprechend den nationalen Anforderungen als medizinische, biologisch gefährliche Abfälle beseitigt werden.
Empfehlungen bei Unfällen während des Umgangs mit Botulinumtoxin:
Wenn beim Umgang mit dem Arzneimittel im vakuumgetrockneten oder im rekonstituierten Zustand ein Unfall auftritt, müssen sofort die im Folgenden beschriebenen geeigneten Maßnahmen eingeleitet werden:
Das Toxin ist sehr hitzeempfindlich. Es ist außerdem empfindlich gegenüber bestimmten chemischen Stoffen.
Verschüttetes Arzneimittel muss aufgewischt werden: im Falle des vakuumgetrockneten Arzneimittels mit einem saugfähigen Material, das mit Natriumhypochloritlösung (Javelwasser) getränkt wurde, oder im Falle des rekonstituierten Arzneimittels mit einem trockenen saugfähigen Material.
Kontaminierte Oberflächen müssen mit einem saugfähigen Material gereinigt werden, das mit Natriumhypochloritlösung (Javelwasser) getränkt wurde. Anschließend trocknen lassen.
Wenn eine Durchstechflasche zerbricht, die Glassplitter vorsichtig aufsammeln und das Arzneimittel, wie oben beschrieben, aufwischen. Schnittverletzungen der Haut vermeiden.
Spritzer auf der Haut mit Natriumhypochloritlösung abwaschen und anschließend mit reichlich Wasser gründlich abspülen.
Wenn Spritzer in die Augen gelangen, die Augen mit reichlich Wasser und einer Augenwaschlösung gründlich ausspülen.
Wenn sich die injizierende Person verletzt (Schnitt- oder Stichverletzungen), wie oben beschrieben vorgehen und die entsprechenden medizinischen Maßnahmen ergreifen.
Diese Hinweise zur Anwendung, Handhabung und Beseitigung müssen strikt eingehalten werden.
Evolus Pharma B.V.
Apollolaan 151
1077 AR Amsterdam
Niederlande
EU/1/19/1364/001
EU/1/19/1364/002
EU/1/19/1364/003
EU/1/19/1364/004
Datum der Erteilung der Zulassung: 27. September 2019
Datum der letzten Verlängerung der Zulassung: 17. Mai 2024
Mai 2024
Ausführliche Informationen zu diesem Arzneimittel sind auf den Internetseiten der Europäischen Arzneimittel-Agentur http://www.ema.europa.eu verfügbar.
Deutschland
Verschreibungspflichtig
Österreich
Rezept- und apothekenpflichtig
Wiederholte Abgabe verboten