Duaklir Genuair 340 Mikrogramm/12 Mikrogramm Pulver zur Inhalation
Jede abgegebene Dosis (die über das Mundstück abgegebene Dosis) enthält 340 Mikrogramm Aclidinium (als 396 Mikrogramm Aclidiniumbromid) und 11,8 Mikrogramm Formoterolfumarat-Dihydrat (Ph.Eur.).
Dies entspricht einer abgemessenen Dosis von 343 Mikrogramm Aclidinium (als 400 Mikrogramm Aclidiniumbromid) und einer abgemessenen Dosis von 12 Mikrogramm Formoterolfumarat-Dihydrat (Ph.Eur.).
Sonstiger Bestandteil mit bekannter Wirkung
Jede abgegebene Dosis enthält etwa 11 mg Lactose (als Monohydrat).
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
Pulver zur Inhalation
Weißes oder fast weißes Pulver in einem weißen Inhalator mit integrierter Dosisanzeige und einer orangen Dosiertaste.
Duaklir Genuair ist indiziert als bronchodilatatorische Erhaltungstherapie zur Linderung von Symptomen bei Erwachsenen mit chronisch-obstruktiver Lungenerkrankung (COPD).
Dosierung
Die empfohlene Dosis beträgt eine Inhalation zweimal täglich.
Wenn eine Dosis ausgelassen wurde, sollte sie so bald wie möglich nachgeholt und die folgende Dosis zur üblichen Zeit angewendet werden. Die folgende Dosis darf nicht verdoppelt werden, um die vergessene Dosis auszugleichen.
Ältere Patienten
Bei älteren Patienten sind keine Dosisanpassungen erforderlich (siehe Abschnitt 5.2).
Nierenfunktionsstörung
Bei Patienten mit Nierenfunktionsstörung sind keine Dosisanpassungen erforderlich (siehe Abschnitt 5.2).
Leberfunktionsstörung
Bei Patienten mit Leberfunktionsstörung sind keine Dosisanpassungen erforderlich (siehe Abschnitt 5.2).
Kinder und Jugendliche
Es gibt keinen relevanten Nutzen von Duaklir Genuair bei Kindern und Jugendlichen unter 18 Jahren in der Indikation COPD.
Art der Anwendung
Zur Inhalation.
Patienten sollten in die korrekte Anwendung des Arzneimittels eingewiesen werden, da der Genuair-Inhalator möglicherweise anders funktioniert als die von den Patienten zuvor angewendeten Inhalatoren. Es ist wichtig, die Patienten anzuweisen, die Bedienungsanleitung in der Packungsbeilage zu lesen.
Vor der ersten Anwendung muss der verschlossene Beutel aufgerissen und der Inhalator entnommen werden. Der Beutel und das Trockenmittel sollten entsorgt werden.
Bedienungsanleitung, siehe Abschnitt 6.6.
Überempfindlichkeit gegen die Wirkstoffe oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
Asthma
Duaklir Genuair sollte nicht bei Asthma angewendet werden; es wurden keine klinischen Studien mit Duaklir Genuair bei Asthma durchgeführt.
Paradoxer Bronchospasmus
In klinischen Studien traten mit Duaklir Genuair in der empfohlenen Dosis keine paradoxen Bronchospasmen auf. Mit anderen Inhalationstherapien wurden jedoch paradoxe Bronchospasmen beobachtet. Bei Auftreten von Bronchospasmen muss die Behandlung abgebrochen und eine andere Therapie in Erwägung gezogen werden.
Nicht zur akuten Anwendung
Duaklir Genuair ist nicht zur Behandlung von akuten Bronchospasmus-Anfällen indiziert.
Kardiovaskuläre Wirkungen
β2-Adrenozeptoragonisten können bei einigen Patienten einen Anstieg von Pulsfrequenz und Blutdruck, Veränderungen im Elektrokardiogramm (EKG), wie beispielsweise eine T-Wellen-Abflachung, eine ST-Senkung und ein verlängertes QTc-Intervall, verursachen. Bei Auftreten solcher Wirkungen kann es notwendig werden, die Behandlung abzubrechen. Lang wirksame β2‑Adrenozeptoragonisten sollten mit Vorsicht angewendet werden bei Patienten mit einer aktuell bestehenden oder früher aufgetretenen Verlängerung des QTc-Intervalls bzw. bei Patienten unter Therapie mit Arzneimitteln, die das QTc-Intervall beeinflussen (siehe Abschnitt 4.5).
Herzrhythmusstörungen, einschließlich Vorhofflimmern und paroxysmaler Tachykardie, wurden nach der Gabe von Duaklir Genuair beobachtet (siehe Abschnitt 4.8). Daher ist Duaklir Genuair mit Vorsicht anzuwenden bei Patienten mit anamnestisch bekannten Herzrhythmusstörungen oder Risikofaktoren für Herzrhythmusstörungen.
Systemische Wirkungen
Duaklir Genuair sollte bei Patienten mit schweren kardiovaskulären Erkrankungen, Krampfleiden, Thyreotoxikose und bei Patienten mit Phäochromozytom nur mit Vorsicht angewendet werden.
Bei Anwendung hoher Dosen von β2-Adrenozeptoragonisten können Wirkungen auf den Stoffwechsel, wie Hyperglykämie und Hypokaliämie, beobachtet werden. In klinischen Phase-III-Studien war die Inzidenz deutlicher Anstiege des Blutzuckerspiegels unter Duaklir Genuair gering (0,1 %) und ähnlich wie unter Placebo. Hypokaliämie ist für gewöhnlich vorübergehend und erfordert keine Supplementierung. Bei Patienten mit schwerer COPD kann die Hypokaliämie durch Hypoxie und Begleitbehandlungen verschärft werden (siehe Abschnitt 4.5). Hypokaliämie erhöht die Anfälligkeit für Herzrhythmusstörungen.
Auf Grund seiner anticholinergen Wirkung sollte Duaklir Genuair bei Patienten mit symptomatischer Prostatahyperplasie, Harnretention oder mit Engwinkelglaukom (selbst wenn der direkte Kontakt des Arzneimittels mit den Augen sehr unwahrscheinlich ist) mit Vorsicht angewendet werden.
Mundtrockenheit, wie sie im Zusammenhang mit einer anticholinergen Therapie beobachtet wurde, kann langfristig mit Zahnkaries assoziiert sein.
Lactosegehalt
Patienten mit der seltenen hereditären Galactoseintoleranz, völligem Lactasemangel oder Glucose-Galactose-Malabsorption sollten dieses Arzneimittel nicht anwenden.
Arzneimittel zur Behandlung von COPD
Die gleichzeitige Anwendung von Duaklir Genuair mit anderen Arzneimitteln, die Anticholinergika und/oder lang wirksame β2-Adrenozeptor-Agonisten enthalten, wurde nicht untersucht und wird nicht empfohlen.
Obwohl keine formalen In-vivo-Studien zur Erfassung von Wechselwirkungen durchgeführt wurden, wurde Duaklir Genuair gleichzeitig mit anderen Arzneimitteln gegen COPD einschließlich kurz wirksamen β2-adrenergen Bronchodilatatoren, Methylxanthinen sowie oralen und inhalierten Steroiden angewendet, ohne dass Arzneimittelwechselwirkungen klinisch nachgewiesen werden konnten.
Behandlung mit Hypokaliämie-verursachenden Arzneimitteln
Die gleichzeitige Behandlung mit Methylxanthin-Derivaten, Steroiden oder nicht-kaliumsparenden Diuretika kann eine mögliche hypokaliämische Wirkung von β2-Adrenozeptoragonisten verstärken. Daher sollte die gleichzeitige Anwendung dieser Arzneimittel nur mit Vorsicht erfolgen (siehe Abschnitt 4.4).
Betablocker
Betablocker können die Wirkung von β2-Adrenozeptoragonisten abschwächen oder ihr entgegenwirken. Wird die Anwendung von Betablockern (einschließlich Augentropfen) notwendig, so sollten kardioselektive Betablocker bevorzugt werden, wobei auch bei deren Anwendung Vorsicht geboten ist.
Andere pharmakodynamische Interaktionen
Duaklir Genuair sollte bei Patienten, die mit Arzneimitteln behandelt werden, welche bekanntermaßen das QTc-Intervall verlängern (wie beispielsweise Monoaminoxidase-Hemmer, trizyklische Antidepressiva, Antihistaminika oder Makrolide), nur mit Vorsicht angewendet werden, da die Wirkung von Formoterol (ein Bestandteil von Duaklir Genuair) auf das kardiovaskuläre System durch diese Arzneimittel verstärkt werden kann. Arzneimittel, die bekanntermaßen das QTc-Intervall verlängern, sind mit einem erhöhten Risiko für ventrikuläre Rhythmusstörungen verbunden.
Stoffwechselinteraktionen
In-vitro-Studien haben gezeigt, dass nicht zu erwarten ist, dass Aclidinium oder seine Metaboliten bei Dosierung im therapeutischen Bereich Wechselwirkungen mit P-Glycoprotein-(P-gp-)Substraten oder mit durch Cytochrom-P-450-Enzyme (CYP450-Enzyme) oder Esterasen metabolisierten Arzneimitteln hervorrufen. In therapeutisch relevanten Konzentrationen führt Formoterol zu keiner Hemmung der CYP450-Enzyme (siehe Abschnitt 5.2).
Schwangerschaft
Bisher liegen keine Erfahrungen mit der Anwendung von Duaklir Genuair bei Schwangeren vor.
Tierexperimentelle Studien haben eine Fetotoxizität für Aclidinium nur bei Dosisspiegeln gezeigt, die viel höher als die maximale Humanexposition waren; und unerwünschte Wirkungen von Formoterol in Reproduktionsstudien nur bei sehr hohen systemischen Expositionsspiegeln (siehe Abschnitt 5.3).
Duaklir Genuair darf während der Schwangerschaft nur dann angewendet werden, wenn der zu erwartende Nutzen die potenziellen Risiken überwiegt.
Stillzeit
Es ist nicht bekannt, ob Aclidinium (und/oder seine Metaboliten) oder Formoterol in die Muttermilch sezerniert wird. Da Studien an Ratten die Ausscheidung geringer Mengen Aclidinium (und/oder seiner Metaboliten) sowie Formoterol in die Milch gezeigt haben, darf die Anwendung von Duaklir Genuair durch stillende Frauen nur in Betracht gezogen werden, wenn der erwartete Nutzen für die Frau größer ist als jedmögliches Risiko für den Säugling.
Fertilität
Studien mit Ratten haben eine leichte Reduzierung der Fertilität nur bei Dosisspiegeln gezeigt, die viel höher waren als die maximale Humanexposition für Aclidinium und Formoterol (siehe Abschnitt 5.3). Es gilt als unwahrscheinlich, dass Duaklir Genuair bei Anwendung in der empfohlenen Dosierung die Fertilität bei Menschen beeinflusst.
Duaklir Genuair hat keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen. Das Auftreten von Verschwommensehen oder Schwindel kann die Verkehrstüchtigkeit oder die Fähigkeit zum Bedienen von Maschinen beeinträchtigen.
Die Darstellung des Sicherheitsprofils beruht auf Erfahrungen mit Duaklir Genuair sowie seinen einzelnen Bestandteilen.
Zusammenfassung des Sicherheitsprofils
Sicherheitsrelevante Daten über Duaklir Genuair in der empfohlenen therapeutischen Dosis liegen für eine Exposition bis zu 12 Monaten aus klinischen Studien sowie aus Erfahrungen nach Markteinführung vor.
Die mit der Anwendung von Duaklir Genuair verbundenen Nebenwirkungen waren vergleichbar mit denen seiner einzelnen Bestandteile. Da Duaklir Genuair die Wirkstoffe Aclidinium und Formoterol enthält, können die mit diesen Bestandteilen verbundenen unerwünschten Wirkungen in gleicher Art und Schwere auch für Duaklir Genuair erwartet werden.
Die am häufigsten berichteten Nebenwirkungen im Zusammenhang mit Duaklir Genuair sind Nasopharyngitis (7,9 %) und Kopfschmerzen (6,8 %).
Tabellarische Zusammenfassung der Nebenwirkungen
Das klinische Entwicklungsprogramm zu Duaklir Genuair wurde an Patienten mit mittelschwerer oder schwerer COPD durchgeführt. Insgesamt wurden 1.222 Patienten mit Duaklir Genuair 340 Mikrogramm/12 Mikrogramm behandelt. Die den Nebenwirkungen zugeordneten Häufigkeitsangaben basieren auf den Rohinzidenzraten, die in gepoolten Analysen von randomisierten, Placebo-kontrollierten klinischen Phase-III-Studien mit Duaklir Genuair 340 Mikrogramm/12 Mikrogramm mit mindestens 6 Monaten Dauer beobachtet wurden, oder auf Erfahrungen mit den Einzelwirkstoffen oder auf Ergebnissen von nach dem Inverkehrbringen durchgeführten Studien.
Bei den Häufigkeitsangaben zu Nebenwirkungen werden folgende Kategorien zugrunde gelegt: Sehr häufig (≥1/10), häufig (≥1/100, <1/10), gelegentlich (≥1/1.000, <1/100), selten (≥1/10.000, <1/1.000), sehr selten (<1/10.000) und nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar).
Systemorganklasse |
Häufigkeit |
|
Infektionen und parasitäre Erkrankungen |
Nasopharyngitis |
Häufig |
Erkrankungen des Immunsystems |
Überempfindlichkeit |
Selten |
Angioödem |
Nicht bekannt |
|
Stoffwechsel- und Ernährungsstörungen |
Hypokaliämie |
Gelegentlich |
Psychiatrische Erkrankungen |
Schlafstörungen |
Häufig |
Agitiertheit |
Gelegentlich |
|
Erkrankungen des Nervensystems |
Kopfschmerzen |
Häufig |
Geschmacksstörung |
Gelegentlich |
|
Augenerkrankungen |
Verschwommenes Sehen |
Gelegentlich |
Herzerkrankungen |
Herzrhythmusstörungen, einschließlich Vorhofflimmern und paroxysmaler Tachykardie |
Gelegentlich |
Erkrankungen der Atemwege, des Brustraums und Mediastinums |
Husten |
Häufig |
Dysphonie |
Gelegentlich |
|
Bronchospasmen (einschließlich paradoxe) |
Selten |
|
Erkrankungen des Gastrointestinaltrakts |
Durchfall |
Häufig |
Stomatitis |
Gelegentlich |
|
Erkrankungen der Haut und des Unterhautzellgewebes |
Ausschlag |
Gelegentlich |
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen |
Myalgie |
Häufig |
Erkrankungen der Nieren und Harnwege |
Harnverhalt |
Gelegentlich |
Untersuchungen |
Anstieg der Kreatinphosphokinase im Blut |
Häufig |
Blutdruckanstieg |
Gelegentlich |
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels.
Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger-Allee 3, D-53175 Bonn, Website: www.bfarm.de anzuzeigen.
Es liegen nur begrenzte Daten zur Behandlung einer Überdosierung mit Duaklir Genuair vor. Hohe Dosierungen Duaklir Genuair können zu übersteigerten anticholinergen und/oder β2-adrenergen Anzeichen und Symptomen führen; zu den häufigsten dieser Anzeichen und Symptome gehören verschwommenes Sehen, Mundtrockenheit, Übelkeit, Muskelkrämpfe, Tremor, Kopfschmerzen, Palpitationen und Bluthochdruck.
Im Falle einer Überdosierung ist Duaklir Genuair abzusetzen. Eine unterstützende und symptomatische Behandlung ist indiziert.
Pharmakotherapeutische Gruppe: Mittel bei obstruktiven Atemwegserkrankungen, Sympathomimetika in Kombination mit Anticholinergika, ATC-Code: R03AL05
Wirkmechanismus
Duaklir Genuair enthält zwei Bronchodilatatoren: Aclidinium ist ein lang wirksamer Muskarin-Rezeptor-Antagonist (auch als Anticholinergikum bezeichnet) und Formoterol ein lang wirksamer β2-Adrenozeptoragonist. Die Kombination dieser Substanzen mit unterschiedlichen Wirkmechanismen führt zu einer additiven Wirksamkeit im Vergleich zur Anwendung einer der beiden Bestandteile allein. Auf Grund der unterschiedlichen Dichte von Muskarin-Rezeptoren und β2-Adrenozeptoren in den zentralen und peripheren Atemwegen der Lunge wird für Muskarinrezeptor-Antagonisten eine stärkere Wirkung bezüglich der Relaxation der zentralen Atemwege erwartet, wohingegen für β2-Adrenozeptoragonisten eine stärkere relaxierende Wirkung auf die peripheren Atemwege erwartet wird; die Relaxation sowohl der zentralen als auch der peripheren Atemwege mittels eines Kombinationspräparats trägt wahrscheinlich zur günstigen Wirkung auf die Lungenfunktion bei.
Weitere Informationen über diese beiden Substanzen sind weiter unten im Text zu finden.
Aclidiniumbromid ist ein kompetitiver, selektiver Muskarinrezeptor-Antagonist mit längerer Verweildauer an den M3-Rezeptoren als an den M2-Rezeptoren. M3-Rezeptoren regeln die Kontraktion der glatten Muskulatur der Luftwege. Inhaliertes Aclidiniumbromid wirkt lokal in den Lungen, wo es an die M3-Rezeptoren der glatten Bronchialmuskulatur antagonistisch bindet und eine Bronchodilatation bewirkt. Es wurde außerdem gezeigt, dass Aclidinium die Symptome von COPD-Patienten lindert, deren krankheitsspezifischen Gesundheitszustand verbessert, die Exazerbationsrate reduziert und die Belastungstoleranz erhöht. Da Aclidiniumbromid schnell im Plasma abgebaut wird, treten wenige systemische anticholinerge Nebenwirkungen auf.
Formoterol ist ein potenter selektiver β2-Adrenozeptoragonist. Die Bronchodilatation wird durch eine direkte Relaxation der glatten Atemwegsmuskulatur induziert, da die Konzentration des zyklischen Adenosinmonophosphats (cAMP) durch die Adenylatcyclase-Aktivierung erhöht wird. Neben einer Verbesserung der Lungenfunktion konnte bei COPD-Patienten durch Behandlung mit Formoterol auch eine Linderung der Symptome und eine gesteigerte Lebensqualität nachgewiesen werden.
Pharmakodynamische Wirkungen
Klinische Wirksamkeitsstudien haben gezeigt, dass Duaklir Genuair klinisch bedeutsame Verbesserungen der Lungenfunktion (gemessen am forcierten exspiratorischen Volumen in einer Sekunde [FEV1]) über eine Dauer von zwölf Stunden nach der Anwendung bewirkt.
Duaklir Genuair zeigte im Vergleich zu Placebo einen schnellen Wirkungseintritt innerhalb von fünf Minuten nach der ersten Inhalation (p < 0,0001). Der für Duaklir Genuair beobachtete Wirkungseintritt war vergleichbar mit der Wirkung des schnell wirksamen β2-Agonisten Formoterol 12 Mikrogramm. Maximale bronchodilatatorische Wirkungen (peak FEV1) im Vergleich zur Baseline wurden ab dem ersten Tag (304 ml) nachgewiesen und über den sechsmonatigen Behandlungszeitraum aufrechterhalten (326 ml).
Elektrophysiologie des Herzens
Im Rahmen von Phase III-Studien mit einer Laufzeit zwischen sechs und zwölf Monaten an insgesamt etwa 4.000 COPD-Patienten wurden bei der Anwendung von Duaklir Genuair im Vergleich zu Aclidinium, Formoterol und Placebo keine klinisch relevanten Auswirkungen auf EKG-Parameter (einschließlich QT-Intervall) beobachtet. Bei einer Subpopulation von 551 Patienten, von denen 114 Duaklir Genuair zweimal täglich erhielten, wurden bei einem 24-stündigen Langzeit-EKG keine klinisch signifikanten Auswirkungen von Duaklir Genuair auf den Herzrhythmus beobachtet.
Klinische Wirksamkeit und Sicherheit
Das klinische Entwicklungsprogramm der Phase III schloss etwa 4.000 Patienten mit einer klinisch diagnostizierten COPD ein und umfasste zwei sechsmonatige randomisierte, placebo- und aktiv-kontrollierte Studien (ACLIFORM-COPD und AUGMENT), eine sechsmonatige Verlängerungsstudie zur AUGMENT-Studie sowie eine weitere zwölfmonatige randomisierte, kontrollierte Studie. In diesen Studien war den Patienten eine Fortsetzung ihrer eingestellten Behandlung mit inhalierten Kortikosteroiden, oralen Kortikosteroiden in niedriger Dosierung, Sauerstofftherapie (falls weniger als 15 Std./Tag) oder Methylxanthinen sowie der Einsatz von Salbutamol als Notfallmedikation gestattet.
Die Wirksamkeit wurde anhand von Messungen der Lungenfunktion, der klinischen Symptomatik, des krankheitsspezifischen Gesundheitszustands, der Verwendung von Notfallmedikation und des Auftretens von Exazerbationen bewertet. In Langzeitsicherheitsstudien erwies sich Duaklir Genuair über einen einjährigen Behandlungszeitraum als dauerhaft wirksam, ohne dass sich Anzeichen für Tachyphylaxie ergaben.
Auswirkungen auf die Lungenfunktion
Duaklir Genuair 340 Mikrogramm/12 Mikrogramm zweimal täglich bewirkte im Vergleich zu Placebo eine anhaltende klinisch bedeutsame Verbesserung der Lungenfunktion (gemessen am FEV1, der forcierten Vitalkapazität und der inspiratorischen Kapazität). In Phase-III-Studien wurde eine klinisch bedeutsame bronchodilatatorische Wirkung innerhalb von fünf Minuten nach Anwendung der ersten Dosis beobachtet; die Bronchodilatation hielt über das gesamte Dosierungsintervall an. Es wurde eine anhaltende Wirkung über die Dauer der sechsmonatigen wie auch der einjährigen Phase-III-Studien beobachtet.
In beiden sechsmonatigen pivotalen Phase-III-Studien wurden zum Nachweis des jeweiligen Beitrags von Formoterol und Aclidinium zur bronchodilatatorischen Wirkung von Duaklir Genuair das FEV1 eine Stunde nach Anwendung und das FEV1 vor Anwendung der Dosis (trough FEV1) (im Vergleich zu Aclidinium 400 Mikrogramm bzw. Formoterol 12 Mikrogramm) als co-primäre Endpunkte definiert.
In der ACLIFORM-COPD-Studie bewirkte Duaklir Genuair eine Verbesserung des FEV1 eine Stunde nach Anwendung von 299 ml bzw. 125 ml gegenüber Placebo bzw. Aclidinium (jeweils p < 0,0001) sowie eine Verbesserung des trough FEV1 von 143 ml bzw. 85 ml gegenüber Placebo bzw. Formoterol (jeweils p < 0,0001). In der AUGMENT-Studie bewirkte Duaklir Genuair eine Verbesserung des FEV1 eine Stunde nach Anwendung von 284 ml bzw. 108 ml gegenüber Placebo bzw. Aclidinium (jeweils p < 0,0001) sowie eine Verbesserung des trough FEV1 von 130 ml gegenüber Placebo (p < 0,0001) und 45 ml gegenüber Formoterol (p = 0,01).
Linderung der Symptome und Verbesserung des krankheitsspezifischen Gesundheitszustands
Atemnot und andere klinische Symptomatik:
Für Duaklir Genuair wurde eine klinisch bedeutsame Verbesserung der Atemnot (gemessen anhand des Transitional Dyspnoea Index [TDI]) mit einer Verbesserung des TDI-Focal-Scores nach sechs Monaten um 1,29 Einheiten im Vergleich zu Placebo in der ACLIFORM-COPD-Studie (p < 0,0001) und um 1,44 Einheiten in der AUGMENT-Studie (p < 0,0001) festgestellt. Der prozentuale Anteil der Patienten mit klinisch bedeutsamen Verbesserungen des TDI-Focal-Scores (definiert als Zunahme um mindestens eine Einheit) war sowohl in der Studie ACLIFORM-COPD (64,8 % vs. 45,5 %; p < 0,001) als auch in der Studie AUGMENT (58,1 % vs. 36,6 %; p < 0,0001) mit Duaklir Genuair höher als mit Placebo.
Die gepoolte Auswertung dieser zwei Studien zeigte, dass Duaklir Genuair mit einer statistisch signifikant größeren Verbesserung des fokalen TDI-Focal-Scores gegenüber Aclidinium (0,4 Einheiten, p = 0,016) oder Formoterol (0,5 Einheiten, p = 0,009) einhergeht. Außerdem erreichte bei Behandlung mit Duaklir Genuair ein höherer Prozentsatz der Patienten eine klinisch bedeutsame Verbesserung des TDI-Focal-Scores sowohl im Vergleich zu Aclidinium als auch zu Formoterol (61,9 % vs. 55,7 % bzw. 57,0 %; p = 0,056 bzw. p = 0,100).
Duaklir Genuair führte gegenüber Placebo, Aclidinium und Formoterol zu einer Verbesserung der täglichen COPD-Symptome wie „Atemnot“, „Brustkorbbeschwerden“, „Husten und Sputum“ (gemessen als E-RS-Gesamtscore) sowie der gesamten nächtlichen Symptome, der gesamten frühmorgendlichen Symptome und der Symptome, die morgendliche Aktivitäten behindern. Diese Verbesserungen waren jedoch nicht immer statistisch signifikant. Aclidinium/Formoterol reduzierte die durchschnittliche Anzahl des nächtlichen Erwachens aufgrund von COPD nicht statistisch signifikant im Vergleich zu Placebo oder Formoterol.
Gesundheitsbezogene Lebensqualität:
Eine Verbesserung der gesundheitsbezogenen Lebensqualität (gemessen mit Hilfe des St. George’s Respiratory Questionnaire [SGRQ]) konnte in der AUGMENT-Studie nachgewiesen werden, mit einer Verbesserung des SGRQ-Gesamtscores im Vergleich zu Placebo um -4,35 Einheiten (p < 0,0001). Der prozentuale Anteil der Patienten in der AUGMENT-Studie, die eine klinisch bedeutsame Verbesserung des SGRQ-Gesamtscores gegenüber der Baseline (definiert als eine Abnahme um mindestens vier Einheiten) erreichte, war mit Duaklir Genuair höher als mit Placebo (58,2 % vs. 38,7 %; p < 0,001). In der Studie ACLIFORM-COPD sank der SGRQ-Gesamtscore im Vergleich zu Placebo jedoch auf Grund eines unerwartet starken Ansprechens auf Placebo (p = 0,598) nur geringfügig, und der prozentuale Anteil der Patienten, die klinisch bedeutsame Verbesserungen gegenüber der Baseline erreichten, lag bei 55,3 % mit Duaklir Genuair und bei 53,2 % mit Placebo (p = 0,669).
In der gepoolten Analyse dieser beiden Studien zeigte sich, dass Duaklir Genuair eine stärkere Verbesserung des SGRQ-Gesamtscores gegenüber Formoterol (-1,7 Einheiten; p = 0,018) oder Aclidinium (-0,79 Einheiten, p = 0,273) bewirkte. Außerdem erreichte bei Behandlung mit Duaklir Genuair ein höherer Prozentsatz der Patienten eine klinisch bedeutsame Verbesserung des SGRQ-Gesamtscores sowohl im Vergleich zu Aclidinium als auch zu Formoterol (56,6 % vs. 53,9 % bzw. 52,2 %; p = 0,603 bzw. p = 0,270).
Reduzierung der COPD-Exazerbationen
Gepoolte Wirksamkeitsanalysen der zwei sechsmonatigen Phase-III-Studien zeigten eine statistisch signifikante Reduzierung der Häufigkeit mittelschwerer bis schwerer Exazerbationen (die eine Behandlung mit Antibiotika oder Kortikosteroiden oder eine Krankenhauseinweisung erforderten) von 29 % für Duaklir Genuair im Vergleich zu Placebo (Häufigkeit pro Patient pro Jahr: 0,29 vs. 0,42; p = 0,036).
Außerdem bewirkte Duaklir Genuair eine gegenüber Placebo statistisch signifikante Verzögerung der Zeitdauer bis zur ersten mittelschweren bis schweren Exazerbation (Hazard Ratio = 0,70; p = 0,027).
Einsatz von Notfallmedikation
Duaklir Genuair bewirkte eine weniger häufige Anwendung von Notfallmedikation über eine Dauer von 6 Monaten im Vergleich zu Placebo (Reduktion um 0,9 Sprühstöße pro Tag [p < 0,0001]), Aclidinium (Reduktion um 0,4 Sprühstöße pro Tag [p < 0,001]) sowie Formoterol (Reduktion um 0,2 Sprühstöße pro Tag [p = 0,062]).
Lungenvolumen, Belastungsausdauer und körperliche Aktivität
Die Wirkung von Duaklir Genuair auf Lungenvolumen, Belastungsausdauer und körperliche Aktivität wurde in einer 8-wöchigen parallelen, randomisierten, Placebo-kontrollierten, klinischen Studie bei COPD-Patienten mit Lungenüberblähung (funktionelle Residualkapazität [FRC] > 120 %) untersucht.
Nach 4-wöchiger Behandlung deutete Duaklir Genuair im Vergleich zu Placebo auf eine Verbesserung bezüglich des primären Endpunktes hin, der Änderung der morgendlichen FRC vor Anwendung der Dosis (trough FRC) gegenüber dem Ausgangswert, der Unterschied war jedoch nicht statistisch signifikant (-0,125 l; 95 %-KI = (-0,259; 0,010); p = 0,069*).
Duaklir Genuair zeigte 2-3 Stunden nach Anwendung Verbesserungen im Vergleich zu Placebo bezüglich des Lungenvolumens (FRC = -0,366 l [95 %-KI = -0,515, -0,216; p < 0,0001]; Residualvolumen [RV] = -0,465 l [95 %-KI = -0,648, -0281; p < 0,0001]) und inspiratorische Kapazität [IC] = 0,293 l [95 %-KI = 0,208, 0,378; p < 0,0001]).
Duaklir Genuair zeigte ebenfalls Verbesserungen bezüglich der Belastungsausdauer im Vergleich zu Placebo nach 8 Wochen Behandlung (55 Sekunden [95 %-KI = 5,6, 104,8; p = 0,0292]; Baseline-Wert: 456 Sekunden).
Nach 4 Wochen Behandlung erhöhte Duaklir Genuair die Anzahl an Schritten pro Tag im Vergleich zu Placebo (731 Schritte pro Tag; 95 %-KI = 279, 1181; p = 0,0016) und reduzierte den Anteil an nicht aktiven Patienten (< 6000 Schritte pro Tag) [40,8 % vs. 54,5 %; p = 0,0001]. Verbesserungen im PROactive-Gesamtscore wurden bei Patienten beobachtet, die mit Duaklir Genuair behandelt wurden im Vergleich zu Placebo (p = 0,0002).
Ein Verhaltensinterventionsprogramm wurde bei beiden Behandlungsarmen in den folgenden 4 Wochen zusätzlich durchgeführt. Die Anzahl an Schritten pro Tag in der Duaklir-Genuair-Behandlungsgruppe wurde aufrechterhalten und führte im Vergleich zu Placebo zu einem Behandlungseffekt von 510 Schritten pro Tag (p = 0,1588) und zu einer Reduktion des Anteils an nicht aktiven Patienten (< 6000 Schritte pro Tag) im Vergleich zu Placebo (41,5 % vs. 50,4 %; p = 0,1134).
*Da der primäre Endpunkt keine statistische Signifikanz erreichte, wurden alle p-Werte für die sekundären Endpunkte am nominalen Signifikanzniveau von 0,05 getestet; es kann kein statistischer Rückschluss gezogen werden.
Kinder und Jugendliche
Die Europäische Arzneimittel-Agentur hat für Duaklir Genuair eine Freistellung von der Verpflichtung zur Vorlage von Ergebnissen zu Studien in allen pädiatrischen Altersklassen mit COPD gewährt (siehe Abschnitt 4.2 bzgl. Informationen zur Anwendung bei Kindern und Jugendlichen).
Bei kombinierter Inhalation von Aclidinium und Formoterol ergaben sich für die einzelnen Bestandteile keine relevanten pharmakokinetischen Unterschiede gegenüber alleiniger Anwendung.
Resorption
Nach Inhalation einer Einzeldosis Duaklir Genuair 340 Mikrogramm/12 Mikrogramm wurden Aclidinium und Formoterol rasch ins Plasma resorbiert und erreichten bei gesunden Probanden Spitzenplasmakonzentrationen innerhalb von fünf Minuten und bei COPD-Patienten innerhalb von 24 Minuten. Bei COPD-Patienten, die während 5 Tagen zweimal täglich mit Duaklir Genuair behandelt wurden, wurden die Spitzenplasmakonzentrationen von Aclidinium und Formoterol im Steady-State innerhalb von fünf Minuten nach der Inhalation erreicht und betrugen 128 pg/ml bzw. 17 pg/ml.
Verteilung
Die Deposition von über den Genuair-Inhalator inhaliertem Aclidinium in der Lunge beträgt durchschnittlich ca. 30 % der abgemessenen Dosis. Die in vitro festgestellte Plasmaproteinbindung von Aclidinium entspricht aufgrund seiner raschen Hydrolyse im Plasma höchstwahrscheinlich der Proteinbindung der entsprechenden Metaboliten; für den Karbonsäure-Metaboliten betrug die Plasmaproteinbindung 87 % und für den Alkohol-Metaboliten 15 %. Das wichtigste Plasmaprotein, das Aclidinium bindet, ist Albumin.
Die Plasmaproteinbindung von Formoterol beträgt zwischen 61 % und 64 % (davon fallen 34 % vor allem auf Albumin). In dem bei therapeutischen Dosen erreichten Konzentrationsbereich werden die Bindungsstellen nicht gesättigt.
Biotransformation
Aclidinium wird rasch und weitgehend in seine pharmakologisch unwirksamen Alkohol- und Karbonsäure-Derivate hydrolysiert.
Nach der Inhalation sind die Plasmaspiegel des Säure-Metaboliten ca. 100-mal höher als diejenigen des Alkohol-Metaboliten und des unveränderten Wirkstoffs.
Die Hydrolyse erfolgt sowohl chemisch (nicht-enzymatisch) als auch enzymatisch durch Esterasen, wobei die Butyrylcholinesterase (Pseudocholinesterase) die am meisten an der Hydrolyse beteiligte menschliche Esterase ist.
Die niedrige absolute Bioverfügbarkeit von inhaliertem Aclidinium (<5 %) ergibt sich daraus, dass Aclidinium, sowohl nach Abgabe in die Lunge als auch nach Verschlucken, eine extensive systemische und prä-systemische Hydrolyse erfährt.
Die Biotransformation über CYP450-Enzyme spielt in der gesamten metabolischen Clearance von Aclidinium eine untergeordnete Rolle.
In vitro-Studien haben gezeigt, dass Aclidinium in der therapeutischen Dosierung bzw. seine Metaboliten keines der Cytochrom-P450 (CYP450)-Enzyme hemmen oder anregen und auch keine Esterasen (Carboxylesterase, Acetylcholinesterase und Butyrylcholinesterase) hemmen.
In vitro-Studien haben gezeigt, dass Aclidinium oder seine Metaboliten keine Substrate oder Inhibitoren von P-Glykoprotein sind.
Formoterol wird primär durch Metabolisierung eliminiert. Der wichtigste Stoffwechselweg ist die direkte Glucuronidierung; ein weiterer Stoffwechselweg ist die O-Demethylierung, gefolgt von Glucuronid-Konjugation. Die O-Demethylierung von Formoterol erfolgt unter Beteiligung der Cytochrom-P450-Isoenzyme CYP2D6, CYP2C19, CYP2C9 und CYP2A6. In therapeutisch relevanten Konzentrationen bewirkt Formoterol keine Hemmung von CYP450-Enzymen.
Elimination
Nach Inhalation von Duaklir Genuair 340 Mikrogramm/12 Mikrogramm lag die anhand von Plasmaprobenahmen bis zu 24 Stunden nach Dosierung beobachtete terminale Eliminationshalbwertzeit für Aclidiniumbromid im Bereich von 11-33 Stunden und für Formoterol im Bereich von 12-18 Stunden.
Die mittleren effektiven Halbwertszeiten*, die sowohl für Aclidinium als auch Formoterol beobachtet wurden (basierend auf dem Kumulations-Verhältnis), betrugen ca. 10 Stunden.
*Halbwertszeit ist konsistent mit der Arzneimittelkumulation entsprechend eines bekannten Dosierungsschemas.
Nach der intravenösen Anwendung von 400 Mikrogramm radioaktiv markiertem Aclidinium bei gesunden Probanden wurde ca. 1 % der Dosis als unverändertes Aclidiniumbromid im Urin ausgeschieden. Bis zu 65 % der Dosis wurden in Form von Metaboliten im Urin und bis zu 33 % in Form von Metaboliten fäkal ausgeschieden.
Nach der Inhalation von 200 Mikrogramm und 400 Mikrogramm Aclidinium durch gesunde Probanden bzw. COPD-Patienten war die Urinausscheidung von unverändertem Aclidinium mit ca. 0,1 % der angewendeten Dosis sehr gering, was darauf hinweist, dass die renale Clearance bei der gesamten Clearance von Aclidinium aus dem Plasma eine untergeordnete Rolle spielt.
Der Großteil einer Formoterol-Dosis wird in der Leber verstoffwechselt, gefolgt von Ausscheidung über die Nieren. Nach Inhalation werden 6-9 % der abgegebenen Dosis im Urin unverändert oder als direkte Konjugate von Formoterol ausgeschieden.
Besondere Patientengruppen
Ältere Patienten
Es wurden keine pharmakokinetischen Studien zur Anwendung von Aclidinium/Formoterol bei älteren Patienten durchgeführt. Da weder bei Arzneimitteln, die Aclidinium enthalten, noch bei solchen, die Formoterol enthalten, Anpassungen der Dosierung bei älteren Patienten erforderlich sind, sind auch für die Anwendung von Aclidinium/Formoterol bei älteren Patienten keine Anpassungen der Dosierung indiziert.
Patienten mit Nieren- und Leberfunktionsstörungen
Es liegen keine Daten speziell zur Anwendung von Aclidinium/Formoterol bei Patienten mit Nieren- und Leberfunktionsstörungen vor. Da weder bei Arzneimitteln, die Aclidinium enthalten, noch bei solchen, die Formoterol enthalten, Anpassungen der Dosierung bei Patienten mit Nieren- oder Leberfunktionsstörungen erforderlich sind, sind auch für die Anwendung von Aclidinium/Formoterol bei solchen Patienten keine Anpassungen der Dosierung indiziert.
Ethnische Zugehörigkeit
Nach wiederholten Inhalationen von Duaklir Genuair 340 Mikrogramm/12 Mikrogramm, war die systemische Exposition von Aclidinium und Formoterol, gemessen anhand der AUC, bei Patienten japanischer und kaukasischer Abstammung ähnlich.
Basierend auf den konventionellen Studien zur Sicherheitspharmakologie, Toxizität bei wiederholter Gabe, Reproduktions- und Entwicklungstoxizität, Genotoxizität und zum kanzerogenen Potenzial lassen die präklinischen Daten keine besonderen Gefahren für den Menschen bei der Anwendung von Aclidinium und Formoterol erkennen.
Die in präklinischen Studien aufgetretenen Wirkungen von Aclidinium bezüglich Reproduktionstoxizität (fetotoxische Wirkungen) und Fertilität (leichte Abnahme der Empfängnisrate und Anzahl der Gelbkörper, Prä- und Postimplantationsverluste) wurden nur nach Expositionen beobachtet, die als ausreichend über der maximalen humantherapeutischen Exposition liegend angesehen werden. Die Relevanz für die klinische Anwendung wird als gering bewertet.
Formoterol führte bei Ratten mit hoher systemischer Formoterol-Exposition sowohl zu reduzierter Fertilität (Implantationsverluste) als auch zu einer Abnahme frühen postnatalen Überlebens und des Geburtsgewichts. Bei Ratten und Mäusen wurde eine leichte Zunahme der Inzidenz von Leiomyomen des Uterus beobachtet, eine Wirkung wird bei Nagern als Klasseneffekt nach Langzeitexposition gegenüber hohen Dosierungen von β2-Adrenorezeptoragonisten angesehen.
In präklinischen Studien zur Untersuchung der Wirkung von Aclidinium/Formoterol auf kardiovaskuläre Parameter zeigten eine erhöhte Herzfrequenz und Herzrhythmusstörungen bei Expositionen, die ausreichend über der maximalen humantherapeutischen Exposition lagen. Die Relevanz für die klinische Anwendung wird als gering bewertet. Diese Wirkungen sind bekannte, bei β2-Agonisten beobachtete, übersteigerte pharmakologische Reaktionen.
Lactose-Monohydrat.
Nicht zutreffend.
3 Jahre
Nach Öffnen des Beutels nicht länger als 60 Tage verwenden.
Für dieses Arzneimittel sind bezüglich der Temperatur keine besonderen Lagerungsbedingungen erforderlich.
Bewahren Sie den Genuair Inhalator bis zum Beginn des Anwendungszeitraums im verschlossenen Beutel auf.
Der Genuair-Inhalator ist ein Multikomponentenprodukt aus Kunststoff [Polykarbonat, Poly(acrylnitril-co-butadien-co-styrol), Paraformaldehyd, Poly(butan-1,4-diylterephthalat), Polypropylen, Polystyrol] und rostfreiem Stahl. Er ist weiß mit einer integrierten Dosisanzeige und einer orangen Dosiertaste. Das Mundstück ist mit einer entfernbaren orangen Schutzkappe bedeckt. Der Inhalator ist zusammen mit einem Kieselgel als Trockenmittel enthaltenden Beutel in einen Aluminiumlaminat-Schutzbeutel eingesiegelt, der sich in einem Umkarton befindet.
Packung mit einem Inhalator mit 30 Dosen.
Packung mit einem Inhalator mit 60 Dosen.
Packung mit 3 Inhalatoren mit jeweils 60 Dosen.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu beseitigen.
Bedienungsanleitung
Erste Schritte
Lesen Sie diese Bedienungsanleitung, bevor Sie mit der Anwendung des Arzneimittels beginnen.
Machen Sie sich mit den einzelnen Teilen Ihres Genuair-Inhalators vertraut.

Vor der Anwendung:
Vor der ersten Anwendung reißen Sie den verschlossenen Beutel auf und entnehmen Sie den Inhalator. Entsorgen Sie den Beutel und das Trockenmittel.
Drücken Sie die orange Taste erst, wenn Sie bereit sind, eine Dosis zu inhalieren.
Ziehen Sie die Kappe ab, indem Sie die auf beiden Seiten sichtbaren Pfeile leicht zusammendrücken (Abbildung B).

SCHRITT 1: Bereiten Sie Ihre Dosis vor
1.1 |
Schauen Sie in die Öffnung des Mundstücks und vergewissern Sie sich, dass sie durch nichts verstopft ist (Abbildung C). |
1.2 |
Prüfen Sie das Kontrollfenster (es sollte rot sein, Abbildung C). 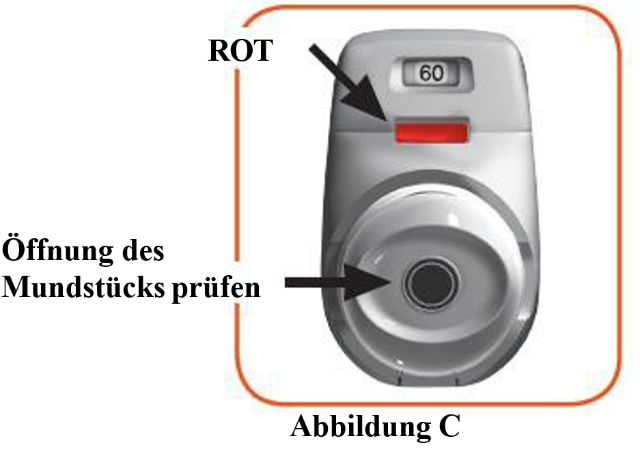 |
1.3 |
Halten Sie den Inhalator waagerecht, sodass das Mundstück zu Ihnen zeigt und die orange Taste nach oben (Abbildung D).  |
1.4 |
Drücken Sie die orange Taste ganz hinunter, um Ihre Dosis zu laden (Abbildung E). Während Sie die Taste nach unten drücken, ändert sich die Farbe des Kontrollfensters von Rot auf Grün. |
1.5 |
Lassen Sie die orange Taste los (Abbildung F).  |
Überprüfen Sie:
1.6 |
Vergewissern Sie sich, dass das Kontrollfenster nun grün ist (Abbildung G). Ihr Arzneimittel kann nun inhaliert werden. Gehen Sie zu „SCHRITT 2: Inhalation Ihres Arzneimittels“.  |
 |
SCHRITT 2: Inhalation Ihres Arzneimittels

2.1 |
Halten Sie den Inhalator von Ihrem Mund entfernt und atmen Sie vollständig aus. Atmen Sie niemals in den Inhalator aus (Abbildung I). 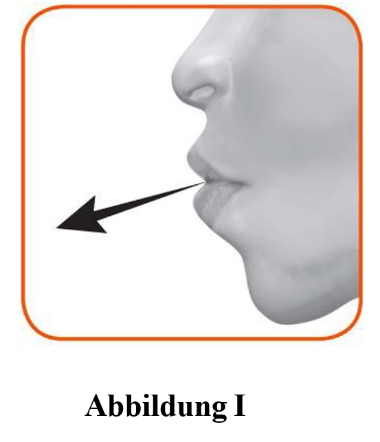 |
2.2 |
Halten Sie Ihren Kopf aufrecht, nehmen Sie das Mundstück zwischen Ihre Lippen und umschließen Sie es eng mit Ihren Lippen (Abbildung J).  |
2.3 |
Nehmen Sie einen kräftigen, tiefen Atemzug durch Ihren Mund. Atmen Sie so lange wie möglich ein.  |
2.4 |
Nehmen Sie den Inhalator aus Ihrem Mund. |
2.5 |
Halten Sie Ihren Atem so lange wie möglich an. |
2.6 |
Atmen Sie langsam und von Ihrem Inhalator weggerichtet aus. |
 |
Überprüfen Sie:
2.7 |
Vergewissern Sie sich, dass das Kontrollfenster nun rot ist (Abbildung K). Das bedeutet, dass Sie Ihr Arzneimittel richtig inhaliert haben.  |
 |
|
|
Setzen Sie nach jeder Anwendung die Schutzkappe zurück auf das Mundstück (Abbildung M), um einer Verschmutzung Ihres Inhalators durch z. B. Staub vorzubeugen. Entsorgen Sie Ihren Inhalator, wenn Sie die Kappe verlieren.  |
Weitere Informationen:
Was sollen Sie tun, wenn Sie versehentlich eine Dosis vorbereitet haben?
Bewahren Sie Ihren Inhalator mit der aufgesetzten Schutzkappe auf, bis es Zeit ist, Ihr Arzneimittel zu inhalieren. Dann ziehen Sie die Kappe ab und beginnen mit Schritt 1.6.
Wie funktioniert die Dosisanzeige?
Die Dosisanzeige zeigt die Gesamtanzahl an Dosen an, die noch im Inhalator enthalten sind (Abbildung N).
Vor der ersten Anwendung enthält jeder Inhalator mindestens 60 Dosen oder mindestens 30 Dosen, je nach Packungsgröße.
Jedes Mal, wenn Sie eine Dosis laden, indem Sie die orange Taste drücken, bewegt sich die
Dosisanzeige ein kleines Stück in Richtung der nächsten Nummer (50, 40, 30, 20, 10 oder 0).
Wann benötigen Sie einen neuen Inhalator?
Sie sollten einen neuen Inhalator besorgen:
Wenn Ihr Inhalator beschädigt zu sein scheint oder wenn Sie die Kappe verlieren, oder
Wenn rote Streifen in der Dosisanzeige erscheinen; dies bedeutet, dass die letzte Dosis bald erreicht ist (Abbildung N), oder
Wenn Ihr Inhalator leer ist (Abbildung O).

Wie sehen Sie, dass Ihr Inhalator leer ist?
Wenn die orange Taste nicht in ihre oberste Position zurückgeht und stattdessen in einer mittleren Position stehen bleibt, haben Sie die letzte Dosis erreicht (Abbildung O). Auch wenn die orange Taste blockiert ist, können Sie Ihre letzte Dosis noch inhalieren. Danach kann der Inhalator nicht mehr verwendet werden und Sie müssen mit der Anwendung eines neuen Inhalators beginnen.

Wie sollen Sie Ihren Inhalator reinigen?
Verwenden Sie NIEMALS Wasser um Ihren Inhalator zu reinigen, da das enthaltene Arzneimittel dadurch beeinträchtigt werden könnte.
Falls Sie Ihren Inhalator dennoch reinigen möchten, wischen Sie mit einem trockenen Tuch oder Papiertuch über die Außenseite des Mundstücks.
Covis Pharma Europe B.V.
Gustav Mahlerplein 2
1082MA Amsterdam
Niederlande
EU/1/14/964/001
EU/1/14/964/002
EU/1/14/964/003
Datum der Erteilung der Zulassung: 19. November 2014
Datum der letzten Verlängerung: 23. August 2019
Juli 2025
Ausführliche Informationen zu diesem Arzneimittel sind auf den Internetseiten der Europäischen Arzneimittel-Agentur unter http://www.ema.europa.eu/ verfügbar.