TUKYSA® 50 mg Filmtabletten
TUKYSA® 150 mg Filmtabletten
TUKYSA 50 mg Filmtabletten
Jede Filmtablette enthält 50 mg Tucatinib.
TUKYSA 150 mg Filmtabletten
Jede Filmtablette enthält 150 mg Tucatinib.
Sonstige Bestandteile mit bekannter Wirkung
Jede 150‑mg‑Filmtablette enthält 27,64 mg Natrium und 30,29 mg Kalium.
Eine 300‑mg‑Dosis TUKYSA enthält 55,3 mg Natrium und 60,6 mg Kalium.
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
Filmtablette (Tablette).
TUKYSA 50 mg Filmtabletten
Runde, gelbe Filmtablette mit der Prägung „TUC“ auf einer Seite und „50“ auf der anderen Seite. Die 50‑mg‑Tablette hat einen Durchmesser von ca. 8 mm.
TUKYSA 150 mg Filmtabletten
Ovale, gelbe Filmtablette mit der Prägung „TUC“ auf einer Seite und „150“ auf der anderen Seite. Die 150‑mg‑Tablette ist ca. 17 mm lang und 7 mm breit.
TUKYSA wird angewendet in Kombination mit Trastuzumab und Capecitabin zur Behandlung von erwachsenen Patienten mit HER2-positivem lokal fortgeschrittenem oder metastasiertem Brustkrebs, die zuvor mindestens 2 gegen HER2 gerichtete Behandlungsschemata erhalten haben.
Die Behandlung mit TUKYSA sollte von einem Arzt eingeleitet und überwacht werden, der in der Anwendung von Arzneimitteln gegen Krebs erfahren ist.
Dosierung
Die empfohlene Dosis beträgt 300 mg Tucatinib (zwei 150‑mg‑Tabletten), die kontinuierlich zweimal täglich in Kombination mit Trastuzumab und Capecitabin wie in der in Tabelle 1 beschriebenen Dosierung eingenommen werden. Weitere Informationen sind in den Fachinformationen der gleichzeitig angewendeten Arzneimittel Trastuzumab und Capecitabin zu finden. Die Bestandteile der Behandlung können in beliebiger Reihenfolge verabreicht werden.
Tabelle 1: Empfohlene Dosierung
Behandlung |
Dosis |
Behandlungstage |
Zeitpunkt relativ zur Nahrungsaufnahme |
Tucatinib |
300 mg oral |
Kontinuierlich |
Unabhängig von den Mahlzeiten |
Capecitabin |
1 000 mg/m2 oral |
Tag 1 bis 14 alle 21 Tage |
Innerhalb von 30 Minuten nach einer Mahlzeit |
Trastuzumab |
|||
Intravenöse Gabe |
Nicht zutreffend |
||
Initialdosis |
8 mg/kg intravenös |
Tag 1 |
|
Nachfolgende Dosen |
6 mg/kg intravenös |
Alle 21 Tage |
|
ODER |
600 mg subkutan |
Alle 21 Tage |
Die Behandlung mit TUKYSA sollte bis zur Krankheitsprogression oder bis zum Auftreten einer nicht vertretbaren Toxizität fortgesetzt werden.
Ausgelassene Dosen
Falls eine Dosis ausgelassen wurde, sollte der Patient die nächste Dosis zur regulär geplanten Zeit einnehmen.
Dosisanpassung
Die empfohlenen Anpassungen der Tucatinib-Dosis für Patienten mit Nebenwirkungen (siehe Abschnitt 4.8) sind in den Tabellen 2 und 3 angegeben. Bezüglich Dosisanpassungen bei Toxizitäten, die mutmaßlich durch das gleichzeitig verabreichte Trastuzumab und Capecitabin hervorgerufen wurden, sind die Fachinformationen dieser Arzneimittel zu konsultieren.
Tabelle 2: Empfohlene Reduktionen der Tucatinib-Dosis bei Nebenwirkungen
Dosisstufe |
Tucatinib-Dosis |
Empfohlene Anfangsdosis |
300 mg zweimal täglich |
Erste Dosisreduktion |
250 mg zweimal täglich |
Zweite Dosisreduktion |
200 mg zweimal täglich |
Dritte Dosisreduktion |
150 mg zweimal täglich1 |
1. Bei Patienten, die 150 mg oral zweimal täglich nicht vertragen, sollte TUKYSA dauerhaft abgesetzt werden.
Tabelle 3: Empfohlene Anpassungen der Tucatinib-Dosis bei Nebenwirkungen
Nebenwirkung |
Schweregrad1 |
Anpassung der Tucatinib-Dosis |
Diarrhö |
Grad 1 und 2 |
Keine Dosisanpassung erforderlich. |
Grad 3 ohne Antidiarrhoika-Behandlung |
Geeignete medizinische Therapie einleiten oder intensivieren. Einnahme von Tucatinib bis zum Rückgang auf ≤ Grad 1 unterbrechen, anschließend Tucatinib-Behandlung auf derselben Dosisstufe fortsetzen. |
|
Grad 3 mit Antidiarrhoika-Behandlung |
Geeignete medizinische Therapie einleiten oder intensivieren. Einnahme von Tucatinib bis zum Rückgang auf ≤ Grad 1 unterbrechen, anschließend Tucatinib-Behandlung auf der nächstniedrigen Dosisstufe fortsetzen. |
|
Grad 4 |
Tucatinib dauerhaft absetzen. |
|
ALT, AST oder Gesamtbilirubin erhöht2 |
Grad 1 Bilirubin (> ULN bis 1,5 × ULN) |
Keine Dosisanpassung erforderlich. |
Grad 2 Bilirubin (> 1,5 bis 3 × ULN) |
Einnahme von Tucatinib bis zum Rückgang auf ≤ Grad 1 unterbrechen, anschließend Tucatinib-Behandlung auf der gleichen Dosisstufe fortsetzen. |
|
Grad 3 ALT oder AST (> 5 bis 20 × ULN) |
Einnahme von Tucatinib bis zum Rückgang auf ≤ Grad 1 unterbrechen, anschließend Tucatinib-Behandlung auf der nächstniedrigen Dosisstufe fortsetzen. |
|
Grad 4 ALT oder AST (> 20 × ULN) |
Tucatinib dauerhaft absetzen. |
|
ALT oder AST > 3 × ULN) |
Tucatinib dauerhaft absetzen. |
|
Sonstige Nebenwirkungen |
Grad 1 und 2 |
Keine Dosisanpassung erforderlich. |
Grad 3 |
Einnahme von Tucatinib bis zum Rückgang auf ≤ Grad 1 unterbrechen, anschließend Tucatinib-Behandlung auf der nächstniedrigen Dosisstufe fortsetzen. |
|
Grad 4 |
Tucatinib dauerhaft absetzen. |
1. Schweregrade basierend auf den allgemeinen Terminologiekriterien für unerwünschte Ereignisse (Common Terminology Criteria for Adverse Events) des National Cancer Institute, Version 4.03
2. Abkürzungen: ULN = obere Normgrenze (upper limit of normal); ALT = Alaninaminotransferase; AST = Aspartataminotransferase
Gleichzeitige Gabe mit CYP2C8‑Inhibitoren
Eine gleichzeitige Anwendung mit starken CYP2C8‑Inhibitoren ist zu vermeiden. Lässt sich die Anwendung zusammen mit einem starken CYP2C8‑Inhibitor nicht vermeiden, sollte die Anfangsdosis von Tucatinib auf 100 mg oral zweimal täglich verringert werden. Nach Absetzen des starken CYP2C8‑Inhibitors seit 3 Eliminationshalbwertszeiten sollte Tucatinib wieder in der Dosierung wie vor Beginn der Behandlung mit dem Inhibitor eingenommen werden (siehe Abschnitte 4.4 und 4.5). Bei Anwendung zusammen mit moderaten CYP2C8‑Inhibitoren sollte die Überwachung auf Nebenwirkungen von TUKYSA verstärkt werden.
Besondere Patientengruppen
Ältere Patienten
Es ist keine Dosisanpassung bei Patienten ab 65 Jahren erforderlich (siehe Abschnitt 5.2). Bei Patienten über 80 Jahren wurde Tucatinib nicht untersucht.
Nierenfunktionsstörung
Bei Patienten mit leichter, mittelschwerer oder schwerer Nierenfunktionsstörung ist keine Dosisanpassung erforderlich (siehe Abschnitt 5.2).
Leberfunktionsstörung
Bei Patienten mit leichter oder mittelschwerer Leberfunktionsstörung ist keine Dosisanpassung erforderlich (siehe Abschnitt 5.2). Für Patienten mit schwerer Funktionsstörung der Leber (Child-Pugh C) wird eine reduzierte Anfangsdosis von 200 mg (zweimal täglich oral) empfohlen.
Kinder und Jugendliche
Die Sicherheit und Wirksamkeit von TUKYSA bei Kindern und Jugendlichen ist nicht erwiesen. Es liegen keine Daten vor.
Art der Anwendung
TUKYSA ist zum Einnehmen. Die Tabletten sind im Ganzen zu schlucken und sollten vorher nicht gekaut, zerkleinert oder geteilt werden (siehe Abschnitt 5.2).
TUKYSA soll ungefähr im Abstand von 12 Stunden jeden Tag zur gleichen Zeit unabhängig von den Mahlzeiten eingenommen werden. TUKYSA kann gleichzeitig mit Capecitabin eingenommen werden.
Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
Laboruntersuchungen
ALT, AST und Bilirubin erhöht
Während der Behandlung mit Tucatinib wurde über erhöhte ALT-, AST- und Bilirubinwerte berichtet (siehe Abschnitt 4.8). ALT, AST und Gesamtbilirubin sollten alle drei Wochen oder bei klinischer Indikation überwacht werden. Je nach Schweregrad der Nebenwirkung sollte die Behandlung mit Tucatinib unterbrochen werden, anschließend sollte die Dosis verringert oder die Behandlung dauerhaft abgesetzt werden (siehe Abschnitt 4.2).
Kreatinin ohne beeinträchtigte Nierenfunktion erhöht
Aufgrund der Hemmung des renalen tubulären Transports von Kreatinin kam es zu einem Anstieg des Serumkreatinins (durchschnittlicher Anstieg: 30 %) ohne Beeinflussung der glomerulären Funktion (siehe Abschnitt 4.8). Nicht auf Kreatinin beruhende alternative Marker wie BUN, Cystatin C oder die berechnete glomeruläre Filtrationsrate (GFR) können zur Ermittlung einer möglicherweise beeinträchtigten Nierenfunktion herangezogen werden.
Diarrhö
Während der Behandlung mit Tucatinib wurde über Diarrhö, auch über schwere Fälle mit Dehydratation, Hypotonie, akuter Nierenschädigung und Tod berichtet (siehe Abschnitt 4.8). Sofern klinisch angezeigt, sollten bei Diarrhö Antidiarrhoika angewendet werden. Bei einer Diarrhö mit Schweregrad ≥ 3 sollte die Behandlung mit Tucatinib unterbrochen werden; anschließend sollte die Dosis verringert oder die Behandlung dauerhaft abgesetzt werden (siehe Abschnitt 4.2). Wenn eine persistierende Diarrhö mit Schweregrad 2 zusammen mit Übelkeit und/oder Erbrechen mit Schweregrad ≥ 2 auftritt, sollte ebenfalls umgehend eine medizinische Behandlung eingeleitet werden. Je nach klinischer Indikation sollten diagnostische Tests durchgeführt werden, um bei Diarrhö mit Schweregrad 3 oder 4 bzw. bei einer Diarrhö beliebigen Schweregrads mit erschwerenden Begleitumständen (Dehydratation, Fieber, Neutropenie) infektiöse Ursachen auszuschließen.
Embryo-fetale Toxizität
Ausgehend von den Ergebnissen tierexperimenteller Studien und seinem Wirkmechanismus kann Tucatinib bei Anwendung an Schwangeren schädliche Wirkungen auf den Fetus haben. In tierexperimentellen Reproduktionsstudien führte die Verabreichung von Tucatinib an trächtige Kaninchen während der Organogenese zu Anomalien bei den Feten. Die Exposition der Muttertiere war dabei ähnlich der klinischen Exposition bei empfohlener Dosierung.
Schwangere sollten über das mögliche Risiko für das ungeborene Kind unterrichtet werden. Frauen im gebärfähigen Alter sollten angewiesen werden, während und bis zu mindestens 1 Woche nach der letzten Dosis der Behandlung eine wirksame Verhütungsmethode anzuwenden (siehe Abschnitt 4.6). Männer mit Partnerinnen im gebärfähigen Alter sollten ebenfalls angewiesen werden, im Zeitraum während und bis zu mindestens 1 Woche nach der letzten Dosis der Behandlung auf wirksame Weise zu verhüten.
Sensitive CYP3A‑Substrate
Tucatinib ist ein starker CYP3A‑Inhibitor. Folglich besitzt Tucatinib das Potenzial für Wechselwirkungen mit Arzneimitteln, die durch CYP3A metabolisiert werden, was zu erhöhten Plasmakonzentrationen des anderen Arzneimittels führen kann (siehe Abschnitt 4.5). Wird Tucatinib gleichzeitig mit anderen Arzneimitteln verabreicht, so ist bezüglich Empfehlungen für die gemeinsame Anwendung mit CYP3A‑Inhibitoren die jeweilige Fachinformation des anderen Arzneimittels zu konsultieren. Eine gleichzeitige Behandlung mit Tucatinib und CYP3A‑Substraten ist zu vermeiden, wenn minimale Konzentrationsänderungen zu schwerwiegenden oder lebensbedrohlichen Nebenwirkungen führen können. Ist eine solche gemeinsame Anwendung unvermeidlich, sollte die Dosis des CYP3A‑Substrats gemäß der Fachinformation des gleichzeitig verabreichten Arzneimittels verringert werden.
P‑gp‑Substrate
Die gleichzeitige Anwendung von Tucatinib mit einem P‑gp‑Substrat führte zu einer Erhöhung der Plasmakonzentrationen dieses Substrats, was die mit P‑gp‑Substraten assoziierte Toxizität verstärken könnte. Es sollte eine Dosisreduktion von P‑gp‑Substraten (einschließlich sensitiver intestinaler Substrate wie Dabigatran) gemäß der Fachinformation des gleichzeitig verabreichten Arzneimittels in Erwägung gezogen werden, und P‑gp‑Substrate sind mit Vorsicht zu verabreichen, wenn minimale Konzentrationsänderungen zu schwerwiegenden oder lebensbedrohlichen Nebenwirkungen führen können.
Starke CYP3A-/moderate CYP2C8‑Induktoren
Die gemeinsame Anwendung von Tucatinib mit einem starken CYP3A- oder einem moderaten CYP2C8‑Induktor führte zu einer Verringerung der Tucatinib-Konzentrationen, wodurch die Wirkung von Tucatinib vermindert sein könnte. Eine gleichzeitige Anwendung mit einem starken CYP3A‑Induktor oder einem moderaten CYP2C8‑Induktor sollte vermieden werden.
Starke/moderate CYP2C8‑Inhibitoren
Die gemeinsame Anwendung von Tucatinib mit einem starken CYP2C8‑Inhibitor führte zu einer Erhöhung der Tucatinib-Konzentrationen, was das Risiko einer durch Tucatinib bedingten Toxizität erhöhen kann. Eine gleichzeitige Anwendung mit starken CYP2C8‑Inhibitoren sollte vermieden werden (siehe Abschnitt 4.2).
Es liegen keine klinischen Daten vor zur Auswirkung der gemeinsamen Anwendung von moderaten CYP2C8‑Inhibitoren auf die Tucatinib-Konzentrationen. Bei moderaten CYP2C8‑Inhibitoren sollte die Überwachung des Patienten auf Nebenwirkungen von Tucatinib verstärkt werden.
Informationen über sonstige Bestandteile
Dieses Arzneimittel enthält 55,3 mg Natrium pro 300‑mg‑Dosis. Dies entspricht 2,75 % der für einen Erwachsenen empfohlenen maximalen täglichen Natriumaufnahme mit der Nahrung.
Dieses Arzneimittel enthält 60,6 mg Kalium pro 300‑mg‑Dosis. Dies ist zu berücksichtigen bei Patienten mit eingeschränkter Nierenfunktion oder solchen, die eine kontrollierte Kalium-Diät (Diät mit niedrigem Kaliumgehalt) einhalten müssen.
Tucatinib wird vorwiegend über CYP2C8 metabolisiert. Es ist ein stoffwechselbasierter Inaktivator von CYP3A und hemmt die renalen Transporter von Metformin und Kreatinin. Tucatinib ist ein Substrat von P‑gp.
Wirkungen von anderen Arzneimitteln auf Tucatinib
CYP3A/CYP2C8‑Induktoren
Eine klinische Studie zur Erfassung von Arzneimittelwechselwirkungen ergab, dass die gleichzeitige Anwendung einer Einzeldosis von 300 mg Tucatinib mit Rifampicin (einem starken CYP3A- und moderaten CYP2C8‑Induktor) zu einer Verringerung der Tucatinib-Konzentrationen führte (0,6‑fache Cmax [90 %‑KI: 0,5; 0,8] und 0,5‑fache AUC [90 %‑KI: 0,4; 0,6]). Die gemeinsame Verabreichung von Tucatinib und starken CYP3A- oder moderaten CYP2C8‑Induktoren wie Rifampicin, Phenytoin, Johanniskraut oder Carbamazepin ist zu vermeiden, da dies die Wirkung von Tucatinib vermindern könnte (siehe Abschnitt 4.4).
CYP2C8‑Inhibitoren
Eine klinische Studie zur Erfassung von Arzneimittelwechselwirkungen ergab, dass die gleichzeitige Anwendung einer Einzeldosis von 300 mg Tucatinib mit Gemfibrozil (einem starken CYP2C8‑Inhibitor) zu erhöhten Tucatinib-Konzentrationen führte (1,6‑fache Cmax [90 %‑KI: 1,5; 1,8] und 3,0‑fache AUC [90 %‑KI: 2,7; 3,5]). Die gemeinsame Verabreichung von Tucatinib und starken CYP2C8‑Inhibitoren wie Gemfibrozil ist zu vermeiden, da dies das Risiko einer durch Tucatinib bedingten Toxizität erhöhen könnte (siehe Abschnitt 4.4).
CYP3A‑Inhibitoren
Eine klinische Studie zur Erfassung von Arzneimittelwechselwirkungen ergab, dass die gleichzeitige Anwendung einer Einzeldosis von 300 mg Tucatinib mit Itraconazol (einem starken CYP3A‑Inhibitor) zu erhöhten Tucatinib-Konzentrationen führte (1,3‑fache Cmax [90 %‑KI: 1,2; 1,4] und 1,3‑fache AUC [90 %‑KI: 1,3; 1,4]). Eine Dosisanpassung ist nicht erforderlich.
Protonenpumpenhemmer
Ausgehend von klinischen Studien zur Erfassung von Wechselwirkungen, die mit Tucatinib durchgeführt wurden, konnten bei der Kombination von Tucatinib und Omeprazol (einem Protonenpumpenhemmer) keine Arzneimittelwechselwirkungen festgestellt werden. Eine Dosisanpassung ist nicht erforderlich.
Wirkungen von Tucatinib auf andere Arzneimittel
CYP3A‑Substrate
Tucatinib ist ein starker CYP3A‑Inhibitor. Eine klinische Studie zur Erfassung von Arzneimittelwechselwirkungen ergab, dass die gleichzeitige Anwendung von Tucatinib und Midazolam (einem sensitiven CYP3A‑Substrat) zu erhöhten Midazolam-Konzentrationen führte (3,0‑fache Cmax [90 %‑KI: 2,6; 3,4] und 5,7‑fache AUC [90 %‑KI: 5,0; 6,5]). Durch die gleichzeitige Verabreichung von Tucatinib mit sensitiven CYP3A‑Substraten wie Alfentanil, Avanafil, Buspiron, Darifenacin, Darunavir, Ebastin, Everolimus, Ibrutinib, Lomitapid, Lovastatin, Midazolam, Naloxegol, Saquinavir, Simvastatin, Sirolimus, Tacrolimus, Tipranavir, Triazolam und Vardenafil können sich die systemischen Expositionen dieser Substrate erhöhen, wodurch die mit dem CYP3A‑Substrat verbundene Toxizität zunehmen kann. Eine gleichzeitige Anwendung von Tucatinib und CYP3A‑Substraten sollte vermieden werden, wenn minimale Konzentrationsänderungen zu schwerwiegenden oder lebensbedrohlichen Nebenwirkungen führen können. Ist eine solche gemeinsame Anwendung unvermeidlich, sollte die Dosis des CYP3A‑Substrats gemäß der Fachinformation des gleichzeitig verabreichten Arzneimittels verringert werden.
P‑gp‑Substrate
Eine klinische Studie zur Erfassung von Arzneimittelwechselwirkungen ergab, dass die gleichzeitige Anwendung von Tucatinib und Digoxin (einem sensitiven P‑gp‑Substrat) zu erhöhten Digoxin-Konzentrationen führte (2,4‑fache Cmax [90 %‑KI: 1,9; 2,9] und 1,5‑fache AUC [90 %‑KI: 1,3; 1,7]). Die gleichzeitige Anwendung von Tucatinib mit einem P‑gp‑Substrat könnte zu einer Erhöhung der Plasmakonzentrationen dieses Substrats führen, was möglicherweise die mit dem P‑gp‑Substrat assoziierte Toxizität verstärkt. Es sollte eine Dosisreduktion von P‑gp‑Substraten (einschließlich sensitiver intestinaler Substrate wie Dabigatran) gemäß der Fachinformation des gleichzeitig verabreichten Arzneimittels in Erwägung gezogen werden, und P‑gp‑Substrate sind mit Vorsicht zu verabreichen, wenn minimale Konzentrationsänderungen zu schwerwiegenden oder lebensbedrohlichen Nebenwirkungen führen können (siehe Abschnitt 4.4).
CYP2C8‑Substrate
Eine klinische Studie zur Erfassung von Arzneimittelwechselwirkungen ergab, dass die gleichzeitige Anwendung von Tucatinib und Repaglinid (einem CYP2C8‑Substrat) zu erhöhten Repaglinid-Konzentrationen führte (1,7‑fache Cmax [90 %‑KI: 1,4; 2,1] und 1,7‑fache AUC [90 %‑KI: 1,5; 1,9]). Eine Dosisanpassung ist nicht erforderlich.
MATE1/2K‑Substrate
Eine klinische Studie zur Erfassung von Arzneimittelwechselwirkungen ergab, dass die gleichzeitige Anwendung von Tucatinib und Metformin (einem MATE1/2‑K‑Substrat) zu erhöhten Metformin-Konzentrationen führte (1,1‑fache Cmax [90 %‑KI: 1,0; 1,2] und 1,4‑fache AUC [90 %‑KI: 1,2; 1,5]). Durch Tucatinib verringerte sich die renale Clearance von Metformin ohne Auswirkungen auf die GFR, gemessen anhand der Iohexol-Clearance und des Cystatin C im Serum. Eine Dosisanpassung ist nicht erforderlich.
CYP2C9‑Substrate
Ausgehend von klinischen Studien zur Erfassung von Wechselwirkungen, die mit Tucatinib durchgeführt wurden, wurden bei der Kombination von Tucatinib und Tolbutamid (einem sensitiven CYP2C9‑Substrat) keine Arzneimittelwechselwirkungen festgestellt. Eine Dosisanpassung ist nicht erforderlich.
Frauen im gebärfähigen Alter/Verhütung bei Männern und Frauen
Erfahrungen an Tieren zeigen, dass eine Anwendung von Tucatinib während der Schwangerschaft zu gesundheitsschädlichen pharmakologischen Wirkungen beim ungeborenen und/oder beim neugeborenen Kind führen könnte. Frauen im gebärfähigen Alter sollten angewiesen werden, eine Schwangerschaft zu vermeiden sowie während und bis zu mindestens 1 Woche nach der Behandlung eine wirksame Verhütungsmethode anzuwenden. Männliche Patienten mit Partnerinnen im gebärfähigen Alter sollten ebenfalls angewiesen werden, im Zeitraum während und bis zu mindestens 1 Woche nach der Behandlung zuverlässig zu verhüten (siehe Abschnitt 4.4).
Siehe auch Abschnitt 4.6 der Fachinformationen von Trastuzumab und Capecitabin.
Schwangerschaft
Bisher liegen keine Erfahrungen mit der Anwendung von Tucatinib bei Schwangeren vor. Tierexperimentelle Studien haben eine Reproduktionstoxizität gezeigt (siehe Abschnitt 5.3). TUKYSA darf während der Schwangerschaft nicht angewendet werden, es sei denn, dass eine Behandlung mit Tucatinib aufgrund des klinischen Zustandes der Frau erforderlich ist. Bei Frauen im gebärfähigen Alter sollte vor Beginn der Behandlung mit Tucatinib der Schwangerschaftsstatus überprüft werden. Sollte die Patientin während der Behandlung schwanger werden, so muss ihr die mögliche Gefahr für das ungeborene/neugeborene Kind erläutert werden.
Stillzeit
Es ist nicht bekannt ob Tucatinib/Metabolite in die Muttermilch übergehen. Ein Risiko für das Neugeborene/Kind kann nicht ausgeschlossen werden. Das Stillen soll während der Behandlung mit TUKYSA unterbrochen werden. Eine Woche nach der Behandlung kann das Stillen fortgesetzt werden.
Fertilität
Es wurden keine Fertilitätsstudien bei Männern oder Frauen durchgeführt. Ausgehend von den Ergebnissen tierexperimenteller Studien kann Tucatinib die Fertilität von Frauen im gebärfähigen Alter beeinträchtigen (siehe Abschnitt 5.3).
TUKYSA hat keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen. Bei der Beurteilung, ob der Patient zur Durchführung von Aufgaben, bei denen Urteilungsvermögen sowie motorische oder kognitive Fähigkeiten erforderlich sind, in der Lage ist, sollte der klinische Zustand des Patienten berücksichtigt werden.
Zusammenfassung des Sicherheitsprofils
Die am häufigsten (≥ 5 %) während der Behandlung berichteten Nebenwirkungen mit Schweregrad 3 oder 4 sind Diarrhö (13 %), erhöhter ALT-Wert (6 %) und erhöhter AST-Wert (5 %).
Schwerwiegende Nebenwirkungen traten bei 29 % der mit Tucatinib behandelten Patienten auf und umfassten Diarrhö (4 %), Erbrechen (3 %) und Übelkeit (2 %).
Bei 6 % der Patienten traten Nebenwirkungen auf, die zum Absetzen von TUKYSA führten; die häufigsten dieser zum Behandlungsabbruch führenden Nebenwirkungen waren Diarrhö (1 %) und erhöhte ALT-Werte (1 %). Nebenwirkungen, die zu einer Dosisreduktion von TUKYSA führten, traten bei 23 % der Patienten auf; die häufigsten zu einer Dosisreduktion führenden Nebenwirkungen waren Diarrhö (6 %), erhöhte ALT-Werte (5 %) und erhöhte AST-Werte (4 %).
Tabellarische Auflistung der Nebenwirkungen
Die in diesem Abschnitt zusammengefassten Daten stammen aus der Anwendung von TUKYSA bei 431 Patienten mit lokal fortgeschrittenem, inoperablem oder metastasiertem HER‑2-positivem Brustkrebs, die TUKYSA in Kombination mit Trastuzumab und Capecitabin im Rahmen zweier Studien – HER2CLIMB und ONT‑380‑005 – erhalten hatten (siehe Abschnitt 5.1). Die mediane Dauer der Exposition gegenüber TUKYSA betrug in diesen Studien 7,4 Monate (Streubreite: < 0,1; 43,6).
In diesem Abschnitt sind die unter der Behandlung beobachteten Nebenwirkungen nach Häufigkeitskategorie aufgeführt. Die Häufigkeitskategorien sind wie folgt definiert: sehr häufig (≥ 1/10); häufig (≥ 1/100, < 1/10); gelegentlich (≥ 1/1 000, < 1/100); selten (≥ 1/10 000, < 1/1 000); sehr selten (< 1/10 000); nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar).
Tabelle 4: Nebenwirkungen
Systemorganklasse |
Häufigkeit |
Nebenwirkung |
Erkrankungen der Atemwege, des Brustraums und Mediastinums |
Sehr häufig |
Epistaxis |
Erkrankungen des Gastrointestinaltrakts |
Sehr häufig |
Diarrhö, Übelkeit, Erbrechen, Stomatitis1 |
Erkrankungen der Haut und des Unterhautgewebes |
Sehr häufig |
Ausschlag2 |
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen |
Sehr häufig |
Arthralgie |
Untersuchungen |
Sehr häufig |
AST erhöht, ALT erhöht, Bilirubin im Blut erhöht3, Gewichtsabnahme |
Stomatitis umfasst Stomatitis, oropharyngeale Schmerzen, Ulzeration im Mund, Schmerzen im Mund, Ulzeration an den Lippen, Glossodynie, Blasenbildung an der Zunge, Lippenbläschen, orale Dysästhesie, Ulzeration an der Zunge, aphthöse Ulzera
Ausschlag umfasst makulopapulöses Exanthem, Exanthem, akneiforme Dermatitis, Erythem, makulöses Exanthem, papulöses Exanthem, pustulöses Exanthem, pruritisches Exanthem, erythematösen Ausschlag, Exfoliation der Haut, Urtikaria, allergische Dermatitis, Palmarerythem, Plantarerythem und Hauttoxizität
Eine Erhöhung des Bilirubinwerts im Blut umfasste auch Hyperbilirubinämie.
Beschreibung ausgewählter Nebenwirkungen
ALT, AST oder Bilirubin erhöht
Im Rahmen der Studie HER2CLIMB traten bei 41 % der Patienten, die mit Tucatinib in Kombination mit Trastuzumab und Capecitabin behandelt wurden, erhöhte ALT-, AST- oder Bilirubinwerte auf. Bei 9 % der Patienten traten Ereignisse mit Schweregrad 3 und höher auf. Erhöhte ALT-, AST- und Bilirubinwerte führten bei 9 % der Patienten zu einer Dosisreduktion und bei 1,5 % zu einem Behandlungsabbruch. Der Median der Zeit bis zum erstmaligen Auftreten erhöhter ALT-, AST- oder Bilirubinwerte beliebigen Schweregrades betrug 37 Tage; in 84 % der Fälle normalisierten sich die Werte wieder, was im Median 22 Tage dauerte. Eine Überwachung und Dosisanpassung (einschließlich Absetzen der Behandlung) sind zu erwägen (siehe Abschnitt 4.4).
Diarrhö
Im Rahmen der Studie HER2CLIMB trat bei 82 % der Patienten, die mit Tucatinib in Kombination mit Trastuzumab und Capecitabin behandelt wurden, eine Diarrhö auf. Bei 13 % der Patienten war der Schweregrad der Diarrhö 3 oder höher. Zwei Patienten, die eine Grad‑4-Diarrhö entwickelten, verstarben anschließend, wobei die Diarrhö zum Tod beitrug. Diarrhö führte bei 6 % der Patienten zu einer Dosisreduktion und bei 1 % zu einem Behandlungsabbruch. Im Median betrug die Zeit bis zum erstmaligen Auftreten einer Diarrhö beliebigen Schweregrades 12 Tage; 81 % der Diarrhö-Ereignisse klangen wieder ab, was im Median 8 Tage dauerte. Eine prophylaktische Anwendung von Antidiarrhoika war nicht erforderlich. Bei weniger als der Hälfte der Behandlungszyklen, in denen über Diarrhöfälle berichtet wurde, kamen Antidiarrhoika zum Einsatz. Im Median wurden die Antidiarrhoika über 3 Tage pro Zyklus angewendet (siehe Abschnitt 4.4).
Erhöhte Kreatininwerte ohne beeinträchtigte Nierenfunktion
Bei Patienten, die mit Tucatinib behandelt wurden, kam es aufgrund der Hemmung des renalen tubulären Transports von Kreatinin zu einem Anstieg des Serumkreatinins ohne Beeinflussung der glomerulären Funktion. In klinischen Studien traten die Serumkreatininerhöhungen (durchschnittlicher Anstieg: 30 %) innerhalb des ersten Zyklus mit Tucatinib auf; während der Behandlung blieben die Werte erhöht, aber stabil und normalisierten sich nach dem Absetzen der Behandlung wieder.
Besondere Patientengruppen
Ältere Patienten
In der Studie HER2CLIMB waren 82 Patienten, die Tucatinib erhielten, ≥ 65 Jahre alt und 8 davon ≥ 75 Jahre. Schwerwiegende Nebenwirkungen traten bei 34 % der Patienten ≥ 65 Jahren auf, im Vergleich zu 28 % bei < 65‑jährigen Patienten. Die Anzahl der Patienten ≥ 75 Jahren war zu gering, um Unterschiede bezüglich der Sicherheit beurteilen zu können.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung über das aufgeführte nationale Meldesystem anzuzeigen.
Deutschland
Bundesinstitut für Arzneimittel und Medizinprodukte
Abt. Pharmakovigilanz
Kurt-Georg-Kiesinger-Allee 3
D-53175 Bonn
Website: https://www.bfarm.de
Österreich
Bundesamt für Sicherheit im Gesundheitswesen
Traisengasse 5
1200 WIEN
ÖSTERREICH
Fax: +43 (0) 50 555 36207
Website: https://www.basg.gv.at/
Es gibt kein spezifisches Antidot und es ist nicht bekannt, ob bei der Behandlung einer Überdosierung mit Tucatinib eine Hämodialyse von Nutzen ist. Im Falle einer Überdosierung sollte die Behandlung mit Tucatinib unterbrochen und allgemeine unterstützende Maßnahmen eingeleitet werden.
Pharmakotherapeutische Gruppe: Antineoplastische Mittel, Proteinkinase‑Inhibitoren, ATC-Code: L01EH03.
Wirkmechanismus
Tucatinib ist ein reversibler, potenter und selektiver Tyrosinkinase‑Inhibitor von HER2. In Tests zur zellulären Signalübertragung erwies sich Tucatinib als > 1 000‑fach selektiver für HER2 im Vergleich zum epidermalen Wachstumsfaktor-Rezeptor. In vitro hemmt Tucatinib die Phosphorylierung von HER2 und HER3, was zu einer Hemmung der nachgelagerten Zellsignalübertragung und Zellproliferation und infolgedessen zum Absterben von Tumorzellen, deren Wachstum durch HER2 gesteuert wird, führt. In vivo hemmt Tucatinib das Wachstum der durch HER2 beeinflussten Tumore und die Kombination aus Tucatinib und Trastuzumab zeigte im Vergleich zur alleinigen Anwendung jedes der Arzneimittel sowohl in vitro als auch in vivo eine verstärkte Antitumorwirkung.
Pharmakodynamische Wirkungen
Elektrophysiologie des Herzens
In einer TQT-Studie an gesunden Probanden wirkte sich die zweimal tägliche Gabe mehrerer Dosen von 300 mg Tucatinib nicht auf das QTc-Intervall aus.
Klinische Wirksamkeit und Sicherheit
Die Wirksamkeit von Tucatinib in Kombination mit Trastuzumab und Capecitabin wurde im Rahmen einer randomisierten, doppelblinden, placebokontrollierten, weltweiten Studie mit einem aktiven Vergleichspräparat beurteilt (HER2CLIMB). Die aufgenommenen Patienten hatten lokal fortgeschrittenen, inoperablen oder metastasierten HER2-positiven Brustkrebs mit oder ohne Hirnmetastasen und hatten zuvor im Rahmen einer neoadjuvanten, adjuvanten oder gegen die Metastasen gerichteten Behandlung Trastuzumab, Pertuzumab und Trastuzumab-Emtansin (T‑DM1) als Monotherapie oder in Kombination erhalten. Die HER2-Überexpression oder -Amplifikation wurde durch eine zentrale Laboranalyse bestätigt.
Patienten mit Hirnmetastasen, einschließlich solche mit unbehandelten oder progredienten Läsionen, kamen für eine Studienaufnahme infrage, vorausgesetzt sie waren neurologisch stabil und benötigten keine sofortige Bestrahlung oder Operation des Gehirns. Patienten, die eine sofortige lokale Intervention benötigten, konnten eine lokale Therapie erhalten und anschließend aufgenommen werden. Die Studie umfasste Patienten mit unbehandelten Hirnmetastasen und Patienten mit behandelten Hirnmetastasen, die seit der letzten Bestrahlung oder Operation des Gehirns entweder stabil oder progredient waren. Patienten waren von der Studie ausgeschlossen, wenn sie weniger als 28 Tage vor der ersten Dosis der Studienbehandlung systemische Kortikosteroide (Tagesgesamtdosis von ≥ 2 mg Dexamethason oder Äquivalent) zur Kontrolle der Symptome von ZNS-Metastasen erhalten hatten. Von der Studie ausgeschlossen waren auch Patienten mit leptomeningealer Erkrankung. Mit HER2-Tyrosinkinase‑Inhibitoren vorbehandelte Patienten waren ausgeschlossen, mit Ausnahme von Patienten, die Lapatinib über höchstens 21 Tage erhalten hatten und dieses Arzneimittel aus anderen Gründen als einer Krankheitsprogression oder einer schweren Toxizität abgesetzt hatten. Bei Patienten mit Hormonrezeptor-positiven Tumoren war eine endokrine Therapie als Begleittherapie nicht erlaubt, mit Ausnahme von Gonadotropin-Releasing-Hormon-Agonisten, die bei prämenopausalen Frauen zur Unterdrückung der Eierstockfunktion angewendet wurden.
Insgesamt 612 Patienten wurden im Verhältnis 2:1 randomisiert einer Behandlung mit Tucatinib in Kombination mit Trastuzumab und Capecitabin (n = 410) oder Placebo in Kombination mit Trastuzumab und Capecitabin (n = 202) zugeteilt. Die Randomisierung wurde nach dem aktuellen oder früheren Vorhandensein von Hirnmetastasen (ja vs. nein), dem Leistungsstatus gemäß Eastern Cooperative Oncology Group (ECOG) (0 vs. 1) und der Region (USA, Kanada oder restliche Welt) stratifiziert.
Die demographischen Merkmale der Patienten waren zwischen den Behandlungsarmen ausgeglichen. Der Median des Alters lag bei 54 Jahren (Streubreite: 25 bis 82); 116 (19 %) der Patienten waren 65 Jahre alt oder älter. 444 der Patienten waren weiß (73 %) und 607 waren weiblich (99 %). Der ECOG-Leistungsstatus der Patienten in der Studie hatte bei 314 (51 %) einen Wert von 1 und bei 298 (49 %) betrug dieser Wert 0. Eine Östrogen- und/oder Progesteronrezeptor-positive Erkrankung lag bei 60 % vor. Bei 48 % der Patienten waren Hirnmetastasen aktuell vorhanden oder anamnestisch bekannt; 23 % dieser Patienten hatten unbehandelte Hirnmetastasen, bei 40 % waren die Hirnmetastasen behandelt, aber stabil und 37 % wiesen behandelte, aber radiographisch progrediente Hirnmetastasen auf. Darüber hinaus zeigten 49 % der Patienten Lungenmetastasen, 35 % hatten Lebermetastasen und 14 % Hautmetastasen. Im Median hatten die Patienten zuvor 4 (Streubreite: 2 bis 17) Linien einer systemischen Therapie sowie 3 (Streubreite: 1 bis 14) Linien zur systemischen Therapie der metastasierten Erkrankung erhalten. Alle Patienten hatten zuvor Trastuzumab enthaltende Therapien und Trastuzumab-Emtansin erhalten, während alle bis auf zwei Patienten zuvor eine Pertuzumab enthaltende Therapie erhalten hatten.
Tucatinib (300 mg) oder Placebo wurde zweimal täglich eingenommen, und zwar bis zur Krankheitsprogression oder bis zum Auftreten einer nicht vertretbaren Toxizität. An Tag 1 von Zyklus 1 wurde Trastuzumab als Aufsättigungsdosis zu 8 mg/kg intravenös verabreicht, gefolgt von einer Erhaltungsdosis von 6 mg/kg an Tag 1 jedes nachfolgenden 21‑tägigen Zyklus. Eine andere Dosierungsmöglichkeit für Trastuzumab war eine Fixdosis von 600 mg, die subkutan an Tag 1 jedes 21‑Tage-Zyklus verabreicht wurde. Capecitabin (1 000 mg/m2 oral zweimal täglich) wurde an den Tagen 1 bis 14 jedes 21‑tägigen Zyklus gegeben.
Der primäre Endpunkt war das durch eine verblindete, unabhängige, zentrale Auswertung (blinded independent central review, BICR) ermittelte progressionsfreie Überleben (progression-free survival, PFS) bei den ersten 480 randomisierten Patienten. In dieser Population betrug die mediane Dauer der Exposition gegenüber Tucatinib 7,3 Monate (Streubreite: < 0,1; 35,1) für Patienten in der Gruppe mit Tucatinib + Trastuzumab + Capecitabin im Vergleich zu 4,4 Monaten (Streubreite: < 0,1; 24,0) unter Placebo für Patienten in der Gruppe mit Placebo + Trastuzumab + Capecitabin. Es wurden ähnliche Unterschiede in der Exposition gegenüber Trastuzumab und Capecitabin beobachtet.
Die sekundären Endpunkte wurden für alle randomisierten Patienten (n = 612) ausgewertet und umfassten das Gesamtüberleben (overall survival, OS), das PFS bei Patienten mit anamnestisch bekannten oder aktuell vorliegenden Hirnmetastasen (PFSHirnMets) sowie die bestätigte objektive Ansprechrate (objective response rate, ORR).
Die Ergebnisse bezüglich des primären und der wichtigsten sekundären Endpunkte stimmten über die vorab festgelegten Subgruppen hinweg überein: Hormonrezeptorstatus, aktuelles oder früheres Vorhandensein von Hirnmetastasen, ECOG-Status und Region. Das durch den Prüfarzt ermittelte PFS entsprach dem PFS, das durch BICR beurteilt wurde.
Die Wirksamkeitsergebnisse aus der primären Analyse sind in Tabelle 5 sowie in den Abbildungen 1 und 2 zusammengefasst.
Tabelle 5: Wirksamkeitsergebnisse aus der Studie HER2CLIMB (primäre Analyse)
Tucatinib + Trastuzumab + Capecitabin |
Placebo + Trastuzumab + Capecitabin |
||
PFS1 |
n = 320 |
n = 160 |
|
Anzahl der Ereignisse (%) |
178 (56) |
97 (61) |
|
Hazard Ratio (95%‑KI)2 |
0,54 (0,42; 0,71) |
||
p‑Wert3 |
< 0,00001 |
||
Median (Monate) (95%‑KI) |
7,8 (7,5; 9,6) |
5,6 (4,2; 7,1) |
|
OS |
n = 410 |
n = 202 |
|
Anzahl der Todesfälle, n (%) |
130 (32) |
85 (42) |
|
Hazard Ratio (95%‑KI)2 |
0,66 (0,50; 0,87) |
||
p‑Wert3 |
0,00480 |
||
Medianes OS (Monate) (95%‑KI) |
21,9 (18,3; 31,0) |
17,4 (13,6; 19,9) |
|
PFSHirnMets4 |
n = 198 |
n = 93 |
|
Anzahl der Ereignisse (%) |
106 (53,5) |
51 (54,8) |
|
Hazard Ratio (95%‑KI)2 |
0,48 (0,34; 0,69) |
||
p‑Wert3 |
< 0,00001 |
||
Median (Monate) (95%‑KI) |
7,6 (6,2; 9,5) |
5,4 (4,1; 5,7) |
|
Bestätigte ORR für Patienten mit messbarer Erkrankung |
n = 340 |
n = 171 |
|
ORR (95%‑KI)5 |
40,6 (35,3; 46,0) |
22,8 (16,7; 29,8) |
|
p‑Wert6 |
0,00008 |
||
CR (%) |
3 (0,9) |
2 (1,2) |
|
PR (%) |
135 (39,7) |
37 (21,6) |
|
DOR |
|||
Mediane DOR in Monaten (95%‑KI)7 |
8,3 (6,2; 9,7) |
6,3 (5,8,; 8,9) |
|
BICR = verblindete, unabhängige zentrale Auswertung (blinded independent central review); KI = Konfidenzintervall; PFS = progressionsfreies Überleben (progression-free survival); OS = Gesamtüberleben (overall survival); ORR = objektive Ansprechrate (objective response rate); CR = Vollremission (complete response); PR = Teilremission (partial response); DOR = Dauer des Ansprechens (duration of response).
Die primäre PFS-Analyse wurde bei den ersten 480 randomisierten Patienten durchgeführt. PFS basierend auf Kaplan-Meier-Analysen.
Hazard Ratio und 95%-Konfidenzintervalle basieren auf dem stratifizierten proportionalen Hazard-Regressionsmodell nach Cox zur Kontrolle von Stratifizierungsfaktoren (aktuelles oder früheres Vorhandensein von Hirnmetastasen, ECOG-Status und Weltregion).
Zweiseitiger p‑Wert beruhend auf dem Neurandomisierungsverfahren zur Kontrolle von Stratifizierungsfaktoren
Die Analyse umfasst Patienten mit anamnestisch bekannten oder aktuell vorliegenden parenchymalen Hirnmetastasen zu Studienbeginn, einschließlich Ziel- und Nicht-Ziel-Läsionen. Umfasst keine Patienten, die nur Duraläsionen aufweisen.
Zweiseitiges exaktes 95%‑Konfidenzintervall, berechnet mittels der Clopper-Pearson-Methode
Cochran-Mantel-Haenszel-Test zur Kontrolle der Stratifizierungsfaktoren (aktuelles oder früheres Vorhandensein von Hirnmetastasen, ECOG-Status und Weltregion)
Berechnet mittels der komplementären Loglog-Transformationsmethode
Abbildung 1. Kaplan‑Meier-Kurven des progressionsfreien Überlebens (gemäß BICR)
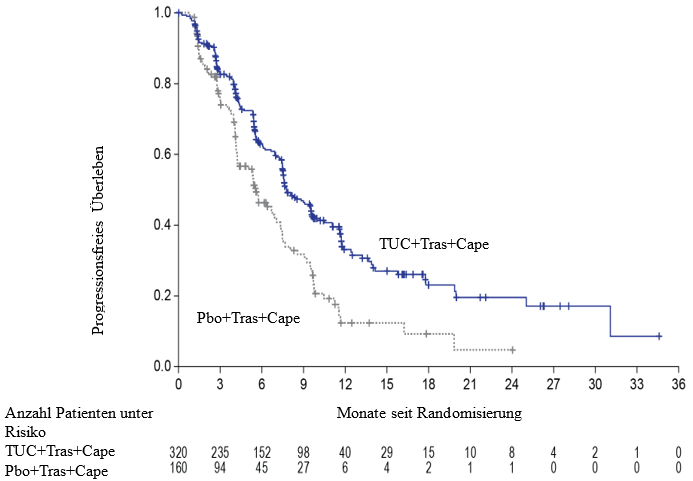
Abbildung 2. Kaplan Meier-Kurven des progressionsfreien Überlebens (gemäß BICR) bei Patienten mit Hirnmetastasen
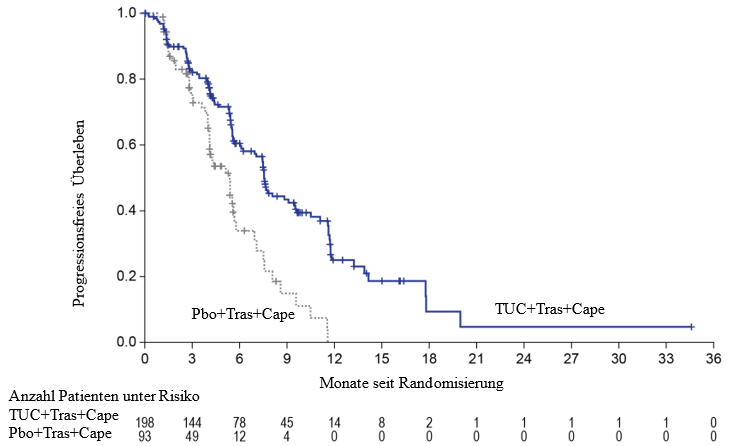
Wie im Prüfplan vorgesehen, wurde etwa zwei Jahre nach der Randomisierung des letzten Patienten die finale OS-Analyse auf der Grundlage von 370 Ereignissen durchgeführt, was einem medianen Follow-up von 29,6 Monaten entsprach. Das mediane OS betrug 24,7 Monate (95%‑KI: 21,6; 28,9) für Patienten im Tucatinib + Trastuzumab + Capecitabin-Arm im Vergleich zu 19,2 Monaten (95%‑KI: 16,4; 21,4) für Patienten im Placebo + Trastuzumab + Capecitabin-Arm (HR = 0,725; 95%‑KI: 0,585; 0,898). Die finale OS-Analyse ist in Abbildung 3 dargestellt.
Abbildung 3. Kaplan Meier-Kurven des Gesamtüberlebens (finale Analyse)
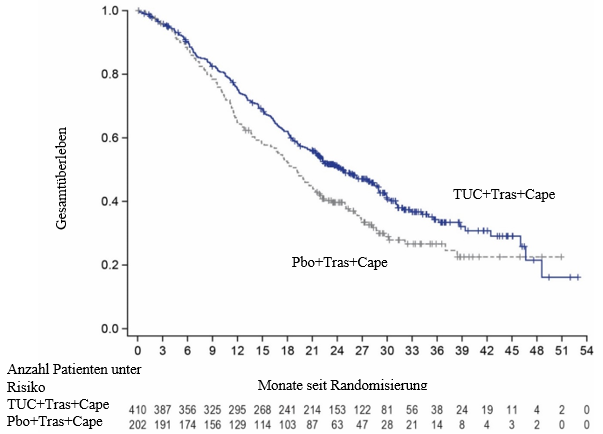
Kinder und Jugendliche
Die Europäische Arzneimittel-Agentur hat für TUKYSA eine Freistellung von der Verpflichtung zur Vorlage von Ergebnissen zu Studien in allen pädiatrischen Altersklassen bei malignen Neoplasmen der Brust gewährt (siehe Abschnitt 4.2 bzgl. Informationen zur Anwendung bei Kindern und Jugendlichen).
Die Plasmaexposition von Tucatinib (AUCinf und Cmax) stieg bei oralen Dosen von 50 bis 300 mg (dem 0,17‑ bis 1‑Fachen der empfohlenen Dosis) dosisproportional an. Nach zweimal täglicher Gabe von 300 mg Tucatinib über 14 Tage zeigte sich bezüglich der AUC eine 1,7‑fache Anreicherung von Tucatinib und eine 1,5‑fache Anreicherung für die Cmax. Die Zeit bis zum Erreichen des Steady-state betrug ca. 4 Tage.
Resorption
Nach einer oralen Einzeldosis von 300 mg Tucatinib dauerte es im Median etwa 2,0 Stunden, bis die Plasmaspitzenkonzentration erreicht war (Streubreite: 1,0 bis 4,0 Stunden).
Auswirkungen der Nahrungsaufnahme
Bei Verabreichung einer Einzeldosis Tucatinib an 11 Probanden nach einer fettreichen Mahlzeit (ca. 58 % Fett, 26 % Kohlenhydrate und 16 % Protein) stieg die mittlere AUCinf um das 1,5‑Fache, die tmax änderte sich von 1,5 Stunden auf 4,0 Stunden und die Cmax blieb unbeeinflusst. Da die Auswirkungen der Nahrungsaufnahme auf die Pharmakokinetik von Tucatinib klinisch nicht relevant waren, kann das Arzneimittel unabhängig von den Mahlzeiten eingenommen werden.
Verteilung
Bei gesunden Probanden lag das scheinbare Verteilungsvolumen von Tucatinib nach einer Einzeldosis von 300 mg bei ca. 1670 l. Die Plasmaproteinbindung bei klinisch relevanten Konzentrationen betrug 97,1 %.
Biotransformation
Tucatinib wird vorwiegend durch CYP2C8 und in geringerem Maße über CYP3A und Aldehydoxidase metabolisiert.
Arzneimittelwechselwirkungsstudien in vitro
Tucatinib ist ein Substrat von CYP2C8 und CYP3A.
In klinisch relevanten Konzentrationen hemmt Tucatinib reversibel CYP2C8 and CYP3A und ist ein zeitabhängiger Inhibitor von CYP3A.
Klinisch relevante Konzentrationen des Arzneimittels besitzen ein geringes Potenzial für eine Hemmung von CYP1A2, CYP2B6, CYP2C9, CYP2C19, CYP2D6 und UGT1A1.
Tucatinib ist ein Substrat von P‑gp und BCRP, aber nicht von OAT1, OAT3, OCT1, OCT2, OATP1B1, OATP1B3, MATE1, MATE2-K und BSEP.
Es hemmt den MATE1/MATE2‑K-vermittelten Transport von Metformin und den OCT2/MATE1-vermittelten Transport von Kreatinin. Der in klinischen Studien beobachtete Anstieg des Serumkreatinins unter Tucatinib ist durch eine Hemmung der tubulären Sekretion von Kreatinin über OCT2 und MATE1 bedingt.
Elimination
Bei gesunden Probanden wird Tucatinib nach einer oralen Einzeldosis von 300 mg mit einer geometrischen mittleren Halbwertszeit von ca. 8,5 Stunden und einer scheinbaren Clearance von 148 l/h aus dem Plasma entfernt.
Ausscheidung
Tucatinib wird vorrangig auf dem hepatobiliären Weg eliminiert; die renale Elimination ist nicht nennenswert. Nach einer oralen Einzeldosis von 300 mg 14C‑Tucatinib wurden ca. 85,8 % der radioaktiv markierten Gesamtdosis in den Fäzes wiedergefunden (15,9 % der verabreichten Dosis als unverändertes Tucatinib) und 4,1 % im Urin; die Gesamtwiederfindung innerhalb von 312 Stunden nach der Arzneimittelgabe betrug 89,9 %. Im Plasma waren etwa 75,6 % der Plasmaradioaktivität unverändert, 19 % ließen sich identifizierten Metaboliten zuschreiben und 5 % waren nicht zuzuordnen.
Besondere Patientengruppen
Ausgehend von einer populationspharmakokinetischen Analyse gemäß der demographischen Merkmale hatten Alter (< 65 Jahre [n = 211]; ≥ 65 Jahre [n = 27]), Albumin (25,0 bis 52,0 g/l), Kreatininclearance (CLcr 60 bis 89 ml/min [n = 89]; CLcr 30 bis 59 ml/min [n =5]), Körpergewicht (40,7 bis 138,0 kg) und ethnische Herkunft (weiß [n = 168], schwarz [n = 53] oder asiatisch [n = 10]) keine klinisch bedeutsame Auswirkung auf die Tucatinib-Exposition. Für Patienten mit stark eingeschränkter Nierenfunktion liegen keine Daten vor.
Nierenfunktionsstörung
Die Pharmakokinetik von Tucatinib wurde nicht in einer speziellen Studie zu Nierenfunktionsstörungen beurteilt.
Leberfunktionsstörung
Leichte (Child‑Pugh A) und mittelschwere (Child‑Pugh B) Leberfunktionsstörungen hatten keine klinisch relevante Auswirkungen auf die Tucatinib-Exposition. Bei Patienten mit schwerer Leberfunktionsstörung (Child‑Pugh C) war die AUCinf von Tucatinib im Vergleich zu Probanden mit normaler Leberfunktion um das 1,6‑Fache erhöht. Es liegen keine Daten für Brustkrebspatienten mit stark eingeschränkter Leberfunktion vor.
Es wurden keine Kanzerogenitätsstudien mit Tucatinib durchgeführt.
In der Standardtestreihe zur Untersuchung der Genotoxizität erwies sich Tucatinib als nicht klastogen und nicht mutagen.
Bei der Anwendung von Dosen ≥ 6 mg/kg/Tag zweimal täglich im Rahmen der Studien zur Toxizität bei wiederholter Gabe an Ratten (entsprechend dem 0,09‑Fachen der Exposition beim Menschen basierend auf der AUC0‑12 in der empfohlenen Dosierung) wurden verminderte Corpora lutea/ Corpus-luteum-Zysten, eine Zunahme interstitieller Zellen in den Ovarien, Uterusatrophie sowie eine Muzifizierung der Vagina beobachtet. Es wurden keine histologischen Auswirkungen auf den Reproduktionstrakt bei männlichen oder weiblichen Javaneraffen oder auf den männlichen Reproduktionstrakt bei Ratten festgestellt, wenn den Tieren Dosen verabreicht wurden, die zu Expositionen von bis zu dem 8‑Fachen (bei Affen) bzw. dem 13‑Fachen (bei Ratten) der Exposition beim Menschen in der empfohlenen Dosierung (basierend auf der AUC0-12) führen.
Embryo-fetale Entwicklungsstudien wurden an Kaninchen und Ratten durchgeführt. Bei trächtigen Kaninchen wurden bei einer Dosis von ≥ 90 mg/kg/Tag vermehrte Resorptionen, geringer Anteil lebender Föten sowie skelettale, viszerale und äußerliche Fehlbildungen festgestellt. Bei dieser Dosierung entspricht die Exposition der Muttertiere in etwa der Humanexposition bei der empfohlenen Dosis basierend auf der AUC. Bei Dosen von ≥ 90 mg/kg/Tag wurden bei trächtigen Ratten ein vermindertes Körpergewicht der Muttertiere und eine geringere Gewichtszunahme beobachtet. Wirkungen auf den Fötus in Form von vermindertem Gewicht und verzögerter Ossifikation wurden bei einer Dosis von ≥ 120 mg/kg/Tag festgestellt. Bei dieser Dosierung ist die Exposition der Muttertiere ungefähr 6‑mal höher als die Humanexposition bei der empfohlenen Dosis basierend auf der AUC.
Tablettenkern
Copovidon (E 1208)
Crospovidon (E 1202)
Natriumchlorid
Kaliumchlorid (E 508)
Natriumhydrogencarbonat (E 500)
Siliciumdioxid, kolloidal, wasserfrei (E 551)
Magnesiumstearat
Mikrokristalline Cellulose
Filmüberzug
Poly(vinylalkohol) (E 1203)
Titandioxid (E 171)
Macrogol 4000 (E 1521)
Talkum (E 553b)
Eisen(III)-hydroxid-oxid x H2O (E 172)
Nicht zutreffend.
3 Jahre.
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
OPA/ALU/PVC-Blisterpackung, mit Aluminiumfolie verschlossen.
TUKYSA 50 mg Filmtabletten
Jeder Umkarton enthält 88 Filmtabletten (11 Blisterpackungen mit je 8 Tabletten).
TUKYSA 150 mg Filmtabletten
Jeder Umkarton enthält 84 Filmtabletten (21 Blisterpackungen mit je 4 Tabletten).
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu beseitigen.
Pfizer Europe MA EEIG
Boulevard de la Plaine 17
1050 Brüssel
Belgien
TUKYSA 50 mg Filmtabletten: EU/1/20/1526/001
TUKYSA 150 mg Filmtabletten: EU/1/20/1526/002
Datum der Erteilung der Zulassung: 11. Februar 2021
Datum der letzten Verlängerung der Zulassung:17. September 2025
November 2025
Ausführliche Informationen zu diesem Arzneimittel sind auf den Internetseiten der Europäischen Arzneimittel-Agentur https://www.ema.europa.eu verfügbar.

VERKAUFSABGRENZUNG IN DEUTSCHLAND
Verschreibungspflichtig
REZEPTPFLICHT/APOTHEKENPFLICHT IN ÖSTERREICH
Rezept- und apothekenpflichtig, wiederholte Abgabe verboten
PACKUNGSGRÖSSEN IN DEUTSCHLAND
TUKYSA® 50 mg: Blisterpackung mit 88 Filmtabletten
TUKYSA® 150 mg: Blisterpackung mit 84 Filmtabletten
PACKUNGSGRÖSSEN IN ÖSTERREICH
TUKYSA® 50 mg: Blisterpackung mit 88 Filmtabletten
TUKYSA® 150 mg: Blisterpackung mit 84 Filmtabletten
REPRÄSENTANT IN DEUTSCHLAND
PFIZER PHARMA GmbH
Friedrichstr. 110
10117 Berlin
Tel.: 030 550055-51000
Fax: 030 550054-10000
REPRÄSENTANT IN ÖSTERREICH
Pfizer Corporation Austria Ges.m.b.H.
Floridsdorfer Hauptstraße 1
A-1210 Wien
Tel.: +43 (0)1 521 15-0