▼Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung zu melden. Hinweise zur Meldung von Nebenwirkungen, siehe Abschnitt 4.8.
Osenvelt™ 120 mg Injektionslösung
Jede Durchstechflasche enthält 120 mg Denosumab in 1,7 ml Lösung (70 mg/ml).
Denosumab ist ein humaner monoklonaler IgG2-Antikörper, der mittels rekombinanter DNA‑Technologie in einer Säugetierzelllinie (Ovarialzellen des Chinesischen Hamsters) hergestellt wird.
Sonstige Bestandteile mit bekannter Wirkung
Jeweils 1,7 ml der Lösung enthalten 79,9 mg Sorbitol (E 420), entsprechend 47 mg/ml, und 0,17 mg Polysorbat 20 (E 432), entsprechend 0,1 mg/ml.
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
Injektionslösung (Injektion).
Klare, farblose bis blassgelbe Lösung mit einem pH-Wert von 5,2.
Prävention skelettbezogener Komplikationen (pathologische Fraktur, Bestrahlung des Knochens, Rückenmarkkompression oder operative Eingriffe am Knochen) bei Erwachsenen mit fortgeschrittenen Krebserkrankungen und Knochenbefall (siehe Abschnitt 5.1).
Behandlung von Erwachsenen und skelettal ausgereiften Jugendlichen mit Riesenzelltumoren des Knochens, die nicht resezierbar sind oder bei denen eine operative Resektion wahrscheinlich zu einer schweren Morbidität führt.
Denosumab ist unter der Verantwortung von medizinischem Fachpersonal anzuwenden.
Dosierung
Ergänzend müssen alle Patienten täglich mindestens 500 mg Calcium und 400 IE Vitamin D erhalten, außer bei bestehender Hyperkalzämie (siehe Abschnitt 4.4).
Patienten, die mit Denosumab behandelt werden, sollen die Packungsbeilage und die Patientenerinnerungskarte ausgehändigt bekommen.
Prävention skelettbezogener Komplikationen bei Erwachsenen mit fortgeschrittenen Krebserkrankungen und Knochenbefall
Die empfohlene Dosis beträgt 120 mg. Diese wird einmal alle 4 Wochen als einzelne subkutane Injektion in den Oberschenkel, die Bauchregion oder den Oberarm angewendet.
Riesenzelltumoren des Knochens
Die empfohlene Dosis von Denosumab beträgt 120 mg. Diese wird einmal alle 4 Wochen und in zusätzlichen Dosen von 120 mg an den Tagen 8 und 15 des ersten Behandlungsmonats als einzelne subkutane Injektion in den Oberschenkel, die Bauchregion oder den Oberarm angewendet.
Patienten in der Phase-II-Studie, bei denen eine komplette Resektion der Riesenzelltumoren des Knochens durchgeführt wurde, erhielten eine zusätzliche 6-monatige Behandlung nach der Operation entsprechend dem Studienprotokoll.
Patienten mit Riesenzelltumoren des Knochens sollen regelmäßig daraufhin untersucht werden, ob sie weiterhin von der Behandlung profitieren. Bei Patienten, deren Erkrankung mit Denosumab beherrscht wird, wurde die Auswirkung einer Unterbrechung oder eines Abbruchs der Therapie nicht untersucht. Allerdings weisen limitierte Daten bei diesen Patienten nicht auf einen Rebound-Effekt nach Abbruch der Behandlung hin.
Nierenfunktionsstörung
Bei Patienten mit Nierenfunktionsstörung ist keine Dosisanpassung erforderlich (siehe Abschnitte 4.4 für Empfehlungen bezüglich der Überwachung von Calcium, 4.8 und 5.2).
Leberfunktionsstörung
Die Sicherheit und Wirksamkeit von Denosumab wurden bei Patienten mit Leberfunktionsstörung nicht untersucht (siehe Abschnitt 5.2).
Ältere Patienten (≥ 65 Jahre)
Bei älteren Patienten ist keine Dosisanpassung erforderlich (siehe Abschnitt 5.2).
Kinder und Jugendliche
Die Sicherheit und Wirksamkeit von Denosumab wurden, mit Ausnahme von skelettal ausgereiften Jugendlichen (im Alter von 12 ‑ 17 Jahren) mit Riesenzelltumoren des Knochens, nicht bei Kindern und Jugendlichen (< 18 Jahre) nachgewiesen.
Osenvelt wird, mit Ausnahme von skelettal ausgereiften Jugendlichen (im Alter von 12 ‑ 17 Jahren) mit Riesenzelltumoren des Knochens, nicht für die Anwendung bei Kindern und Jugendlichen (< 18 Jahre) empfohlen (siehe Abschnitt 4.4).
Behandlung von skelettal ausgereiften Jugendlichen mit Riesenzelltumoren des Knochens, die nicht resezierbar sind oder bei denen eine operative Resektion wahrscheinlich zu einer schweren Morbidität führt: Die Dosierung entspricht derjenigen für Erwachsene.
In tierexperimentellen Studien wurde eine Inhibition des RANK/RANK-Liganden (RANKL) mit einer Hemmung des Knochenwachstums und mit einem Fehlen des Zahndurchbruchs in Verbindung gebracht, wobei diese Veränderungen nach Beenden der RANKL-Inhibition teilweise reversibel waren (siehe Abschnitt 5.3).
Art der Anwendung
Zur subkutanen Anwendung.
Für Anleitungen zur Anwendung, Handhabung und Entsorgung, siehe Abschnitt 6.6.
Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
Schwere, unbehandelte Hypokalzämie (siehe Abschnitt 4.4).
Nicht verheilte Läsionen aus Zahnoperationen oder Operationen im Mundbereich.
Rückverfolgbarkeit
Um die Rückverfolgbarkeit biologischer Arzneimittel zu verbessern, müssen die Bezeichnung des Arzneimittels und die Chargenbezeichnung des angewendeten Arzneimittels eindeutig dokumentiert werden.
Ergänzung mit Calcium und Vitamin D
Eine Ergänzung mit Calcium und Vitamin D ist, außer bei bestehender Hyperkalzämie, bei allen Patienten erforderlich (siehe Abschnitt 4.2).
Hypokalzämie
Eine bestehende Hypokalzämie muss vor Beginn der Denosumab-Therapie korrigiert werden. Während der Denosumab-Therapie kann Hypokalzämie zu jeder Zeit auftreten. Eine Kontrolle der Calciumspiegel ist (1.) vor der Denosumab-Anfangsdosis, (2.) innerhalb von 2 Wochen nach der Anfangsdosis, (3.) wenn verdächtige Symptome einer Hypokalzämie auftreten (siehe Abschnitt 4.8 zu Symptomen), durchzuführen. Zusätzliche Kontrollen des Calciumspiegels sollen bei Patienten mit Risikofaktoren für eine Hypokalzämie während der Therapie oder sofern sie anderweitig aufgrund des klinischen Zustandes des Patienten indiziert sind, erwogen werden.
Patienten sollen dazu aufgefordert werden, Symptome, die auf eine Hypokalzämie hinweisen, zu berichten. Wenn während der Behandlung mit Denosumab eine Hypokalzämie auftritt, können eine zusätzliche Calciumergänzung sowie zusätzliche Kontrollen erforderlich werden.
Nach Markteinführung wurde über schwere symptomatische Hypokalzämie (einschließlich Fälle mit tödlichem Ausgang) berichtet (siehe Abschnitt 4.8). Die meisten Fälle traten in den ersten Wochen nach Therapiebeginn auf, sie können jedoch auch später auftreten.
Nierenfunktionsstörung
Bei Patienten mit schwerer Nierenfunktionsstörung (Kreatinin-Clearance < 30 ml/min) oder bei dialysepflichtigen Patienten besteht ein höheres Risiko, eine Hypokalzämie zu entwickeln. Das Risiko, eine Hypokalzämie und einen begleitenden Parathormon-Anstieg zu entwickeln, erhöht sich mit steigendem Grad der Nierenfunktionsstörung. Eine regelmäßige Kontrolle der Calciumspiegel ist bei diesen Patienten besonders wichtig.
Kieferosteonekrose (osteonecrosis of the jaw, ONJ)
ONJ wurde häufig bei Patienten berichtet, die mit Denosumab behandelt wurden (siehe Abschnitt 4.8).
Der Beginn der Behandlung/eines neuen Behandlungszyklus soll bei Patienten mit nicht verheilten offenen Weichteilläsionen im Mundraum verschoben werden. Eine zahnärztliche Untersuchung mit präventiver Zahnbehandlung und einer individuellen Nutzen-Risiko-Bewertung wird vor der Behandlung mit Denosumab empfohlen.
Die folgenden Risikofaktoren sollen bei der Einschätzung des Risikos des Patienten für die Entwicklung von ONJ berücksichtigt werden:
Wirksamkeit des Arzneimittels, das die Knochenresorption inhibiert (höheres Risiko bei hochwirksamen Präparaten), Art der Anwendung (höheres Risiko für parenterale Anwendung) und kumulative Dosis einer Therapie zur Behandlung der Knochenresorption.
Krebs, Begleiterkrankungen (z. B. Anämie, Koagulopathien, Infektionen), Rauchen.
Begleittherapien: Corticosteroide, Chemotherapie, Angiogeneseinhibitoren, Bestrahlung im Kopf-Hals-Bereich.
Schlechte Mundhygiene, Erkrankung des Zahnfleisches, schlecht passende Zahnprothesen, vorbestehende Zahnerkrankung, invasive Zahnbehandlungen (z. B. Zahnextraktionen).
Alle Patienten sollen dazu angehalten werden, eine gute Mundhygiene einzuhalten, zahnärztliche Routineuntersuchungen durchführen zu lassen und unverzüglich jegliche Symptome im Mundraum wie Lockerung der Zähne, Schmerzen oder Schwellungen oder nicht heilende wunde Stellen oder Ausfluss während der Behandlung mit Denosumab zu berichten. Während der Behandlung sollen invasive zahnärztliche Eingriffe nur nach sorgfältiger Abwägung und nicht zeitnah zur Denosumab-Anwendung durchgeführt werden.
Der Behandlungsplan der Patienten, die eine ONJ entwickeln, soll in enger Zusammenarbeit zwischen dem behandelnden Arzt und einem Zahnarzt oder Kieferchirurgen mit Erfahrung mit ONJ erstellt werden. Bis zum Rückgang des Zustandes und zur Abschwächung der dazu beitragenden Risikofaktoren sollte, falls möglich, eine vorübergehende Unterbrechung der Behandlung mit Denosumab erwogen werden.
Osteonekrose des äußeren Gehörgangs
Bei der Anwendung von Denosumab wurde über Osteonekrose des äußeren Gehörgangs berichtet. Zu den möglichen Risikofaktoren für eine Osteonekrose des äußeren Gehörgangs zählen die Anwendung von Steroiden und Chemotherapie und/oder lokale Risikofaktoren wie z. B. Infektionen oder Traumata. Die Möglichkeit einer Osteonekrose des äußeren Gehörgangs soll bei Patienten in Betracht gezogen werden, die Denosumab erhalten und mit Ohrsymptomen, einschließlich chronischer Ohrinfektionen, vorstellig werden.
Atypische Femurfrakturen
Über atypische Femurfrakturen wurde bei Patienten berichtet, die Denosumab erhielten (siehe Abschnitt 4.8). Atypische Femurfrakturen können in subtrochantären und diaphysären Bereichen des Femurs nach geringem oder ohne Trauma auftreten. Spezifische radiologische Befunde kennzeichnen diese Ereignisse. Über atypische Femurfrakturen wurde ebenfalls bei Patienten mit bestimmten Begleiterkrankungen (z. B. Vitamin-D-Mangel, Rheumatoide Arthritis, Hypophosphatasie) und bei der Anwendung bestimmter Wirkstoffe (z. B. Bisphosphonate, Glukokortikoide, Protonenpumpen-Inhibitoren) berichtet. Diese Ereignisse sind auch ohne antiresorptive Therapie aufgetreten. Vergleichbare Frakturen, über die im Zusammenhang mit Bisphosphonaten berichtet wurde, sind häufig bilateral; daher soll bei Patienten, die unter Behandlung mit Denosumab eine Femurschaftfraktur erlitten haben, der kontralaterale Femur untersucht werden. Abhängig von einer Patientenbeurteilung, die auf einer individuellen Nutzen-Risiko-Einschätzung basiert, soll bei Patienten mit Verdacht auf eine atypische Femurfraktur ein Abbruch der Denosumab-Therapie erwogen werden. Während der Behandlung mit Denosumab sollen die Patienten angewiesen werden, neu auftretende oder ungewöhnliche Oberschenkel-, Hüft- oder Leistenschmerzen zu berichten. Patienten mit solchen Symptomen sollen auf eine unvollständige Femurfraktur hin untersucht werden.
Hyperkalzämie nach Behandlungsende bei Patienten mit Riesenzelltumoren des Knochens und bei Patienten mit Skelettwachstum
Eine klinisch signifikante Hyperkalzämie mit erforderlichem Krankenhausaufenthalt und akuter Nierenschädigung als Komplikation wurde Wochen bis Monate nach Behandlungsende bei mit Denosumab behandelten Patienten mit Riesenzelltumoren des Knochens berichtet.
Nach Behandlungsende sind Patienten auf Anzeichen und Symptome einer Hyperkalzämie zu überwachen, und eine regelmäßige Überprüfung des Serumcalciumspiegels ist in Betracht zu ziehen. Zudem muss die Notwendigkeit einer Ergänzung mit Calcium und Vitamin D neu bewertet werden (siehe Abschnitt 4.8).
Denosumab wird nicht für Patienten empfohlen, bei denen sich das Skelett im Wachstum befindet (siehe Abschnitt 4.2). Eine klinisch signifikante Hyperkalzämie wurde auch bei dieser Patientengruppe Wochen bis Monate nach Behandlungsende berichtet.
Sonstige
Patienten, die mit Denosumab behandelt werden, sollen nicht gleichzeitig mit anderen Denosumab‑enthaltenden Arzneimitteln (für Osteoporose-Indikationen) behandelt werden.
Patienten, die mit Denosumab behandelt werden, sollen nicht gleichzeitig mit Bisphosphonaten behandelt werden.
Malignität bei Riesenzelltumoren des Knochens oder Progression zu einer metastasierten Erkrankung ist ein seltenes Ereignis und ein bekanntes Risiko bei Patienten mit Riesenzelltumoren des Knochens. Patienten sollen hinsichtlich radiologischer Anzeichen von Malignität, neuer Strahlendurchlässigkeit oder Osteolyse überwacht werden. Vorliegende klinische Daten weisen nicht auf ein erhöhtes Risiko einer Malignität bei Patienten mit Riesenzelltumoren des Knochens hin, die mit Denosumab behandelt wurden.
Warnhinweise für sonstige Bestandteile
Dieses Arzneimittel enthält 79,9 mg Sorbitol pro Durchstechflasche, entsprechend 47 mg/ml. Die additive Wirkung gleichzeitig angewendeter Sorbitol (oder Fructose)-haltiger Arzneimittel und die Einnahme von Sorbitol (oder Fructose) über die Nahrung ist zu berücksichtigen.
Dieses Arzneimittel enthält weniger als 1 mmol Natrium (23 mg) pro 120-mg-Dosis, d. h. es ist nahezu „natriumfrei“.
Dieses Arzneimittel enthält 0,17 mg Polysorbat 20 pro Durchstechflasche, entsprechend 0,1 mg/ml. Polysorbate können allergische Reaktionen hervorrufen.
Es wurden keine Studien zur Erfassung von Wechselwirkungen durchgeführt.
In klinischen Studien wurde Denosumab in Kombination mit üblichen Antitumor-Behandlungen und bei Patienten, die vorher Bisphosphonate erhalten hatten, angewendet. Es gab keine klinisch relevanten Änderungen in den minimalen Serumkonzentrationen und der Pharmakodynamik von Denosumab (N‑Telopeptid im Urin (uNTX/Cr), adjustiert nach Kreatinin) durch begleitende Chemotherapie und/oder Hormontherapie oder durch vorherige intravenöse Bisphosphonat-Exposition.
Schwangerschaft
Bisher liegt keine oder nur eine begrenzte Datenmenge zur Anwendung von Denosumab bei Schwangeren vor. Tierexperimentelle Studien zeigten eine Reproduktionstoxizität (siehe Abschnitt 5.3).
Die Anwendung von Denosumab während der Schwangerschaft und bei Frauen im gebärfähigen Alter, die keine Verhütungsmethode anwenden, wird nicht empfohlen. Frauen sollen darauf hingewiesen werden, während und für mindestens 5 Monate nach der Denosumab-Behandlung nicht schwanger zu werden. Jegliche Wirkung von Denosumab ist während des zweiten und dritten Trimesters der Schwangerschaft wahrscheinlich größer, da monoklonale Antikörper auf lineare Weise durch die Plazenta transportiert werden, während die Schwangerschaft fortschreitet. Die höchste Menge wird während des dritten Trimesters transferiert.
Stillzeit
Es ist nicht bekannt, ob Denosumab in die Muttermilch übergeht. Ein Risiko für das Neugeborene/Kind kann nicht ausgeschlossen werden. Studien mit Knockout-Mäusen weisen darauf hin, dass das Fehlen von RANKL während der Schwangerschaft die Reifung der Brustdrüsen und damit die Milchproduktion nach der Geburt beeinträchtigen kann (siehe Abschnitt 5.3). Es muss eine Entscheidung darüber getroffen werden, ob das Stillen zu unterbrechen ist oder ob auf die Denosumab‑Behandlung verzichtet werden soll. Dabei sind sowohl der Nutzen des Stillens für das Neugeborene/Kind als auch der Nutzen der Therapie für die Frau zu berücksichtigen.
Fertilität
Es liegen keine Daten zur Wirkung von Denosumab auf die Fortpflanzungsfähigkeit des Menschen vor. Tierexperimentelle Studien weisen nicht auf direkte oder indirekte schädigende Wirkungen in Hinsicht auf die Fortpflanzungsfähigkeit hin (siehe Abschnitt 5.3).
Denosumab hat keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Zusammenfassung des Sicherheitsprofils
Das Gesamtsicherheitsprofil stimmt in allen zugelassenen Anwendungsgebieten von Denosumab überein.
Über Hypokalzämie wurde sehr häufig nach Denosumab-Anwendung berichtet, meistens innerhalb der ersten beiden Wochen. Eine Hypokalzämie kann schwer und symptomatisch sein (siehe Abschnitt 4.8 – Beschreibung ausgewählter unerwünschter Wirkungen). Die Abnahmen des Serumcalciums konnten im Allgemeinen mit einer Calcium- und Vitamin D-Ergänzung angemessen behandelt werden. Die häufigsten unerwünschten Wirkungen von Denosumab sind muskuloskelettale Schmerzen. Fälle von Kieferosteonekrose (siehe Abschnitte 4.4 und 4.8 – Beschreibung ausgewählter unerwünschter Wirkungen) wurden häufig bei Patienten, die Denosumab anwenden, beobachtet.
Liste der unerwünschten Wirkungen in Tabellenform
Die folgende Konvention wurde, basierend auf den Inzidenzraten in vier klinischen Studien der Phase III, zwei der Phase II und der Erfahrung nach Markteinführung, für die Klassifikation der unerwünschten Wirkungen verwendet (siehe Tabelle 1): sehr häufig (≥ 1/10), häufig (≥ 1/100, < 1/10), gelegentlich (≥ 1/1 000, < 1/100), selten (≥ 1/10 000, < 1/1 000), sehr selten (< 1/10 000) und nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar). Innerhalb jeder Häufigkeitsgruppe und Systemorganklasse werden die unerwünschten Wirkungen nach abnehmendem Schweregrad aufgeführt.
Tabelle 1: Unerwünschte Wirkungen, die bei Patienten mit fortgeschrittenen Krebserkrankungen und Knochenbefall, Multiplem Myelom oder mit Riesenzelltumoren des Knochens berichtet wurden
Systemorganklassen gemäß MedDRA |
Häufigkeitskategorie |
Unerwünschte Wirkungen |
Gutartige, bösartige und nicht spezifizierte Neubildungen (einschl. Zysten und Polypen) |
Häufig |
Neues primäres Malignom1 |
Erkrankungen des Immunsystems |
Selten |
Arzneimittelüberempfindlichkeit1 |
Selten |
Anaphylaktische Reaktion1 |
|
Stoffwechsel- und Ernährungsstörungen |
Sehr häufig |
Hypokalzämie1, 2 |
Häufig |
Hypophosphatämie |
|
Gelegentlich |
Hyperkalzämie nach Behandlungsende bei Patienten mit Riesenzelltumoren des Knochens3 |
|
Erkrankungen der Atemwege, des Brustraums und Mediastinums |
Sehr häufig |
Dyspnoe |
Erkrankungen des Gastrointestinaltrakts |
Sehr häufig |
Diarrhö |
Häufig |
Zahnextraktion |
|
Erkrankungen der Haut und des Unterhautgewebes |
Häufig |
Hyperhidrose |
Gelegentlich |
Lichenoide Arzneimittelexantheme1 |
|
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen |
Sehr häufig |
Muskuloskelettale Schmerzen1 |
Häufig |
Kieferosteonekrose1 |
|
Gelegentlich |
Atypische Femurfraktur1 |
|
Nicht bekannt |
Osteonekrose des äußeren Gehörgangs3, 4 |
1 Siehe Abschnitt „Beschreibung ausgewählter unerwünschter Wirkungen“
2 Siehe Abschnitt „Andere spezielle Populationen“
3 Siehe Abschnitt 4.4
4 Klasseneffekt
Beschreibung ausgewählter unerwünschter Wirkungen
Hypokalzämie
Eine höhere Inzidenz von Hypokalzämie wurde in klinischen Studien zur Prävention von SRE (skeletal related events) bei Patienten, die mit Denosumab behandelt wurden, im Vergleich zu Zoledronsäure beobachtet.
Die höchste Inzidenz von Hypokalzämie wurde in einer Phase-III-Studie bei Patienten mit Multiplem Myelom beobachtet. Hypokalzämie wurde bei 16,9 % der Patienten, die mit Denosumab behandelt wurden, und bei 12,4 % der Patienten, die mit Zoledronsäure behandelt wurden, berichtet. Ein Absinken der Serumcalciumspiegel Grad 3 trat bei 1,4 % der mit Denosumab behandelten Patienten und bei 0,6 % der mit Zoledronsäure behandelten Patienten auf. Ein Absinken der Serumcalciumspiegel Grad 4 trat bei 0,4 % der mit Denosumab behandelten Patienten und bei 0,1 % der mit Zoledronsäure behandelten Patienten auf.
In drei aktiv-kontrollierten klinischen Studien der Phase III bei Patienten mit fortgeschrittenen Krebserkrankungen und Knochenbefall wurde bei 9,6 % der mit Denosumab und bei 5,0 % der mit Zoledronsäure behandelten Patienten über Hypokalzämie berichtet.
Ein Absinken der Serumcalciumspiegel Grad 3 trat bei 2,5 % der mit Denosumab und 1,2 % der mit Zoledronsäure behandelten Patienten auf. Ein Absinken der Serumcalciumspiegel Grad 4 trat bei 0,6 % der mit Denosumab und 0,2 % der mit Zoledronsäure behandelten Patienten auf (siehe Abschnitt 4.4).
In zwei einarmigen klinischen Studien der Phase II bei Patienten mit Riesenzelltumoren des Knochens wurde bei 5,7 % der Patienten über Hypokalzämie berichtet. Keines der unerwünschten Ereignisse wurde als schwerwiegend eingestuft.
Nach Markteinführung wurde über schwere symptomatische Hypokalzämie (einschließlich Fälle mit tödlichem Ausgang) berichtet, wobei die Mehrzahl der Fälle in den ersten Wochen nach Therapiebeginn auftrat. Beispiele klinischer Manifestationen schwerer symptomatischer Hypokalzämie schlossen QT-Intervallverlängerungen, Tetanie, Krampfanfälle und veränderten mentalen Status (einschließlich Koma) ein (siehe Abschnitt 4.4). In klinischen Studien schlossen die Symptome einer Hypokalzämie Parästhesien oder Muskelsteifheit, Zuckungen, Spasmen und Muskelkrämpfe ein.
Kieferosteonekrose (ONJ)
Die Inzidenz von ONJ war in klinischen Studien bei längerer Expositionsdauer höher. ONJ wurde auch nach dem Ende der Behandlung mit Denosumab diagnostiziert, wobei die Mehrheit der Fälle innerhalb von 5 Monaten nach der letzten Dosis auftrat. Patienten mit einer Vorgeschichte einer ONJ oder Osteomyelitis des Kiefers, bestehendem Zahn- oder Kieferbefund, der eine Operation im Mundbereich erfordert, nicht verheilten operativen Zahn‑/Mundeingriffen oder jedwedem geplanten invasiven zahnärztlichen Eingriff waren aus den klinischen Studien ausgeschlossen.
Eine höhere Inzidenz von ONJ wurde in klinischen Studien zur Prävention von SRE bei Patienten, die mit Denosumab behandelt wurden, im Vergleich zu Zoledronsäure beobachtet. Die höchste Inzidenz von ONJ wurde in einer Phase-III-Studie bei Patienten mit Multiplem Myelom beobachtet. In der doppelt verblindeten Behandlungsphase dieser Studie wurde ONJ bei 5,9 % der Patienten, die mit Denosumab behandelt wurden (mediane Exposition von 19,4 Monaten; Bereich 1 – 52), und bei 3,2 % der Patienten, die mit Zoledronsäure behandelt wurden, bestätigt. Bei Beendigung der doppelt verblindeten Behandlungsphase dieser Studie lag die nach Patientenjahren adjustierte Inzidenz einer bestätigten ONJ in der Denosumab-Gruppe (mediane Exposition von 19,4 Monaten; Bereich: 1 – 52) bei 2,0 pro 100 Patientenjahre während des ersten Behandlungsjahres, bei 5,0 im zweiten Jahr und danach bei 4,5. Die mediane Zeit bis zum Auftreten einer ONJ lag bei 18,7 Monaten (Bereich: 1 – 44).
In den primären Behandlungsphasen von drei aktiv-kontrollierten klinischen Studien der Phase III bei Patienten mit fortgeschrittenen Krebserkrankungen und Knochenbefall wurde ONJ bei 1,8 % der mit Denosumab (mediane Exposition von 12,0 Monaten; Bereich: 0,1 – 40,5) und 1,3 % der mit Zoledronsäure behandelten Patienten bestätigt. Die klinischen Charakteristika dieser Fälle waren in den Behandlungsgruppen ähnlich. Unter den Patienten mit bestätigter ONJ hatten die meisten (81 % in beiden Behandlungsgruppen) eine Vorgeschichte von Zahnextraktion, schlechter Mundhygiene und/oder Verwendung von Zahnersatz. Die meisten Patienten erhielten eine Chemotherapie oder hatten eine erhalten.
Die Studien bei Patienten mit Mamma- oder Prostatakarzinom schlossen eine verlängerte Behandlungsphase mit Denosumab ein (mediane Gesamtexposition von 14,9 Monaten; Bereich: 0,1 – 67,2). Eine ONJ wurde bei 6,9 % der Patienten mit Mamma- und Prostatakarzinom während der verlängerten Behandlungsphase bestätigt.
Die nach Patientenjahren adjustierte Gesamtinzidenz einer bestätigten ONJ lag bei 1,1 pro 100 Patientenjahre während des ersten Behandlungsjahres, bei 3,7 im zweiten Jahr und danach bei 4,6. Die mediane Zeit bis zum Auftreten einer ONJ betrug 20,6 Monate (Bereich: 4 – 53).
In einer nicht randomisierten, retrospektiven Beobachtungsstudie bei 2 877 mit Denosumab oder Zoledronsäure behandelten Krebspatienten in Schweden, Dänemark und Norwegen lag der 5-Jahres-Inzidenzanteil medizinisch bestätigter ONJ bei 5,7 % (95 % KI: 4,4; 7,3; mediane Nachbeobachtungszeit von 20 Monaten [Bereich: 0,2 – 60]) in der mit Denosumab behandelten Patientenkohorte und bei 1,4 % (95 % KI: 0,8; 2,3; mediane Nachbeobachtungszeit von 13 Monaten [Bereich: 0,1 – 60]) in der mit Zoledronsäure behandelten Patientenkohorte. Der 5-Jahres-Inzidenzanteil von ONJ bei Patienten, die von Zoledronsäure auf Denosumab wechselten, lag bei 6,6 % (95 % KI: 4,2; 10,0; mediane Nachbeobachtungszeit von 13 Monaten [Bereich: 0,2 – 60]).
In einer Studie der Phase III bei Patienten mit nicht metastasiertem Prostatakarzinom (einer Patientenpopulation, für die Denosumab nicht indiziert ist) und mit längerer Behandlungsexposition von bis zu 7 Jahren lag die nach Patientenjahren adjustierte Inzidenz einer bestätigten ONJ bei 1,1 pro 100 Patientenjahre während des ersten Behandlungsjahres, bei 3,0 im zweiten Jahr und danach bei 7,1.
In einer offenen, klinischen Langzeitstudie der Phase II bei Patienten mit Riesenzelltumoren des Knochens (Studie 6, siehe Abschnitt 5.1) wurde eine ONJ bei 6,8 % der Patienten, darunter bei einem Jugendlichen, bestätigt (mediane Anzahl von 34 Dosen; Bereich: 4 – 116). Am Ende der Studie betrug die mediane Dauer der Studienteilnahme, einschließlich der Nachbeobachtungsphase zur Beurteilung der Sicherheit, 60,9 Monate (Bereich: 0 – 112,6). Die nach Patientenjahren adjustierte Inzidenz einer bestätigten ONJ lag bei insgesamt 1,5 pro 100 Patientenjahre (0,2 pro 100 Patientenjahre während des ersten Behandlungsjahres, 1,5 im zweiten Jahr, 1,8 im dritten Jahr, 2,1 im vierten Jahr, 1,4 im fünften Jahr und danach 2,2). Die mediane Zeit bis zu einer ONJ betrug 41 Monate (Bereich: 11 – 96).
Studie 7 wurde durchgeführt, um Patienten mit Riesenzelltumoren des Knochens (GCTB, giant cell tumour of bone), die in Studie 6 behandelt wurden, für weitere 5 Jahre oder länger nachzuverfolgen. ONJ wurde bei 6 der 51 Patienten (11,8 %), die einer mittleren Gesamtdosis von 42 Dosen Denosumab exponiert waren, berichtet. Drei dieser ONJ-Fälle wurden ärztlich bestätigt.
Arzneimittelbedingte Überempfindlichkeitsreaktionen
Nach der Markteinführung wurde bei Patienten, die Denosumab erhielten, über Ereignisse von Überempfindlichkeit, einschließlich seltener Fälle von anaphylaktischen Reaktionen, berichtet.
Atypische Femurfrakturen
Insgesamt wurde im klinischen Studienprogramm bei Patienten, die mit Denosumab behandelt wurden, gelegentlich über atypische Femurfrakturen berichtet, wobei sich das Risiko bei längerer Behandlungsdauer erhöhte. Ereignisse traten während der Behandlung und bis zu 9 Monate nach Behandlungsende auf (siehe Abschnitt 4.4).
Im klinischen Studienprogramm für GCTB wurde bei Patienten, die mit Denosumab behandelt wurden, häufig über atypische Femurfrakturen (AFF) berichtet. In Studie 6 bei Patienten mit Riesenzelltumoren des Knochens betrug die Inzidenz bestätigter AFF 0,95 % (5/526). In der Folgestudie 7 lag die Inzidenz bestätigter AFF bei mit Denosumab behandelten Patienten bei 3,9 % (2/51).
Muskuloskelettale Schmerzen
Muskuloskelettale Schmerzen, einschließlich schwerer Fälle, wurden nach Markteinführung bei Patienten berichtet, die mit Denosumab behandelt wurden. In klinischen Studien traten muskuloskelettale Schmerzen sehr häufig sowohl in den Denosumab‑ als auch in den Zoledronsäure-Behandlungsgruppen auf. Muskuloskelettale Schmerzen, die zum Abbruch der Studienbehandlung führten, traten selten auf.
Neues primäres Malignom
In den primären doppelblinden Behandlungsphasen von vier aktiv-kontrollierten klinischen Studien der Phase III bei Patienten mit fortgeschrittenen Krebserkrankungen und Knochenbefall wurde über neue primäre Malignome berichtet bei 54/3 691 (1,5 %) der Patienten, die mit Denosumab behandelt wurden (mediane Exposition von 13,8 Monaten; Bereich: 1,0 – 51,7), und bei 33/3 688 (0,9 %) der Patienten, die mit Zoledronsäure behandelt wurden (mediane Exposition von 12,9 Monaten; Bereich: 1,0 – 50,8).
Die kumulative Inzidenz nach einem Jahr betrug 1,1 % für Denosumab und 0,6 % für Zoledronsäure.
Es war für einzelne oder Gruppen von Krebserkrankungen kein behandlungsbedingtes Muster zu erkennen.
In Studie 6 lag bei Patienten mit Riesenzelltumoren des Knochens die Inzidenz des Auftretens neuer Malignome, einschließlich maligner Erkrankungen des Knochens und außerhalb des Knochens, bei 3,8 % (20/526). In der Folgestudie 7 lag die Inzidenz bei mit Denosumab behandelten Patienten bei 11,8 % (6/51).
Lichenoide Arzneimittelexantheme
Lichenoide Arzneimittelexantheme (z. B. Lichen planus-artige Reaktionen) wurden nach Markteinführung bei Patienten berichtet.
Kinder und Jugendliche
Denosumab wurde in einer offenen Studie untersucht, in die 28 skelettal ausgereifte Jugendliche mit Riesenzelltumoren des Knochens eingeschlossen wurden. Basierend auf diesen limitierten Daten schien das Profil der unerwünschten Ereignisse mit dem der Erwachsenen vergleichbar zu sein.
Eine klinisch signifikante Hyperkalzämie nach Behandlungsende wurde nach Markteinführung bei Kindern und Jugendlichen berichtet (siehe Abschnitt 4.4).
Andere spezielle Populationen
Nierenfunktionsstörung
In einer klinischen Studie bei Patienten ohne fortgeschrittene Krebserkrankung mit schwerer Nierenfunktionsstörung (Kreatinin-Clearance < 30 ml/min) oder bei dialysepflichtigen Patienten lag ein höheres Risiko vor, eine Hypokalzämie zu entwickeln, wenn keine Calciumergänzung erfolgte. Das Risiko, eine Hypokalzämie während der Denosumab-Behandlung zu entwickeln, erhöht sich mit steigendem Grad der Nierenfunktionsstörung. In einer klinischen Studie bei Patienten ohne fortgeschrittene Krebserkrankung entwickelten 19 % der Patienten mit schwerer Nierenfunktionsstörung (Kreatinin-Clearance < 30 ml/min) und 63 % der dialysepflichtigen Patienten eine Hypokalzämie trotz Calciumergänzung. Die Gesamtinzidenz einer klinisch signifikanten Hypokalzämie lag bei 9 %.
Begleitende Erhöhungen der Parathormonspiegel wurden ebenfalls bei Patienten mit schwerer Nierenfunktionsstörung oder bei dialysepflichtigen Patienten beobachtet, die Denosumab erhielten. Die Überwachung der Calciumspiegel sowie eine adäquate Einnahme von Calcium und Vitamin D sind bei Patienten mit Nierenfunktionsstörung besonders wichtig (siehe Abschnitt 4.4).
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Bundesinstitut für Impfstoffe und biomedizinische Arzneimittel, Paul-Ehrlich-Institut, Paul-Ehrlich-Str. 51-59, 63225 Langen, Tel: +49 6103 77 0, Fax: +49 6103 77 1234, Website: www.pei.de, anzuzeigen.
Es gibt keine Erfahrung mit Überdosierung in klinischen Studien. Denosumab wurde in klinischen Studien in Dosierungen von bis zu 180 mg alle 4 Wochen und 120 mg einmal wöchentlich über 3 Wochen angewendet.
Pharmakotherapeutische Gruppe: Mittel zur Behandlung von Knochenerkrankungen, andere Mittel mit Einfluss auf die Knochenstruktur und die Mineralisation, ATC-Code: M05BX04.
Osenvelt ist ein biologisch / biotechnologisch hergestelltes Arzneimittel, das im Wesentlichen einem bereits zugelassenen Arzneimittel gleicht. Ausführliche Informationen sind auf den Internetseiten der Europäischen Arzneimittel-Agentur https://www.ema.europa.eu verfügbar.
Wirkmechanismus
RANKL tritt als Transmembranprotein oder lösliches Protein auf. RANKL ist essenziell für die Bildung, die Funktion und das Überleben von Osteoklasten, dem einzigen Zelltyp, der für die Knochenresorption verantwortlich ist. Erhöhte Osteoklastenaktivität, stimuliert durch RANKL, ist ein Schlüsselmediator des Knochenabbaus bei Knochenmetastasen und Multiplem Myelom. Denosumab ist ein humaner monoklonaler Antikörper (IgG2), der mit hoher Affinität und Spezifität an RANKL bindet. Dadurch wird die RANKL/RANK-Interaktion verhindert, woraus sich eine reduzierte Anzahl und Funktion von Osteoklasten ergibt. Infolgedessen werden die Knochenresorption und die Tumor‑induzierte Knochenzerstörung vermindert.
Riesenzelltumoren des Knochens charakterisieren sich durch neoplastische Stromazellen, die den RANK‑Liganden exprimieren, und Osteoklasten-ähnliche Riesenzellen, die RANK exprimieren. Denosumab bindet bei Patienten mit Riesenzelltumoren des Knochens an den RANK-Liganden und reduziert oder eliminiert signifikant Osteoklasten-ähnliche Riesenzellen. Folglich wird die Osteolyse reduziert und proliferatives Tumorstroma durch nicht-proliferativen, differenzierten, dicht gewobenen neuen Knochen ersetzt.
Pharmakodynamische Wirkungen
In klinischen Studien der Phase II bei Patienten mit fortgeschrittenen Krebserkrankungen und Knochenbefall führten subkutane (s.c.) Dosen von Denosumab, angewendet entweder alle 4 Wochen (Q4W) oder alle 12 Wochen, zu einer schnellen Reduktion von Knochenresorptionsmarkern (uNTX/Cr, Serum‑CTx) mit medianen Reduktionen von ungefähr 80 % für uNTX/Cr innerhalb von 1 Woche, unabhängig von einer vorausgehenden Bisphosphonat-Therapie oder uNTX/Cr-Werten zu Studienbeginn. In den klinischen Studien der Phase III bei Patienten mit fortgeschrittenen Krebserkrankungen und Knochenbefall hielt die mediane Senkung von uNTX/Cr von ungefähr 80 % über 49 Wochen der Denosumab-Behandlung (120 mg alle 4 Wochen) an.
Immunogenität
Während der Behandlung mit Denosumab können sich Antikörper gegen Denosumab entwickeln. Es wurde kein offensichtlicher Zusammenhang zwischen der Entwicklung von Antikörpern und der Pharmakokinetik, dem klinischen Ansprechen oder unerwünschten Ereignissen beobachtet.
Klinische Wirksamkeit und Sicherheit bei Patienten mit Knochenmetastasen von soliden Tumoren
Die Wirksamkeit und Sicherheit von 120 mg Denosumab s.c. alle 4 Wochen oder 4 mg Zoledronsäure (dosisangepasst bei reduzierter Nierenfunktion) i.v. alle 4 Wochen wurden in drei randomisierten, doppelblinden, aktiv-kontrollierten Studien bei i.v.-Bisphosphonat-naiven Patienten mit fortgeschrittenen Krebserkrankungen und Knochenbefall verglichen: Erwachsene mit Mammakarzinom (Studie 1), anderen soliden Tumoren oder Multiplem Myelom (Studie 2) und kastrationsresistentem Prostatakarzinom (Studie 3). Innerhalb dieser aktiv-kontrollierten klinischen Studien wurde die Sicherheit bei 5 931 Patienten untersucht. Patienten mit einer Vorgeschichte von ONJ oder Osteomyelitis im Kieferbereich, bestehendem Zahn- oder Kieferbefund, der eine Operation im Mundbereich erfordert, nicht verheilter Zahn-/Mundoperation oder jedwedem geplanten invasiven zahnärztlichen Eingriff waren für den Einschluss in diese Studien nicht geeignet. Die primären und sekundären Endpunkte untersuchten das Auftreten von ein oder mehreren skelettbezogenen Komplikationen (SREs, skeletal related events). In Studien, die die Überlegenheit von Denosumab gegenüber Zoledronsäure zeigten, wurde Patienten Denosumab unverblindet in einer vorab festgelegten, 2 Jahre dauernden Extensionsbehandlungsphase angeboten. Ein SRE wurde wie folgt definiert: pathologische Fraktur (vertebral oder nicht-vertebral), Bestrahlung des Knochens (einschließlich der Anwendung von Radioisotopen), operative Eingriffe am Knochen oder Rückenmarkkompression.
Denosumab reduzierte bei Patienten mit Knochenmetastasen von soliden Tumoren das Risiko, ein SRE sowie multiple SREs (erstes und folgende) zu entwickeln (siehe Tabelle 2).
Tabelle 2: Ergebnisse zur Wirksamkeit bei Patienten mit fortgeschrittenen Krebserkrankungen und Knochenbefall
Studie 1 |
Studie 2 |
Studie 3 |
Fortgeschrittene Krebserkrankungen kombiniert |
|||||
Denosumab |
Zoledron-säure |
Denosumab |
Zoledron-säure |
Denosumab |
Zoledron-säure |
Denosumab |
Zoledron-säure |
|
n |
1 026 |
1 020 |
886 |
890 |
950 |
951 |
2 862 |
2 861 |
Erstes SRE | ||||||||
Mediane Zeit (Monate) |
NR |
26,4 |
20,6 |
16,3 |
20,7 |
17,1 |
27,6 |
19,4 |
Differenz der medianen Zeit (Monate) |
NA |
4,2 |
3,5 |
8,2 |
||||
HR (95 % KI) / RRR (%) |
0,82 (0,71; 0,95) / 18 |
0,84 (0,71; 0,98) / 16 |
0,82 (0,71; 0,95) / 18 |
0,83 (0,76; 0,90) / 17 |
||||
Nicht-Unterlegenheit / Überlegenheit p-Werte |
< 0,0001† / 0,0101† |
0,0007† / 0,0619† |
0,0002† / 0,0085† |
< 0,0001 / < 0,0001 |
||||
Anteil an Patienten (%) |
30,7 |
36,5 |
31,4 |
36,3 |
35,9 |
40,6 |
32,6 |
37,8 |
Erstes und folgendes SRE* | ||||||||
Mittelwert Anzahl/Patient |
0,46 |
0,60 |
0,44 |
0,49 |
0,52 |
0,61 |
0,48 |
0,57 |
Rate Ratio (95 % KI) / RRR (%) |
0,77 (0,66; 0,89) / 23 |
0,90 (0,77; 1,04) / 10 |
0,82 (0,71; 0,94) / 18 |
0,82 (0,75; 0,89) / 18 |
||||
Überlegenheit p‑Wert |
0,0012† |
0,1447† |
0,0085† |
< 0,0001 |
||||
SMR pro Jahr |
0,45 |
0,58 |
0,86 |
1,04 |
0,79 |
0,83 |
0,69 |
0,81 |
Erstes SRE oder erste HCM | ||||||||
Mediane Zeit (Monate) |
NR |
25,2 |
19,0 |
14,4 |
20,3 |
17,1 |
26,6 |
19,4 |
HR (95 % KI) / RRR (%) |
0,82 (0,70; 0,95) / 18 |
0,83 (0,71; 0,97) / 17 |
0,83 (0,72; 0,96) / 17 |
0,83 (0,76; 0,90) / 17 |
||||
Überlegenheit p‑Wert |
0,0074 |
0,0215 |
0,0134 |
< 0,0001 |
||||
Erste Bestrahlung des Knochens | ||||||||
Mediane Zeit (Monate) |
NR |
NR |
NR |
NR |
NR |
28,6 |
NR |
33,2 |
HR (95 % KI) / RRR (%) |
0,74 (0,59; 0,94) / 26 |
0,78 (0,63; 0,97) / 22 |
0,78 (0,66; 0,94) / 22 |
0,77 (0,69; 0,87) / 23 |
||||
Überlegenheit p‑Wert |
0,0121 |
0,0256 |
0,0071 |
< 0,0001 |
||||
NR = nicht erreicht (not reached); NA = nicht verfügbar (not available); HCM = Tumor-Hyperkalzämie (hypercalcaemia of malignancy); SMR = skelettale Morbiditätsrate; HR = Hazard Ratio; RRR = Relative Risikoreduktion. †Adjustierte p‑Werte sind für Studien 1, 2 und 3 dargestellt (Endpunkte erstes SRE und erstes und folgende SRE); *Alle skelettalen Ereignisse über die Zeit gewertet; nur Ereignisse, die ≥ 21 Tage nach dem vorausgegangenen Ereignis auftraten, wurden gezählt.
** Einschließlich NSCLC, Nierenzellkarzinom, kolorektales Karzinom, kleinzelliges Bronchialkarzinom, Blasenkarzinom, Kopf-Hals-Tumoren, GI/Urogenitalkarzinom und andere, ausgenommen Mamma- und Prostatakarzinom.
Abbildung 1: Kaplan-Meier-Kurven der Zeit bis zum Auftreten des ersten SRE in der Studie
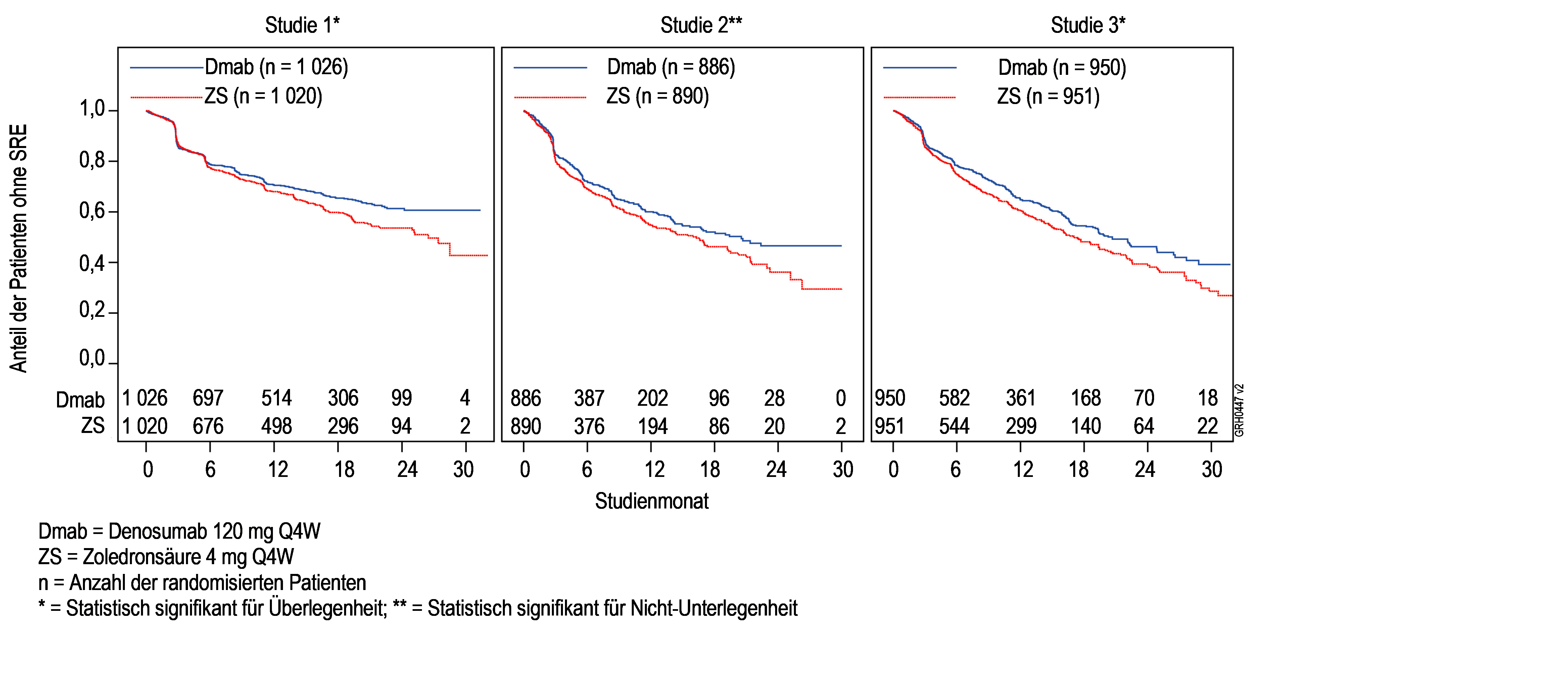
Fortschreiten der Erkrankung und Gesamtüberleben bei Knochenmetastasen von soliden Tumoren
Das Fortschreiten der Erkrankung war in allen drei Studien und in der planmäßigen, kombinierten Analyse aller drei Studien zwischen Denosumab und Zoledronsäure vergleichbar.
In Studien 1, 2 und 3 war das Gesamtüberleben zwischen Denosumab und Zoledronsäure bei Patienten mit fortgeschrittenen Krebserkrankungen und Knochenbefall vergleichbar: Patientinnen mit Mammakarzinom (Hazard Ratio und 95 % KI betrugen 0,95 [0,81; 1,11]), Patienten mit Prostatakarzinom (Hazard Ratio und 95 % KI betrugen 1,03 [0,91; 1,17]) und Patienten mit anderen soliden Tumoren oder Multiplem Myelom (Hazard Ratio und 95 % KI betrugen 0,95 [0,83; 1,08]). Eine Post-hoc-Analyse von Studie 2 (Patienten mit anderen soliden Tumoren oder Multiplem Myelom) untersuchte das Gesamtüberleben für die 3 für die Stratifikation verwendeten Tumorentitäten (nicht-kleinzelliges Bronchialkarzinom, Multiples Myelom und andere). Das Gesamtüberleben war länger für Denosumab bei nicht-kleinzelligem Bronchialkarzinom (Hazard Ratio [95 % KI] von 0,79 [0,65; 0,95]; n = 702), länger für Zoledronsäure bei Multiplem Myelom (Hazard Ratio [95 % KI] von 2,26 [1,13; 4,50]; n = 180) und vergleichbar zwischen Denosumab und Zoledronsäure bei anderen Tumorentitäten (Hazard Ratio [95 % KI] von 1,08 [0,90; 1,30]; n = 894). Diese Studie war nicht kontrolliert in Bezug auf prognostische Faktoren und anti-neoplastische Behandlungen. In einer planmäßigen kombinierten Analyse der Studien 1, 2 und 3 war das Gesamtüberleben zwischen Denosumab und Zoledronsäure vergleichbar (Hazard Ratio und 95 % KI betrugen 0,99 [0,91; 1,07]).
Wirkung auf Schmerzen
Die Zeit bis zur Linderung von Schmerzen (d. h. Abnahme um ≥ 2 Punkte des BPI‑SF Worst Pain Score seit Studienbeginn) war zwischen Denosumab und Zoledronsäure in jeder Studie und in den integrierten Analysen vergleichbar. In einer Post-hoc-Analyse des kombinierten Datensatzes war die mediane Zeit bis zur Verschlimmerung von Schmerzen (> 4 Punkte im Worst Pain Score) bei Patienten mit mäßigem oder keinem Schmerz zu Studienbeginn bei Denosumab im Vergleich zu Zoledronsäure verzögert (198 versus 143 Tage) (p = 0,0002).
Klinische Wirksamkeit bei Patienten mit Multiplem Myelom
Denosumab wurde in einer internationalen, randomisierten (1:1), doppelblinden, aktiv-kontrollierten Studie untersucht, in der Denosumab bei Patienten mit neu diagnostiziertem Multiplem Myelom mit Zoledronsäure verglichen wurde; Studie 4.
In diese Studie wurden 1 718 Patienten mit Multiplem Myelom und mindestens einer Knochenläsion randomisiert, um 120 mg Denosumab subkutan alle 4 Wochen (Q4W) oder 4 mg Zoledronsäure intravenös (i.v.) alle 4 Wochen (dosisadjustiert nach Nierenfunktion) zu erhalten. Primärer Zielparameter war der Nachweis der Nicht-Unterlegenheit hinsichtlich der Zeit bis zur ersten während der Studie aufgetretenen skelettbezogenen Komplikation (SRE) gegenüber Zoledronsäure. Sekundäre Zielparameter schlossen Überlegenheit hinsichtlich der Zeit bis zum ersten SRE, Überlegenheit hinsichtlich der Zeit bis zum ersten und folgenden SRE sowie Gesamtüberleben ein. Ein SRE wurde wie folgt definiert: pathologische Fraktur (vertebral oder nicht-vertebral), Bestrahlung des Knochens (einschließlich der Anwendung von Radioisotopen), chirurgische Eingriffe am Knochen oder Rückenmarkkompression.
Über beide Studienarme hinweg waren 54,5 % der Patienten für eine autologe PBSZ-Transplantation vorgesehen. 95,8 % der Patienten erhielten als Erstlinientherapie einen neuartigen, gegen das Myelom gerichteten Wirkstoff bzw. planten dessen Anwendung (neuartige Behandlungen schlossen Bortezomib, Lenalidomid oder Thalidomid ein). 60,7 % der Patienten hatten ein vorhergehendes SRE. Über beide Studienarme hinweg lag die Anzahl der Patienten mit Stadium I, Stadium II und Stadium III nach ISS bei Diagnose bei 32,4 %, 38,2 % bzw. 29,3 %.
Die mediane Zahl der angewendeten Dosen lag für Denosumab bei 16 und für Zoledronsäure bei 15.
Ergebnisse zur Wirksamkeit aus Studie 4 sind in Abbildung 2 und Tabelle 3 dargestellt.
Abbildung 2: Kaplan-Meier-Kurve der Zeit bis zum ersten während der Studie aufgetretenen SRE bei Patienten mit neu diagnostiziertem Multiplem Myelom
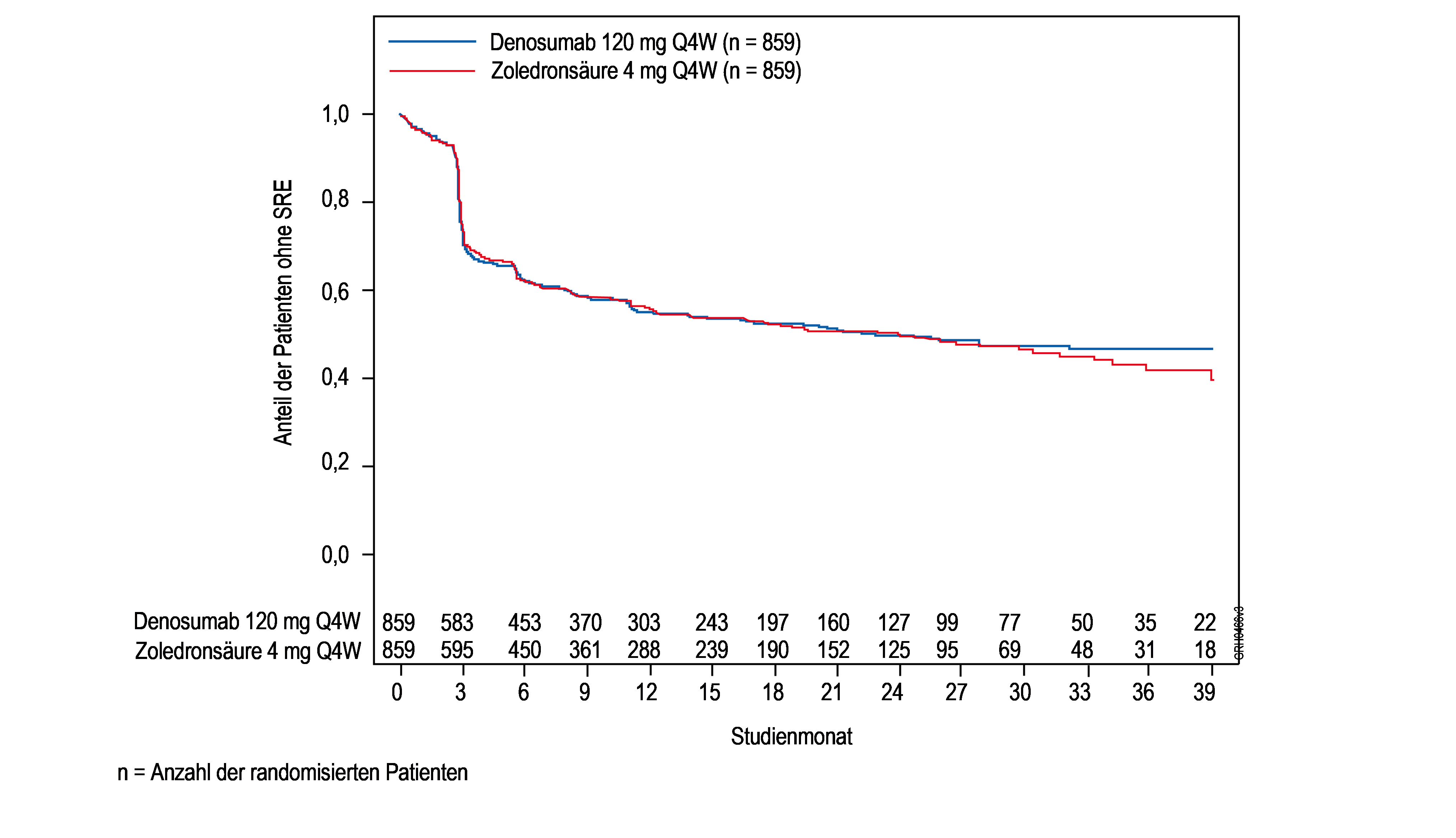
Tabelle 3: Ergebnisse zur Wirksamkeit von Denosumab verglichen mit Zoledronsäure bei Patienten mit neu diagnostiziertem Multiplem Myelom
Denosumab |
Zoledronsäure |
|
Erstes SRE | ||
Anzahl von Patienten mit SREs (%) |
376 (43,8) |
383 (44,6) |
Mediane Zeit bis zum SRE (Monate) |
22,8 (14,7; n. b.) |
23,98 (16,56; 33,31) |
Hazard Ratio (95 % KI) |
0,98 (0,85; 1,14) |
|
Erstes und folgendes SRE | ||
Mittlere Anzahl an Ereignissen/Patient |
0,66 |
0,66 |
Rate Ratio (95 % KI) |
1,01 (0,89; 1,15) |
|
Skelettale Morbiditätsrate pro Jahr |
0,61 |
0,62 |
Erstes SRE oder erste HCM | ||
Mediane Zeit (Monate) |
22,14 (14,26; n. b.) |
21,32 (13,86; 29,7) |
Hazard Ratio (95 % KI) |
0,98 (0,85; 1,12) |
|
Erste Bestrahlung des Knochens | ||
Hazard Ratio (95 % KI) |
0,78 (0,53; 1,14) |
|
Gesamtüberleben | ||
Hazard Ratio (95 % KI) |
0,90 (0,70; 1,16) |
|
n. b. = nicht bestimmbar
HCM = Tumor-Hyperkalzämie (hypercalcaemia of malignancy)
Klinische Wirksamkeit und Sicherheit bei Erwachsenen und skelettal ausgereiften Jugendlichen mit Riesenzelltumoren des Knochens
Die Sicherheit und Wirksamkeit von Denosumab wurden in zwei offenen, einarmigen Studien der Phase II (Studien 5 und 6) untersucht, die 554 Patienten mit Riesenzelltumoren des Knochens einschlossen, welche entweder nicht resezierbar waren oder bei denen eine Operation zu einer schweren Morbidität geführt hätte, sowie in einer prospektiven, multizentrischen, offenen Phase-IV-Studie (Studie 7), in der die Langzeitsicherheit für Patienten, die die Studie 6 abgeschlossen hatten, beurteilt wurde. Die Patienten erhielten 120 mg Denosumab subkutan alle 4 Wochen mit einer Aufsättigungsdosis von 120 mg an den Tagen 8 und 15. Patienten, die die Behandlung mit Denosumab abbrachen, wurden anschließend in die Nachbeobachtungsphase zur Beurteilung der Sicherheit für mindestens 60 Monate aufgenommen. Eine erneute Behandlung mit Denosumab während der Nachbeobachtungsphase zur Beurteilung der Sicherheit war bei Patienten erlaubt, die anfänglich auf die Behandlung mit Denosumab angesprochen hatten (z. B. bei einem Rezidiv).
Studie 5 schloss 37 erwachsene Patienten mit histologisch bestätigten nicht-resezierbaren oder rezidivierten Riesenzelltumoren des Knochens ein. Der Hauptergebnisparameter der Studie war die Ansprechrate, definiert entweder als Elimination von Riesenzellen um mindestens 90 % gegenüber dem Ausgangsbefund (oder komplette Elimination von Riesenzellen in Fällen, in denen Riesenzellen < 5 % der Tumorzellen ausmachten) oder ein durch radiologische Messungen bestätigtes Fehlen einer Progression der Zielläsion in Fällen, bei denen kein histopathologischer Befund vorlag. Von den 35 in die Wirksamkeitsanalyse eingeschlossenen Patienten zeigten 85,7 % (95 % KI: 69,7; 95,2) ein Ansprechen auf die Denosumab-Behandlung. Alle 20 Patienten (100 %) mit einer histologischen Auswertung erfüllten die Ansprechkriterien. Bei den verbleibenden 15 Patienten zeigte sich bei 10 (67 %) keine Progression der Targetläsion in den radiologischen Untersuchungen.
Studie 6 schloss 535 Erwachsene oder skelettal ausgereifte Jugendliche mit Riesenzelltumoren des Knochens ein. Von diesen Patienten waren 28 im Alter von 12 ‑ 17 Jahren. Die Patienten wurden einer von drei Kohorten zugewiesen: Kohorte 1 umfasste Patienten mit operativ nicht therapierbarer Erkrankung (z. B. sakrale, spinale oder multiple Läsionen, einschließlich Lungenmetastasen); Kohorte 2 umfasste Patienten mit operativ therapierbarer Erkrankung, deren geplante Operation zu einer schweren Morbidität geführt hätte (z. B. Gelenkresektion, Gliedmaßenamputation oder Hemipelvektomie); Kohorte 3 umfasste Patienten, die zuvor an Studie 5 teilgenommen hatten und in diese Studie übernommen wurden. Das Hauptziel war die Beurteilung des Sicherheitsprofils von Denosumab bei Patienten mit Riesenzelltumoren des Knochens. Zu den sekundären Ergebnisparametern der Studie zählten die Zeit bis zur Krankheitsprogression (basierend auf der Einschätzung des Prüfarztes) für Kohorte 1 und der Anteil der Patienten ohne jegliche Operation zum Monat 6 für Kohorte 2.
In Kohorte 1 hatten bei der abschließenden Analyse 28 von den 260 behandelten Patienten (10,8 %) eine Krankheitsprogression. In Kohorte 2 hatten sich 219 der 238 (92,0 %; 95 % KI: 87,8 %, 95,1 %) auswertbaren Patienten, die mit Denosumab behandelt wurden, bis Monat 6 keiner Operation unterzogen. Von den 239 Patienten in Kohorte 2, deren Zielläsionen bei Studienbeginn oder während der Studie nicht in der Lunge oder im Weichteilgewebe lokalisiert waren, konnte bei insgesamt 82 Patienten (34,3 %) eine Operation während der Studie vermieden werden. Insgesamt waren die Wirksamkeitsergebnisse bei skelettal ausgereiften Jugendlichen ähnlich wie bei Erwachsenen.
An Studie 7 nahmen 85 erwachsene Patienten teil, die zuvor in die Studie 6 aufgenommen wurden und diese abgeschlossen hatten. Es war den Patienten möglich, die Denosumab-Behandlung für GCTB zu erhalten, und alle Patienten wurden 5 Jahre lang nachbeobachtet. Das Hauptziel war die Beurteilung des Langzeitsicherheitsprofils von Denosumab bei Patienten mit Riesenzelltumoren des Knochens.
Wirkung auf Schmerzen
In der abschließenden Analyse der kombinierten Kohorten 1 und 2 wurde bei 30,8 % der Risikopatienten (d. h. denjenigen, die zu Studienbeginn einen Worst Pain Score von ≥ 2 hatten) innerhalb von 1 Behandlungswoche und bei ≥ 50 % in Woche 5 eine klinisch bedeutsame Reduktion des schlimmsten Schmerzes (d. h. Abnahme um ≥ 2 Punkte seit Studienbeginn) berichtet. Diese Verbesserungen des Schmerzes blieben bei allen nachfolgenden Untersuchungen erhalten.
Kinder und Jugendliche
Die Europäische Arzneimittel-Agentur hat für Denosumab eine Freistellung von der Verpflichtung zur Vorlage von Ergebnissen zu Studien in allen pädiatrischen Altersklassen zur Prävention skelettbezogener Komplikationen bei Patienten mit Knochenmetastasen und in der pädiatrischen Altersklasse unter 12 Jahren bei der Behandlung von Riesenzelltumoren des Knochens gewährt (siehe Abschnitt 4.2 bzgl. Informationen zur Anwendung bei Kindern und Jugendlichen).
In Studie 6 wurde Denosumab in einer Gruppe von 28 jugendlichen Patienten (im Alter von 13 ‑ 17 Jahren) mit Riesenzelltumoren des Knochens untersucht, die eine Ausreifung des Skeletts – definiert über mindestens einen ausgereiften langen Knochen (z. B. geschlossene epiphysäre Wachstumsfuge des Humerus) und ein Körpergewicht ≥ 45 kg – erreicht hatten. Bei einem jugendlichen Patienten mit operativ nicht therapierbarer Erkrankung (n = 14) kam es während der anfänglichen Behandlung zu einem Rezidiv. Dreizehn der 14 Patienten mit operativ therapierbarer Erkrankung, deren geplante Operation zu einer schweren Morbidität geführt hätte, hatten sich bis Monat 6 keiner Operation unterzogen.
Resorption
Nach subkutaner Anwendung betrug die Bioverfügbarkeit 62 %.
Biotransformation
Denosumab ist als natives Immunglobulin ausschließlich aus Aminosäuren und Kohlenhydraten aufgebaut, und es ist unwahrscheinlich, dass es über den Mechanismus des hepatischen Metabolismus ausgeschieden wird. Es ist zu erwarten, dass die Metabolisierung und Elimination dem Weg des Abbaus von Immunglobulinen folgen und in der Degradierung zu kleinen Peptiden und einzelnen Aminosäuren resultieren.
Elimination
Bei Patienten mit fortgeschrittener Krebserkrankung, die wiederholte Dosierungen von 120 mg alle 4 Wochen erhielten, wurde eine ungefähr 2‑fache Akkumulation der Denosumab-Serumkonzentrationen beobachtet. Ein Steady-State wurde nach 6 Monaten erreicht, was der zeitunabhängigen Pharmakokinetik entsprach. Bei Patienten mit Multiplem Myelom, die 120 mg alle 4 Wochen erhielten, variierten die medianen Talspiegel zwischen den Monaten 6 und 12 um weniger als 8 %. Bei Patienten mit Riesenzelltumoren des Knochens, die 120 mg alle 4 Wochen mit einer Aufsättigungsdosis an den Tagen 8 und 15 erhielten, wurde ein Steady-State innerhalb des ersten Monats der Behandlung erreicht. Zwischen Woche 9 und 49 variierten die medianen Talspiegel um weniger als 9 %. Bei Patienten, die die Anwendung von 120 mg alle 4 Wochen abgebrochen haben, betrug die mittlere Halbwertszeit 28 Tage (Bereich 14 bis 55 Tage).
Eine pharmakokinetische Populationsanalyse ergab keine Hinweise auf klinisch signifikante Änderungen der systemischen Exposition von Denosumab im Steady-State in Bezug auf Alter (18 bis 87 Jahre), ethnische Zugehörigkeit (Schwarze, Hispanos, Asiaten und Kaukasier wurden untersucht), Geschlecht, Entität solider Tumoren oder Patienten mit Multiplem Myelom. Ein steigendes Körpergewicht war mit einer verminderten systemischen Exposition assoziiert, und umgekehrt. Die Änderungen wurden nicht als klinisch relevant angesehen, da auf Knochenumsatzmarkern basierende pharmakodynamische Wirkungen über einen breiten Körpergewichtsbereich konsistent waren.
Linearität/Nicht‑Linearität
Denosumab zeigte eine nicht-lineare Pharmakokinetik mit Dosen über einen breiten Dosierungsbereich, jedoch annähernd dosisproportionale Anstiege nach Exposition mit Dosen von 60 mg (oder 1 mg/kg) und höher. Die Nicht-Linearität resultiert wahrscheinlich aus einem bei niedrigen Konzentrationen wichtigen sättigbaren zielstruktur-vermittelten Eliminationsweg.
Nierenfunktionsstörung
In Studien mit Denosumab (60 mg, n = 55 und 120 mg, n = 32) bei Patienten ohne fortgeschrittene Krebserkrankung, aber mit unterschiedlichen Graden der Nierenfunktion, einschließlich dialysepflichtiger Patienten, hatte der Grad der Nierenfunktionsstörung keine Auswirkung auf die Pharmakokinetik von Denosumab. Daher ist eine Dosisanpassung bei Nierenfunktionsstörungen nicht notwendig. Es ist keine Überwachung der Nierenfunktion bei der Denosumab-Anwendung erforderlich.
Leberfunktionsstörung
Es wurde keine spezifische Studie bei Patienten mit Leberfunktionsstörung durchgeführt. Im Allgemeinen werden monoklonale Antikörper nicht über den Mechanismus des hepatischen Metabolismus eliminiert. Es wird nicht davon ausgegangen, dass eine Leberfunktionsstörung die Pharmakokinetik von Denosumab beeinflusst.
Ältere Patienten
Insgesamt wurden keine Unterschiede bezüglich Sicherheit oder Wirksamkeit zwischen geriatrischen Patienten und jüngeren Patienten beobachtet. Kontrollierte klinische Studien mit Denosumab bei Patienten im Alter von über 65 Jahren mit fortgeschrittenen Krebserkrankungen und Knochenbefall zeigten eine vergleichbare Wirksamkeit und Sicherheit bei älteren und bei jüngeren Patienten. Es ist keine Dosisanpassung für ältere Patienten erforderlich.
Kinder und Jugendliche
Bei skelettal ausgereiften Jugendlichen (im Alter von 12 ‑ 17 Jahren) mit Riesenzelltumoren des Knochens, die 120 mg alle 4 Wochen mit einer Aufsättigungsdosis an den Tagen 8 und 15 erhielten, war die Pharmakokinetik von Denosumab ähnlich, wie sie bei erwachsenen Patienten mit Riesenzelltumoren des Knochens beobachtet wurde.
Da die biologische Aktivität von Denosumab bei Tieren spezifisch für nicht-menschliche Primaten ist, wurde die Untersuchung von genetisch veränderten („Knockout“) Mäusen oder die Anwendung von anderen biologischen Inhibitoren des RANK/RANKL-Signalwegs, wie OPG‑Fc und RANK‑Fc, verwendet, um die pharmakodynamischen Eigenschaften von Denosumab in Nagetiermodellen zu evaluieren.
In Mausmodellen zu Knochenmetastasen von Östrogenrezeptor-positivem und ‑negativem menschlichem Mammakarzinom, Prostatakarzinom und nicht-kleinzelligem Bronchialkarzinom reduzierte OPG‑Fc osteolytische, osteoblastische und osteolytische/osteoblastische Läsionen, verzögerte die Entstehung von de novo-Knochenmetastasen und reduzierte das Tumorwachstum im Skelett. Wenn OPG‑Fc in diesen Modellen mit Hormontherapie (Tamoxifen) oder Chemotherapie (Docetaxel) kombiniert wurde, gab es eine additive Hemmung von Tumorwachstum im Skelett bei Mamma-, Prostata- oder Bronchialkarzinom. In einem Mausmodell zur Tumorinduktion in der Brustdrüse reduzierte RANK‑Fc die hormoninduzierte Proliferation des Brustdrüsenepithels und verzögerte die Tumorentstehung.
Standardtests zur Untersuchung des genotoxischen Potenzials von Denosumab wurden nicht durchgeführt, da solche Tests für dieses Molekül nicht relevant sind. Bedingt durch seine Eigenschaften ist es jedoch unwahrscheinlich, dass Denosumab ein genotoxisches Potenzial besitzt.
Das karzinogene Potenzial von Denosumab wurde nicht in tierexperimentellen Langzeitstudien untersucht.
In Studien zur Toxizität mit einmaliger oder wiederholter Anwendung bei Javaneraffen hatten Denosumab-Dosierungen, die in einer 2,7‑ bis 15‑fach höheren systemischen Exposition im Vergleich zur empfohlenen humantherapeutischen Dosis resultierten, keinen Einfluss auf die kardiovaskuläre Physiologie, die männliche oder die weibliche Fertilität und verursachten keine spezifischen Toxizitäten an Zielorganen.
In einer Studie mit Javaneraffen, die im Zeitraum, der dem ersten Trimester einer Schwangerschaft entspricht, mit Denosumab behandelt wurden, verursachten Denosumab-Dosierungen, die in einer 9‑mal höheren systemischen Exposition im Vergleich zur empfohlenen humantherapeutischen Dosis resultierten, keine Toxizität im Muttertier oder Schädigung des Fötus während einer Periode, die dem ersten Trimester entsprach, wobei fetale Lymphknoten nicht untersucht wurden.
In einer anderen Studie mit Javaneraffen, bei denen Denosumab während der gesamten Trächtigkeit in Dosierungen angewendet wurde, die hinsichtlich der systemischen Exposition um das 12‑Fache über der humantherapeutischen Dosis lagen, kam es vermehrt zu Totgeburten und postnataler Mortalität, abnormem Knochenwachstum, welches in einer reduzierten Knochenstärke, reduzierter Hämatopoese und Zahnfehlstellung resultierte, Fehlen von peripheren Lymphknoten sowie verringertem Wachstum der Neugeborenen. Es wurde kein NOAEL (no observed adverse effect level – Dosis ohne beobachtete schädigende Wirkung) für den Einfluss auf die Reproduktion ermittelt. Sechs Monate nach der Geburt regenerierten sich die Knochenveränderungen, und es zeigte sich keine Wirkung auf den Zahndurchbruch. Allerdings blieb die Wirkung auf die Lymphknoten und die Zahnfehlstellung bestehen, und in einem Tier wurde eine minimale bis mäßige Mineralisierung in mehreren Geweben beobachtet (Zusammenhang mit der Behandlung ungewiss). Es zeigte sich kein Hinweis auf eine Schädigung des Muttertieres vor der Geburt; schädliche Wirkungen auf das Muttertier traten während der Geburt selten auf. Die Entwicklung der mütterlichen Milchdrüsen verlief normal.
In präklinischen Studien zur Knochenqualität bei Affen unter Langzeitbehandlung mit Denosumab ging eine Reduktion des Knochenumsatzes mit einer Verbesserung der Knochenstärke und mit normaler Knochenhistologie einher.
In transgenen männlichen Mäusen, die humane RANK-Liganden (huRANKL) exprimieren („Knockin-Mäuse“) und bei denen eine transkortikale Fraktur ausgelöst worden war, verzögerte Denosumab im Vergleich zur Kontrolle den Abbau des Knorpels und den Umbau des Fraktur-Kallus. Die biomechanische Stärke war jedoch nicht nachteilig beeinflusst.
Knockout-Mäuse ohne RANK oder RANKL zeigten in präklinischen Studien eine fehlende Milchproduktion aufgrund einer Hemmung der Brustdrüsenreifung (lobulo-alveoläre Drüsenentwicklung während der Schwangerschaft) und eine Beeinträchtigung der Lymphknotenbildung. Neonatale RANK/RANKL-Knockout-Mäuse zeigten ein reduziertes Körpergewicht, reduziertes Knochenwachstum, veränderte Wachstumsfugen und ein Fehlen des Zahndurchbruchs. Reduziertes Knochenwachstum, veränderte Wachstumsfugen und eine Beeinträchtigung des Zahndurchbruchs wurden ebenfalls in Studien bei neonatalen Ratten beobachtet, denen RANKL-Inhibitoren verabreicht wurden. Diese Veränderungen waren nach Absetzen des RANKL-Inhibitors partiell reversibel. Adoleszente Primaten, die im Vergleich zur klinischen Exposition mit 2,7‑ und 15‑fachen Dosen (10 und 50 mg/kg Dosis) von Denosumab behandelt wurden, zeigten abnorme Wachstumsfugen. Daher könnte die Behandlung mit Denosumab bei Kindern mit offenen Wachstumsfugen zu einem beeinträchtigten Knochenwachstum und zu einer Hemmung des Zahndurchbruchs führen.
Essigsäure*
Natriumacetat-Trihydrat (zur pH‑Wert-Einstellung)*
Sorbitol (E 420)
Polysorbat 20 (E 432)
Wasser für Injektionszwecke
* Der Acetatpuffer wird durch Mischen von Essigsäure mit Natriumacetat-Trihydrat gebildet.
Da keine Kompatibilitätsstudien durchgeführt wurden, darf dieses Arzneimittel nicht mit anderen Arzneimitteln gemischt werden.
4 Jahre.
Osenvelt kann nach der Entnahme aus dem Kühlschrank bei Temperaturen von maximal 30 °C für einen einmaligen Zeitraum von bis zu 63 Tagen in der Originalverpackung aufbewahrt werden, wobei das ursprüngliche Verfallsdatum nicht überschritten werden darf. Falls erforderlich, kann Osenvelt innerhalb dieser 63 Tage einmalig in den Kühlschrank zurückgelegt und dort bis zum ursprünglichen Verfallsdatum aufbewahrt werden.
Verwerfen Sie Osenvelt, wenn es nicht innerhalb des einmaligen Zeitraums von 63 Tagen außerhalb des Kühlschranks oder bis zum ursprünglichen Verfallsdatum verwendet wird, je nachdem, was zuerst eintritt.
Im Kühlschrank lagern (2 °C – 8 °C).
Nicht einfrieren.
Die Durchstechflasche im Umkarton aufbewahren, um den Inhalt vor Licht zu schützen.
1,7 ml Lösung in einer Durchstechflasche zum Einmalgebrauch aus Glas Typ I mit einem (Butyl-) Gummistopfen und einem Aluminiumsiegel mit Flip-off-Deckel.
Packung mit 1, 3 oder 4 Durchstechflaschen.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
Vor der Anwendung soll die Osenvelt-Lösung optisch kontrolliert werden. Injizieren Sie die Lösung nicht, falls sie sichtbare Partikel enthält oder trübe oder verfärbt ist.
Nicht schütteln.
Um Beschwerden an der Injektionsstelle zu vermeiden, soll die Durchstechflasche vor der Injektion Raumtemperatur (bis zu 30 °C) annehmen und die Injektion soll langsam erfolgen.
Der gesamte Inhalt der Durchstechflasche soll injiziert werden.
Für die Anwendung von Denosumab wird eine 27-Gauge-Nadel empfohlen.
Die Durchstechflasche soll nicht erneut angestochen werden.
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu beseitigen.
Celltrion Healthcare Hungary Kft.
1062 Budapest
Váci út 1-3. WestEnd Office Building B torony
Ungarn
EU/1/24/1904/001
EU/1/24/1904/002
EU/1/24/1904/003
Datum der Erteilung der Zulassung: 14. Februar 2025
Januar 2026
Ausführliche Informationen zu diesem Arzneimittel sind auf den Internetseiten der Europäischen Arzneimittel-Agentur https://www.ema.europa.eu verfügbar.
Verschreibungspflichtig
Celltrion Healthcare Deutschland GmbH
61348 Bad Homburg vor der Höhe
Tel: 030 346494150
E-Mail: infoDE@celltrionhc.com