▼Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung zu melden. Hinweise zur Meldung von Nebenwirkungen, siehe Abschnitt 4.8.
Opdualag 240 mg/80 mg Konzentrat zur Herstellung einer Infusionslösung
Jeder ml Konzentrat zur Herstellung einer Infusionslösung enthält 12 mg Nivolumab (nivolumab) und 4 mg Relatlimab (relatlimab).
Eine Durchstechflasche mit 20 ml enthält 240 mg Nivolumab und 80 mg Relatlimab.
Nivolumab und Relatlimab sind humane Immunglobulin‑G4‑(IgG4) monoklonale Antikörper, die mittels rekombinanter DNA‑Technologie aus Ovarialzellen des Chinesischen Hamsters gewonnen werden.
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
Konzentrat zur Herstellung einer Infusionslösung (steriles Konzentrat).
Klare bis opaleszierende, farblose bis leicht gelbe Flüssigkeit, die praktisch keine Schwebstoffe enthält.
Die Lösung hat einen pH‑Wert von ca. 5,8 und eine Osmolalität von ca. 310 mOsm/kg.
Opdualag ist für die Erstlinienbehandlung des fortgeschrittenen (nicht resezierbaren oder metastasierten) Melanoms mit Tumorzell‑PD‑L1‑Expression < 1 % bei Erwachsenen und Jugendlichen im Alter ab 12 Jahren indiziert.
Die Behandlung muss von einem auf dem Gebiet der Krebsbehandlung erfahrenen Arzt eingeleitet und überwacht werden.
Patienten, die mit Opdualag behandelt werden, ist die Patientenkarte auszuhändigen und sie müssen über die Risiken von Opdualag informiert werden (siehe Packungsbeilage).
PD‑L1‑Testung
Patienten sollten basierend auf einer mittels validierten Tests bestätigten Tumor‑PD‑L1‑Expression für die Behandlung mit Opdualag selektiert werden (siehe Abschnitte 4.4 und 5.1).
Dosierung
Die empfohlene Dosis für Erwachsene und Jugendliche im Alter ab 12 Jahren beträgt 480 mg Nivolumab und 160 mg Relatlimab alle 4 Wochen als intravenöse Infusion über 30 Minuten verabreicht. Diese Dosis ist für jugendliche Patienten mit einem Gewicht von mindestens 30 kg belegt (siehe Abschnitt 5.2)
Die Behandlung mit Opdualag sollte so lange fortgesetzt werden, wie ein klinischer Nutzen besteht oder bis die Behandlung vom Patienten nicht mehr vertragen wird. Eine Dosissteigerung oder ‑reduktion wird nicht empfohlen. Je nach individueller Sicherheit und Verträglichkeit ist möglicherweise ein Aufschieben einer Dosis oder ein dauerhafter Abbruch der Behandlung erforderlich. Richtlinien zum dauerhaften Absetzen oder Aufschieben von Dosen werden in Tabelle 1 beschrieben. Detaillierte Richtlinien zur Behandlung immunvermittelter Nebenwirkungen werden im Abschnitt 4.4 beschrieben.
Tabelle 1: Empfohlene Behandlungsmodifikationen für Opdualag
Immunvermittelte Nebenwirkung |
Schweregrad |
Behandlungsmodifikation |
Immunvermittelte Pneumonitis |
Pneumonitis Grad 2 |
Dosis(en) aufschieben bis sich die Symptome zurückgebildet haben, radiologisch erkennbare Veränderungen sich gebessert haben und die Behandlung mit Corticosteroiden beendet ist |
Pneumonitis Grad 3 oder 4 |
Setzen Sie die Behandlung dauerhaft ab |
|
Immunvermittelte Kolitis |
Diarrhö oder Kolitis Grad 2 oder 3 |
Dosis(en) aufschieben bis sich die Symptome zurückgebildet haben und die Behandlung mit Corticosteroiden, falls erforderlich, beendet ist |
Diarrhö oder Kolitis Grad 4 |
Setzen Sie die Behandlung dauerhaft ab |
|
Immunvermittelte Hepatitis |
Erhöhung der Aspartat‑Aminotransferase (AST) oder Alanin‑Aminotransferase (ALT) auf das mehr als 3‑Fache und bis zu 5‑Fache des oberen Normalwertes (Upper Limit of Normal, ULN) |
Dosis(en) aufschieben bis die Laborwerte auf den Ausgangswert zurückgegangen sind und die Behandlung mit Corticosteroiden, falls erforderlich, beendet ist |
Erhöhung von AST oder ALT auf mehr als das 5‑Fache des ULN, unabhängig vom Ausgangswert |
Setzen Sie die Behandlung dauerhaft ab |
|
Immunvermittelte Nephritis und Nierenfunktionsstörung |
Kreatinin‑Erhöhung Grad 2 oder 3 |
Dosis(en) aufschieben bis das Kreatinin auf den Ausgangswert zurückgegangen ist und die Behandlung mit Corticosteroiden beendet ist |
Kreatinin‑Erhöhung Grad 4 |
Setzen Sie die Behandlung dauerhaft ab |
|
Immunvermittelte Endokrinopathien |
Symptomatische Grad 2 oder 3 Hypothyreose, Hyperthyreose, Hypophysitis |
Dosis(en) aufschieben bis sich die Symptome zurückgebildet haben und die Behandlung mit Corticosteroiden (falls nötig bei Symptomen akuter Entzündung) beendet ist. Die Behandlung mit Opdualag sollte begleitend zur Hormonsubstitutionstherapiea fortgeführt werden, sofern keine Symptome auftreten |
Grad 4 Hypothyreose |
Setzen Sie die Behandlung dauerhaft ab |
|
Immunvermittelte Nebenwirkungen der Haut |
Ausschlag Grad 3 |
Dosis(en) aufschieben bis sich die Symptome zurückgebildet haben und die Behandlung mit Corticosteroiden beendet ist |
Verdacht auf Stevens‑Johnson‑Syndrom (SJS) oder toxische epidermale Nekrolyse (TEN) |
Dosis(en) aufschieben |
|
Ausschlag Grad 4 |
Setzen Sie die Behandlung dauerhaft ab (siehe Abschnitt 4.4) |
|
Immunvermittelte Myokarditis |
Grad 2 Myokarditis |
Dosis(en) aufschieben bis sich die Symptome zurückgebildet haben und die Behandlung mit Corticosteroiden beendet istb |
Grad 3 oder 4 Myokarditis |
Setzen Sie die Behandlung dauerhaft ab |
|
Andere immunvermittelte Nebenwirkungen |
Grad 3 (erstes Auftreten) |
Dosis(en) aufschieben |
Grad 4 oder wiederauftretender Grad 3; persistierender Grad 2 oder 3 trotz Behandlungsmodifikation; Fälle, in denen die Corticosteroiddosis nicht auf 10 mg Prednison oder das entsprechende Äquivalent pro Tag reduziert werden kann |
Setzen Sie die Behandlung dauerhaft ab |
|
Myokarditis‑Myositis-Myasthenia‑gravis‑Overlap-Syndromc |
Grad 2 Myokarditis-Myositis-Myasthenia‑gravis-Overlap-Syndrom |
Dosis(en) aufschieben bis sich die Symptome zurückgebildet haben und die Behandlung mit Corticosteroiden beendet istb |
Grad 3 oder 4 Myokarditis-Myositis‑Myasthenia‑gravis-Overlap‑Syndrom |
Behandlung dauerhaft absetzen |
|
Hinweis: Toxizitätsgrade entsprechen den Kriterien des National Cancer Institute (National Cancer Institute Common Terminology Criteria for Adverse Events), Version 5.0 (NCI‑CTCAE v5). | ||
Spezielle Patientenpopulationen
Kinder und Jugendliche
Die Sicherheit und Wirksamkeit von Opdualag bei Kindern unter 12 Jahren ist nicht erwiesen. Es liegen keine Daten vor (siehe Abschnitt 5.2).
Ältere Menschen
Bei älteren Patienten (≥ 65 Jahre) ist keine Dosisanpassung erforderlich (siehe Abschnitt 5.2).
Nierenfunktionsbeeinträchtigung
Bei Patienten mit leichter oder mäßiger Niereninsuffizienz ist keine Dosisanpassung erforderlich (siehe Abschnitt 5.2). Die Daten von Patienten mit schwerer Niereninsuffizienz sind begrenzt und lassen keine Schlussfolgerungen für diese Population zu.
Beeinträchtigung der Leber
Bei Patienten mit leicht oder mäßig eingeschränkter Leberfunktion ist keine Dosisanpassung erforderlich (siehe Abschnitt 5.2). Die Daten von Patienten mit schwerer Leberfunktionsstörung sind begrenzt und lassen keine Schlussfolgerungen für diese Population zu.
Art der Anwendung
Opdualag ist nur zur intravenösen Anwendung vorgesehen. Es wird als intravenöse Infusion über einen Zeitraum von 30 Minuten verabreicht.
Opdualag darf nicht als intravenöse Druck‑ oder Bolus‑Injektion verabreicht werden.
Opdualag kann ohne Verdünnung angewendet werden oder kann mit einer Natriumchlorid‑Injektionslösung 9 mg/ml (0,9 %) oder einer Glucose‑Injektionslösung 50 mg/ml (5 %) verdünnt werden (siehe Abschnitt 6.6).
Für Anweisungen zur Zubereitung und Handhabung des Arzneimittels vor der Anwendung siehe Abschnitt 6.6.
Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
Rückverfolgbarkeit
Um die Rückverfolgbarkeit biologischer Arzneimittel zu verbessern, müssen die Bezeichnung des Arzneimittels und die Chargenbezeichnung des angewendeten Arzneimittels eindeutig dokumentiert werden.
Beurteilung des PD‑L1‑Status
Es ist wichtig, für die Beurteilung des PD‑L1‑Tumorstatus eine gut validierte und robuste Methode zu verwenden.
Immunvermittelte Nebenwirkungen
Unter Nivolumab in Kombination mit Relatlimab können immunvermittelte Nebenwirkungen auftreten, die ein geeignetes Management erfordern, einschließlich Einleitung einer Corticosteroid‑Behandlung und Behandlungsmodifikationen (siehe Abschnitt 4.2).
Immunvermittelte Nebenwirkungen, die mehr als ein Körpersystem betreffen, können gleichzeitig auftreten.
Patienten sollten engmaschig überwacht werden (mindestens bis zu 5 Monate nach der letzten Dosis), da Nebenwirkungen unter Opdualag jederzeit während oder nach der Behandlung auftreten können.
Bei vermuteten immunvermittelten Nebenwirkungen sollte zur Bestätigung der Ätiologie oder zum Ausschluss anderer Ursachen eine angemessene Abklärung durchgeführt werden. In Abhängigkeit vom Schweregrad der Nebenwirkung sollte die Behandlung mit Opdualag aufgeschoben und den Patienten Corticosteroide gegeben werden. Wenn eine Immunsuppression mit Corticosteroiden zur Behandlung von Nebenwirkungen eingesetzt wird, sollte die Corticosteroidtherapie nach Besserung der Nebenwirkungen über mindestens einen Monat ausgeschlichen werden. Ein zu schnelles Ausschleichen kann zur Verschlechterung oder Wiederauftreten der Nebenwirkung führen. Wenn es trotz Corticosteroidanwendung zu einer Verschlechterung oder keiner Besserung kommt, sollten zusätzlich nicht‑steroidale Immunsuppressiva gegeben werden.
Bei Patienten mit einer bestehenden Autoimmunerkrankung (autoimmune disease, AID) deuten Daten aus Beobachtungsstudien darauf hin, dass das Risiko für immunvermittelte Nebenwirkungen nach einer Therapie mit Immun-Checkpoint-Inhibitoren im Vergleich zu Patienten ohne bestehende AID erhöht sein kann. Darüber hinaus traten häufig Schübe der zugrunde liegenden AID auf, die jedoch meistens leicht und beherrschbar waren. Allerdings liegen speziell zur Kombination von Nivolumab und Relatlimab nur sehr wenige Daten vor.
Die Behandlung mit Opdualag sollte nicht fortgesetzt werden, solange der Patient immunsuppressive Dosen von Corticosteroiden oder andere Immunsuppressiva erhält. Prophylaktisch können Antibiotika gegeben werden, um opportunistische Infektionen bei Patienten zu verhindern, die immunsuppressiv behandelt werden.
Opdualag muss bei jeder schweren wiederauftretenden immunvermittelten Nebenwirkung und bei jeder lebensbedrohlichen immunvermittelten Nebenwirkung dauerhaft abgesetzt werden.
Immunvermittelte Pneumonitis
Unter Nivolumab in Kombination mit Relatlimab wurden schwere Pneumonitiden oder interstitielle Lungenerkrankungen, einschließlich eines tödlichen Falls, beobachtet (siehe Abschnitt 4.8). Die Patienten sollten auf Anzeichen und Symptome einer Pneumonitis wie beispielsweise radiologische Veränderungen (z. B. fokale milchglasartige Dichteanhebung, fleckige Infiltrate), Dyspnoe und Hypoxie überwacht werden. Infektiöse und krankheitsbedingte Ursachen sollten ausgeschlossen werden.
Bei Pneumonitis Grad 3 oder 4 muss Opdualag dauerhaft abgesetzt und mit einer Behandlung mit Corticosteroiden in einer Dosierung von 2 bis 4 mg/kg/Tag Methylprednisolon‑Äquivalent begonnen werden.
Bei (symptomatischer) Pneumonitis Grad 2 sollte die Behandlung mit Opdualag aufgeschoben und mit einer Behandlung mit Corticosteroiden in einer Dosierung von 1 mg/kg/Tag Methylprednisolon‑Äquivalent begonnen werden. Bei einer Besserung kann die Behandlung mit Opdualag nach dem Ausschleichen der Corticosteroide fortgesetzt werden. Wenn es trotz der Behandlung mit Corticosteroiden zu einer Verschlechterung oder keiner Besserung kommt, sollte die Corticosteroid‑Dosis auf 2 bis 4 mg/kg/Tag Methylprednisolon‑Äquivalent erhöht werden und Opdualag muss dauerhaft abgesetzt werden.
Immunvermittelte Kolitis
Unter Nivolumab in Kombination mit Relatlimab wurden schwere Diarrhö oder Kolitis beobachtet (siehe Abschnitt 4.8). Patienten sollten auf Diarrhö und weitere Symptome einer Kolitis wie Abdominalschmerzen und Schleim und/oder Blut im Stuhl überwacht werden. Cytomegalievirus (CMV)‑Infektion/‑Reaktivierung wurde bei Patienten mit Corticosteroid‑refraktärer immunvermittelter Kolitis berichtet. Infektiöse und andere Ursachen der Diarrhö sind deshalb durch geeignete Labortests und zusätzliche Untersuchungen auszuschließen. Falls sich die Diagnose der Corticosteroid‑refraktären Kolitis bestätigt, sollte zusätzlich zu dem Corticosteroid ein anderes Immunsuppressivum oder ein Austausch der Corticosteroidtherapie in Betracht gezogen werden.
Bei Diarrhö oder Kolitis Grad 4 muss Opdualag dauerhaft abgesetzt werden und es sollte eine Behandlung mit Corticosteroiden in einer Dosierung von 1 bis 2 mg/kg/Tag Methylprednisolon‑Äquivalent begonnen werden.
Bei Diarrhö oder Kolitis Grad 3 sollte die Behandlung mit Opdualag aufgeschoben und eine Behandlung mit Corticosteroiden in einer Dosierung von 1 bis 2 mg/kg/Tag Methylprednisolon‑Äquivalent begonnen werden. Bei einer Besserung kann die Behandlung mit Opdualag nach dem Ausschleichen der Corticosteroide fortgesetzt werden. Wenn es trotz der Behandlung mit Corticosteroiden zu einer Verschlechterung oder keiner Besserung kommt, muss die Behandlung mit Opdualag dauerhaft abgesetzt werden.
Bei Diarrhö oder Kolitis Grad 2 sollte die Behandlung mit Opdualag aufgeschoben werden. Bei anhaltenden Beschwerden sollte mit Corticosteroiden in einer Dosierung von 0,5 bis 1 mg/kg/Tag Methylprednisolon‑Äquivalent behandelt werden. Bei einer Besserung kann die Behandlung mit Opdualag nach dem Ausschleichen der Corticosteroide bei Bedarf fortgesetzt werden. Wenn es trotz der Behandlung mit Corticosteroiden zu einer Verschlechterung oder keiner Besserung kommt, sollte die Corticosteroid‑Dosis auf 1 bis 2 mg/kg/Tag Methylprednisolon‑Äquivalent erhöht werden und Opdualag muss dauerhaft abgesetzt werden.
Immunvermittelte Hepatitis
Unter Nivolumab in Kombination mit Relatlimab wurden schwere Hepatitiden beobachtet (siehe Abschnitt 4.8). Patienten sollten auf Anzeichen und Symptome einer Hepatitis wie ein Anstieg der Transaminasen und des Gesamtbilirubins überwacht werden. Infektiöse und krankheitsbedingte Ursachen sind auszuschließen.
Bei Erhöhung von AST oder ALT unabhängig vom Ausgangswert auf mehr als das 5‑Fache des ULN, Erhöhung des Gesamtbilirubins auf mehr als das 3‑Fache des ULN oder gleichzeitiger Erhöhung von AST oder ALT auf mehr als das 3‑Fache des ULN und Erhöhung des Gesamtbilirubins auf mehr als das 2‑Fache des ULN muss Opdualag dauerhaft abgesetzt werden und es sollte eine Behandlung mit Corticosteroiden in einer Dosierung von 1 bis 2 mg/kg/Tag Methylprednisolon‑Äquivalent begonnen werden.
Bei Erhöhung von AST/ALT auf das mehr als 3‑Fache und das bis zu 5‑Fache des ULN oder Erhöhung des Gesamtbilirubins auf das mehr als 1,5‑Fache und das bis zu 3‑Fache des ULN sollte die Behandlung mit Opdualag aufgeschoben werden. Bei anhaltenden Erhöhungen dieser Laborwerte sollte mit Corticosteroiden in einer Dosierung von 0,5 bis 1 mg/kg/Tag Methylprednisolon‑Äquivalent behandelt werden. Bei einer Besserung kann die Behandlung mit Opdualag nach dem Ausschleichen der Corticosteroide bei Bedarf fortgesetzt werden. Wenn es trotz der Behandlung mit Corticosteroiden zu einer Verschlechterung oder keiner Besserung kommt, sollte die Corticosteroid‑Dosis auf 1 bis 2 mg/kg/Tag Methylprednisolon‑Äquivalent erhöht werden und Opdualag muss dauerhaft abgesetzt werden.
Immunvermittelte Nephritis und Nierenfunktionsstörung
Unter Nivolumab in Kombination mit Relatlimab wurden schwere Nephritiden und Nierenfunktionsstörungen beobachtet (siehe Abschnitt 4.8). Die Patienten sind auf Anzeichen und Symptome einer Nephritis oder Nierenfunktionsstörung zu überwachen. Bei den meisten Patienten tritt eine asymptomatische Kreatininerhöhung im Serum auf. Krankheitsbedingte Ursachen sind auszuschließen.
Bei einer Kreatininerhöhung im Serum Grad 4 muss Opdualag dauerhaft abgesetzt werden und es sollte eine Behandlung mit Corticosteroiden in einer Dosierung von 1 bis 2 mg/kg/Tag Methylprednisolon‑Äquivalent begonnen werden.
Bei einer Kreatininerhöhung im Serum Grad 2 oder 3 sollte die Behandlung mit Opdualag aufgeschoben und eine Behandlung mit Corticosteroiden in einer Dosierung von 0,5 bis 1 mg/kg/Tag Methylprednisolon‑Äquivalent begonnen werden. Bei einer Besserung kann die Behandlung mit Opdualag nach dem Ausschleichen der Corticosteroide fortgesetzt werden. Wenn es trotz der Behandlung mit Corticosteroiden zu einer Verschlechterung oder keiner Besserung kommt, sollte die Corticosteroid‑Dosis auf 1 bis 2 mg/kg/Tag Methylprednisolon‑Äquivalent erhöht werden und Opdualag muss dauerhaft abgesetzt werden.
Immunvermittelte Endokrinopathien
Unter Nivolumab in Kombination mit Relatlimab wurden schwere Endokrinopathien, einschließlich Hypothyreose, Hyperthyreose, Nebenniereninsuffizienz (einschließlich sekundärer Nebennierenrindeninsuffizienz), Hypophysitis (einschließlich Hypophyseninsuffizienz) und Diabetes mellitus beobachtet. Unter Nivolumab‑Monotherapie wurden Fälle von diabetischer Ketoazidose beobachtet und könnten möglicherweise auch unter Nivolumab in Kombination mit Relatlimab auftreten (siehe Abschnitt 4.8).
Patienten sollten hinsichtlich klinischer Anzeichen und Symptome von Endokrinopathien und Hyperglykämie und Veränderungen der Schilddrüsenfunktion überwacht werden (zu Beginn der Behandlung, regelmäßig während der Behandlung und wenn es nach klinischer Beurteilung angezeigt ist). Patienten können mit Ermüdung/Fatigue, Kopfschmerzen, psychischen Veränderungen, Abdominalschmerzen, Veränderung der Stuhlgewohnheiten und Hypotonie oder unspezifischen Symptomen vorstellig werden, die anderen Ursachen, wie etwa Gehirnmetastasen oder der zugrundeliegenden Erkrankung, ähneln können. Bis eine andere Ätiologie identifiziert worden ist, sollten Anzeichen oder Symptome von Endokrinopathien als immunvermittelt betrachtet werden.
Schilddrüsenfunktionsstörung
Bei symptomatischer Hypothyreose sollte die Behandlung mit Opdualag aufgeschoben und bei Bedarf mit einer Hormonsubstitutionstherapie begonnen werden. Bei symptomatischer Hyperthyreose sollte die Behandlung mit Opdualag aufgeschoben und bei Bedarf eine Behandlung mit Thyreostatika begonnen werden. Bei Verdacht auf eine akute Entzündung der Schilddrüse sollte auch eine Behandlung mit Corticosteroiden in einer Dosierung von 1 bis 2 mg/kg/Tag Methylprednisolon‑Äquivalent in Betracht gezogen werden. Bei einer Besserung kann die Behandlung mit Opdualag nach dem Ausschleichen der Corticosteroide bei Bedarf fortgesetzt werden. Die Schilddrüsenfunktion sollte weiterhin überwacht werden, um sicherzustellen, dass die passende Hormonsubstitutionstherapie angewandt wird. Bei lebensbedrohlicher (Grad 4) Hyperthyreose oder Hypothyreose muss Opdualag dauerhaft abgesetzt werden.
Nebenniereninsuffizienz
Bei schwerwiegender (Grad 3) oder lebensbedrohlicher (Grad 4) Nebenniereninsuffizienz muss Opdualag dauerhaft abgesetzt werden. Bei symptomatischer Nebenniereninsuffizienz Grad 2 sollte die Behandlung mit Opdualag aufgeschoben und bei Bedarf mit einer physiologischen Corticosteroid‑Ersatztherapie begonnen werden. Die Nebennierenfunktion und Hormonspiegel sollten weiterhin überwacht werden, um sicherzustellen, dass die passende Corticosteroid‑Ersatztherapie angewandt wird.
Hypophysitis
Bei lebensbedrohlicher (Grad 4) Hypophysitis muss Opdualag dauerhaft abgesetzt werden Bei symptomatischer Hypophysitis Grad 2 oder 3 sollte die Behandlung mit Opdualag aufgeschoben und bei Bedarf mit einer Hormonsubstitutionstherapie begonnen werden. Bei Verdacht auf akute Entzündung der Hypophyse sollte auch eine Behandlung mit Corticosteroiden in einer Dosierung von 1 bis 2 mg/kg/Tag Methylprednisolon‑Äquivalent in Betracht gezogen werden. Bei einer Besserung kann die Behandlung mit Opdualag nach dem Ausschleichen der Corticosteroide bei Bedarf fortgesetzt werden. Die Hypophysenfunktion und Hormonspiegel sollten weiterhin überwacht werden, um sicherzustellen, dass die passende Hormonsubstitutionstherapie angewandt wird.
Diabetes mellitus
Bei symptomatischem Diabetes sollte die Behandlung mit Opdualag aufgeschoben und bei Bedarf mit einer Insulinersatztherapie begonnen werden. Der Blutzuckerspiegel sollte weiterhin überwacht werden, um sicherzustellen, dass die passende Insulinersatztherapie angewandt wird. Bei lebensbedrohlichem Diabetes muss Opdualag dauerhaft abgesetzt werden.
Immunvermittelte Nebenwirkungen der Haut
Unter Nivolumab in Kombination mit Relatlimab wurden schwerer Ausschlag beobachtet (siehe Abschnitt 4.8). Die Behandlung mit Opdualag sollte bei Ausschlag Grad 3 aufgeschoben und bei Ausschlag Grad 4 abgesetzt werden. Schwerer Ausschlag sollte mit hochdosiertem Corticosteroid in einer Dosierung von 1 bis 2 mg/kg/Tag Methylprednisolon‑Äquivalent behandelt werden.
Seltene Fälle von SJS und TEN, manche davon mit tödlichem Ausgang, wurden bei einer Nivolumab‑Monotherapie beobachtet und könnten möglicherweise unter Nivolumab in Kombination mit Relatlimab auftreten. Wenn ein Verdacht auf Symptome oder Anzeichen für SJS oder TEN besteht, sollte die Behandlung mit Opdualag aufgeschoben und der Patient an eine spezialisierte Abteilung zur Beurteilung und Behandlung überwiesen werden. Wenn sich beim Patienten unter der Anwendung von Opdualag SJS oder TEN bestätigt haben, wird die dauerhafte Absetzung der Behandlung empfohlen (siehe Abschnitt 4.2).
Vorsicht ist geboten, wenn für einen Patienten, der zuvor bei Behandlung mit anderen immunstimulierenden Krebsmedikamenten eine schwere oder lebensbedrohliche Hautreaktion erlitten hat, die Anwendung von Opdualag erwogen wird.
Immunvermittelte Myokarditis
Unter Nivolumab in Kombination mit Relatlimab wurde schwere immunvermittelte Myokarditis beobachtet. Die Diagnose einer Myokarditis erfordert ein hohes Maß an Aufmerksamkeit. Patienten mit kardialen oder kardiopulmonalen Symptomen sollten auf eine mögliche Myokarditis untersucht werden. Falls eine Myokarditis vermutet wird, sollte unverzüglich eine Hochdosistherapie mit Steroiden (Prednison 1 bis 2 mg/kg/Tag oder Methylprednisolon 1 bis 2 mg/kg/Tag) eingeleitet werden und unverzüglich eine kardiologische Untersuchung mit umfassender Diagnostik nach aktuellen klinischen Leitlinien veranlasst werden. Sobald die Diagnose einer Myokarditis gestellt wurde, sollte die Behandlung mit Opdualag aufgeschoben oder dauerhaft abgesetzt werden, wie unten beschrieben.
Bei Myokarditis Grad 3 oder 4 muss Opdualag dauerhaft abgesetzt werden und es sollte eine Behandlung mit Corticosteroiden in einer Dosierung von 2 bis 4 mg/kg/Tag Methylprednisolon‑Äquivalent begonnen werden (siehe Abschnitt 4.2).
Bei Myokarditis Grad 2 sollte die Behandlung mit Opdualag aufgeschoben und eine Behandlung mit Corticosteroiden in einer Dosierung von 1 bis 2 mg/kg/Tag Methylprednisolon‑Äquivalent begonnen werden. Bei einer Besserung kann eine Fortsetzung der Behandlung mit Opdualag nach dem Ausschleichen der Corticosteroide erwogen werden. Wenn es trotz der Behandlung mit Corticosteroiden zu einer Verschlechterung oder keiner Besserung kommt, sollte die Corticosteroid‑Dosis auf 2 bis 4 mg/kg/Tag Methylprednisolon‑Äquivalent erhöht werden und Opdualag muss dauerhaft abgesetzt werden (siehe Abschnitt 4.2).
Andere immunvermittelte Nebenwirkungen
Die folgenden klinisch signifikanten immunvermittelten Nebenwirkungen wurden bei Patienten, die mit Nivolumab in Kombination mit Relatlimab behandelt wurden, berichtet: Uveitis, Pankreatitis, Gastritis, Guillain‑Barré‑Syndrom, Myositis/Rhabdomyolyse, Myasthenia gravis, Myokarditis‑Myositis‑Myasthenia‑gravis‑Overlap‑Syndrom, Enzephalitis, hämolytische Anämie, Vogt‑Koyanagi‑Harada‑Syndrom (VKH).
Die folgenden zusätzlichen klinisch signifikanten immunvermittelten Nebenwirkungen wurden bei Nivolumab‑Monotherapie oder Nivolumab in Kombination mit anderen zugelassenen Wirkstoffen berichtet: Demyelinisierung, autoimmune Neuropathie (einschließlich Gesichtsnerv‑ und Abduzensparese), myasthenes Syndrom, aseptische Meningitis, Sarkoidose, Duodenitis, Hypoparathyreoidismus und nicht‑infektiöse Zystitis.
Bei vermuteten immunvermittelten Nebenwirkungen sollte zur Bestätigung der Ätiologie oder zum Ausschluss anderer Ursachen eine angemessene Abklärung durchgeführt werden. In Abhängigkeit vom Schweregrad der Nebenwirkung sollte die Behandlung mit Opdualag aufgeschoben und den Patienten Corticosteroide gegeben werden. Bei einer Besserung kann die Behandlung mit Opdualag nach dem Ausschleichen der Corticosteroide fortgesetzt werden. Opdualag muss bei jeder schweren wiederauftretenden immunvermittelten Nebenwirkung und bei jeder lebensbedrohlichen immunvermittelten Nebenwirkung dauerhaft abgesetzt werden.
Fälle von Myokarditis‑Myositis‑Myasthenia‑gravis‑Overlap‑Syndrom (welches sich als Überlappung von zwei oder allen drei Erkrankungen äußert), einige davon mit tödlichem Ausgang, wurden unter Nivolumab in Kombination mit Relatlimab berichtet. Eine frühzeitige Erkennung und ein konsequentes Behandlungsmanagement sind entscheidend, um die damit verbundene Morbidität und das Mortalitätsrisiko zu reduzieren.
Bei einem Myokarditis‑Myositis‑Myasthenia‑gravis‑Overlap‑Syndrom Grad 3 oder 4 muss Opdualag dauerhaft abgesetzt werden (siehe Abschnitt 4.2). Entsprechend klinischer Indikation ist eine Corticosteroid-Behandlung einzuleiten.
Bei einem Myokarditis‑Myositis‑Myasthenia‑gravis‑Overlap‑Syndrom Grad 2 muss Opdualag abgesetzt und entsprechend klinischer Indikation eine Corticosteroid-Behandlung eingeleitet werden (siehe Abschnitt 4.2). Bei einer Besserung kann eine Fortsetzung der Behandlung mit Opdualag nach dem Ausschleichen der Corticosteroide erwogen werden. Wenn es trotz der Behandlung mit Corticosteroiden zu einer Verschlechterung oder keiner Besserung kommt, ist die Corticosteroid-Dosis wie klinisch indiziert anzupassen und Opdualag muss dauerhaft abgesetzt werden.
Weitere wichtige Warnhinweise und Vorsichtsmaßnahmen, einschließlich Klasseneffekten
Bei mit PD‑1‑Inhibitoren behandelten Patienten wurde nach Markteinführung eine Abstoßung von soliden Organtransplantaten berichtet. Die Behandlung mit Nivolumab in Kombination mit Relatlimab kann das Abstoßungsrisiko bei Empfängern solider Organtransplantate erhöhen. Bei diesen Patienten sollte der Nutzen der Behandlung mit Nivolumab in Kombination mit Relatlimab gegen das Risiko einer möglichen Organabstoßung abgewogen werden.
Hämophagozytische Lymphohistiozytose (HLH) wurde unter Nivolumab als Monotherapie, Nivolumab in Kombination mit Relatlimab und Nivolumab in Kombination mit anderen Wirkstoffen beobachtet. Unter Nivolumab in Kombination mit Relatlimab wurde ein Todesfall berichtet. Vorsicht ist geboten, wenn Nivolumab in Kombination mit Relatlimab gegeben wird. Wenn HLH bestätigt wird, sollte die Gabe von Nivolumab in Kombination mit Relatlimab abgebrochen und die HLH‑Behandlung begonnen werden.
Bei Patienten, die vor oder nach einer allogenen hämatopoetischen Stammzelltransplantation (HSZT) mit Nivolumab behandelt wurden, wurde über rasch einsetzende und schwere Transplantat‑Wirt‑Reaktionen (Graft‑versus‑Host‑Krankheit, Graft‑versus‑Host disease [GvHD]), einige davon mit tödlichem Ausgang, berichtet. Die Behandlung mit Nivolumab in Kombination mit Relatlimab kann das Risiko schwerer GvHD und Todesfälle bei Patienten erhöhen, die zuvor eine allogene HSZT hatten, vor allem bei Patienten mit GvHD in der Vorgeschichte. Bei diesen Patienten sollte der Nutzen der Behandlung mit Nivolumab in Kombination mit Relatlimab gegen das mögliche Risiko abgewogen werden.
Infusionsreaktionen
In klinischen Studien mit Nivolumab in Kombination mit Relatlimab wurden schwere Infusionsreaktionen berichtet (siehe Abschnitt 4.8). Falls eine schwere oder lebensbedrohliche Infusionsreaktion auftritt, muss die Infusion von Opdualag abgebrochen und eine geeignete medizinische Behandlung eingeleitet werden. Patienten mit leichter oder mäßiger Infusionsreaktion können Opdualag unter engmaschiger Überwachung und präventiver Behandlung gemäß lokaler Richtlinien zur Prophylaxe von Infusionsreaktionen erhalten.
Patienten, die aus der pivotalen klinischen Studie bei fortgeschrittenem Melanom ausgeschlossen waren
Patienten mit aktiver Autoimmunerkrankung, mit Erkrankungen, die eine systemische Behandlung mit mittel‑ oder hochdosierten Corticosteroiden oder immunsuppressiven Arzneimitteln erfordern, mit uvealem Melanom, aktiven oder unbehandelten Hirn‑ oder leptomeningealen Metastasen sowie Patienten mit Myokarditis in der Vorgeschichte, mit auf das > 2‑Fache des ULN erhöhten Troponinwerten oder ECOG‑Performance‑Status ≥ 2 waren von der pivotalen klinischen Studie zu Nivolumab in Kombination mit Relatlimab ausgeschlossen. Ohne weitere Daten sollte Nivolumab in Kombination mit Relatlimab bei diesen Patientenpopulationen mit Vorsicht nach sorgfältiger Abwägung des potenziellen Nutzen/Risikos im individuellen Einzelfall angewendet werden.
Patientenkarte
Jeder Arzt, der Opdualag verschreibt, muss die Risiken der Behandlung mit Opdualag mit dem Patienten besprechen. Der Patient erhält die Patientenkarte und wird angewiesen, die Karte stets bei sich zu tragen.
Sowohl Nivolumab als auch Relatlimab sind humane monoklonale Antikörper und daher wurden keine Wechselwirkungsstudien durchgeführt. Da monoklonale Antikörper nicht von Cytochrom‑P450‑Enzymen (CYPs) oder anderen Enzymen des Wirkstoffmetabolismus abgebaut werden, ist nicht zu erwarten, dass die Pharmakokinetik von Relatlimab oder Nivolumab durch die Hemmung oder Induktion dieser Enzyme durch gleichzeitig verabreichte Arzneimittel beeinflusst wird.
Es ist nicht zu erwarten, dass Nivolumab und Relatlimab die Pharmakokinetik anderer Wirkstoffe beeinflussen, die von CYP‑Enzymen metabolisiert werden, da Nivolumab und Relatlimab keine signifikante Modulation von Zytokinen bewirken und daher keine Auswirkungen auf die Expression von Cytochrom‑P450‑Enzymen haben.
Systemische Immunsuppression
Vor Beginn der Behandlung mit Nivolumab in Kombination mit Relatlimab sollte die Anwendung systemischer Corticosteroide und anderer Immunsuppressiva wegen der potenziellen Beeinflussung der pharmakodynamischen Aktivität vermieden werden. Nach Beginn der Behandlung mit Nivolumab in Kombination mit Relatlimab können jedoch systemische Corticosteroide und andere Immunsuppressiva zur Behandlung immunvermittelter Nebenwirkungen angewendet werden.
Frauen im gebärfähigen Alter/Verhütung
Die Anwendung von Opdualag bei Frauen im gebärfähigen Alter, die nicht verhüten, wird nicht empfohlen, es sei denn, der klinische Nutzen überwiegt das potenzielle Risiko. Zuverlässige Verhütungsmethoden sind für mindestens 5 Monate nach der letzten Gabe von Opdualag anzuwenden.
Schwangerschaft
Bisher liegen nur sehr begrenzte Erfahrungen mit der Anwendung von Nivolumab in Kombination mit Relatlimab bei Schwangeren vor. Basierend auf dem Wirkmechanismus und den Daten aus tierexperimentellen Studien kann Nivolumab in Kombination mit Relatlimab bei einer schwangeren Frau den Fötus schädigen. Bei tierexperimentellen Reproduktionsstudien mit Nivolumab wurde embryofetale Toxizität festgestellt (siehe Abschnitt 5.3). Humanes IgG4 passiert die Plazentaschranke und Nivolumab und Relatlimab sind IgG4; daher können Nivolumab und Relatlimab potenziell von der Mutter auf den wachsenden Fetus übertragen werden. Die Anwendung von Opdualag während der Schwangerschaft und bei Frauen im gebärfähigen Alter, die nicht verhüten, wird nicht empfohlen, es sei denn, der klinische Nutzen überwiegt das potenzielle Risiko.
Stillzeit
Es ist nicht bekannt, ob Nivolumab und/oder Relatlimab in die Muttermilch übergehen. Es ist bekannt, dass Human‑IgGs in den ersten Tagen nach der Geburt in die Muttermilch übergehen; bald darauf nehmen diese auf niedrige Konzentrationen ab. Daher kann ein Risiko für den gestillten Säugling in diesem kurzen Zeitraum nicht ausgeschlossen werden. Anschließend kann Opdualag während der Stillzeit angewendet werden, wenn dies aus klinischer Sicht notwendig ist.
Fertilität
Es wurden keine Studien durchgeführt, um die Auswirkung von Nivolumab und/oder Relatlimab auf die Fertilität zu untersuchen. Daher ist die Auswirkung von Nivolumab und/oder Relatlimab auf die männliche oder weibliche Fertilität unbekannt.
Opdualag hat einen geringen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen. Aufgrund potenzieller Nebenwirkungen wie Ermüdung/Fatigue und Schwindelgefühl (siehe Abschnitt 4.8) sollten Patienten angewiesen werden, beim Autofahren oder beim Bedienen von Maschinen vorsichtig zu sein, bis sie sicher sind, nicht durch Opdualag beeinträchtigt zu werden.
Zusammenfassung des Sicherheitsprofils
Nivolumab in Kombination mit Relatlimab ist mit immunvermittelten Nebenwirkungen assoziiert (siehe unten „Beschreibung einzelner Nebenwirkungen“). Die Behandlungsrichtlinien für diese Nebenwirkungen werden im Abschnitt 4.4 beschrieben.
Die häufigsten Nebenwirkungen sind Ermüdung/Fatigue (41 %), Muskel‑ und Skelettschmerzen (32 %), Ausschlag (29 %), Arthralgie (26 %), Diarrhö (26 %), Pruritus (26 %), Kopfschmerzen (20 %), Übelkeit (19 %), Husten (16 %), verminderter Appetit (16 %), Hypothyreose (16 %), Abdominalschmerzen (14 %), Vitiligo (13 %), Fieber (12 %), Obstipation (11 %), Harnwegsinfektion (11 %), Dyspnoe (10 %) und Erbrechen (10 %).
Die häufigsten schwerwiegenden Nebenwirkungen sind Nebenniereninsuffizienz (1,4 %), Anämie (1,4 %), Rückenschmerzen (1,1 %), Kolitis (1,1 %), Diarrhö (1,1 %), Myokarditis (1,1 %), Pneumonie (1,1 %) und Harnwegsinfektion (1,1 %). Die Inzidenz von Grad‑3‑5‑Nebenwirkungen bei Patienten mit fortgeschrittenem (nicht resezierbarem oder metastasiertem) Melanom betrug 43 % für mit Nivolumab in Kombination mit Relatlimab und 35 % für mit Nivolumab behandelte Patienten.
Tabellarische Aufstellung der Nebenwirkungen
Die Sicherheit von Nivolumab in Kombination mit Relatlimab wurde bei 355 Patienten mit fortgeschrittenem (nicht resezierbarem oder metastasiertem) Melanom untersucht (Studie CA224047). In Tabelle 2 sind die Nebenwirkungen aufgeführt, die im Datensatz für Patienten, die mit Nivolumab in Kombination mit Relatlimab behandelt wurden, mit einer medianen Nachbeobachtungszeit von 19,94 Monaten berichtet wurden. Die oben und in Tabelle 2 aufgeführten Häufigkeiten basieren auf der Häufigkeit von Nebenwirkungen jeglicher Ursache. Diese Nebenwirkungen sind nach Systemorganklassen und Häufigkeit geordnet. Häufigkeiten sind wie folgt definiert: sehr häufig (≥1/10); häufig (≥1/100, <1/10); gelegentlich (≥1/1 000, <1/100); selten (≥1/10 000, <1/1 000); sehr selten (<1/10 000) und nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar). Innerhalb jeder Häufigkeitsgruppe sind die Nebenwirkungen nach abnehmendem Schweregrad aufgeführt.
Tabelle 2: Nebenwirkungen in klinischen Studien
Infektionen und parasitäre Erkrankungen | |
Sehr häufig |
Harnwegsinfektion |
Häufig |
Infektion der oberen Atemwege |
Gelegentlich |
Follikulitis |
Erkrankungen des Blutes und des Lymphsystems | |
Sehr häufig |
Anämiea, Lymphopeniea, Neutropeniea, Leukopeniea |
Häufig |
Thrombozytopeniea, Eosinophilie |
Gelegentlich |
Hämolytische Anämie |
Endokrine Erkrankungen | |
Sehr häufig |
Hypothyreose |
Häufig |
Nebenniereninsuffizienz, Hypophysitis, Hyperthyreose, Thyroiditis |
Gelegentlich |
Hypophyseninsuffizienz, Hypogonadismus |
Stoffwechsel‑ und Ernährungsstörungen | |
Sehr häufig |
Verminderter Appetit |
Häufig |
Diabetes mellitus, Hypoglykämiea, Gewichtsverlust, Hyperurikämie, Hypoalbuminämie, Dehydrierung |
Psychiatrische Erkrankungen | |
Häufig |
Verwirrtheitszustand |
Erkrankungen des Nervensystems | |
Sehr häufig |
Kopfschmerzen |
Häufig |
Periphere Neuropathie, Schwindelgefühl, Dysgeusie |
Gelegentlich |
Enzephalitis, Guillain‑Barré‑Syndrom, Optikusneuritis, Myasthenia gravis, Myokarditis‑Myositis‑Myasthenia‑gravis‑Overlap‑Syndromc |
Augenerkrankungen | |
Häufig |
Uveitis, Sehverschlechterung, trockene Augen, vermehrte Tränensekretion |
Gelegentlich |
Vogt‑Koyanagi‑Harada‑Syndrom, okuläre Hyperämie |
Herzerkrankungen | |
Häufig |
Myokarditis |
Gelegentlich |
Perikarderguss |
Gefäßerkrankungen | |
Häufig |
Phlebitis |
Erkrankungen der Atemwege, des Brustraums und Mediastinums | |
Sehr häufig |
Dyspnoe, Husten |
Häufig |
Pneumonitisb, Nasenverstopfung |
Gelegentlich |
Asthma, Pleuraerguss |
Erkrankungen des Gastrointestinaltrakts | |
Sehr häufig |
Diarrhö, Erbrechen, Übelkeit, Abdominalschmerzen, Obstipation |
Häufig |
Kolitis, Pankreatitis, Gastritis, Dysphagie, Stomatitis, trockener Mund |
Gelegentlich |
Ösophagitis |
Selten |
Exokrine Pankreasinsuffizienz |
Nicht bekannt |
Zöliakie |
Leber‑ und Gallenerkrankungen | |
Häufig |
Hepatitis |
Gelegentlich |
Cholangitis |
Erkrankungen der Haut und des Unterhautgewebes | |
Sehr häufig |
Ausschlag, Vitiligo, Pruritus |
Häufig |
Alopezie, lichenoide Keratose, Lichtempfindlichkeitsreaktion, trockene Haut |
Gelegentlich |
Pemphigoid, Psoriasis, Urtikaria |
Skelettmuskulatur‑, Bindegewebs‑ und Knochenerkrankungen | |
Sehr häufig |
Muskel‑ und Skelettschmerzen, Arthralgie |
Häufig |
Arthritis, Muskelspasmen, muskuläre Schwäche |
Gelegentlich |
Myositis, Sjögren‑Syndrom, Polymyalgia rheumatica, rheumatoide Arthritis, systemischer Lupus erythematodes |
Erkrankungen der Nieren und Harnwege | |
Häufig |
Nierenversagen, Proteinurie |
Gelegentlich |
Nephritis |
Erkrankungen der Geschlechtsorgane und der Brustdrüse | |
Gelegentlich |
Azoospermie |
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort | |
Sehr häufig |
Ermüdung/Fatigue, Fieber |
Häufig |
Ödeme, grippeähnliche Erkrankungen, Schüttelfrost |
Selten |
Serositis |
Untersuchungen | |
Sehr häufig |
AST‑Anstiega, ALT‑Anstiega, Hyponatriämiea, Kreatinin‑Anstiega, Anstieg der alkalischen Phosphatasea, Hyperkaliämiea, Hypokalziämiea, Hypomagnesiämiea, Hyperkalziämiea, Hypokaliämiea |
Häufig |
Bilirubin‑Anstiega, Hypernatriämiea, Hypermagnesiämiea, Troponin‑Anstieg, Anstieg der Gamma‑Glutamyltransferase, Anstieg der Laktatdehydrogenase im Blut, Lipase‑Anstieg, Amylase‑Anstieg |
Gelegentlich |
Anstieg des C‑reaktiven Proteins, Anstieg der Blutkörperchensenkungsgeschwindigkeit |
Verletzung, Vergiftung und durch Eingriffe bedingte Komplikationen | |
Häufig |
Reaktionen im Zusammenhang mit einer Infusion |
a Die Häufigkeitsangaben bei den Laborwerten entsprechen dem Anteil an Patienten, bei denen es zu einer Verschlechterung gegenüber den Ausgangslaborwerten gekommen ist. | |
Beschreibung einzelner Nebenwirkungen
Immunvermittelte Pneumonitis
Unter der Behandlung mit Nivolumab in Kombination mit Relatlimab trat bei 5,1 % der Patienten Pneumonitis, einschließlich einer interstitiellen Lungenerkrankung und Lungeninfiltration, auf. Die Inzidenz von Grad‑3/4‑Ereignissen betrug 0,8 %. Bei 0,28 % der Patienten traten Todesfälle auf. Die mediane Zeit bis zum Auftreten betrug 28 Wochen (Spanne: 3,6‑94,4). Bei 83,3 % der Patienten kam es zu einer Rückbildung nach einer medianen Zeit von 12,0 Wochen (Spanne: 2,1‑29,7+). Bei 1,7 % der Patienten führte eine immunvermittelte Pneumonitis zu einem dauerhaften Absetzen von Nivolumab in Kombination mit Relatlimab und bei 55,6 % der Patienten mit einer immunvermittelten Pneumonitis waren hochdosierte Corticosteroide (Prednison ≥ 40 mg pro Tag oder Äquivalent) erforderlich.
Immunvermittelte Kolitis
Unter der Behandlung mit Nivolumab in Kombination mit Relatlimab traten bei 15,8 % der Patienten Diarrhö, Kolitis oder vermehrter Stuhlgang auf. Die Inzidenz von Grad‑3/4‑Ereignissen betrug 2,0 %. Die mediane Zeit bis zum Auftreten betrug 14 Wochen (Spanne: 0,1‑95,6). Bei 92,7 % der Patienten kam es zu einer Rückbildung nach einer medianen Zeit von 3,9 Wochen (Spanne: 0,1‑136,9+). Bei 2,0 % der Patienten führte eine immunvermittelte Kolitis zu einem dauerhaften Absetzen von Nivolumab in Kombination mit Relatlimab und bei 33,9 % der Patienten mit einer immunvermittelten Kolitis waren hochdosierte Corticosteroide (Prednison ≥ 40 mg pro Tag oder Äquivalent) erforderlich.
Immunvermittelte Hepatitis
Unter der Behandlung mit Nivolumab in Kombination mit Relatlimab traten bei 13,2 % der Patienten Anomalien bei Leberfunktionstests auf. Die Inzidenz von Grad‑3/4‑Ereignissen betrug 3,9 %. Die mediane Zeit bis zum Auftreten betrug 11 Wochen (Spanne: 2,0‑144,9). Bei 78,7 % der Patienten kam es zu einer Rückbildung nach einer medianen Zeit von 6,1 Wochen (Spanne: 1,0‑88,1+). Bei 2,0 % der Patienten führte eine immunvermittelte Hepatitis zu einem dauerhaften Absetzen von Nivolumab in Kombination mit Relatlimab und bei 38,3 % der Patienten mit einer immunvermittelten Hepatitis waren hochdosierte Corticosteroide erforderlich.
Immunvermittelte Nephritis und Nierenfunktionsstörung
Unter der Behandlung mit Nivolumab in Kombination mit Relatlimab trat bei 4,5 % der Patienten eine Nephritis oder Nierenfunktionsstörung auf. Die Inzidenz von Grad‑3/4‑Ereignissen betrug 1,4 %. Die mediane Zeit bis zum Auftreten betrug 21 Wochen (Spanne: 1,9‑127,9). Bei 81,3 % der Patienten kam es zu einer Rückbildung nach einer medianen Zeit von 8,1 Wochen (Spanne: 0,9‑91,6+). Bei 1,1 % der Patienten führten eine immunvermittelte Nephritis und Nierenfunktionsstörung zum dauerhaften Absetzen von Nivolumab in Kombination mit Relatlimab und bei 25,0 % der Patienten mit einer immunvermittelten Nephritis und Nierenfunktionsstörung waren hochdosierte Corticosteroide (Prednison ≥ 40 mg pro Tag oder Äquivalent) erforderlich.
Immunvermittelte Endokrinopathien
Unter der Behandlung mit Nivolumab in Kombination mit Relatlimab traten bei 26 % der Patienten Endokrinopathien auf.
Schilddrüsenerkrankungen, einschließlich Hypothyreose oder Hyperthyreose, traten bei 20,8 % der Patienten auf. Es traten keine Grad‑3/4‑Schilddrüsenerkrankungen auf. Nebenniereninsuffizienz (einschließlich akuter Nebennierenrindeninsuffizienz) wurde bei 4,8 % der Patienten berichtet. Die Inzidenz von Grad‑3/4‑Ereignissen einer Nebenniereninsuffizienz war 1,4 %. Es trat keine Grad‑3/4‑Hypophyseninsuffizienz auf. Hypophysitis trat bei 1,1 % der Patienten auf. Die Inzidenz von Grad‑3/4‑Hypophysitis betrug 0,3 %. Diabetes mellitus (einschließlich Diabetes mellitus Typ 1) trat bei 0,3 % der Patienten auf. Die Inzidenz von Grad‑3/4‑Diabetes mellitus betrug 0,3 %.
Die mediane Zeit bis zum Auftreten dieser Endokrinopathien betrug 13 Wochen (Spanne: 1,0‑73,0). Bei 27,7 % der Patienten kam es zu einer Rückbildung. Die Zeit bis zur Rückbildung betrug 0,4 bis 176,0+ Wochen. Bei 1,1 % der Patienten führten immunvermittelte Endokrinopathien zum dauerhaften Absetzen von Nivolumab in Kombination mit Relatlimab und bei 7,4 % der Patienten mit immunvermittelten Endokrinopathien waren hochdosierte Corticosteroide (Prednison ≥ 40 mg pro Tag oder Äquivalent) erforderlich.
Immunvermittelte Nebenwirkungen der Haut
Unter der Behandlung mit Nivolumab in Kombination mit Relatlimab trat bei 45,1 % der Patienten Ausschlag, einschließlich Pruritis und Vitiligo, auf. Die Inzidenz von Grad‑3/4‑Ereignissen betrug 1,4 %. Die mediane Zeit bis zum Auftreten betrug 8 Wochen (Spanne: 0,1‑116,4). Bei 47,5 % der Patienten kam es zu einer Rückbildung. Die Zeit bis zum Auftreten der Rückbildung betrug 0,1‑166,9+ Wochen. Bei 0,3 % der Patienten führten immunvermittelte Nebenwirkungen der Haut zu einem dauerhaften Absetzen von Nivolumab in Kombination mit Relatlimab und bei 3,8 % der Patienten mit immunvermittelten Nebenwirkungen der Haut waren hochdosierte Corticosteroide (Prednison ≥ 40 mg pro Tag oder Äquivalent) erforderlich.
Immunvermittelte Myokarditis
Unter der Behandlung mit Nivolumab in Kombination mit Relatlimab trat bei 1,4 % der Patienten eine Myokarditis auf. Die Inzidenz von Grad‑3/4‑Ereignissen betrug 0,6 %. Die mediane Zeit bis zum Auftreten betrug 4,14 Wochen (Spanne: 2,1‑6,3). Bei 100 % der Patienten kam es zu einer Rückbildung nach einer medianen Zeit von 3 Wochen (Spanne: 1,9‑14,0). Bei 1,4 % der Patienten führte eine Myokarditis zum dauerhaften Absetzen von Nivolumab in Kombination mit Relatlimab und bei 100 % der Patienten mit einer immunvermittelten Myokarditis waren hochdosierte Corticosteroide (Prednison ≥ 40 mg pro Tag oder Äquivalent) erforderlich.
Reaktionen im Zusammenhang mit einer Infusion
Unter der Behandlung mit Nivolumab in Kombination mit Relatlimab traten bei 6,8 % der Patienten Überempfindlichkeits‑/Infusionsreaktionen auf. Alle Ereignisse waren vom Grad 1/2.
Laborwertanomalien
Der Anteil der Patienten, bei denen es unter Nivolumab in Kombination mit Relatlimab zu einer Veränderung der Laborwerte auf eine Grad‑3‑ oder 4‑Anomalie gegenüber dem Ausgangswert kam, war 3,6 % für Anämie 5,2 % für Lymphopenie, 0,3 % für Neutropenie, 0,6 % für Anstieg der alkalischen Phosphatase, 2,9 % für AST‑Anstieg, 3,5 % für ALT‑Anstieg, 0,3 % für Anstieg des Gesamtbilirubins, 0,9 % für Kreatinin‑Anstieg, 1,5 % für Hyponatriämie, 1,8 % für Hyperkaliämie, 0,3 % für Hypokaliämie, 0,9 % für Hyperkalziämie, 0,6 % für Hypokalziämie, 0,9 % für Hypermagnesiämie und 0,6 % für Hypomagnesiämie.
Immunogenität
In der Studie CA224047 lag bei den Patienten, deren Daten hinsichtlich des Auftretens von Anti-Wirkstoff-Antikörpern auswertbar waren, die Inzidenz der während der Behandlung aufgetretenen Antikörper gegen Relatlimab bzw. der neutralisierenden Antikörper gegen Relatlimab in der Opdualag‑Gruppe bei 5,6 % (17/301) bzw. 0,3 % (1/301). Die Inzidenz von während der Behandlung aufgetretenen Antikörpern gegen Nivolumab bzw. neutralisierenden Antikörpern gegen Nivolumab in der Opdualag‑Gruppe betrug 4,0 % (12/299) bzw. 0,3 % (1/299), ähnlich den in der Nivolumab‑Gruppe beobachteten Inzidenzen von 6,7 % (19/283) bzw. 0,4 % (1/283). Es gab keine Hinweise auf eine Veränderung von Pharmakokinetik, Wirksamkeit oder Sicherheitsprofil bei Entstehung von Antikörpern gegen Nivolumab oder Relatlimab.
Spezielle Patientenpopulationen
Ältere Menschen
Insgesamt wurden in Bezug auf die Sicherheit keine Unterschiede zwischen älteren (≥ 65 Jahre) und jüngeren Patienten berichtet (siehe Abschnitt 5.1).
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen‑Risiko‑Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung anzuzeigen am:
Bundesinstitut für Impfstoffe und biomedizinische Arzneimittel
Paul-Ehrlich-Institut
Paul-Ehrlich-Str. 51-59
63225 Langen
Tel: +49 6103 77 0
Fax: +49 6103 77 1234
Website: www.pei.de
Bei Überdosierung müssen die Patienten sorgfältig auf Anzeichen oder Symptome von Nebenwirkungen beobachtet und es muss unverzüglich eine adäquate symptomatische Behandlung eingeleitet werden.
Pharmakotherapeutische Gruppe: Antineoplastische Mittel, monoklonale Antikörper, ATC‑Code: L01FY02.
Wirkmechanismus
Opdualag ist eine Fix‑Dosis‑Kombination (Fixed Dose Combination, FDC) aus Nivolumab, einem Inhibitor des „Programmed Cell Death“‑1‑(PD‑1)‑Rezeptors (Anti‑PD‑1) und Relatlimab, einem Lymphozyten‑Aktivierungsgen‑3‑Inhibitor (Anti‑LAG‑3).
Die Bindung der PD‑1‑Liganden, PD‑L1 und PD‑L2, an den PD‑1‑Rezeptor, der sich auf T‑Zellen befindet, hemmt die T‑Zellproliferation und Zytokinausschüttung. Bei einigen Tumoren tritt eine Hochregulierung von PD‑1‑Liganden auf, und die Signalübertragung über diesen Signalweg kann zur Hemmung der aktiven T‑Zell‑Immunüberwachung von Tumoren beitragen. Nivolumab ist ein humaner monoklonaler IgG4‑Antikörper, der an den PD‑1‑Rezeptor bindet, die Interaktion mit seinen Liganden PD‑L1 und PD‑L2 blockiert und die über den PD‑1‑Signalweg vermittelte Hemmung der Immunantwort, einschließlich der Anti‑Tumor‑Immunantwort, reduziert. In genidentischen Mausmodellen führte eine Blockade der PD‑1‑Aktivität zu einer Verringerung des Tumorwachstums.
Relatlimab ist ein humaner monoklonaler IgG4‑Antikörper, der an den LAG‑3‑Rezeptor bindet, seine Interaktion mit Liganden, einschließlich MHC II, blockiert und die über den LAG‑3‑Signalweg vermittelte Hemmung der Immunantwort reduziert. Die Antagonisierung dieses Signalwegs fördert die T‑Zellproliferation und Zytokinausschüttung.
Die Kombination von Nivolumab (Anti‑PD‑1) und Relatlimab (Anti‑LAG‑3) führt zu einer erhöhten T‑Zell‑Aktivierung im Vergleich zur Aktivität eines der beiden Antikörper allein. In genidentischen Mausmodellen verstärkt die LAG‑3‑Blockade die Anti‑Tumoraktivität einer PD‑1‑Blockade und hemmt damit das Tumorwachstum und fördert die Tumorregression.
Klinische Wirksamkeit und Sicherheit
Randomisierte Phase‑II/III‑Studie mit Nivolumab in Kombination mit Relatlimab vs. Nivolumab bei Patienten mit zuvor unbehandeltem metastasiertem oder nicht resezierbarem Melanom (CA224047)
Sicherheit und Wirksamkeit von Nivolumab in Kombination mit Relatlimab zur Behandlung von Patienten mit zuvor unbehandeltem metastasiertem oder nicht resezierbarem Melanom wurden in einer randomisierten, doppelblinden Phase‑II/III‑Studie (CA224047) untersucht. In die Studie wurden Patienten mit einem ECOG‑Performance‑Status von 0 oder 1 und histologisch bestätigtem Melanom im Stadium III (nicht resezierbar) oder Stadium IV gemäß American Joint Committee on Cancer (AJCC) Klassifikation, Version 8, eingeschlossen. Die Patienten durften zuvor eine adjuvante oder neoadjuvante Melanomtherapie erhalten haben (Anti‑PD‑1‑, Anti‑CTLA‑4‑ oder BRAF‑MEK‑Therapie waren erlaubt, solange zwischen der letzten Dosis der Therapie und dem Datum des Rezidivs mindestens 6 Monate vergangen waren; eine Interferontherapie war erlaubt, solange die letzte Dosis mindestens 6 Wochen vor der Randomisierung verabreicht wurde). Patienten mit aktiver Autoimmunerkrankung, mit Myokarditis in der Vorgeschichte, mit einem auf das > 2‑Fache des ULN erhöhten Troponinwertes oder einem ECOG‑Performance‑Status ≥ 2, Patienten mit Erkrankungen, die eine systemische Behandlung mit mittel‑ oder hochdosierten Corticosteroiden oder immunsuppressiven Arzneimitteln erfordern, Patienten mit uvealem Melanom und aktiven oder unbehandelten Hirn‑ oder leptomeningealen Metastasen wurden aus der Studie ausgeschlossen (siehe Abschnitt 4.4).
Insgesamt wurden 714 Patienten randomisiert und erhielten entweder Nivolumab in Kombination mit Relatlimab (n = 355) oder Nivolumab (n = 359). Die Patienten im Kombinations‑Arm erhielten 480 mg Nivolumab/160 mg Relatlimab über 60 Minuten alle 4 Wochen. Die Patienten im Nivolumab‑Arm erhielten 480 mg Nivolumab alle 4 Wochen. Die Randomisierung wurde stratifiziert nach Tumor‑PD‑L1‑Expression (≥ 1 % vs. < 1) unter Verwendung des PD‑L1‑IHC 28‑8 pharmDx‑Assays und der LAG‑3‑Expression (≥ 1 % vs. < 1), bestimmt mithilfe eines analytisch validierten LAG‑3‑IHC‑Assays, dem BRAF‑V600‑Mutationsstatus sowie dem M‑Stadium gemäß Version 8 der AJCC‑Klassifikation (M0/M1alle[0] versus M1alle[1]). Die Patienten wurden bis zur Progression der Erkrankung oder bis zum Auftreten nicht akzeptabler Toxizität behandelt. Tumorbeurteilungen wurden gemäß der „Response Evaluation Criteria in Solid Tumours“ (RECIST), Version 1.1, zum ersten Mal 12 Wochen nach Randomisierung und dann bis zu 52 Wochen alle 8 Wochen und anschließend alle 12 Wochen bis zur Progression der Erkrankung oder der Beendigung der Therapie, je nachdem, was später erfolgte, durchgeführt. Das primäre Wirksamkeitskriterium war das progressionsfreie Überleben (Progression‑Free Survival, PFS), das von einem unabhängigen zentralen Komitee (Blinded Independent Central Review, BICR) bestimmt wurde. Die sekundären Wirksamkeitskriterien waren das Gesamtüberleben (Overall Survival, OS) und die Gesamtansprechrate (Overall Response Rate, ORR) gemäß BICR. Die hierarchische Reihenfolge der statistischen Tests war PFS, gefolgt von OS und dann ORR. Die primären und sekundären Wirksamkeitskriterien wurden in der Gesamtpopulation (Intention to treat, ITT) beurteilt. Es wurde keine formale Prüfung der ORR durchgeführt, da der formale Vergleich des OS statistisch nicht signifikant war.
Die Ausgangsmerkmale der Gruppen waren in der ITT-Population etwa gleich. Das mediane Alter war 63 Jahre (Spanne: 20‑94), darunter 47 % ≥ 65 Jahre und 19 % ≥ 75 Jahre. Die Mehrheit der Patienten war weiß (97 %) und männlich (58 %). Der ECOG‑Performance‑Status zu Beginn war 0 (67 %) oder 1 (33 %). Die Mehrheit der Patienten hatte eine Erkrankung im Stadium IV gemäß AJCC (92 %); 38,9 % hatten ein Stadium M1c, 2,4 % hatten eine Erkrankung im Stadium M1d, 8,7 % hatten vorherige systemische Therapien, 36 % der Patienten hatten zu Studienbeginn einen LDH‑Ausgangswert über dem ULN. 39 % der Patienten hatten ein BRAF‑Mutations‑positives Melanom, 75 % hatten LAG‑3 ≥ 1 % und 41 % der Patienten hatten eine PD‑L1‑Tumorzell‑Expression von ≥ 1 %. Die Patienten mit quantifizierbarer Tumor‑PD‑L1‑Expression waren gleichmäßig auf die zwei Behandlungsgruppen verteilt. Im Allgemeinen waren die demografischen Daten und die medizinischen Ausgangsmerkmale bei Patienten mit PD‑L1‑Expression < 1 % in den Behandlungsarmen vergleichbar.
Bei der Primäranalyse in der ITT‑Population mit einer medianen Nachbeobachtungszeit von 13,21 Monaten (Spanne: 0‑33,1 Monate) wurde eine statistisch signifikante Verbesserung des PFS beobachtet, mit einem medianen PFS von 10,12 Monaten in der Gruppe von Patienten, die mit Nivolumab in Kombination mit Relatlimab behandelt wurden, im Vergleich zu 4,63 Monaten in der Nivolumab‑Gruppe (HR = 0,75; 95 % CI: 0,62; 0,92; p = 0,0055). Zum Zeitpunkt der präspezifizierten finalen OS‑Analyse in der ITT‑Population mit einer medianen Nachbeobachtungszeit von 19,3 Monaten war das OS nicht statistisch signifikant (HR = 0,80; 95 % CI: 0,64; 1,01).
Präspezifizierte Subgruppenanalyse nach PD‑L1‑Expression < 1 %
Die Hauptwirksamkeitsergebnisse für die Subgruppe von Patienten mit Tumor‑PD‑L1‑Expression < 1 % aus einer explorativen Analyse mit medianer Nachbeobachtung von 17,78 Monaten (Spanne: 0,26‑40,64 Monate) sind in Tabelle 3 zusammengefasst.
Tabelle 3: Wirksamkeitsergebnisse bei Patienten mit Tumorzell‑PD‑L1‑Expression < 1 % (CA224047)
Nivolumab + Relatlimab |
Nivolumab |
|
Progressionsfreies Überleben |
||
Hazard‑Ratio (95 % CI)a |
0,68 (0,53; 0,86) |
|
Median in Monaten |
6,7 |
3,0 |
Rate (95 % CI) nach 12 Monaten |
42,3 |
26,9 |
Gesamtüberlebenb |
||
Hazard‑Ratio (95 % CI)a |
0,78 (0,59; 1,04) |
|
Median in Monaten |
NR |
27,0 |
Rate (95 % CI) nach 12 Monaten |
73,9 |
67,4 |
Rate (95 % CI) nach 24 Monaten |
59,6 |
53,1 |
Gesamtansprechen (%) |
36,4 |
24,1 |
(95 % CI) |
(29,8; 43,3) |
(18,5; 30,4) |
Vollständiges Ansprechen (%) |
25 (12,0) |
20 (9,4) |
Teilweises Ansprechen (%) |
51 (24,4) |
31 (14,6) |
Stabile Krankheit (%) |
41 (19,6) |
31 (14,6) |
a Hazard‑Ratio mit einem unstratifizierten Cox‑Modell für proportionale Hazards berechnet. | ||
Die Kaplan‑Meier‑Kurven des PFS und OS bei Patienten mit Tumorzell‑PD‑L1‑Expression < 1 % sind in den Abbildungen 1 bzw. 2 dargestellt.
Abbildung 1: Kaplan‑Meier‑Kurven des PFS bei Patienten mit Tumorzell‑PD‑L1‑Expression < 1 % (CA224047)
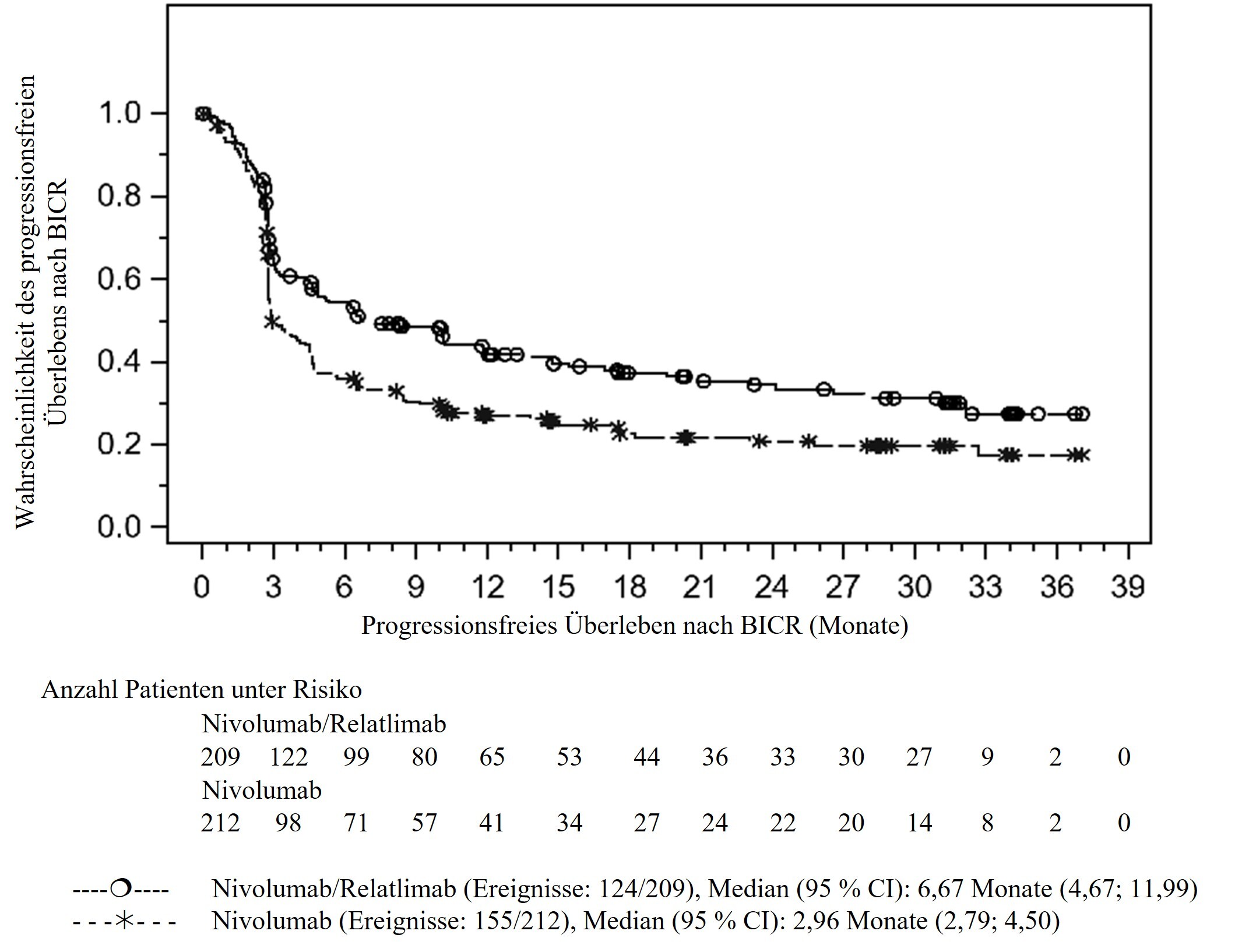
Abbildung 2: Kaplan‑Meier‑Kurven des OS bei Patienten mit Tumorzell‑PD‑L1‑Expression < 1 % (CA224047)
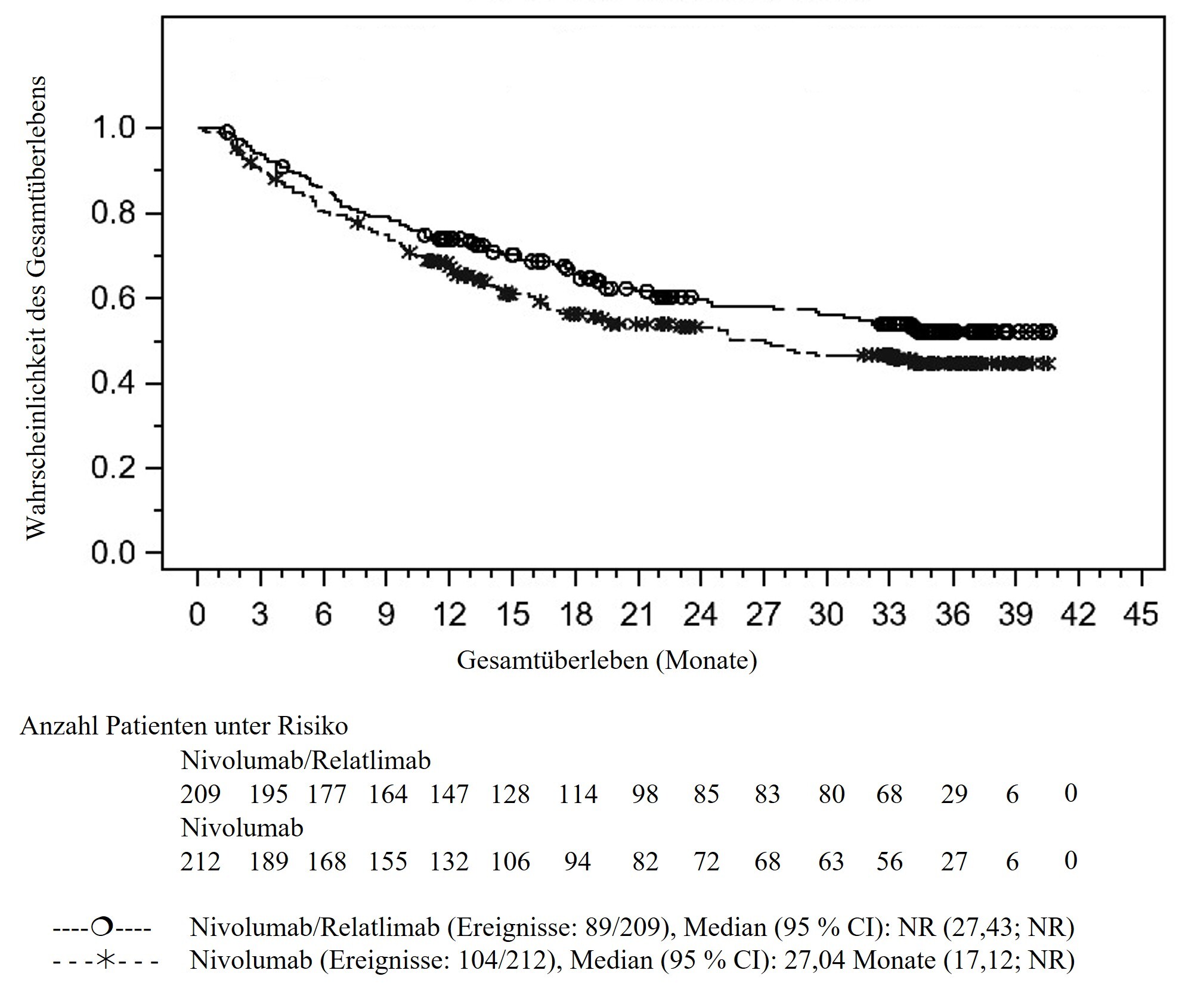
Die Pharmakokinetik (PK) von Relatlimab nach der Verabreichung von Nivolumab in Kombination mit Relatlimab wurde bei Patienten mit verschiedenen Krebserkrankungen charakterisiert, die Relatlimab‑Dosen von 20 bis 800 mg alle 2 Wochen und 160 bis 1440 mg alle 4 Wochen entweder als Monotherapie oder in Kombination mit Nivolumab‑Dosen von 80 oder 240 mg alle 2 Wochen oder 480 mg alle 4 Wochen erhielten.
Steady‑State Konzentrationen von Relatlimab wurden nach 16 Wochen mit 4‑wöchentlichem Behandlungsregime erreicht, und die systemische Akkumulation betrug das 1,9‑Fache. Die durchschnittliche Relatlimab‑Konzentration (Cavg) nach der ersten Dosis stieg bei Dosen ≥ 160 mg alle 4 Wochen proportional zur Dosis an.
Tabelle 4: Geometrischer Mittelwert (CV %) der Steady‑State‑Expositionen von Nivolumab und Relatlimab nach einer Fix‑Dosiskombination von 480 mg Nivolumab und 160 mg Relatlimab alle 4 Wochen
Cmax (μg/ml) |
Cmin (μg/ml) |
Cavg (μg/ml) |
|
Relatlimab |
62,2 (30,1) |
15,3 (64,3) |
28,8 (44,8) |
Nivolumab |
187 (32,9) |
59,7 (58,6) |
94,4 (43,3) |
Basierend auf Populations‑PK‑Analysen wurde prognostiziert, dass eine Infusionsdauer von 30 min und 60 min der Nivolumab‑ und Relatlimab‑FDC zu ähnlichen (< 1 % abweichenden) Expositionen von Nivolumab und Relatlimab führt.
In der Studie CA224047 war der geometrische Mittelwert Cmin für Nivolumab im Steady‑State im Behandlungsarm mit Nivolumab in Kombination mit Relatlimab mit einem geometrischen Mittelwert‑Verhältnis von 0,931 (95 % CI: 0,855‑1,013) ähnlich wie im Nivolumab‑Arm.
Verteilung
Der geometrische Mittelwert (CV %) für das Verteilungsvolumen im Steady‑State beträgt für Nivolumab 6,65 l (19,2 %) und für Relatlimab 6,65 l (19,8 %).
Biotransformation
Nivolumab und Relatlimab sind therapeutische monoklonale IgG4 Antikörper, die voraussichtlich durch Lysosomen oder Rezeptor‑vermittelte Endozytose zu kleinen Peptiden, Aminosäuren und kleinen Kohlenhydraten katabolisiert werden.
Elimination
Die Nivolumab‑Clearance ist im Steady‑State um 21,1 % niedriger [geometrischer Mittelwert (CV %), 7,57 ml/h (40,1 %)] als nach der ersten Dosis [9,59 ml/h (40,3 %)] und die terminale Halbwertszeit (t1/2) beträgt 26,5 Tage (36,4 %).
Die Relatlimab‑Clearance ist im Steady‑State um 9,7 % niedriger [geometrischer Mittelwert (CV %), 5,48 ml/h (41,3 %)] als nach der ersten Dosis [6,06 ml/h (38,9 %)]. Nach Verabreichung von Relatlimab 160 mg und Nivolumab 480 mg alle 4 Wochen beträgt der geometrische Mittelwert (CV %) der effektiven Halbwertszeit (t1/2) von Relatlimab 26,2 Tage (37 %).
Spezielle Patientenpopulationen
Eine Populations‑PK‑Analyse ergab, dass die folgenden Faktoren keinen klinisch relevanten Einfluss auf die Clearance von Nivolumab und Relatlimab hatten: Alter (Spanne: 17 bis 92 Jahre), Geschlecht, [männlich (1056) und weiblich (657)] oder ethnische Herkunft [kaukasisch (1655), afroamerikanisch (167) und asiatisch (41)]. Das Körpergewicht (Spanne: 37 bis 170 kg) war eine signifikante Kovariate für die Nivolumab‑ und Relatlimab‑PK. Es gibt jedoch keine klinisch relevanten Auswirkungen auf die Expositions‑Wirkungs‑Analyse.
Kinder und Jugendliche
Begrenzte Daten legen nahe, dass die Clearance und das Verteilungsvolumen von Nivolumab bei jugendlichen Patienten mit soliden Tumoren um 36 % bzw. 16 % geringer waren als bei erwachsenen Referenzpatienten. Es ist nicht bekannt, ob das Gleiche für Melanompatienten gilt und ob die Clearance und das Verteilungsvolumen von Relatlimab bei Jugendlichen hier ebenfalls geringer sind als bei Erwachsenen. Bei gleicher empfohlener Dosis wird jedoch basierend auf Populations‑PK‑Simulationen erwartet, dass die Nivolumab‑ und Relatlimab‑Exposition bei Jugendlichen mit einem Gewicht von mindestens 30 kg zu einer ähnlichen Sicherheit und Wirksamkeit wie bei Erwachsenen führt.
Nierenfunktionsbeeinträchtigung
Die Auswirkung einer eingeschränkten Nierenfunktion auf die Clearance von Nivolumab und Relatlimab wurde in einer Populations‑PK‑Analyse bei Patienten mit leichter oder mäßiger Niereninsuffizienz im Vergleich zu Patienten mit normaler Nierenfunktion untersucht. Es wurden keine klinisch bedeutsamen Unterschiede in der Clearance von Nivolumab oder Relatlimab zwischen Patienten mit Niereninsuffizienz und Patienten mit normaler Nierenfunktion festgestellt.
Beeinträchtigung der Leber
Die Auswirkung einer eingeschränkten Leberfunktion auf die Clearance von Nivolumab und Relatlimab wurde in einer Populations‑PK‑Analyse bei Patienten mit leichter Leberfunktionsstörung (Gesamtbilirubin [total bilirubin, TB] kleiner oder gleich dem oberen Normalwert [upper limit of normal, ULN] und AST größer als ULN oder TB größer als das 1‑ bis 1,5‑Fache des ULN und beliebige AST) oder mäßiger Leberfunktionsstörung (TB größer als das 1,5‑ bis 3‑Fache des ULN und beliebige AST) im Vergleich zu Patienten mit normaler Leberfunktion untersucht. Es wurden keine klinisch bedeutsamen Unterschiede in der Clearance von Nivolumab oder Relatlimab zwischen Patienten mit eingeschränkter Leberfunktion und Patienten mit normaler Leberfunktion festgestellt.
Immunogenität
Die beobachtete niedrige Inzidenzrate des Auftretens behandlungsbedingter Anti‑Nivolumab‑Antikörper und behandlungsbedingter Anti‑Relatlimab‑Antikörper hatte keine Auswirkungen auf die Pharmakokinetik von Nivolumab und Relatlimab.
Nivolumab in Kombination mit Relatlimab
Es wurden keine tierexperimentellen Studien zu Nivolumab in Kombination mit Relatlimab durchgeführt, um das kanzerogene Potential, die Genotoxizität oder Reproduktions‑ und Entwicklungstoxizität zu beurteilen.
In einer 1‑monatigen Studie an Affen, die mit Nivolumab und Relatlimab behandelt wurden, wurden Entzündungen im zentralen Nervensystem (Plexus choroideus, Gefäßsystem, Hirnhäute, Rückenmark) und im Reproduktionstrakt (Nebenhoden, Samenblasen und Hoden) beobachtet. Obwohl für diese Auswirkungen mit der Kombination keine Sicherheitsgrenzen festgelegt wurden, traten sie bei Dosen auf, die signifikant höhere Expositionen (13‑fach für Nivolumab und 97‑fach für Relatlimab) als dasjenige annehmen, was bei Patienten erreicht wird.
Relatlimab
Es liegen keine Daten aus tierexperimentellen Studien zur Wirkung von Relatlimab auf die Schwangerschaft und Reproduktion vor. In einer Studie zur embryofötalen Toxizität bei Mäusen unter Verwendung von murinen Anti‑LAG3‑Antikörpern wurden keine Wirkungen auf die Mütter oder die Entwicklung beobachtet. Die Auswirkungen von Relatlimab auf die pränatale und postnatale Entwicklung wurden nicht untersucht; basierend auf dem Wirkmechanismus kann die Blockade von LAG‑3 durch Relatlimab jedoch eine ähnlich negative Wirkung auf die Schwangerschaft haben wie Nivolumab. Fertilitätsstudien wurden mit Relatlimab nicht durchgeführt.
Nivolumab
In Mausmodellen zur Schwangerschaft wurde gezeigt, dass durch eine Blockade des PD‑1/PD‑L1‑Signalwegs die Toleranz gegenüber dem Fötus gestört wird und die Abortrate steigt. Die Wirkungen von Nivolumab auf die prä‑ und postnatale Entwicklung wurden in einer Studie an Affen untersucht, die Nivolumab nach Einsetzen der Organogenese im ersten Trimester bis zur Geburt zweimal wöchentlich in 8‑ oder 35‑facher Exposition desjenigen erhielten, was mit der klinischen Dosierung von 3 mg/kg Nivolumab beobachtet wird (AUC). Mit Beginn des dritten Trimesters trat eine dosisabhängige Steigerung der Abortrate und der neonatalen Sterblichkeit auf.
Die anderen Nachkommen der mit Nivolumab behandelten Weibchen überlebten bis zur geplanten Termination ohne mit der Behandlung in Zusammenhang stehende klinische Symptome, Abweichungen von der normalen Entwicklung, Auswirkung auf das Organgewicht oder makro‑ oder mikroskopische pathologische Veränderungen. Die Ergebnisse für Wachstumsindizes sowie teratogene, verhaltensneurologische, immunologische und klinisch‑pathologische Parameter waren im gesamten postnatalen Zeitraum von 6 Monaten mit denen der Kontrollgruppe vergleichbar. Basierend auf dem Wirkmechanismus könnte eine Exposition des Fötus mit Nivolumab und ähnlich mit Relatlimab jedoch das Risiko für die Entwicklung immunvermittelter Erkrankungen erhöhen oder die normale Immunantwort verändern. Bei PD‑1‑ und PD‑1/LAG‑3‑Knockout‑Mäusen sind immunvermittelte Erkrankungen berichtet worden. Fertilitätsstudien wurden für Nivolumab nicht durchgeführt.
Histidin
Histidinhydrochlorid‑Monohydrat
Saccharose
Diethylentriaminpentaessigsäure (Pentetsäure)
Polysorbat 80 (E 433)
Wasser für Injektionszwecke
Da keine Kompatibilitätsstudien durchgeführt wurden, darf dieses Arzneimittel nicht mit anderen Arzneimitteln gemischt werden. Opdualag sollte nicht gleichzeitig mit anderen Arzneimitteln über dieselbe intravenöse Infusionsleitung infundiert werden.
Ungeöffnete Durchstechflasche
3 Jahre
Nach der Zubereitung der Infusion
Die chemische und physikalische Haltbarkeit der gebrauchsfertigen Lösung ab dem Zeitpunkt der Zubereitung hat sich folgendermaßen dargestellt (die Zeiten verstehen sich inklusive der Anwendungsdauer):
Zubereitung der Infusion |
Chemische und physikalische Haltbarkeit der gebrauchsfertigen Lösung |
|
Lichtgeschützte Aufbewahrung bei 2 °C bis 8 °C |
Aufbewahrung bei Raumtemperatur (≤25 °C) und Raumbeleuchtung |
|
Unverdünnt oder verdünnt mit Natriumchlorid‑Injektionslösung 9 mg/ml (0,9 %) |
30 Tage |
24 Stunden (von insgesamt 30 Tagen Aufbewahrung) |
Verdünnt mit Glucose‑Injektionslösung 50 mg/ml (5 %) |
7 Tage |
24 Stunden (von insgesamt 7 Tagen Aufbewahrung) |
Aus mikrobiologischer Sicht sollte die zubereitete Infusionslösung, unabhängig vom Verdünnungsmittel, sofort verwendet werden. Hinsichtlich einer nicht sofortigen Anwendung liegt die Verantwortung über die Aufbewahrungsdauer und die Aufbewahrungsbedingungen der gebrauchsfertigen Lösung beim Anwender und sollte 24 Stunden bei 2 °C bis 8 °C nicht überschreiten, es sei denn, die Zubereitung wurde unter kontrollierten und validierten aseptischen Bedingungen durchgeführt (siehe Abschnitt 6.6).
Im Kühlschrank lagern (2 °C ‑ 8 °C).
Nicht einfrieren.
Die Durchstechflasche im Umkarton aufbewahren, um den Inhalt vor Licht zu schützen.
Die ungeöffneten Durchstechflaschen können bis zu 72 Stunden bei kontrollierter Raumtemperatur (bis zu 25 °C) gelagert werden.
Aufbewahrungsbedingungen nach Zubereitung der Infusion, siehe Abschnitt 6.3.
Packung mit einer 25‑ml‑Durchstechflasche (Glas Typ 1), mit einem Stopfen (beschichtetes Butylgummi) und gelbem Flip‑Off‑Verschluss aus Aluminium. Jedes Fläschchen ist mit 21,3 ml Lösung gefüllt, was eine Überfüllung von 1,3 ml umfasst.
Opdualag wird als Einzeldosis‑Durchstechflasche geliefert und enthält keine Konservierungsmittel. Die Zubereitung muss von geschultem Personal nach den Regeln bewährter Verfahren, insbesondere hinsichtlich Asepsis, durchgeführt werden.
Opdualag kann für die intravenöse Verabreichung verwendet werden, entweder:
ohne Verdünnung, nach der Überführung in ein Infusionsbehältnis mittels einer geeigneten sterilen Spritze; oder
nach Verdünnung gemäß der nachfolgenden Anleitung:
Die Endkonzentration der Infusion sollte zwischen 3 mg/ml Nivolumab und 1 mg/ml Relatlimab und bis zu 12 mg/ml Nivolumab und 4 mg/ml Relatlimab liegen.
Das Gesamtvolumen der Infusion darf 160 ml nicht übersteigen. Für Patienten, die weniger als 40 kg wiegen, darf das Gesamtvolumen der Infusion 4 ml pro Kilogramm Körpergewicht des Patienten nicht übersteigen.
Um das Opdualag‑Konzentrat zu verdünnen, verwenden Sie entweder:
Natriumchlorid‑Injektionslösung 9 mg/ml (0,9 %); oder
Glucose‑Injektionslösung 50 mg/ml (5 %).
Zubereitung der Infusion:
Untersuchen Sie das Opdualag‑Konzentrat auf Schwebstoffteilchen oder Verfärbung. Durchstechflasche nicht schütteln. Opdualag ist eine klare bis opaleszierende, farblose bis leicht gelbe Lösung. Verwerfen Sie die Durchstechflasche, wenn die Lösung trüb ist, Verfärbungen aufweist oder Fremdschwebstoffe enthält.
Entnehmen Sie die benötigte Menge Opdualag‑Konzentrat mit einer geeigneten sterilen Spritze und überführen Sie das Konzentrat in einen sterilen Behälter zur intravenösen Gabe (Ethylvinylacetat [EVA], Polyvinylchlorid [PVC] oder Polyolefin).
Verdünnen Sie die Opdualag‑Lösung gegebenenfalls mit der benötigten Menge Natriumchlorid‑Injektionslösung 9 mg/ml (0,9 %) oder Glucose‑Injektionslösung 50 mg/ml (5 %). Um das Zubereiten der Infusionslösung zu erleichtern, kann das Konzentrat auch direkt in einen vorgefüllten Infusionsbeutel, der die entsprechende Menge Natriumchlorid‑Injektionslösung 9 mg/ml (0,9 %) oder Glucose‑Injektionslösung 50 mg/ml (5 %) enthält, gegeben werden.
Infusion vorsichtig durch manuelle Drehung mischen. Nicht schütteln.
Anwendung
Die Opdualag‑Infusion darf nicht als intravenöse Druck‑ oder Bolus‑Injektion verabreicht werden.
Verabreichen Sie die Opdualag‑Infusion intravenös über einen Zeitraum von 30 Minuten.
Die Verwendung eines Infusionssets und eines sterilen, pyrogenfreien In‑Line‑ oder Zusatzfilters mit geringer Proteinbindung (Porengröße: 0,2 bis 1,2 μm) wird empfohlen.
Die Opdualag‑Infusion ist kompatibel mit EVA‑, PVC‑ und Polyolefin‑Behältern, PVC‑Infusionssets und In‑Line‑Filtern mit Polyethersulfon (PES)‑, Nylon‑ und Polyvinylidenfluorid (PVDF)‑Membranen mit einer Porengröße von 0,2 bis 1,2 μm.
Andere Arzneimittel dürfen nicht gleichzeitig über dieselbe Infusionsleitung verabreicht werden.
Spülen Sie die Infusionsleitung am Ende der Opdualag‑Infusion mit Natriumchlorid‑Injektionslösung 9 mg/ml (0,9 %) oder Glucose‑Injektionslösung 50 mg/ml (5 %).
Entsorgung
Verbliebene Restmengen der Infusionslösung nicht zur weiteren Verwendung aufheben. Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu beseitigen.
Bristol‑Myers Squibb Pharma EEIG
Plaza 254
Blanchardstown Corporate Park 2
Dublin 15, D15 T867
Irland
EU/1/22/1679/001
Datum der Erteilung der Zulassung: 15. September 2022
Februar 2026
Ausführliche Informationen zu diesem Arzneimittel sind auf den Internetseiten der Europäischen Arzneimittel‑Agentur https://www.ema.europa.eu/ verfügbar.
Verschreibungspflichtig
Bristol-Myers Squibb GmbH & Co. KGaA
Arnulfstraße 29
80636 München
Medizinische Information
Telefon: 0800 0752002
E-Mail: medwiss.info@bms.com
www.bmsmedinfo.de