Anapen 500 Mikrogramm Injektionslösung
Jeder Milliliter enthält 1,7 mg Epinephrin (Adrenalin).
Eine Dosis von 0,3 ml enthält 500 Mikrogramm Epinephrin (Adrenalin).
Sonstige Bestandteile mit bekannter Wirkung:
Natriumchlorid, Natriummetabisulfit (Ph.Eur.) (E 223)
Jede 0,3 ml Dosis (500 Mikrogramm) enthält 1,8 mg Natriumchlorid und 0,51 mg Natriummetabisulfit (Ph.Eur.) (E 223).
Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
Injektionslösung
Klare farblose Lösung praktisch ohne Partikel.
Notfallbehandlung von akuten allergischen Reaktionen (Anaphylaxie), verursacht durch Erdnüsse oder andere Nahrungsmittel, Arzneimittel, Insektenbisse oder -stiche und andere Allergene sowie belastungsinduzierte oder idiopathische Anaphylaxie.
Der Patient sollte immer 2 Autoinjektoren bei sich tragen für den Fall, dass die erste Verabreichung fehlschlägt oder die Dosis nicht ausreichend ist.
Dosierung
Die wirksame Dosis liegt normalerweise in einem Bereich von 5 – 10 Mikrogramm pro Kilogramm Körpergewicht, es können aber in einigen Fällen auch höhere Dosen notwendig sein.
Erwachsene:
Die empfohlene Dosis beträgt 300 Mikrogramm bei Personen mit einem Körpergewicht unter 60 kg Körpergewicht. Die empfohlene Dosis bei Personen über 60 kg Körpergewicht beträgt 300 bis 500 Mikrogramm, abhängig von der klinischen Bewertung.
Bei einer fehlenden klinischen Verbesserung oder falls eine Verschlechterung eintritt, kann eine zweite Injektion mit einem zusätzlichen Anapen 5 bis 15 Minuten nach der ersten Injektion angewendet werden. Es wird empfohlen, dass den Patienten zwei Anapen verschrieben werden, die sie zu jeder Zeit bei sich tragen sollten.
Wenn eine zweite Injektion notwendig ist, wird empfohlen diese in den gegenüberliegenden Oberschenkel zu injizieren.
Kinder und Jugendliche:
Anwendung bei Kindern: Anapen 500 ist nicht zur Anwendung bei Kindern empfohlen.
Die geeignete Dosis kann 150 Mikrogramm (Anapen Junior) oder 300 Mikrogramm (Anapen 300) Epinephrin (Adrenalin) sein, abhängig vom Körpergewicht des Kindes und nach dem Ermessen des Arztes. Kindern und Jugendlichen mit einem Körpergewicht über 30 kg sollte Anapen 300 Mikrogramm verordnet werden. Der Anapen Junior 150 Mikrogramm-Autoinjektor ist für die Verabreichung einer Einzeldosis von 150 Mikrogramm Epinephrin (Adrenalin) ausgelegt. Bei Kindern, die weniger als 15 kg wiegen, kann eine Dosierung unter 150 Mikrogramm nicht mit ausreichender Genauigkeit verabreicht werden. Daher wird die Anwendung außer in lebensbedrohlichen Situationen und unter ärztlicher Aufsicht nicht empfohlen.
Art der Anwendung
Zur intramuskulären Anwendung.
Anapen besteht aus einer Fertigspritze mit Epinephrin in einer automatischen Injektionsvorrichtung. Das Ganze wird als Autoinjektor bezeichnet.
Eine Anapen-Injektion muss unverzüglich nach dem Auftreten von Anzeichen und Symptomen eines anaphylaktischen Schocks intramuskulär verabreicht werden. Diese können innerhalb weniger Minuten nach dem Kontakt mit dem Allergen auftreten und manifestieren sich am häufigsten in Form von Urtikaria, Hautrötung (Flushing) oder Angioödem; schwerere Reaktionen betreffen das Kreislauf- und das Atmungssystem. Anapen darf nur in die anterolaterale Partie des Oberschenkels, nicht in das Gesäß injiziert werden. Die Stelle, an der die Spritze gesetzt wurde, kann nach der Injektion für ca. 10 Sekunden leicht massiert werden. Mit dem Autoinjektor kann durch die Kleidung oder direkt in die Haut injiziert werden.
Der Anapen Autoinjektor ist für die sofortige Selbstverabreichung bei Personen mit Anaphylaxie in der Anamnese bestimmt. Er ist für die Verabreichung einer Einzeldosis von 500 Mikrogramm (0,3 ml) Epinephrin (Adrenalin) ausgelegt. Aus Stabilitätsgründen verbleiben nach dem Gebrauch 0,75 ml in der Spritze, aber dieser Rest kann nicht erneut verwendet werden und ist auf sichere Weise zu entsorgen.
Der Patient/Betreuer sollte über folgende Schritte informiert werden, die nach jeder Anwendung von Anapen zu beachten sind:
Sofort einen Rettungswagen rufen und „Anaphylaxie“ als Grund angeben, auch wenn sich die Symptome zu verbessern scheinen (siehe Abschnitt 4.4).
Patienten, die bei Bewusstsein sind, sollten mit erhöhten Beinen flach hingelegt jedoch in die sitzende Position gebracht werden, wenn sie Atemschwierigkeiten haben. Bewusstlose Patienten sollten in die stabile Seitenlage gebracht werden.
Soweit dies möglich ist, sollte eine andere Person bis zum Eintreffen der ärztlichen Versorgung beim Patienten bleiben.
Überempfindlichkeit gegen Epinephrin (Adrenalin) oder einen der sonstigen in Abschnitt 6.1 aufgeführten Bestandteile (siehe Abschnitt 4.4 für weitere Informationen in Bezug auf Natriummetabisulfite). Für die Verwendung von Anapen während eines allergischen Notfalls gibt es jedoch keine absoluten Kontraindikationen.
Alle Patienten, die einen Anapen verschrieben bekommen, sollten eine detaillierte Anweisung für den Gebrauch erhalten, damit sie die Einsatzmöglichkeiten und die korrekte Anwendung verstehen (siehe Abschnitt 6.6). Es wird auch dringend geraten, den Patienten nahestehende Personen (z.B. Familienmitglieder, Pflegepersonal, Kollegen) über den korrekten Gebrauch von Anapen aufzuklären, falls in einer Notfallsituation eine Unterstützung durch diese Personen notwendig wird.
Anapen ist ausschließlich als unterstützende Notfalltherapie angezeigt, und die Patienten sollten angewiesen werden, nach einer Verabreichung unverzüglich einen Arzt aufzusuchen, damit eine engmaschige Überwachung der anaphylaktischen Episode und ggf. eine weitere Behandlung erfolgen kann.
Der Patient/Betreuer sollte über die Möglichkeit des Auftretens einer biphasischen Anaphylaxie in Kenntnis gesetzt werden, die durch eine vorübergehende Behebung der Episode, gefolgt vom Wiederauftreten der Symptome einige Stunden später gekennzeichnet ist.
Bei unter Asthma leidenden Patienten besteht möglicherweise das Risiko einer schweren anaphylaktischen Reaktion.
Bei Patienten mit Herzkrankheiten, z. B. Koronar- und Herzmuskelerkrankungen (Angina pectoris kann ausgelöst werden), Cor pulmonale, Herzrhythmusstörungen oder Tachykardie, ist Vorsicht geboten. Bei Patienten mit Schilddrüsenüberfunktion, Herz-Kreislauferkrankungen (schwere Angina pectoris, obstruktive Kardiomyopathien und ventrikuläre Arrhythmien und Hypertonie), Phäochromozytom, hohem intraokulären Druck, schweren Nierenfunktionsstörungen, Prostataadenom mit Restharnbildung, Hyperkalzämie, Hypokaliämie, Diabetes oder bei älteren oder schwangeren Patienten besteht die Gefahr von Nebenwirkungen nach Anwendung von Epinephrin (Adrenalin). Eine wiederholte lokale Injektion kann, bedingt durch eine Gefäßverengung, zu einer Nekrose an der Injektionsstelle führen. Eine versehentliche intravaskuläre Injektion kann aufgrund eines plötzlichen Anstiegs des Blutdrucks zu einer Hirnblutung führen. Eine versehentliche Injektion in Hände oder Füße kann aufgrund einer Gefäßverengung zu einer Verringerung der Durchblutung in den angrenzenden Bereichen führen.
Dieses Arzneimittel enthält weniger als 1 mmol Natrium (23 mg) pro Dosis, d. h. es ist nahezu „natriumfrei“.
Patienten sollten im Hinblick auf verwandte Allergene gewarnt und wann immer möglich untersucht werden, so dass ihre spezifischen Allergene charakterisiert werden können.
Anapen enthält Natriummetabisulfit, das bei empfindlichen Patienten, vor allem bei solchen mit einer asthmatischen Vorerkrankung, zu allergischen Reaktionen einschließlich anaphylaktischer Symptome und Bronchospasmus führen kann. Patienten mit diesen Beschwerden müssen genauestens darüber informiert werden, unter welchen Umständen sie Anapen anwenden dürfen.
Bei übergewichtigen und adipösen Patienten, die eine dickere subkutane Fettschicht haben, besteht die Gefahr, dass das Adrenalin das Muskelgewebe nicht erreicht. Dies kann zu einer suboptimalen Wirkung führen.
Durch trizyklische Antidepressiva, kombinierte Serotonin-Noradrenalin-Antidepressiva wie Venlafaxin, Sibutramin oder Milnacipran und Monoaminooxidase-Hemmer (plötzlicher Blutdruckanstieg und mögliche Herzrhythmusstörungen) sowie COMT-Hemmer, Schilddrüsenhormone, Theophyllin, Oxytocin, Parasympatholytika, bestimmte Antihistaminika (Diphenhydramin, Chlorpheniramin), Levodopa und Alkohol können die Wirkungen von Epinephrin (Adrenalin) verstärkt werden.
Wenn Epinephrin (Adrenalin) gleichzeitig mit nicht-selektiven Beta-Rezeptorenblockern verabreicht wird, können schwere Hypertonie und Bradykardie auftreten.
Die gleichzeitige Behandlung mit Sympathomimetika kann die Wirkungen von Epinephrin (Adrenalin) verstärken.
Bei gleichzeitiger Gabe von Anapen und Arzneimitteln, die das Herz für Arrhythmien sensibilisieren können, wie z. B. Digitalis, Chinidin und halogenierte Anästhetika, ist Vorsicht geboten.
Durch die Gabe von schnell wirkenden Vasodilatatoren oder Alpha-Rezeptorenblockern kann der pressorischen Wirkung von Epinephrin (Adrenalin) entgegengewirkt werden. Durch Beta-Rezeptorenblocker, insbesondere nicht-selektive Beta-Rezeptorenblocker, können die anti-anaphylaktischen Wirkungen des Adrenalins (Epinephrins) antagonisiert werden.
Epinephrin (Adrenalin) hemmt die Insulinsekretion. Daher kann bei Diabetikern eine Erhöhung der Insulindosis oder die Erhöhung der Dosis einer anderen blutzuckersenkenden Therapie erforderlich sein.
Fertilität
Da Adrenalin ein Wirkstoff ist, der natürlich im Körper vorkommt, ist es unwahrscheinlich, dass dieses Arzneimittel schädliche Wirkungen auf die Fertilität hat.
Schwangerschaft
Es liegen keine hinreichenden oder gut kontrollierten Studien über die Anwendung von Epinephrin (Adrenalin) bei schwangeren Frauen vor. Epinephrin (Adrenalin) sollte während der Schwangerschaft nur angewendet werden, wenn der potenzielle Nutzen für die Mutter das potenzielle Risiko für das ungeborene Kind überwiegt. Epinephrin (Adrenalin) kann zu einer dramatischen Verringerung der Durchblutung der Plazenta führen, allerdings geschieht dies auch bei einem anaphylaktischen Schock.
Stillzeit
Epinephrin (Adrenalin) ist nicht oral bioverfügbar; von dem gegebenenfalls in die Muttermilch übergetretenen Epinephrin (Adrenalin) werden keine Auswirkungen auf den gestillten Säugling erwartet.
Nach der Gabe von Epinephrin (Adrenalin) wird empfohlen, dass Patienten kein Kraftfahrzeug lenken oder Maschinen bedienen, da sie möglicherweise immer noch die Wirkungen eines anaphylaktischen Schocks spüren.
Das Auftreten von Nebenwirkungen ist abhängig von der individuellen Empfindlichkeit des einzelnen Patienten und von der angewendeten Dosis.
Die folgende Tabelle beruht auf Erfahrungen in der Anwendung von Adrenalin. Die Nebenwirkungen sind klassifiziert nach dem bevorzugten Begriff der MedDRA-Organsystemklassen und Häufigkeit; Häufigkeiten sind definiert als: Sehr häufig (≥1/10), häufig (≥1/100, <1/10), gelegentlich (≥1/1.000, <1/100), selten (≥1/10.000, <1/1.000), sehr selten (<1/10.000), nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar).
Organsystemklasse |
Häufigkeit |
Nebenwirkung |
Stoffwechsel- und Ernährungstörungen |
Nicht bekannt |
Hyperglykämie, Hypokaliämie, metabolische Azidose |
Psychiatrische Erkrankungen |
Nicht bekannt |
Angstgefühle, Halluzinationen |
Erkrankungen des Nervensystems |
Nicht bekannt |
Kopfschmerzen, Schwindel, Tremor, Synkopen |
Augenerkrankungen |
Nicht bekannt |
Mydriasis |
Herzerkrankungen |
Nicht bekannt |
Tachykardie, Herzrhythmusstörungen (Kammerflimmern/Herzstillstand), Palpitationen |
Gefäßerkrankungen |
Nicht bekannt |
plötzlicher Blutdruckanstieg (bis hin zur Hirnblutung), Vasokonstriktion (z. B. in der Haut, den Schleimhäuten und Nieren), Kältegefühl an den Extremitäten |
Erkrankungen der Atemwege, des Brustraums und Mediastinums |
Nicht bekannt |
Atembeschwerden |
Erkrankungen des Gastrointestinaltrakts |
Nicht bekannt |
Übelkeit, Erbrechen |
Erkrankungen der Nieren und Harnwege |
Nicht bekannt |
Miktionsstörungen mit Harnverhalt |
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort |
Nicht bekannt |
Schwitzen, Hautblässe, Schwäche, Beklommenheit, Nervosität, Muskeltremor |
Anapen enthält Natriummetabisulfit, das bei dafür anfälligen Patienten allergieähnliche Reaktionen hervorrufen kann, u.a. anaphylaktische Reaktionen, oder lebensbedrohliche oder weniger schwerwiegende Asthmaanfälle.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels.
Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger-Allee 3, D-53175 Bonn, Website: www.bfarm.de anzuzeigen.
Eine Überdosierung oder versehentliche intravaskuläre Injektion von Epinephrin (Adrenalin) kann durch den plötzlichen Blutdruckanstieg zu Hirnblutungen führen. Durch periphere Gefäßverengung und kardiale Stimulation kann es zu einem akuten Lungenödem kommen, das zum Tod führen kann.
Die blutdrucksteigernde Wirkung von Epinephrin (Adrenalin) kann durch die Verabreichung von schnell wirkenden Vasodilatatoren oder Alpha-Rezeptorenblockern aufgehoben werden. Folgt auf eine solche Maßnahme eine länger anhaltende Hypotonie, kann ein blutdrucksteigerndes Arzneimittel wie Noradrenalin verabreicht werden.
Ein akutes Lungenödem mit Atmungsbehinderung nach einer Epinephrin (Adrenalin)-Überdosierung sollte durch Gabe eines schnell wirkenden Alpha-Rezeptorenblockers wie Phentolamin und/oder mit intermittierender positiver Druckbeatmung behandelt werden.
Eine Epinephrin (Adrenalin)-Überdosierung kann auch zu vorübergehender Bradykardie mit anschließender Tachykardie führen; darauf können potenziell tödliche Herzrhythmusstörungen folgen, die mit Beta-Rezeptorenblockern behandelt werden können. Vor oder gleichzeitig mit der Gabe von Betablockern müssen Alpha-Rezeptorenblocker verabreicht werden, um damit die durch Alpha-Rezeptoren vermittelten Wirkungen auf die periphere Durchblutung zu kontrollieren.
Pharmakotherapeutische Gruppe: Herzstimulantien, außer Herzglykoside, adrenerge und dopaminerge Mittel, Epinephrin
ATC-Code: C01CA24
Epinephrin (Adrenalin) ist ein natürlich vorkommendes Katecholamin, das vom Nebennierenmark als Reaktion auf körperliche Anstrengung oder Stress sezerniert wird. Es ist ein sympathomimetisches Amin, das ein starkes Stimulans sowohl der Alpha- als auch der Beta-Rezeptoren ist, und seine Auswirkungen auf die Zielorgane sind daher komplex. Es ist das Mittel der Wahl zur raschen Linderung von Hypersensibilitätsreaktionen, Allergien oder idiopathischen bzw. durch Belastung ausgelösten Anaphylaxien.
Epinephrin (Adrenalin) hat über die Stimulation der Alpha-Rezeptoren eine stark gefäßverengende Wirkung; dies wirkt der Vasodilatation und der erhöhten Gefäßpermeabilität entgegen, die zu einem Verlust an intravaskulärer Flüssigkeit und anschließender Hypotonie führen kann, den wichtigsten pharmakotoxikologischen Merkmalen eines anaphylaktischen Schocks. Durch seine Stimulation der bronchialen Beta-Rezeptoren übt Epinephrin (Adrenalin) eine starke bronchodilatatorische Wirkung aus, welche Keuchen und Dyspnoe mildert. Epinephrin (Adrenalin) lindert auch Pruritus, Urtikaria und Angioödem, die mit einer Anaphylaxie verbunden sind.
Epinephrin (Adrenalin) wird im Körper schnell inaktiviert, hauptsächlich in der Leber durch die Enzyme Catechol-O-Methyl-Transferase (COMT) und Monoaminooxidase (MAO). Der Großteil einer Dosis Epinephrin (Adrenalin) wird in Form von Metaboliten im Urin ausgeschieden. Die Plasma-Halbwertszeit beträgt etwa 2 – 3 Minuten. Bei subkutaner oder intramuskulärer Injektion kann jedoch die lokale Vasokonstriktion die Resorption verzögern, so dass die Wirkungen länger anhalten können, als nach der Halbwertszeit anzunehmen wäre.
Epinephrin (Adrenalin) findet seit vielen Jahren verbreitete Anwendung in der klinischen Behandlung von allergischen Notfällen. Es liegen keine für den Arzt relevanten präklinischen Daten vor, die über die Informationen hinausgehen, die bereits in den anderen Abschnitten der Fachinformation enthalten sind.
Natriumchlorid
Natriummetabisulfit (Ph.Eur.) (E 223)
Salzsäure (zur Einstellung des pH Wertes)
Wasser für Injektionszwecke
Da keine Kompatibilitätsstudien durchgeführt wurden, darf dieses Arzneimittel nicht mit anderen Arzneimitteln gemischt werden.
16 Monate
Nicht über 25°C lagern.
In der Originalpackung aufbewahren, um den Inhalt vor Licht zu schützen.
Der Anapen sollte liegend gelagert werden.
Anapen besteht aus einer Fertigspritze zur einmaligen Anwendung in einer automatischen Injektionsvorrichtung (Autoinjektor).
Die Spritze enthält eine Epinephrin (Adrenalin)-Lösung. Der Autoinjektor gibt 0,3 ml dieser Lösung ab.
Das Primärbehältnis ist eine Glasspritze, die an einem Ende mit einem Gummi-Kolben und am anderen Ende durch eine Gummi-Abdeckkappe für die Nadel verschlossen ist.
Spritze
BD (Becton Dickinson) Borosilikatglas Typ 1, 27G ½’’
Freiliegende Nadellänge: 10 mm ± 1.5 mm.
Kolben
BD (Becton Dickinson) schwarz, Chlorbutylgummi PH 701/50
Packungsgrößen: 1 oder 2 Fertigpens in thermogeformtem Schutztray und Umkarton.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
Siehe Abschnitt 4.2 in Bezug auf die Schritte, die vom Patienten/Betreuer nach der Anwendung jedes Anapen zu befolgen sind.
Es ist sehr wichtig, dass der Patient detaillierte Informationen zur Anwendung des Anapen erhält.
Nur zur einmaligen Anwendung.
Der Anapen sollte nach Ablauf des auf dem Etikett angegebenen Verfalldatums nicht mehr verwendet werden.
Entsorgen und ersetzen Sie den Autoinjektor nach Ablauf des Verfalldatums.
Die Lösung sollte regelmäßig durch das Sichtfenster überprüft werden. Entsorgen und ersetzten Sie den Anapen, wenn die Lösung trüb oder verfärbt ist oder Partikel enthält.
Das integrierte Arzneimittel, wie im untenstehenden Abschnitt „Gebrauchsanweisung“ gezeigt wird, sollte regelmäßig überprüft werden, damit der Anapen in Notfallsituationen verwendet werden kann.
Gebrauchsanweisung
Für Demonstrations- und Übungszwecke können unter den folgenden Kontaktdaten behördlich zugelassene Schulungsmaterialien abgerufen werden:
Website: www.Anapen2.de
Tel.: 030 3465 5460-0
A. Die Teile des Anapen Autoinjektors:
Vor der Benutzung des Anapen Autoinjektors sollte der Patient über die Komponenten des Autoinjektors informiert werden. Die Abbildung zeigt die einzelnen Komponenten.
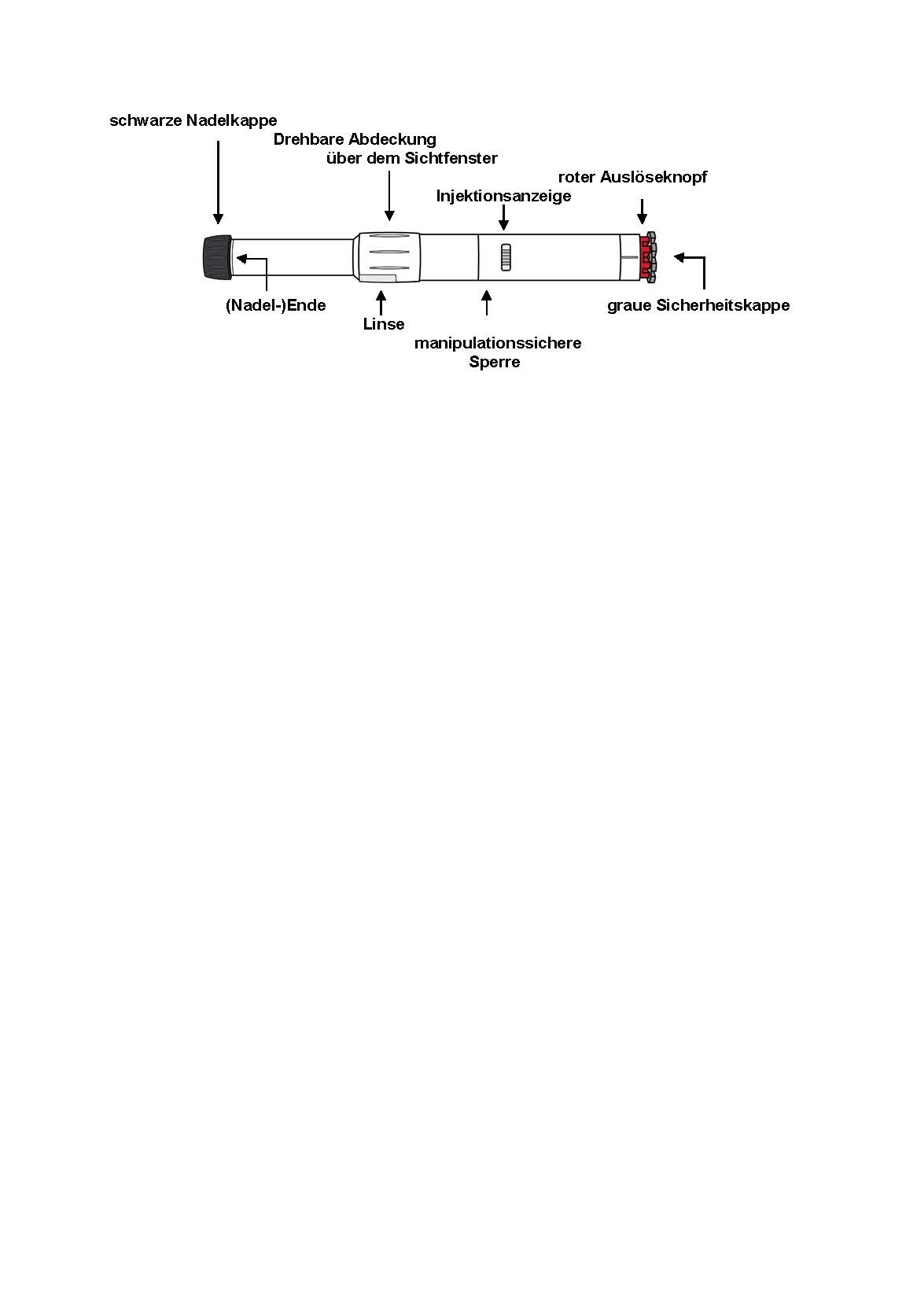
Drehbare Abdeckung über dem Sichtfenster: Der Patient dreht die Abdeckung über den Sichtfenstern, um die Linsen über den Sichtfenstern des Autoinjektors auszurichten
Sichtfenster: Vor der Injektion sieht der Patient durch die Linse in dieses Fenster, um zu überprüfen, dass die Lösung klar ist und angewendet werden kann.
Injektionsanzeige: Vor der Injektion ist durch die Injektionsanzeige ein weißer Kunststoffkolben zu sehen. Dies bedeutet, dass der Anapen Autoinjektor nicht versehentlich ausgelöst oder manipuliert wurde. Nach der Injektion wird die Injektionsanzeige rot. Dies zeigt an, dass der Anapen Autoinjektor korrekt ausgelöst wurde.
Schwarze Nadelkappe (wiederverwendbar): Diese Kappe dient zum Schutz der Nadel, wenn der Anapen Autoinjektor nicht benutzt wird. Die Nadelkappe wird vor der Injektion abgezogen. Nach der Injektion wird die schwarze Nadelkappe umgedreht und wieder auf dasselbe Ende des Anapen Autoinjektors aufgesteckt, um die Nadel abzudecken.
Graue Sicherheitskappe: Sie deckt den roten Auslöseknopf ab und verhindert, dass dieser versehentlich hineingedrückt wird.
Die schwarze Nadelkappe und die graue Sicherheitskappe dürfen erst entfernt werden, wenn der Anapen Autoinjektor angewendet werden muss.
B. Überprüfung des Anapen Autoinjektors
Vor der Anwendung des Anapen Autoinjektors muss der Patient Folgendes prüfen:
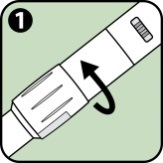 |
1. Die Abdeckung über den Sichtfenstern wie vom Pfeil angezeigt vollständig gegen den Uhrzeigersinn drehen, um die Linsen über den Sichtfenstern des Autoinjektors auszurichten. |
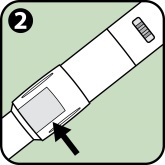 |
2. Durch die Linse in das Sichtfenster sehen. Die Lösung muss klar und farblos sein. Wenn die Lösung getrübt oder verfärbt ist oder Schwebeteilchen enthält, muss der Anapen Autoinjektor entsorgt werden. |
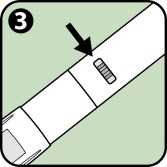 |
3. Darauf achten, dass die Injektionsanzeige nicht rot ist. Eine rote Anzeige bedeutet, dass der Anapen Autoinjektor bereits ausgelöst wurde und entsorgt werden muss. |
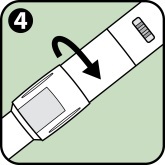 |
4. Die Abdeckung über den Sichtfenstern wie vom Pfeil angezeigt vollständig im Uhrzeigersinn zurückdrehen um sicherzustellen, dass beide Sichtfenster abgedeckt sind. Den Anapen Autoinjektor dann zurück in seine Verpackung legen, bis dieser benutzt werden muss. |
C. Anwendung des Anapen Autoinjektors
Wenn die schwarze Nadelkappe abgenommen wurde, darf das offene (Nadel‑)Ende des Anapen Autoinjektors nicht mit dem Daumen, den Fingern oder der Hand berührt werden.
Bei der Benutzung des Anapen Autoinjektors ist Folgendes zu beachten:
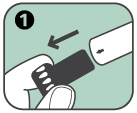 |
1. Schwarze Nadelkappe abziehen. Dazu muss man kräftig ziehen. Es wird gleichzeitig ein grauer Nadelschutz entfernt. |
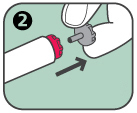 |
2. Die graue Sicherheitskappe vom roten Auslöseknopf entfernen. |
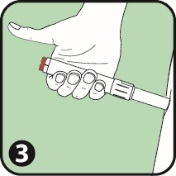 |
3. Das offene (Nadel-)Ende des Anapen Autoinjektors gegen die Außenseite des Oberschenkels halten. Der Anapen Autoinjektor kann gegebenenfalls auch durch leichte Kleidung hindurch, wie z. B. Jeansstoff, Baumwolle oder Polyester angewendet werden. |
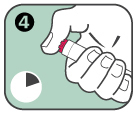 |
4. Den roten Auslöseknopf drücken, bis ein Klicken zu hören ist. Den Anapen Autoinjektor 10 Sekunden lang gegen die Außenseite des Oberschenkels halten und anschließend langsam vom Schenkel abnehmen. Die Injektionsstelle leicht massieren. |
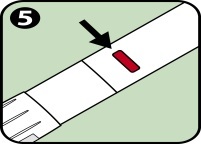 |
5. Die Injektionsanzeige wird rot. Dies zeigt an, dass die Injektion vollständig abgeschlossen ist. Wenn die Injektionsanzeige nicht rot ist, muss die Injektion mit einem neuen Anapen wiederholt werden. |
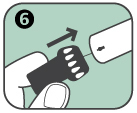 |
6. Nach der Injektion ragt die Nadel aus dem Autoinjektor heraus. Das breite Ende der schwarzen Nadelkappe wird auf das offene (Nadel-)Ende des Anapen Autoinjektors (in der gezeigten Pfeilrichtung) gesteckt, um die Nadel abzudecken. |
Sofort nach der Anwendung von Anapen muss der Patient unter der Notrufnummer (112) einen Rettungswagen anfordern und als Grund „Anaphylaxie“ angeben. Der Patient muss den Rettungssanitätern erklären, dass er eine Adrenalin-Injektion in seinen Oberschenkelmuskel erhalten hat und ihnen den Karton sowie diese Anweisungen zeigen.
Nicht verwendete Arzneimittel oder Abfallmaterial sind entsprechend den örtlichen Anforderungen zu entsorgen.
Bioprojet Pharma
9 rue Rameau
75002 Paris
Frankreich
Örtlicher Vertreter
Bioprojet Deutschland GmbH, Bismarckstr. 63, 12169 Berlin
Tel.: 030/3465 5460-0
E-Mail: info@bioprojet.de
Medizinische Information
Tel.: 0251/60935 599
E-Mail: arzneimittelnebenwirkung@bioprojet.com
97202.00.00
Datum der Erteilung der Zulassung: 22.01.2019
Datum der Verlängerung der Zulassung: 18.01.2025
April 2026
Verschreibungspflichtig